无机固态锂离子电池电解质的研究进展
刘 娇,怀永建,王海文
(中航锂电(洛阳)有限公司,河南洛阳471003)
无机固态锂离子电池电解质的研究进展
刘 娇,怀永建,王海文
(中航锂电(洛阳)有限公司,河南洛阳471003)
无机固态锂离子电池因其高安全性、高能量密度和宽的工作温度范围,成为研究的热点。综述了LiPON、石榴石型和硫化物电解质的离子电导率及其应用于全固态锂离子电池的研究。
无机固态电解质;LiPON;石榴石结构;硫化物电解质;全固态锂离子电池
目前使用的锂离子电池含有可燃性液态有机物,容易出现腐蚀电极、电解液挥发、漏液,甚至发生爆炸燃烧等安全问题,很大程度上限制了锂离子电池的应用领域。尽管聚合物电解质的使用在一定程度上缓解了安全问题,但是没有从根本上解决。无机固体锂离子电解质的使用可以彻底解决因可燃性有机电解液造成的锂离子电池的安全性隐患[2]。使用无机固态电解质在能量密度、工作温度范围和循环寿命方面有更好的性能。本文综述了几种主要的锂离子无机固态电解质材料(LiPON型、GARNET型、硫化物电解质)的研究与进展。
1 无机固态电解质概述
理想的无机固态锂离子电解质应满足以下要求[1]:(1)在工作温度下具有良好离子电导率,具有极小的或几乎没有晶界电阻;(2)具有极低的电子电导率;(3)在电池工作电压范围内有较高的电化学稳定性,一般要求电化学窗口高于5.0 V (.Li/Li+);(4)化学稳定性好,与电极材料不发生化学反应。
2 无机固态电解质的研究
目前,用于锂离子电池的无机固态电解质包括晶态固态电解质和非晶态固态电解质(也称玻璃态电解质)两大类。无机晶态固态电解质包括层状Li3N、钙钛矿型、钠快离子导体(NASICON)、锂快离子导体(LISICON)、石榴石型(GARNET)等,玻璃态固态电解质包括LiPON型、氧化物和硫化物电解质[2]。由于Li3N、钙钛矿型和NASICON的电化学稳定性差,不适合用于高电压锂离子电池[3],在此不作综述。本文主要综述以下几种应用前景较好和新型的固态电解质。
2.1 LiPON型
LiPON电解质最早于1992年由美国橡树岭国家实验室利用射频磁控溅射装置,在高纯N2气氛中溅射高纯Li3PO4靶材获得,该材料在27℃下的离子电导率为2×10-6S/cm,电化学窗口达5.5 V[4]。LiPON是一种理想的薄膜锂离子电池电解质材料,其化学性质和电化学性质稳定,与很多电极材料兼容性好。目前主要用于薄膜电池,这种电池结构简单,倍率性能及循环性能都比较优异。虽然此电解质的电导率并不高,由于其成膜性好,一般采用溅射技术制备,电解质层很薄且与电极的界面接触较好,使得电池的整体电阻较小。一般常用的薄膜沉积方法有射频磁控溅射沉积、脉冲激光沉积、喷雾热解、电子束蒸发法、离子束辅助真空热蒸发等[5]。
Kim等[6]认为LiPON电解质的电导率与其含氮量无关,而是取决于薄膜沉积的条件,不同的沉积方法制备的电解质薄膜材料对电池的性能有影响,目前LiPON含氮量与其电导率的关系尚不明确。Ribeiro等[7]采用射频溅射法,并对比不同的氮气气压和溅射功率,以确定最佳的溅射参数,结果表明气压为0.03 Pa,功率为150 W时最优,35℃时其电导率为10-6S/cm。
韩国研究者Koo等[8]采用LiPON电解质制备了LiCoO2/ LiPON/Li可弯曲的柔性无机薄膜电池。所制备的电池在无弯曲及不同弯曲程度下的充放电曲线,弯曲后电池的容量有一定程度的衰减,但是100次循环后性能没有明显变化。将所制薄膜电池反复弯折20 000次后,其电压保持率高达99.73%,表明LiPON材料在柔性薄膜电池方面具有很好的应用前景。
2.2 GARNET型
石榴石型结构是由Thangadurai和Weppner等[9]发现的一种新型锂无机固态电解质材料,基体结构通式为Li5La3M2O12(M=Nb,Ta),与理想石榴石结构相比,每个单胞多出16个额外的Li+。由于其具有良好的室温离子电导率(10-4S/cm),低的电子导电性,高的化学稳定性,与电极材料良好的相容性,在解决传统有机电解液的泄露等安全问题方面具有很好的应用前景。
为了提高石榴石的离子电导率,掺杂是一种常见有效的方法。主要是对Li5ALa2M2O12中A位置和M位置的掺杂[10]。A位一般是掺杂半径较大的二价碱土金属离子(Ca2+、Sr2+、Ba2+),得到富锂石榴石结构电解质,掺杂后材料的晶胞体积增大,有利于锂离子的迁移,因而可以提高材料的电导率。Thangadurai和Weppner[11]的研究表明,Li6ALa2Nb2O12(A=Ca、Sr、Ba)的电导率随着碱土金属离子半径的增加而增加,掺杂Ba具有最高的晶相电导率(6×10-6S/cm,22℃),活化能为0.44 eV。M位一般掺杂四价金属离子(Zr4+、Sn4+),由于Li7La3Zr2O12对锂金属兼容性好而受到更多研究者的关注。Murugan等[12]合成了Li7La3Zr2O12,其电导率为3×10-4S/cm(25℃),材料暴露在潮湿的空气中几周后仍保持化学稳定性。之后,Murugan等[13]报道了掺杂Y的Li7La3Zr2O12,其室温下体相和总电导率分别为9.56×10-4S/cm和8.10×10-4S/cm。
减小晶界电阻也可以提高总的离子电导率。Kumazaki等[14]在Li7La3Zr2O12中复合无定型的Al和Si,25℃下的电导率为6.8×10-4S/cm,研究发现在材料晶体界面有Li-Al-Si-O的无定型体和纳米级的 LiAlSiO4晶体,促进了锂离子在Li7La3Zr2O12晶体之间传导,从而提高了材料的总电导率。Cao等[15]采用固相法合成Li7-La3Zr2-Ta O12(LLZTO,=0.25),研究了煅烧温度对材料电导率的影响,在1 175℃下煅烧36 h制备的材料具有室温下最高电导率(2.9×10-4S/cm)。另外,研究发现,加入质量分数为1%的Li3PO4可以使LLZTO电导率提高到7.2×10-4S/cm,此时的活化能改变较小,Li3PO4可以改善LLZTO晶体之间的接触。由于石榴石粒子硬,因而粒子之间只能发生点接触,晶粒间电阻较大。日本丰田自动车株式会社的专利[16]报道在石榴石之间加入粒径小于石榴石型电解质的磷酸根锂离子导体,通过在石榴石型化合物晶粒间配置可发生塑性形变的磷酸根锂离子导体,能够降低晶粒间电阻。
Kotobuki等[17]采用固相法(1 200℃,24 h)合成Li5La3Ta2O12(LLTa),室温下材料的电导率为1.3×10-4S/cm,并组装Li-CoO2/LLTa/Li电池进行电化学性能研究。图1为所得电池循环伏安曲线。由图表明材料具有良好的可逆性,将前面组装的电池置于充满氩气手套箱内一年之后测得循环伏安曲线仍具有很好的可逆性。
2.3 硫化物电解质
硫化物电解质是目前导电率最高的一类固态电解质,室温下可达10-4~10-3S/cm,且电化学窗口在5 V以上,在锂离子电池中应用前景较好[18]。氧化物电解质中用硫原子代替氧原子成为硫化物,因为硫的电负性比氧小,对锂离子的束缚力小,同时硫原子的离子半径较大,离子的通道较大,有利于离子的迁移[19],因而硫化物比氧化物具有更高的离子电导率。
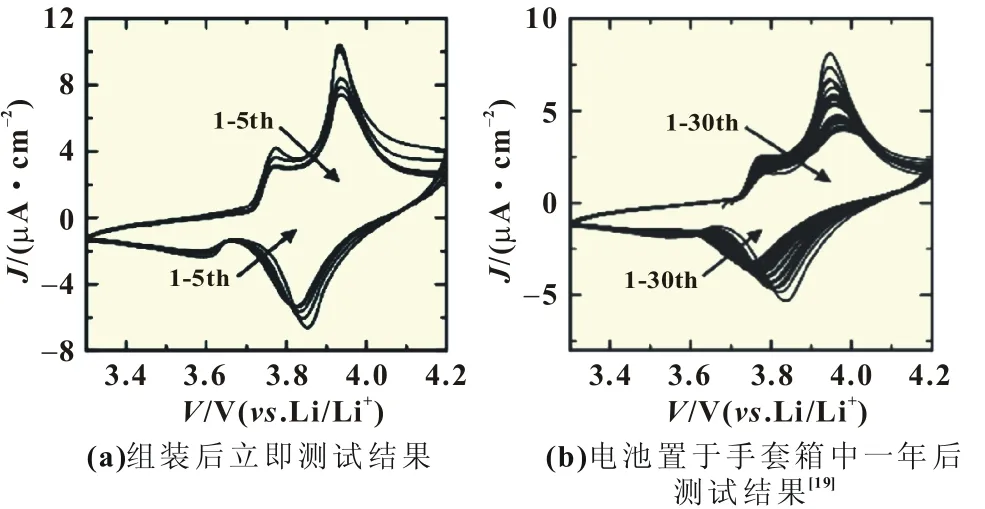
图1 LiCoO2/LLTa/Li全固态锂离子电池循环伏安曲线
但是硫化物对水分敏感,在空气中缓慢生成H2S气体。为了抑制Li2S-P2S5中H2S的生成,可以调节原材料Li2S和P2S5的比例,Hayashi等[20]的研究表明当Li2S和P2S5的比例为75∶25时产生H2S最少,此时获得的硫化物电解质材料对应于原酸Li3PS4的组成。为了进一步提高Li3PS4的稳定性,Hayashi课题组向其中添加碱性氧化物可以与H2S反应来减少气体的产生,研究表明上述反应的Δ为负值,反应是自发进行的。90 Li3PS4·10 ZnO表现出较好的电导率和大于5 V的电化学窗口。组装固态电池In/90 Li3PS4·10 ZnO/LiCoO2,其首次放电容量约为90 mAh/g,70次循环之后库仑效率保持100%[21]。
2011 年,日本东京工业大学研究者[21]采用高温固相法合成Li10GeP2S12,其室温离子电导率高达0.012 S/cm,与有机电解液相当。以LiCoO2和In分别为正极和负极材料组装全固态锂电池。在14 mA/g的电流密度下,首次充放电比容量分别为135和124 mAh/g,效率为91.8%,第8次充放电比容量分别为122和121 mAh/g。
尽管Li10GeP2S12有如此高的电导率,但是材料中含有昂贵的Ge,同时硫化物存在对水分敏感的问题。Ong等[23]采用第一性原理计算对Ge和S位进行替换,以期望寻找到更好的替代材料。计算表明,对Ge采用同价元素Si、P替换,材料具有相似的相稳定性、电化学稳定性和锂离子电导率,当O对S进行替换时,相稳定性和电导率都变差。Philipp Bron等[24]用Sn来代替Li10GeP2S12中的Ge,Sn代替昂贵的Ge,使材料的成本降低,采用Li2S、P2S5和Li4[SnS4]为原材料合成Li10SnP2S12。实验表明,在27℃时Li10SnP2S12体相离子电导率达0.007 S/cm,总电导率为0.004 S/cm,具有较大的晶界阻抗,有望通过合成条件的优化来减小晶界阻抗。
Seion等[25]最近报道了Li2S-P2S5玻璃陶瓷体系固态电解质,最高的离子电导率为0.017 S/cm,最低活化能为 17 kJ/mol,比之前报道[24]的Li10GeP2S12具有更高的电导率。对材料热处理条件优化使晶界阻抗减小,对空位也产生了影响,从而提高了锂离子的传导,但是热处理过程会增加电解质和电极材料的界面阻抗,该课题组下一步的研究计划是减小此界面阻抗。
由于硫化物和电极材料是固-固接触,比传统液态锂离子电池中的固-液接触的阻抗大,为了增加固态电解质和电极材料的接触,正极采用正极活性材料和固态电解质的混合物。虽然硫化物电解质导电率较高且有较好的电化学稳定性,由于在正极活性物质和硫化物固态电解质界面之间形成了高阻抗空间电荷层导致其倍率性能差。为了抑制这样高阻抗层形成,可以在固态电解质表面包覆只有离子电导的氧化物,避免硫化物固态直接接触正极材料[26-27]。
Ohta等[26]在LiCoO2表面包覆不同厚度的Li4Ti5O12,交流阻抗表明,随着包覆厚度增加阻抗先减小,后增加,当包覆的平均厚度为5 nm时有最小的阻抗(44 Ω),而未包覆LiCoO2阻抗值有910 Ω。以Li-In合金为负极,Li3.25Ge0.25P0.75S4为电解质,放电性能和交流阻抗一致,包覆厚度为5 nm的样品在电流密度高达10 mA/cm2时,放电比容量约为44 mAh/g,倍率性能得到显著提升。
Takada等[28]综述了固态电解质和电极界面结构设计问题,在正极材料表面包覆操作较复杂而且不能保证包覆一层均匀的薄层。采用二维的纳米片状氧化物作为缓冲层将取得更好的效果,这种纳米片状氧化物可以通过对层状基体氧化物的剥离实现。研究表明[29]纳米片状TaO3具有电子绝缘和合适锂离子通过的通道,适合用于缓冲层,实验表明引入TaO3缓冲层后界面阻抗比之前降低了两个数量级。由于LiCoO2兼具离子和电子导电性,表面有偏析现象,掺杂Al后,产物LiAl0.08Co0.92O2中的Al主要分布在表面,自发形成一层只有离子电导的缓冲层,研究表明掺杂Al的LiCoO2在1下放电比容量为115 mAh/g,5下的放电比容量为84 mAh/g,相比于包覆Li4Ti5O12更显著地提高了固态离子电池的倍率性能[30],倍率比较如图2所示。
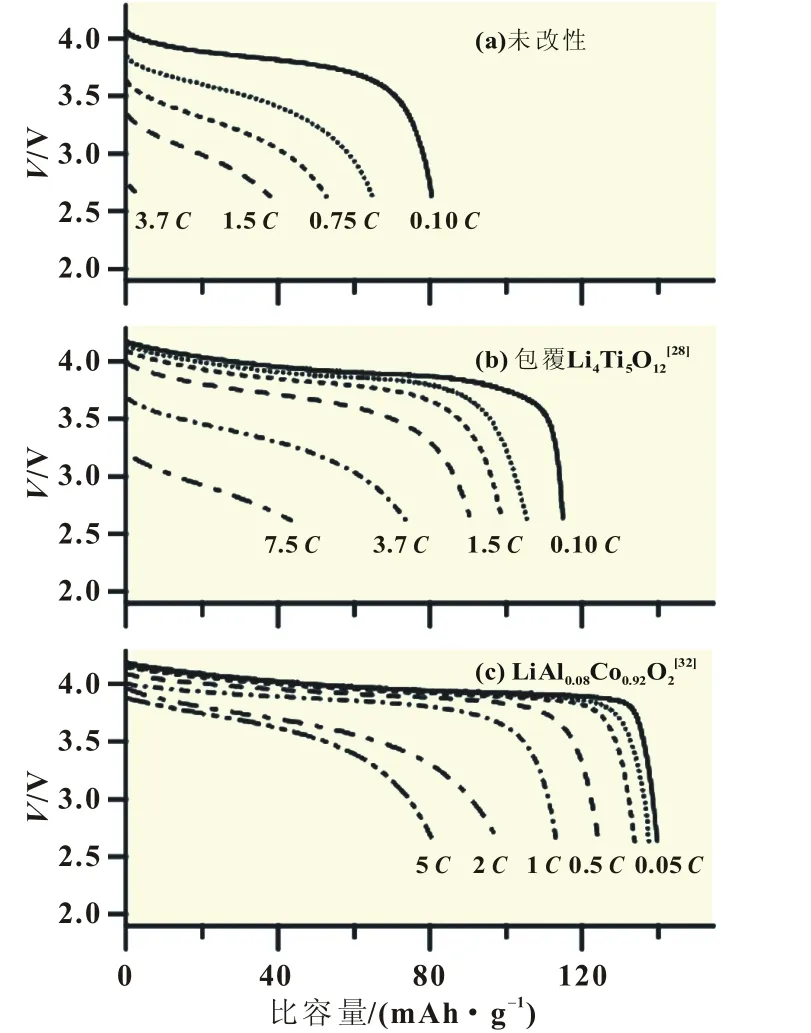
图2 LiCoO2电极材料(电解质为Li3.25Ge0.25P0.75S4)的倍率性能比较
3 结语
发展全固态电解质对于解决锂离子电池的安全性具有战略意义。目前对于锂离子无机固态电解质的研究主要集中于如何提高电解质的离子电导率、提高电解质与电极的相容性、减少与电极的界面阻抗等。LiPON由于成膜性好主要用于薄膜锂离子电池。硫化物电解质电导率最高达到~10-2S/cm,有望应用于大容量全固态电池,然而与电极的相容性差,存在界面问题。目前已有策略来降低界面阻抗,并取得了良好的进展,但是需要进一步完善和优化电池结构设计。未来大容量全固态锂离子电池在储能和动力领域将更进一步发展。
[1]朱永明,任雪峰,李宁.无机固态锂离子电解质的研究进展[J].化学通报,2010,12:1073-1079.
[2]丁飞,张晶,杨凯,等.锂离子无机固体电解质研究进展[J].电源技术,2007,31(6):496-499.
[3]KNAUTH P.Inorganic solid Li ion conductors:an overview[J].Solid State Ionics,2009,180(14):911-916.
[4]BATES J,DUDNEY N,GRUZALSKI G,et al.Electrical properties of amorphous lithium electrolyte thin films[J].Solid State Ionics, 1992,53:647-654.
[5]赵胜利,文九巴,樊丽梅,等.锂磷氧氮(LiPON)薄膜的制备及应用进展[J].电池,2006,35(6):459-461.
[6]KIM Y G,WADLEY H.Lithium phosphorous oxynitride films synthesized by a plasma-assisted directed vapor deposition approach[J]. Journal of Vacuum Science&Technology A,2008,26(1):174-183.
[7]RIBEIRO J,SOUSA R,CARMO J,et al.Enhanced solid-state electrolytes made of lithium phosphorous oxynitride films[J].Thin Solid Films,2012,522:85-89.
[8]KOO M,PARK K,LEE S H,et al.Bendable inorganic thin-film battery for fully flexible electronic systems[J].Nano Letters,2012,12 (9):4810-4816.
[9]THANGADURAI V,KAACK H,WEPPNER W.Novel fast lithium ion conduction in garnet-type Li5La3M2O12(M=Nb,Ta)[J].Journal of the American Ceramic Society,2003,86(3):437-440.
[10]权周,钟耀东,强颖怀,等.新型石榴石结构锂快离子导体Li5La3M2O12的研究进展[J].电源技术,2010,34(5):51-519.
[11]THANGADURAI V,WEPPNER W.Li6ALa2Nb2O12(A=Ca,Sr,Ba): A new class of fast lithium ion conductors with garnet-like structure[J].Journal of the American Ceramic Society,2005,88(2):411-418.
[12]MURUGAN R,THANGADURAI V,WEPPNER W.Fast lithium ion conduction in garnet-type Li7La3Zr2O12[J].Angewandte Chemie International Edition,2007,46(41):7778-7781.
[13]MURUGAN R,RAMAKUMAR S,JANANI N.High conductive yttrium doped Li7La3Zr2O12cubic lithium garnet[J].Electrochemistry Communications,2011,13(12):1373-1375.
[14]KUMAZAKI S,IRIYAMA Y,KIM K,et al.High lithium ion conductive Li7La3Zr2O12by inclusion of both Al and Si[J].Electrochemistry Communications,2011,13(5):509-512.
[15]CAO Y,LI Y,GUO X.Densification and lithium ion conductivity of garnet-type Li7-La3Zr2-Ta O12(=0.25) solid electrolytes[J]. Chinese Physics B,2013,22(7):078201.
[16]陶山博司,川本浩二.固体电解质、固体电解质片及固体电解质的制造方法:中国,200980133549.5[P].2011-07-20.
[17]KOTOBUKI M,KANAMURA K.Fabrication of all-solid-state battery using Li5La3Ta2O12ceramic electrolyte[J].Ceramics International,2013,39(6):6481-6487.
[18]HAYASHI A,TATSUMISAGO M.Invited paper:Recent development of bulk-type solid-state rechargeable lithium batteries with sulfide glass-ceramic electrolytes[J].Electronic Materials Letters,2012,8(2):199-207.
[19]TSUTOMU M A,MASAHIRO T.Preparation and characterization of lithium ion-conducting oxysulfide glasses[J].Solid State Ionics, 2000,136:1015-1023.
[20]MURAMATSU H,HAYASHI A,OHTOMO T,et al.Structural change of Li2S-P2S5sulfide solid electrolytes in the atmosphere[J]. Solid State Ionics,2011,182(1):116-119.
[21]HAYASHI A,MURAMATSU H,OHTOMO T,et al.Improvement of chemical stability of Li3PS4glass electrolytes by adding MO (M=Fe,Zn,and Bi)nanoparticles[J].Journal of Materials Chemistry A,2013,1(21):6320-6326.
[22]KAMAYA N,HOMMA K,YAMAKAWA Y,et al.A lithium superionic conductor[J].Nature Materials,2011,10(9):682-686.
[23]ONG S P,MO Y,RICHARDS W D,et al.Phase stability,electrochemical stability and ionic conductivity of the Li10±1MP2X12(M= Ge,Si,Sn,Al or P,and X=O,S or Se)family of superionic conductors[J].Energy&Environmental Science,2013,6(1):148-156.
[24]BRON P,JOHANSSON S,ZICK K,et al.Li10SnP2S12:An afford able lithium superionic conductor[J].Journal of the American Chemical Society,2013,135(42):15694-15697.
[25]SEINO Y,OTA T,TAKADA K,et al.A sulphide lithium super ion conductor is superior to liquid ion conductors for use in rechargeable batteries[J].Energy&Environmental Science,2014,7(2): 627-631.
[26]OHTA N,ZHANG L,MA R,et al.Enhancement of the high-rate capability of solid-state lithium batteries by nanoscale interfacial modification[J].Advanced Materials,2006,18(17):2226-2229.
[27]TAKADA K,OHTA N,ZHANG L,et al.Interfacial phenomena in solid-state lithium battery with sulfide solid electrolyte[J].Solid State Ionics,2012,225:594-597.
[28]TAKADA K.Interfacial Nanoarchitectonics for solid-state lithium batteries[J].Langmuir,2013,29(24):7538-7541.
[29]XU X,TAKADA K,FUKUDA K,et al.Tantalum oxide nanomesh as self-standing one nanometre thick electrolyte[J].Energy&Environmental Science,2011,4(9):3509-3512.
[30]XU X,TAKADA K,WATANABE K,et al.Self-organized core-shell structure for high-power electrode in solid-state lithium batteries [J].Chemistry of Materials,2011,23(17):3798-3804.
Recent progress of inorganic solid electrolyte for lithium ion batteries research
Inorganic solid-state lithium ion battery with good safety, high energy density and wide operating temperature had become the study focus.The ionic conductivity and application in all solid lithium battery of LiPON, garnet and sulfide electrolyte were viewed.
inorganic solid electrolyte;LiPON;garnet;sulfide electrolyte;all-solid-state lithium ion batteries
TM 912
A
1002-087 X(2015)10-2308-04

2015-03-14
刘娇(1986—),女,湖北省人,工程师,硕士,主要研究方向为锂离子电池材料。
刘娇

