消化道异位胰腺的MDCT表现分析
1.中山大学附属第三医院放射科2.中山大学附属第三医院病理科(广东 广州 510630)
陈秀珍1 黄文薮1 陈建宁2覃 杰1 曾昭吝1 朱康顺1
消化道异位胰腺的MDCT表现分析
1.中山大学附属第三医院放射科2.中山大学附属第三医院病理科(广东 广州 510630)
陈秀珍1黄文薮1陈建宁2覃 杰1曾昭吝1朱康顺1
目的分析消化道异位胰腺的多层螺旋CT(MDCT)表现,提高诊断的准确性和鉴别诊断能力。方法回顾性分析25例经组织病理学证实的消化道异位胰腺的MDCT资料,患者术前均行多排螺旋CT平扫、三期增强扫描及三维重建,观察病灶的位置、大小、长径与短径的比值、形态、密度、强化方式、强化程度、生长方式、病灶边界、病灶表面及周围粘膜情况,总结该病的CT表现特点。结果25例均为单发病灶,9例(36%)发生在胃部,9例(36%)在十二指肠,5例(20%)在空肠,2例(8%)在回肠;大小为6mm-25mm;胃病灶LD/SD>1.4的有7例(78%);十二指肠病灶LD/SD>1.4的有5例(55%);空回肠病灶LD/SD均为1.0。15例(60%)为类圆形,4例为圆形,4例呈不规则形,2例表现为胃肠壁局部增厚。11例(44%)起源于黏膜下及肌层,21例(84%)累及黏膜下层。病灶平扫密度均匀,增强扫描均呈持续性强化,类似胰腺强化方式;13例(53%)病灶强化程度与正常胰腺组织相仿;2例显示导管征;20例(80%)病灶向腔内生长,18例(72%)病灶边界欠清楚。结论消化道异位胰腺的CT表现具有一定特征性,熟悉其特点可提高对该病的诊断水平。
异位胰腺;消化道;体层摄影术;X线摄像机
异位胰腺又称为迷走胰腺或副胰腺,属于先天畸形,是正常胰腺解剖部位以外的孤立胰腺组织,和正常胰腺之间无任何解剖、血管关系[1],文献报道发病率约为1%~13%[2]。异位胰腺易发生囊性变、坏死,引起黏膜脱垂甚至癌变,有学者认为,一旦发现异位胰腺,就应该将其手术切除[3];也有学者认为无症状者可定期随访,对于有症状者,则主张积极治疗[45]。由于患者临床表现及实验室检查均缺乏特异性,异位胰腺常易误诊。本文回顾性分析了25例经手术病理证实的消化道异位胰腺患者的临床、CT及病理资料,探讨其MDCT表现特征及诊断价值。
1 资料与方法
1.1 一般资料收集本院2010年1月至2014年12月经手术病理证实的消化道异位胰腺25例。其中男性15例,女性10例;年龄范围14岁~59岁,平均年龄39.8岁。17例患者临床表现为腹痛,2例为其他腹部不适,2例为黑便,2例为恶心,2例无明显症状,因体检偶然发现。24例患者行胃镜检查。
1.2 CT检查方法采用Toshiba 320排螺旋CT或Toshiba 64排螺旋CT机扫描。检查前患者禁食6小时以上,扫描前30分钟口服温水800ml~1000ml,检查前10分钟肌肉注射654-2针剂15mg。扫描开始前再次口服温水500ml~800ml,适度充盈胃肠道,并对患者进行呼吸训练以减少呼吸所致的运动伪影。扫描参数:管电压120kv,管电流160mA~200 mA,层厚及层间距均为5mm,螺距0.8。增强扫描所用对比剂为碘普罗胺(300mgI/ ml),经高压注射器给药,剂量1.5ml/kg,注射流率3.0ml/s,注射对比剂后28秒开始动脉期扫描,间隔30秒行门脉期扫描,再间隔65秒行静脉期扫描。原始数据在后台工作站重建冠状位,重建层厚3mm,重建间隔2mm,部分病变显示不清者,再进行多角度多平面分析。
1.3 CT图像分析由2名具有10年以上腹部影像诊断工作经验的放射科医师对病变的CT征象进行观察分析,当两者意见不统一时,以讨论后的一致意见为准。包括①病变部位;②病灶大小,测量长径和短径;③病灶形态:分圆形、类圆形和不规则形;④病灶边界:分清晰、不清晰;⑤病灶密度,分均匀、不均匀;⑥强化特点:以正常胰腺为参考,分为强化程度低于、类似、高于正常胰腺组织组;⑦病灶生长方式:分向胃肠道腔内生长、向腔外生长、向腔内外生长;⑧病灶表面粘膜情况:包括是否完整、强化程度(以周围正常胃肠道粘膜为参考);⑨有无导管征(中央脐凹征)。
2 结 果
2.1 异位胰腺的术前CT诊断25例异位胰腺中,8例术前CT诊断正确;8例诊断为间质瘤;2例诊断为胃窦癌;7例漏诊,其中2例回肠异位胰腺者合并肠套叠,1例胃异位胰腺者合并十二指肠间质瘤,1例空肠异位胰腺者合并结肠癌,余3例漏诊患者中2例发生在十二指肠,1例发生在空肠。
2.2 异位胰腺的发生部位本组25例均为单发病灶。位于胃部9例(36%),其中胃窦7例,胃小弯2例;位于十二指肠9例(36%),其中球部6例,降段3例;位于空肠5例(20%);位于回肠2例(8%)。其中位于黏膜下层及肌层11例(44%);位于黏膜下层7例(28%);位于肌层4例(16%);位于黏膜及黏膜下层2例(8%);位于黏膜下、肌层及浆膜层1例(4%)。
2.3 异位胰腺病灶大小及形态病灶长径(LD)为6mm~25mm,平均15.82±6.42mm;短径(SD)为5mm~25mm,平均(12.00±5.39) mm;LD/SD为1~2.38,平均1.40±0.42。其中胃病灶LD/SD平均为1.67±0.45;LD/SD>1.4的有7例(78%);十二指肠病灶LD/SD平均为1.58±0.32;LD/SD>1.4的有5例(55%);空回肠病灶LD/SD均为1.0。20例(80%)病灶向腔内生长,5例(20%)向腔内外生长,22例(88%)长轴平行于胃肠道壁。15例(60%)为类圆形,4例为圆形,4例呈不规则形,2例表现为胃壁局部增厚。边界不清楚的18例(72%),边界清楚的7例(28%)。
2.4 异位胰腺的CT动态增强特征25例病灶CT平扫时密度均匀,20例(80%)密度与胰腺组织相仿,5例密度低于正常胰腺组织,病灶内部均未出现出血、坏死、钙化。增强扫描时21例(82%)病灶均匀强化,2例病灶内出现小斑片状低密度影(如图1),2例病灶内出现管状低密度影(如图2)。增强扫描病灶均呈持续性强化,类似于正常胰腺组织的强化方式;强化程度与正常的胰腺组织相似者13例(52%)(如图3),病灶强化程度高于正常胰腺组织者6例(如图4),低于正常胰腺者6例。9例胃异位胰腺及3例十二指肠异位胰腺表面覆盖的黏膜完整连续,增强扫描时明显强化;余6例十二指肠异位胰腺及7例空回肠异位胰腺表面黏膜均显示不清。
2.5 异位胰腺并发的疾病25例患者中,合并胃癌的2例,肠癌1例,壶腹癌1例,胰腺神经内分泌肿瘤1例,十二指肠间质瘤1例;合并有胃炎、息肉、溃疡的共18例(72%),其中慢性浅表性胃炎13例(52%);发生回肠的2例患者均合并肠套叠(如图5)。
2.6 异位胰腺的治疗及随访所有患者均行外科手术切除术,术后通过电话或门诊复查随访4个月-51个月,平均(29.6±5.6)月,均无复发或死亡者。
3 讨 论
异位胰腺是一种先天异常,发病机理不明,普遍认为是胚胎发育过程中胰腺组织异常迁移所致,可发生于任何年龄,以40岁~60岁常见[1]。异位胰腺可出现在腹腔的任何部位,以胃及十二指肠最多,其次是空肠,偶见于肺部,纵隔或胆囊等部位[1,2,6,7]。胃异位胰腺多发生在胃窦、其次为胃小弯处,最常见的部位是位于距幽门1厘米~6厘米的胃窦大弯侧,本组病例中9例位于胃部,其中7例位于胃窦,2例位于胃小弯,与文献报道相符。十二指肠异位胰腺主要位于乏特氏(Vater)乳头以上,尤以十二指肠球部较多见;本组病例中有9例位于十二指肠;其中6例位于球部,3例位于降段[8]。病灶绝大多数起源于黏膜下层,少数起源于固有肌层或黏膜层[9,10],本组病例累及黏膜下的有21例(84%),其中累及黏膜下层及肌层的有11例(44%)。
异位胰腺临床缺乏特异性,其临床表现与病灶的解剖部位、大小、黏膜受累情况及并发症有关,与病灶的功能状态也有一定的关系[3,11]。如位于胃窦部可引起幽门梗阻,位于乏特氏壶腹部可引起胆道梗阻,位于肠道可引起肠梗阻或肠套叠等。本组病例中有2例发生于回肠的异位胰腺,均引起肠套叠,可能是因为长期的压迫及局部分泌刺激导致相应肠壁血运不佳出现动力异常而引发肠套叠。异位胰腺常并发有浅表性胃炎、萎缩性胃炎、胃溃疡、胃(肠)癌、糜烂及胃息肉,其中以浅表性胃炎为多,可能与胰腺异位导致消化道壁结构异常有关,其本身压迫导致黏膜萎缩,分泌蛋白酶和碱性胰液刺激、破坏局部组织和血管[12]。本组病例合并胃(肠)癌的有3例;有18例(72%)合并了胃炎、溃疡或息肉,其中有13例(52%)是浅表性胃炎。
异位胰腺常单个分布,偶见多个,质韧,直径常在5mm~30mm。本组病例均为单个分布,长径在10mm~20mm之间的有17例(68%)。kim等[7]认为,胃异位胰腺长径/短径(LD/SD)一般大于1.4,这是胃异位胰腺与其他黏膜下病变的鉴别点之一,Wei等[1]报道胃部异位胰腺结节的LD/SD明显大于十二指肠异位胰腺结节。本研究中胃异位胰腺的LD/SD均大于1.4,发生在胃的LD/SD>十二指肠>空回肠,也就是病灶越靠近消化道远端越趋于圆形,可能是由于越靠近消化道远端肠壁紧张性越低,蠕动更频繁,使得异位胰腺结节更小更圆。
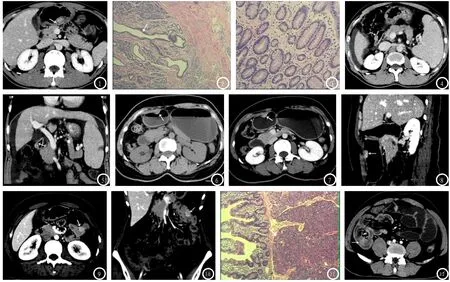
图1-3 胃异位胰腺。图1为门脉期横断位图。胃窦部小弯侧见一类圆形肿块向腔内突出,宽基底与肠壁相连,长轴平扫与胃壁,强化程度略低于正常胰腺组织,内见斑片状低密度影(箭头),表面黏膜完整、连续。图2病理(HE*100)示病灶内见囊状扩张的导管(箭头)。图3病理(HE*200)病灶以导管为主。图4-5 十二指肠异位胰腺。图4为门脉期横断位图。十二指肠球部见一结节影(箭头)向腔内、外生长,大小约15*12mm,强化程度与正常胰腺组织相仿。图5为门脉期冠状位图。病灶内见一低密度导管征(箭头)。图6-8 胃异位胰腺。图6为横断位平扫图,图7、8分别为门脉期横断位、矢状位图。胃窦部大弯侧见一类圆形软组织灶向腔内突出(箭头),宽基底与胃壁相连,密度均匀,长轴平行于胃壁,平扫密度与正常胰腺组织相似,强化程度与胰腺组织相仿。图9-11 空肠异位胰腺。图9、10分别为门脉期横断位、冠状位图。空肠上段可见一结节影向腔内突出,强化程度高于正常胰腺组织,表面黏膜完整、连续,明显强化(箭头)。图11病理(HE*100)示空肠黏膜下见胰腺组织影,以腺泡为主(箭头)。图12 回肠异位胰腺并肠套叠。横断位CT增强示回肠末端可见同心圆状肠套叠影,套叠肠壁可见一结节影向腔内突出(箭头),大小约21*21mm。
异位胰腺CT平扫多表现为类圆形,密度均匀,与正常胰腺组织密度相似,边界多不清楚,与胃肠道壁呈宽基底相接,多向腔内生长,长轴平行于胃肠道壁。增强扫描时病灶强化方式类似于正常胰腺组织,呈持续性强化。病灶的强化程度则与其病理组成密切相关[13],Gaspar Fuentes于1973年按构成比例的不同将异位胰腺分为4型[14]:Ⅰ型具有完整结构的腺泡、导管和胰岛成分;Ⅱ型仅有胰管构成;Ⅲ型由腺泡组织构成(外分泌型);Ⅳ型由胰岛细胞构成(内分泌型)。实际上,异位胰腺不是由单一细胞组织,而是由不同比例的腺泡、导管及胰岛细胞多种成分混合组成[15],以腺泡为主要成分者强化显著,高于正常胰腺;以导管为主要成分者,强化明显弱于正常胰腺,甚至弱于背部肌肉组织;腺泡、导管混合型者其强化程度接近正常胰腺组织。本研究中有13例病灶强化程度与正常胰腺相似,病理为腺泡、导管混在构成;强化程度高于正常胰腺组织的6例病灶以腺泡为主要成分;6例强化程度低于正常胰腺组织的病灶病理则以导管为主。Cho等[16]认为,CT增强,尤其是门脉期时,能较好的显示黏膜下型的胃异位胰腺覆盖有完整的黏膜。本组病例中,有12例(其中胃9例,十二指肠3例)在门脉期可见病灶内侧面黏膜完整并明显强化,十二指肠、空回肠病灶表面黏膜的显示率不高,可能是由于小肠难以完全舒张、充盈良好,容易产生伪影而导致观察不清。消化道异位胰腺内部可发生囊状改变,可能是因为异位胰腺合并慢性胰腺炎假性囊肿形成,也可能是起源于导管上皮的小囊肿内衬有分泌功能的上皮,或导管的异常扩张而发生囊状改变。本组病例中,有2例可见小囊状影,2例可见扩张导管影,术后病理证实均为扩张的小导管(如图1、2)。
疑为该病的患者行消化道造影检查对异位胰腺诊断有帮助,主要表现为圆形充盈缺损,其中央存留钡剂呈脐状凹陷,称为导管征或中央脐凹征[3],这是异位胰腺中央导管的出口,Hazzan等[17]认为导管征或中央脐凹征是异位胰腺的特点,看到此征象可以诊断为异位胰腺,但这种特点很难在<1.5cm的病灶中发现,CT检查中,此征象的显示率并不高。本组仅有2例出现导管征(如图2),可能与本组研究中导管为主型的病例较少有关。
异位胰腺的误诊、漏诊率较高,需与间质瘤、胃肠癌、平滑肌瘤等鉴别。间质瘤多位于胃底、胃体,腔外生长多见,当病灶较小时,边界多清晰,较大者多合并钙化、坏死、出血、囊变,强化不均匀。胃肠癌起自黏膜层,黏膜破坏、中断,胃肠壁僵硬,病灶密度不均匀,轻中度强化,可发生淋巴结及远处转移。平滑肌瘤多位于胃贲门部,强化程度较异位胰腺低,可有带蒂表现。本组漏诊的异位胰腺中,4例合并其他疾病,均以单一疾病考虑而被漏掉。3例发生在小肠的病灶,体积较小,再加上肠腔舒张不良,肠道充盈欠佳,肠壁观察欠清,误以为肠道蠕动局部增厚,故怀疑胃肠道病变时,应胃肠道充分准备后再进行MDCT检查。
综上所述,消化道异位胰腺CT表现有一定的特征性,当典型部位(胃窦、胃小弯、十二指肠乳头以上)发现小于3cm的类圆形软组织肿块,位于黏膜下,表面的黏膜层完整,长轴与胃肠壁平行,宽基底与胃肠壁相连,强化程度及方式与胰腺相似时,需想到异位胰腺的可能,当病灶内见导管征或中央脐凹征时,更增加诊断此病的信心,但最终确诊仍需病理证实。
1. Wei R, Wang Q, Chen Q, et al. Upper gastrointestinal tract heterotopic pancreas: findings from CT and endoscopic imaging with histopathologic correlation[J]. Clinical Imaging,2011,35(5):353-359.
2. Attwell A, Sams S, Fukami N.Diagnosis of ectopic pancreas by endoscopic ultrasound with fine-needle aspiration[J]. World J Gastroenterol,2015,21(8):2367-2373.
3. 周太成,陈双,赖东明,等.异位胰腺的临床认识进展[J].解剖与临床,2007,12(1):62-64.
4. 代鸿,黄秀川,李涛.20例异位胰腺的诊断和治疗[J].内分泌外科杂志,2008,2(5):304-307.
5. Margolin DJ.Endoscopya s s i s t e d l a p a r o s c o p i c r e s e c t i o n o f g a s t r i c heterotopic pancreas[J].Am Surg,2008,74(9):829-831.
6. Kung JW,Brown A, Kruskal JB, et al. Heterotopic pancreas: typical and atypical imaging findings[J].Clinical Radiology,2010,65(5):403-407.
7. Kim JY, Lee JM, Kim KW, et al. Ectopic pancreas: CT findings with emphasis on differentiation from small gastrointestinal stromal tumor and leiomyoma[J]. Radiology,2009,252(1):92-100.
8. 窦丽娜,徐青.消化道异位胰腺CT表现(附6例报告及文献复习)[J].临床放射学杂志,2012,31(12):1752-1754.
9. 屠霖,徐佳,曹晖.异位胰腺误诊为胃肠间质瘤的临床分析[J].中华胃肠外科杂志,2014(4):348-351.
10.Mulholland KC, Wallace WD, Epanomeritakis E,et al. Pseudocyst formation in gastric ectopic pancreas[J].Journal of the pancreas,2004,5(6):498-501. 11.杜龙龙,姚庆东,殷薇薇,等.消化道异位胰腺的CT误诊分析[J].实用放射学杂志,2012,28(12):1910-1913.
12.赵苏苏,余泽前,王剑蓉,等.异位胰腺的临床特点及病理特征:附36例报告[J].中国普通外科杂志,2013,22(3):337-339.
13.王倩,杨学华,高剑波,等.异位胰腺的CT表现与病理联系[J].实用放射学杂志,2014(5):815-817.
14.Gaspar Fuentes A, Campos Tarrech J M, Fernandez Burgi J L,et al. Pancreatic ectopias[J]. Rev Esp Enferm Apar Dig,1973,39(3):255-268.
15.郭宁,张劲松,袁怀平,等.胃部异位胰腺MSCT表现[J].实用放射学杂志, 2014,30(9):1486-1489.
16.Cho J, Shin K, Kwon S, et al. Heterotopic Pancreas in the Stomach: CT Findings1[J]. Radiology,2000,217(1):139.
17.Hazzan D,Peer G,Shiloni E.Symptomatic heterotopic pancreas of stomach[J]. Isr Med Assoc J,2002,4(5):388-389.
(本文编辑: 汪兵)
Multi-detector Row Computed Tomography Features of Ectopic Pancreas in the Gastrointestinal Tract
CHEN Xiu-zhen, HUANG Wen-sou, CHEN Jian-ning, et al., Department of Radiology, the Third Affiliated Hospital of Sun Yat-sen University, Guangzhou 510630, China
ObjectiveTo analyze the multi-detector computed tomography (MDCT) features of ectopic pancreas in the gastrointestinal tract in order to improve the diagnostic accuracy of the disease.MethodsCT findings were reviewed retrospectively in 25 cases with ectopic pancreas confirmed by surgery and pathology.All patients underwent plain CT, contrast-enhanced scanning with three phases and three dimensional reconstruction.Analyze the location, size, the long diameter (LD)/the short diameter(SD), shape, attenuation, contrast-enhancement pattern and grade of the lesions, growth pattern, border, as well as enhancement of the overlying mucosa.ResultsAll 25 cases were of single lesion.9cases were in the gastric.9 cases were in the duodenum, 5 cases were in the jejunum, 2 cases were in the ileum. The max axes ranged from 6-25mm, 7 cases the LD/SD ratio is greater than 1.4 in gastric ectopic pancreas, 5 cases the LD/SD ratio is greater than 1.4 in duodenum. the LD/SD ratio of the jejunum and ileum lesion is 1.0.15 cases were ovoid in shape, 4 cases were sphere, 4 cases were irregular shape, 2 cases were manifested as Localized thickening of the gastrointestinalwall. 11cases were located in the submucosa and muscularis.The ectopic pancreas was continuously enhanced in all cases,The contrast enhancement grade was similar to that of the normal pancreatic tissue in 13 cases. 2 case showed central duct sign. 20 cases were endoluminal growth pattern.ConclusionGastrointestinal tract ectopic pancreas has certian MDCT charateristics. It can help us to improve the diagnostic ability of the disease to familiar with these features.
Ectopic Pancreas; Gastrointestinal Tract; Tomography; X-ray Computed
R322.4+91
A
10.3969/j.issn.1672-5131.2015.07.019
2015-05-28
朱康顺

