钡离子对镍基钙钛矿分解氨的影响
陈为强,丁彤,马智,谢洪燕
(天津大学化工学院,天津 300072)
新能源的开发已经成为世界各国普遍关注的问题之一,氢能[1]以无污染、可重复利用、燃烧值高等优点而成为人们的首选。目前工业上制氢主要以烃类重整[2-3]、电解水制氢[4-5]、甲醇制氢[6-7]和氨分解法[8]为主。烃类重整制备的氢气含有COx,极易造成催化剂中毒,脱除非常困难;电解水制氢是一种比较成熟的工艺,但能耗太高;甲醇制氢原料丰富,能耗较低,产生COx易使催化剂中毒;氨分解法产生氢气纯度高,无有毒副产物,工艺简单,成本低廉,适合中小型制氢。
目前,氨分解催化剂的活性成分主要是以贵金属(Ru[9]、Ir、Pt 等)和过渡金属(Fe、Ni[10-11]、Co、Mo 等)[12]为主,助剂主要是碱金属、碱土金属和贵金属,其中K[13]、Ba 和Cs 都是氨催化分解催化剂的最理想助剂。倪平等[14]研究了Ba 修饰的Ir/SiO2负载型催化剂(Ba-Ir/SiO2)在氨催化分解反应的作用,结果表明,随着Ba 添加量的增加,氨分解的活性呈先增加后减小的趋势,w(Ba)=10%时,催化剂转化率最高,可达到84%。
LaNiO3因为具有钙钛矿(ABO3)型结构,有良好的氧化还原活性,价格低廉以及高热稳定性,对氨分解反应有很好的催化活性。因对于钙钛矿ABO3,容忍因子t 与离子半径之间的关系可表达为t=(RA+RX)/[ 2(RB+RX)],容忍因子一般介于0.78~1.05 之间。对于LaNiO3,掺杂阳离子而不改变它的钙钛矿结构,A 位掺杂的离子半径为76~138nm。钡离子半径为135nm,在容忍范围之内。
本文研究了Ba 改性的LaNiO3催化剂在氨催化分解中的催化活性和结构变化,并应用XRD、SEM、TEM 进行表征。
1 实验部分
1.1 仪器与试剂
La(NO3)2·6H2O,Ba(NO3)2·3H2O,Ni(NO3)2·6H2O,柠檬酸,C2H5OH,SiO2,MCM-41 等均为分析纯。Panalytical 公司的X′Pert Pro 型X 射线衍射仪,辐射源为CoKα;PHILIPS XL-30 ESEM;荷兰菲利普FEI 公司的Tecnai G2 F20 场发射电子显微镜;SC-200 型气相色谱仪(GC,色谱柱为GDX-401)。
1.2 催化剂的的制备
首先,称取一定质量的硝酸镧、硝酸钡、硝酸镍、柠檬酸固体粉末分别置于不同的烧杯中,加入适量蒸馏水,搅拌至完全溶解。将硝酸镍、硝酸镧和硝酸钡溶液分别倒入大烧杯中混合并不断搅拌15min,之后将柠檬酸溶液倒入并搅拌,在超声波发生器中超声10min 使溶液均匀混合。将载体加入到混合溶液中,搅拌,在红外灯照射下直至干燥爆燃。第二,将此固体粉末放入烘箱中于110℃干燥2h,进一步脱去其中的水分,将粉末移至坩埚并在400℃下预煅烧2h,以分解柠檬酸及硝酸盐,取出压片成形,在800℃的温度下煅烧8h。最后将制得的催化剂样品破碎过筛,取20~40 目颗粒样品进行活性评价。
制得催化剂分别为La1-xBaxNiO3为掺杂Ba 量为x 的镧系镍基钙钛矿。
La0.9Ba0.1NiO3/MCM-41 为掺杂钡量为0.1,载体为MCM-41 的镧系镍基钙钛矿。
1.3 催化剂的活性评价
催化剂活性评价在常压固定床石英管反应器中进行。在300~800℃范围内对氨分解反应进行了催化剂活性测试。反应器内径8mm,催化剂装填量为1.0mL,空速10000mL/h·mLcat,原料气为纯氨。反应产物用102G 气相色谱仪分析(GDX-401 色谱柱60~80 目,热导检测器,柱温50℃,热导80℃,H2载气,稳压0.01MPa),尾气用稀硫酸溶液吸收,然后经过湿式气体流量计后放空。
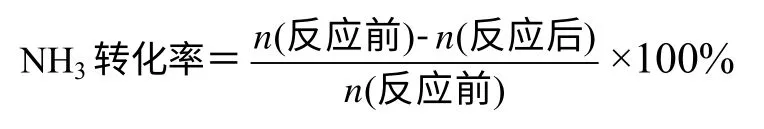
1.4 催化剂的表征
1.4.1 XRD 表征结果与讨论
图1 为La1-xBaxNiO3(x=0.05~0.5)样品的XRD图,从图中可以看出,当x=0.05 时,衍射峰跟LaNiO3相似,只在35°~37°有峰强较小的杂峰,为BaNiO2.36,当x 增大到0.1 时,杂峰衍射强度增强,当x 增大到0.2 时,在35°~39°有两个很强的衍射峰,分别为产生Ba3Ni3O8和BaNiO2杂相,当x增大到0.5 时,在35°~39°、50°~52°、68°~69°有较强的衍射峰,为NiLa2O4的峰特征,27°~28°衍射峰为不明物相。
随着x 增大,引起衍射峰的变化,表明用Ba2+部分代替La3+引起杂相[15]产生;从结构上看,x=0.05~0.1 时催化剂结构近于LaNiO3,为钙钛矿结构;x=0.2 时催化剂的结构LaNiO3有很大不同;x=0.5 时,因为有大量的NiLa2O4,则不是钙钛矿 结构。
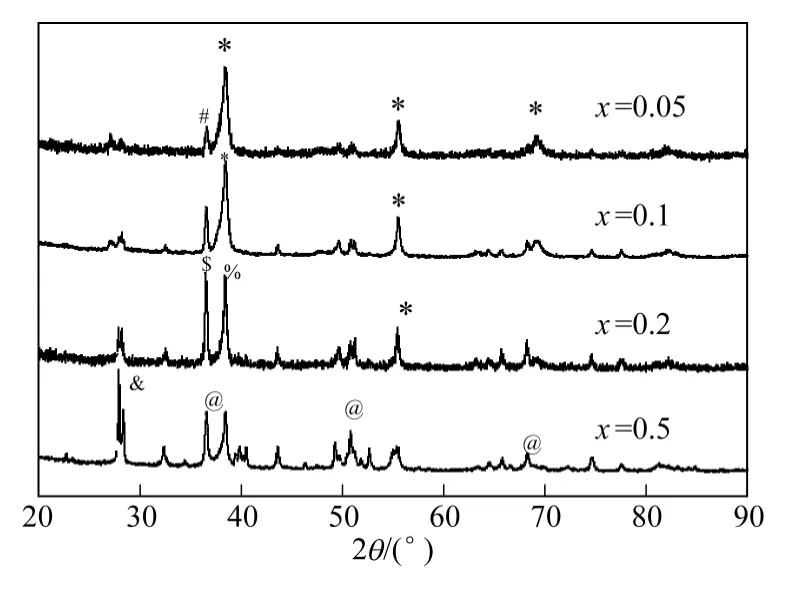
图1 La1-xBaxNiO3 样品的XRD 图
1.4.2 SEM 表征结果与讨论
样品La0.9Ba0.1NiO3/MCM-41 的扫描电镜形貌如图2 所示,可以看到La0.9Ba0.1NiO3/MCM-41 的颗粒较大,约5μm,成片状,表面结构致密,灰白成管状的为载体 MCM-41,深色部分为活性组分La0.9Ba0.1NiO3。因为载体可使活性组分分散在载体表面上,获得较高的比表面积,提高单位质量活性组分的催化效率。因此反应过程中在样品表面的活性组分接触比表面积较大,利于其与NH3反应。
1.4.3 TEM 表征结果与讨论
La0.9Ba0.1NiO3/MCM-41 的透射电镜图如图3 所示,浅灰色有规整介孔结构的为载体MCM-41,黑色为活性组分,可以看到,溶胶凝胶法制备的该催化剂仍保留了规整的介孔结构,钙钛矿颗粒均匀的分散在载体MCM-41 上,粒径只有3~7nm,有利于NH3和活性组分更好地接触,从而有利于催化反 应的进行,因此该催化剂具有很好的催化活性。

图2 La0.9Ba0.1NiO3/MCM-41SEM 电镜图

图3 La0.9Ba0.1NiO3/MCM-41 的透射电镜图
2 结果讨论
2.1 添加电子助剂对催化剂分解氨的活性影响
从图4 可以看出,通过掺杂电子助剂Li、Na、K、Ba 以及不掺杂,发现5 种催化剂对氨分解程度差别比较明显是在450℃,其中掺杂Ba 分解率为7.6%,另外4种差别不大,有明显差别的是在540℃,依次为 La0.9Ba0.1NiO3(85.58%)、La0.9Li0.1NiO3(63.86%)、La0.9K0.1NiO3(50.5%)、La0.9Na0.1NiO3(43.37%)、LaNiO3(42.5%),完全分解温度,掺杂La0.9Ba0.1NiO3为650℃,其他4 种催化剂均大于700℃。可知Li、Na、K、Ba 均能促进氨分解,但是Ba 为最好的电子助剂。
2.2 钡离子掺杂量对催化剂分解氨的活性影响
通过改变钡离子的掺杂量发现(图5),在400℃之前氨的分解率低,5 种催化剂差别不大,随着温度升高催化剂的催化活性提高,在540℃时,催化剂的氨分解率相差最大,其中x=0.1 时,氨分解率为85.58%,x=0.05 为75.3%,x=0.7 为63.3%,x=0.3为55.07%,x=0.5 为41.74%。可以看出催化剂催化分解氨随着钡掺杂量先升高后降低,La1-xBaxNiO3当x=0.1 时,即在La0.9Ba0.1NiO3时催化剂活性最高。

图4 添加不同电子助剂的催化剂分解氨的活性
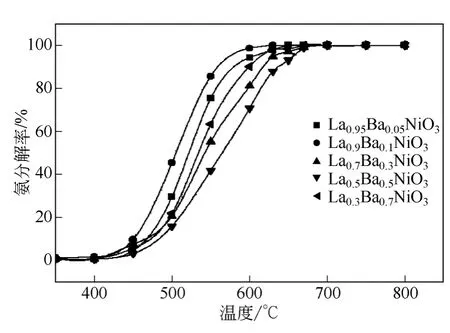
图5 不同掺杂量的钡离子催化剂分解氨活性
2.3 钡离子掺杂量对催化剂结构的影响
根据XRD 分析可以看出,La1-xBaxNiO3中,随着x 增大,催化剂的结构发生变化,在x=0.05 为钙钛矿结构,随着x 增大到0.5 时,催化剂为非钙钛矿结构。在催化剂催化分解氨时钙钛矿结构的催化性能比非钙钛矿高。
2.4 不同载体对催化剂分解氨的活性影响
LaNiO3负载于SiO2比另两种常见载体Al2O3、MgO 有更高的催化活性[17]。对于两种结构的SiO2,即普通结构SiO2和介孔分子筛结构MCM-41[16],La0.9Ba0.1NiO3在两者为载体上对氨分解反应催化性能的影响如图6。由图6 可知,以MCM-41 为载体的催化剂,无论在低温区(350~500℃)还是高温区(500~800℃),催化活性都高于LaNiO3/SiO2和LaNiO3,氨在350℃时开始分解,500℃时氨转化率达86.85%,在575℃时氨完全分解。而LaNiO3/SiO2催化剂氨在400℃时才开始分解,500℃时氨转化率仅为40.2%,在646℃时氨才完全分解。由此可以得到,在氨分解反应中,MCM-41 比SiO2更有利于提高LaNiO3的催化活性,是一种很好的催化剂 载体。

图6 不同载体对催化剂分解氨活性
3 结 论
以柠檬酸为络合剂,采用溶胶凝胶法合成催化剂,通过掺杂Li、Na、K、Ba 改变掺杂量和载体,比较完全分解氨制氢的温度,发现最好的掺杂离子为钡离子,最佳掺杂量为x=0.1,并且发现最好的载体为MCM-41,该催化剂使氨完全分解温度由650℃降为575℃。通过XRD 表征发现,随着Ba含量的增加,催化剂的结构发生变化,从x=0.05、0.1 的基本钙钛矿结构到x=0.5 的含有大量杂相的非钙钛矿结构。钙钛矿结构的氨完全分解的温度比非钙钛矿的较低,证明钙钛矿晶型结构有利于降低分解氨的温度。
[1] 张聪. 世界氢能技术研究和应用新进展[J]. 新能源,2014(8):54-59.
[2] 张云洁,李金英. 天然气制氢工艺现状及发展[J]. 广州化工,2012,40(13):41-42.
[3] 陈恒志,郭正奎. 天然气制氢反应器的研究进展[J]. 化工进展,2012,31(1):10-18.
[4] 于娇娇,苏伟,孙艳. 水制氢技术研究进展[J]. 化学工业与工程,2012,29(5):58-63.
[5] 楚婷婷,王慧,冯彩霞,等. 可见光分解水制氢催化剂研究进展[J]. 化工进展,2012,31(10):2228-2233.
[6] 都学敏,党政,张智峰,等. 甲醇水溶液超声波制氢实验研究[J]. 化工学报,2011,62(6):1669-1674.
[7] 闫月君,刘启斌,隋军,等. 甲醇水蒸气催化重整制氢技术研究进展[J]. 化工进展,2012,31(7):1468-1476.
[8] 苏玉蕾,王少波. 氨分解制氢技术[J]. 舰船防化,2009(6):6-9.
[9] Chen Jiuling,Zhu Zhonghua,Wang Shaobin. Effects of nitrogen doping on the structure of carbon nanotubes (CNTs) and activity of Ru/CNTs in ammonia decomposition[J]. Chemical Engineering Journal,2010,156(2):404-410.
[10] Zheng Weiqing,Zhang Jian,Ge Qingjie. Effects of CeO2addition on Ni/Al2O3catalysts for the reaction of ammonia decomposition to hydrogen[J]. Applied Catalysis B:Environmental,2008,80 (2) :98-105.
[11] Cao Jian-Liang,Yan Zhao-Li,Deng Qing-Fang. Mesoporous modified-red-mud supported Ni catalysts for ammonia decomposition to hydrogen[J]. International Journal of Hydrogen Energy,2014,39(11):5747-5755.
[12] 倪平,储伟,王立楠,等.氨催化分解制备无COx的氢气催化剂研究进展[J].化工进展,2006,25(7):739-743.
[13] Yin Shuang-Feng,Xu Bo-Qing,Wang Shui-Ju. Nanosized Ru on high-surface-area superbasic ZrO2-KOH for efficient generation of hydrogen via ammonia decomposition[J]. Applied Catalysis A:General,2006,301(2):202-210.
[14] 倪平,储伟,罗仕忠,等.钡修饰Ir/SiO2催化剂对氨分解促进作用的研究[J].合成化学,2007,15(4):407-411.
[15] 亓淑艳,冯静. K+掺杂对钙钛矿氧化物 La0.7Sr0.3-xKxMnO3(0.05≤x≤0.3)的结构及磁性的影响[J]. 应用化学,2008,25(7):825-828.
[16] Huang Ruihuan , Lan Bingyan , Chen Zhongying. Catalytic ozonation of p-chlorobenzoic acid over MCM-41 and Fe loaded MCM-41[J]. Chemical Engineering Journal,2012,180 :19-24.
[17] Choudhary T V,Sivadinarayana C,Goodman D W. Catalytic ammonia decomposition:COx-free hydrogen production for fuel cell applications[J]. Catalysis Letters,2001,72(3-4):197-201.

