吉西他滨联合顺铂对Ⅲ期乳腺癌患者ER、MMP-9及雌激素影响研究
曲靓靓,王晶,王芳
(1.辽宁医学院附属第一医院 肿瘤科,辽宁 锦州 121000;2.辽宁省锦州市中心医院 妇产科,辽宁 锦州 121000;3.辽河石油勘探局康复医院 康复一科,辽宁 葫芦岛 125100)
吉西他滨联合顺铂对Ⅲ期乳腺癌患者ER、MMP-9及雌激素影响研究
曲靓靓1Δ,王晶2,王芳3
(1.辽宁医学院附属第一医院 肿瘤科,辽宁 锦州 121000;2.辽宁省锦州市中心医院 妇产科,辽宁 锦州 121000;3.辽河石油勘探局康复医院 康复一科,辽宁 葫芦岛 125100)
目的 探究吉西他滨联合顺铂对Ⅲ期乳腺癌患者雌激素受体(estrogen receptor,ER)、基质金属蛋白酶(matrix metalloprotein,MMP)及雌激素影响。方法 收集辽宁医学院附属第一医院肿瘤科收治的乳腺癌患者93例,根据随机对照表分为对照组和试验组。2组患者均实施乳腺癌手术,术后对照组采用顺铂化疗方案,第一天静脉滴注顺铂90 mg/m2,21 d为1个疗程,连续用药6个疗程;试验组采用顺铂联合吉西他滨化疗,第1天和第8天静脉滴注1000 mg/m2吉西他滨,第3~5天静脉滴注顺铂90 mg/m2,每28天为1个周期,连续用药2周期,治疗结束后对比分析2组临床疗效及雌激素受体(estrogen receptor,ER)、MMP-9、雌激素水平、不良反应发生率。 结果 与治疗前比较,治疗后2组患者血清ER、MMP-9、雌酮(estrone,E1)、雌二醇(estradiol,E2)水平降低(P<0.05),FSH、LH水平升高(P<0.05);与对照组治疗后比较,试验组患者的血清ER、MMP-9、E1、E2水平较低(P<0.05),FSH、LH水平较高(P<0.05);试验组不良反应发生率为6.38%,对照组为15.22%,2组不良反应发生率比较差异无统计学意义。结论 吉西他滨联合顺铂对Ⅲ期乳腺癌患者疗效显著,可改善临床症状,并能显著降低患者血清ER、MMP-9、E1、E2水平、提高FSH、LH水平。
吉西他滨;顺铂;Ⅲ期乳腺癌患者;ER;MMP-9;雌激素
乳腺癌是女性最常见的恶性肿瘤之一,好发于40~60岁的女性[1],发病机制为乳腺上皮细胞在多种致癌因子作用下,发生基因突变,致使细胞增生失控,乳房腺上皮细胞的多种致癌因子诱导基因突变[2],无限增殖的癌细胞侵蚀正常组织,破坏乳房结构,患者出现乳腺肿块、乳腺疼痛、乳头溢液等主要症状。Ⅲ期乳腺癌患者癌肿增多超过5 cm,周围存在广泛粘连,免疫治疗是继传统化疗、放疗、内分泌治疗等非手术治疗之后的乳腺癌重要治疗方法[3],但大部分Ⅲ期乳腺癌患者仍出现复发以及转移,需要进行化疗、放疗和手术等二次治疗,令患者痛苦难忍。有研究显示[4],吉西他滨联合顺铂对复发转移性乳腺癌疗效较好,本研究选取93例Ⅲ期乳腺癌患者,探讨吉西他滨联合顺铂对Ⅲ期乳腺癌患者ER、MMP-9及雌激素影响。
1 资料与方法
1.1 一般资料 收集2013年11月~2015年8月肿瘤科收治的乳腺癌患者93例,均为女性患者,按国际抗癌协会TNM临床分期均属于Ⅲ期,年龄23~45岁,平均年龄(33.74±3.76)岁,其中38例导管癌,35例浸润性导管癌,11例浸润性小叶癌,9例未分化癌。采用随机数字分配法,随机分配为试验组与对照组,其中试验组47例,年龄26~45岁,平均年龄(34.85±4.22)岁;对照组46例,年龄23~41岁,平均年龄(33.58±3.85)岁,2组患者年龄、体重、病程、病理类型以及病情等一般资料差异无统计学意义。本实验经本院医学伦理协会批准,全程跟踪随访。
纳入标准:①诊断符合《中国进展期乳腺癌共识指南》[5]中Ⅲ期乳腺癌的诊断标准具备以下临床特点:乳房内肿块Ⅲ度硬度、乳腺疼痛、乳头溢液、乳头改变、皮肤改变、腋窝淋巴结肿大等症状;②X线检查显示肿块、结节病变、钙化影以及皮肤增厚征群,导管影改变,超声显像检查显示癌肿向周围侵润形成回声带,皮肤增厚或凹陷;③CT检查、肿瘤标志物、组织活检等实验室检查均确诊为乳腺癌Ⅲ期;④患者自愿参与本实验,并签署知情同意书。排除标准:①药物过敏史,接受免疫抑制剂治疗的患者,乙肝、艾滋病等严重传染性疾病患者;②严重呼吸循环系统、慢性消化系统疾病以及严重心、肝、肾等多脏器功能障碍或衰竭;③恶性肿瘤、癫痫等神经系统疾病。
1.2 方法
1.2.1 治疗方法:2组患者均实施乳腺癌手术,根据患者病情选择手术方式,术前维持麻醉,术中心率、血压、动脉血氧饱和度等均保持正常范围,呼气末二氧化碳分压维持在30~35 mmHg。术中1 h进行清扫腋窝淋巴结,手术缝合皮肤停止用药,术后给予肌松拮抗剂,诱导患者恢复意识和自主呼吸,拔除气管插管。术后对照组采用顺铂(云南生物谷药业股份有限公司,国药准字H20043888)化疗方案,第一天静脉滴注顺铂90 mg/m2,21 d为1个疗程,连续用药6个疗程。试验组应用顺铂联合吉西他滨化疗,第1天和第8天静脉滴注1000 mg/m2吉西他滨,第3~5天静脉滴注顺铂90 mg/m2,每28天为1周期,连续用药2周期,化疗前给予地塞米松和5羟色胺受体阻断剂预防消化道反应。
1.2.2 观察指标
① 疗效评定标准:根据世界卫生组织推荐《实体瘤疗效评价标准》[6],疗效评定标准如下,治疗结束后病灶完全消失,乳腺疼痛、乳头溢液、皮肤凹陷、腋窝淋巴结肿大等临床症状和体征完全消失为显效;最大径之和缩小≥30%,临床症状和体征明显改善为有效;头颅CT或MRI发现新病灶,临床症状和体征无改善或加重,最大径之和缩小不足30%或增大为无效。记录并分析总有效率,总有效率=[(显效例数+有效例数)/本组患者例数]×100%。
② 2组患者ER、MMP-9、雌激素水平检测:于患者治疗前后采取空腹外周静脉血3 mL,置于无菌无抗凝管内,静置30 min,3000 r/min离心15 min,取上清液,收集其血清标本于-70 ℃冰柜内冷冻保存。实验时,取出并进行解冻,采用日本日立7170全自动生化仪,实施ELISA法检测雌激素受体(estrogen receptor,ER)水平,实施双抗体夹心(ELISA)法检测患者血清基质金属蛋白酶-9(MMP-9)水平,实施放射免疫检测技术(ELISA)法检测患者血清雌酮(estrone,E1)、雌二醇(estradiol,E2)、促卵泡生成素(follicle stimulating hormone ,FSH)与促黄体生成素(luteinizing hormone,LH)水平。

2 结果
2.1 2组患者治疗后疗效比较 与对照组治疗后相比,试验组临床总有效率较高(χ2=4.18,P<0.05)。见表1。
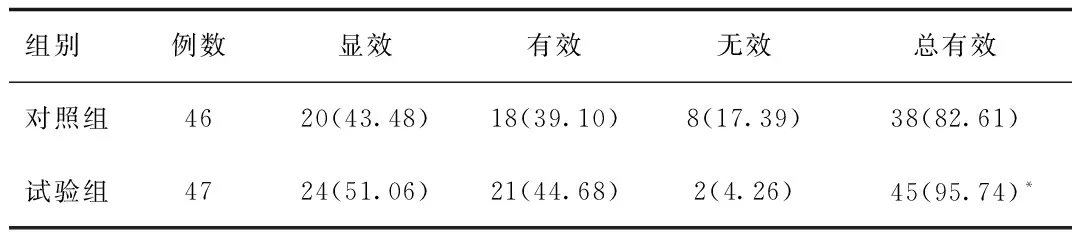
表1 2组患者治疗后疗效比较[n(%)]Tab.1 Comparison of clinical efficacy between two groups post-treatment[n(%)]
*P<0.05,与对照组治疗后比较,compared with control group post-treatment
2.2 2组患者血清ER、MMP-9水平比较 治疗前2组患者血清ER、MMP-9水平比较差异无统计学意义;治疗后2组血清ER、MMP-9水平下降(P<0.05);与对照组治疗后比较,试验组血清ER、MMP-9水平较低(P<0.05)。见表2。

表2 2组患者治疗前后血清ER、MMP-9水平比较Tab.2 Comparison of ER, MMP-9 between two groups pre- and post-treatment ±s)
*P<0.05,与同组治疗前比较,compared with the same group pre-treatment;#P<0.05,与对照组治疗后比较,compared with control group post-treatment
2.3 雌激素水平比较 治疗前2组患者血清E1、E2、FSH、LH水平比较差异无统计学意义;治疗后2组血清E1、E2水平下降(P<0.05),FSH、LH水平上升(P<0.05);与对照组治疗后相比,试验组血清E1、E2水平较低(P<0.05),FSH、LH水平较高(P<0.05)。见表3。
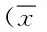
表3 2组患者治疗前后雌激素水平比较 ±s)Tab.3 Comparison of estrogen between two groups pre- and ±s)
*P<0.05,与同组治疗前比较,compared with the same group pre-treatment;#P<0.05,与对照组治疗后比较,compared with control group post-treatment
2.4 安全性评价 试验组出现1例头痛,1例恶心呕吐,1例皮肤色素沉着,总不良反应发生率为6.38%(3/47);对照组出现2例头痛、1例血肌酸酐轻度上升、2例恶心呕吐,2例皮疹,总不良反应发生率为15.22% (7/46) ,2组不良反应比较,差异无统计学意义(χ2=1.89,P>0.05)。
3 讨论
乳腺癌是导致妇女死亡最常见的恶性肿瘤之一,死亡比例占所有妇女癌症的17%,死亡率居女性各类恶性肿瘤的首位[7]。Ⅲ期乳腺癌患者的癌细胞突变并丧失正常细胞功能,癌细胞脱落随着血行转移以及淋巴结等通路转移至全身,使乳腺癌临床治愈越发困难,病情容易反复。本实验针对Ⅲ期乳腺癌患者选取手术治疗联合化疗的方案,控制病情,有效预防癌细胞复发转移,改善患者身体状况,试验组化疗方案本研究选择当今热议的吉西他滨联合顺铂治疗。吉西他滨(dFDC, 2-二氟脱氧胞苷)是一种破坏细胞复制的二氟核苷类抗代谢物抗癌药[8],参与DNA合成和修复过程,对脱氧核苷酸的生成具有影响作用,临床应用于中、晚期非小细胞肺癌的治疗。本研究显示,治疗后与对照组相比,试验组临床总有效率较高,患者出现的不良反应均为一过性可耐受,经对症处理后均恢复。证实吉西他滨联合顺铂对Ⅲ期乳腺癌患者的临床疗效明显优于单用顺铂治疗,有效改善患者的临床症状,安全性高。
雌激素是女性相关的重要内分泌指标,对机体内分泌紊乱,尤其是雌激素分泌过多,孕激素以及黄体酮分泌量降低,诱发的乳腺上皮细胞、纤维组织增生以及乳腺癌变具有诊断作用。ER是诊断和治疗乳腺癌的分子标志和靶点[9],广泛存在于乳腺内,可与激素发生特异性结合,组成雌激素-受体复合物,发挥其生物学效应。曾有研究显示,乳腺增生以及乳腺癌的发生伴随着ER水平的升高[10]。基质金属蛋白酶-9(matrix metalloproteinase- 9, MMP- 9)是Ⅳ型胶原酶糖化形成的促炎蛋白酶,具有降解和重塑细胞外基质的功能,维持细胞外基质的动态平衡,对肿瘤具有监测作用,体内的含量与肿瘤严重程度呈正相关。研究显示,治疗后与对照组相比,试验组血清E1、E2水平较低,FSH、LH水平较高,ER、MMP-9水平较低(P<0.05),证实吉西他滨联合顺铂对Ⅲ期乳腺癌患者显著降低患者血清ER、MMP-9、E1、E2水平、提高FSH、LH水平,抑制癌细胞转移扩散,阻止病情进展。
本实验通过对本院肿瘤科收治的乳腺癌93例患者临床疗效、ER、MMP-9、雌激素、不良反应进行研究,证实了吉西他滨联合顺铂对Ⅲ期乳腺癌患者疗效显著,可改善临床症状,并能显著降低患者血清ER、MMP-9、E1、E2水平、提高FSH、LH水平,适宜临床推广。
[1] 李秋云. Pak1基因在乳腺癌组织中的表达及临床意义[J]. 重庆医学, 2010:646-649.
[2] 周长鑫. 趋化因子受体5及其基因多态性与乳腺浸润性导管癌相关性的研究[D]. 泰安:泰山医学院,2010.
[3] 李荣国, 赵悦, 马晓(综述),等. 乳腺癌免疫治疗的研究进展[J]. 中国普通外科杂志,2013,22(11):1484-1489.
[4] 刘先领,曾惠爱,马芳,等.吉西他滨联合顺铂治疗复发转移性乳腺癌的疗效观察[J]. 肿瘤防治研究, 2011,38(9):1055-1057.
[5] 中国女医师协会临床肿瘤学专业委员会. 中国进展期乳腺癌共识指南(CABC 2015)[J]. 癌症进展, 2015(3):223-245.
[6] 刘秋华, 林榕波. 实体瘤疗效评价标准(RECIST)指南1.1版[C]//第十二届全国临床肿瘤大会暨2009年CSCO学术年会. 2009.
[7] 艾婷, 周军, 陈爱军. 乳腺癌血管生成靶向治疗策略的研究进展[J]. 广东医学, 2013, 34(9):1457-1459.
[8] 张明宛,郭坤元,许晓军. 吉西他滨应用于非霍奇金淋巴瘤的研究进展[J]. 实用医学杂志, 2014,30(16):2680-2682.
[9] 廉馨,史丹,李洪艳. 新型雌激素受体ER-α36与乳腺癌[J]. 中国生物化学与分子生物学报, 2015,31(1):34-37.
[10] 张晓梅,赵陆,刘鹏,等. 乳腺增生和乳腺癌中ER、PR、CerbB-2和P53表达差异的临床意义[J]. 浙江临床医学,2009,11(9):902-905.
(编校:王冬梅)
Effect of gemcitabine combined with cisplatin on ER, MMP-9 and estrogen in patients with stage III breast cancer
QU Liang-liang1Δ, WANG Jing2, WANG Fang3
(1. Department of Oncology, The First Affiliated Hospital of Liaoning Medical University, Jinzhou 121000, China; 2. Department of Obstetrics and Gynecology,Jinzhou Central Hospital of Liaoning Province, Jinzhou121000,China;3.Department of Rehabilitation, Rehabilitation Hospital of Liaohe Petroleum Exploration Bureau, Jinzhou125100,China)
ObjectiveTo explore the effect of gemcitabine combined with cisplatin on ER, MMP-9 and estrogen in patients with stage III breast cancer.Methods93 patients with breast cancer were collected and randomly divided into control group and experimental group.Two groups were all under breast cancer surgery, control group was treated with cisplatin chemotherapy,1st day of intravenous infusion of cisplatin 90 mg/m2, 21 days for a course of treatment, continuous treatment of 6 courses. Experimental group were treated with cisplatin combined with gemcitabine chemotherapy, 1st and 8th days of intravenous infusion of 1000 mg/m2gemcitabine, 3~5d, intravenous drip of cisplatin 90 mg/m2, every 28 days a cycle, continuous administration of 2 cycles,After treatment, the clinical efficacy of the two groups, the level of ER, MMP-9, estrogen and the incidence of adverse reactions were compared.ResultsCompared with before treatment,the levels of serum MMP-9,E1, E2, ER were decreased (P<0.05), and the level of LH and FSH were increased (P<0.05) of two group post-treatment.Compared with control group post-treatment, the levels of serum ER, MMP-9,E1, E2 were lower in experimental group (P<0.05), and the LH and FSH levels were higher (P<0.05).The incidence of adverse reactions of experimental group was 6.38%, and control group was 15.22%, the incidence of adverse reactions in the two groups was no significant difference.ConclusionGemcitabine combined with cisplatin in the treatment of patients with breast cancer has a significant effect, and can improve the clinical symptoms, reduce the serum ER, E1, MMP-9, E2 levels, improve FSH, LH level.
gemcitabine; cisplatin; Ⅲ breast cancer patients; ER; MMP-9; estrogen
曲靓靓,通信作者,女,本科,副主任护师,护士长,研究方向:肿瘤护理,E-mail:1417139@qq.com。
R655.8
A
1005-1678(2015)12-0046-03

