Ni2P/Ti-MCM-41的催化加氢脱硫性能
宋 华, 王紫东, 宋华林, 王 健, 李 锋
(1. 东北石油大学 化学化工学院, 黑龙江 大庆 163318;2. 东北石油大学 石油与天然气化工省重点实验室, 黑龙江 大庆 163318;3. 牡丹江医学院 医学影像学院, 黑龙江 牡丹江 157011)
Ni2P/Ti-MCM-41的催化加氢脱硫性能
宋 华1,2, 王紫东1, 宋华林3, 王 健1, 李 锋1,2
(1. 东北石油大学 化学化工学院, 黑龙江 大庆 163318;2. 东北石油大学 石油与天然气化工省重点实验室, 黑龙江 大庆 163318;3. 牡丹江医学院 医学影像学院, 黑龙江 牡丹江 157011)
以MCM-41和Ti-MCM-41介孔分子筛为载体,低温还原法(400℃)制备了磷化镍催化剂。采用XRD、BET、FT-IR、Py-FT-IR、XPS、CO吸附等手段对催化剂进行了表征。采用固定床反应器,以二苯并噻吩为模型化合物,评价了磷化镍催化剂的加氢脱硫催化性能。结果表明,金属Ti的引入可以增强载体和催化剂的B酸和L酸酸性;金属Ti因其电子助剂的作用,能够促进更细小尺寸的Ni2P活性相的形成。在反应温度340℃、反应压力3.0 MPa、质量空速(MHSV)3.5 h-1、V(H2)/V(Oil)=650的条件下,Ni2P/Ti-MCM-41催化二苯并噻吩加氢脱硫反应的转化率高达99.38%,与相同条件下制备的Ni2P/MCM-41相比,提高了约17百分点。Ni2P/Ti-MCM-41催化剂具有更优的原料处理能力和更佳的催化活性的原因可归结为金属Ti的电子效应、活性相的尺寸和分散度以及催化剂适宜的酸性。
加氢脱硫; 磷化镍; Ti-MCM-41; 二苯并噻吩
环保要求的日益严格,以及原油储量和质量逐渐降低,对生产低硫、超低硫清洁油品技术提出了更高的要求,燃油脱硫技术已逐步转向深度以及超深度脱硫领域[1]。过渡金属磷化物,尤其是Ni2P,不仅具有高的加氢脱硫(HDS)和加氢脱氮(HDN)催化活性和稳定性,又具有耐腐蚀、耐磨、防水等特性,是目前国内外加氢脱硫催化剂研究的热点[2]。非负载型Ni2P催化剂的比表面积较小,分散性差,故需要将Ni2P负载于比表面积较大的载体上。纯硅MCM-41分子筛虽然具有孔分布均匀、比表面积大、利于活性相的分散、吸附能力强、孔径可调等独特性质,但其水热稳定性较差、酸性弱,影响了其在催化剂中的应用。
金属Ti具有可交换性及价态可变性的特点,将其引入分子筛骨架后,可增加分子筛中的晶格缺陷数量,提高了分子筛的氧化还原能力[3];还可使分子筛骨架中的羟基活化,并产生L酸性中心,明显改善其表面酸性。此外,Song等[4]研究表明,金属Ti因其电子助剂的作用,有助于催化剂中Ni2P活性相的形成。
Song等[5]提出了以次磷酸铵为磷源,在低还原温度(390℃)、流动H2条件下,程序升温还原法制备Ni2P催化剂的方法。笔者将金属Ti引入MCM-41分子筛,制备Ti-MCM-41载体,并采用低还原温度(400℃)程序升温法,制备了Ni2P/Ti-MCM-41催化剂。采用连续流动式固定床高压微型反应装置,以二苯并噻吩(DBT)为探针,考察了载体中引入金属Ti对Ni2P/MCM-41加氢脱硫催化活性的影响,并从反应机理角度深入分析了金属Ti在催化加氢脱硫反应中的作用。
1 实验部分
1.1 试剂
正硅酸四乙酯(TEOS)、十六烷基三甲基溴化铵(CTAB),分析纯,天津市科密欧化学试剂有限公司产品;钛酸四丁酯(TBOT)、 NaOH,分析纯,天津市永大化学试剂研发中心产品;异丙醇、氯化镍,分析纯,沈阳市华东试剂厂产品;次磷酸铵,分析纯,Aladdin chemistry Co. Ltd产品;二苯并噻吩,分析纯,美国商品(New Jersey,USA);十氢萘,分析纯,北京化工厂产品;正十二烷,分析纯,成都市科龙化工试剂厂产品;氢气,工业级,大庆雪龙气体公司产品;氨水,分析纯,哈尔滨市化工试剂厂产品。
1.2 MCM-41和Ti-MCM-41分子筛的制备
采用文献方法[6]制备MCM-41介孔分子筛,记为M41。
向模板剂CTAB水溶液中滴加TEOS,使n(CTAB)/n(TEOS)=0.14,再向其中滴加TBOT的异丙醇溶液,加入NaOH调节溶液的pH值为10.5~11.0;加热至78℃,持续搅拌2 h,除去异丙醇和其他由于TEOS和TBOT水解产生的醇,于100℃下晶化3 d;冷却、过滤,用去离子水洗涤至洗涤液为中性,经干燥、焙烧,制得n(Ti)/n(Si)为0.015的Ti-MCM-41分子筛粉末,记为TM41。
1.3 催化剂制备
分别以M41和TM41为载体,采用低还原温度程序升温法制备Ni2P/M41和Ni2P/TM41催化剂。
将氯化镍、次磷酸铵溶解于蒸馏水中,加入M41浸渍10 h,干燥,在高纯H2气氛和400℃下还原处理2 h,降至室温,切换O2-N2混合气(O2体积分数0.5%)钝化处理2 h,获得Ni质量分数为7.9%、n(Ni)/n(P)为1/2、n(Ti)/n(Si)为0.015的Ni2P/M41。以相同步骤制备Ni2P/TM41。
1.4 催化剂表征
采用日本理学公司D/max-2200PC型X射线衍射仪对催化剂进行XRD分析。CuKα辐射,管电压40 kV,管电流30 mA;2θ扫描速率10°/min,扫描范围10°~80°。采用NOVA2000e测定仪低温(-196℃)N2吸附法测定催化剂比表面积。采用德国布鲁克公司Tensor 27傅里叶红外光谱仪对催化剂进行红外分析,扫描范围400~4000 cm-1,KBr压片。采用美国Quantachrome公司Autosorb-1-C化学吸附仪完成样品CO吸附表征,热导池检测(TCD),脉动法, He作为载气。
1.5 催化剂活性评价
以质量分数2%二苯并噻吩、1%十二烷烃(内标物)和97%十氢萘的混合溶液作为模型化合物,在280~340℃、反应压力3.0 MPa、V(H2)/V(Oil)=650、质量空速3.5 h-1的条件下进行催化加氢反应,评价催化剂的加氢脱硫催化活性。采用GC-14C气相色谱仪(火焰离子检测器)测定液体产物组成。
2 结果与讨论
2.1 Ni2P/M41和Ni2P/TM41催化剂的表征结果
2.1.1 M41和TM41的FT-IR分析
图1为M41和TM41的FT-IR谱。图1中,1085 cm-1处的吸收峰归属于Si—O—Si键的反对称伸缩振动,807、1250 cm-1处的吸收峰归属于Si—O—Si键的对称伸缩振动,450 cm-1处的吸收峰归属于Si—O—Si的弯曲振动[7];960 cm-1处的吸收峰可归为SiO4四面体通过Si—O—Ti键与金属Ti结合后的弯曲振动[8],表明金属Ti进入了分子筛骨架中,与Si原子和O原子成键。
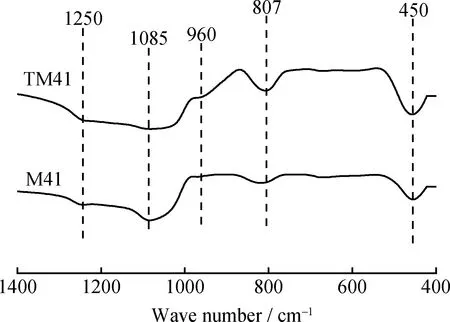
图1 M41和TM41的FT-IR谱
2.1.2 BET分析
表1为载体M41、TM41及其制备的催化剂Ni2P/M41和Ni2P/TM41的BET表征结果。由表1可知,与M41相比,TM41的比表面积(SBET)、孔容(VBJH)和孔径(D)均变小,这是由于M41骨架中晶格缺陷少,当骨架中Ti4+(0.068 nm)取代了Si4+(0.041 nm)后,可以增加晶格缺陷数量,改变了Si4+周围的几何结构[9]。Ni2P/M41和Ni2P/TM41催化剂的SBET、VBJH和D较对应的载体均降低,这表明Ni物种和P物种均负载到了载体的表面和孔道内,并且部分阻塞了载体的孔道。
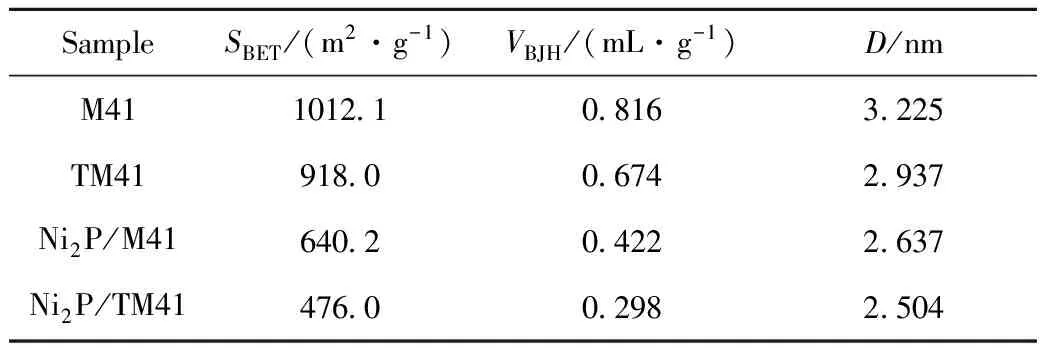
表1 载体M41、TM41及催化剂Ni2P/M41和Ni2P/TM41的织构性质
D—Pore diameter,D≈4(VBJH/SBET)
2.1.3 XRD分析
图2为Ni2P/M41和Ni2P/TM41的XRD谱。由图2可见,Ni2P/M41和Ni2P/TM41均在2θ为22°处出现1个宽峰,归属于M41S载体的无定型多孔结构;在2θ为40.7°、44.6°、47.3°和54.1°处均出现了归属于Ni2P活性相的(PDF 03-0953)特征衍射峰,且未见Ni或Ni12P5相的特征衍射峰,表明催化剂样品中的磷化镍物种均以单一的Ni2P形式存在。值得注意的是,向载体中引入金属Ti后,Ni2P活性相的特征衍射峰变宽。一般而言,峰强度变强变宽说明形成了更多、尺寸更小的活性相。通过Scherrer公式[10-11]计算得出的晶粒尺寸证实了这一点。Ni2P/TM41的Ni2P晶粒尺寸(Dc)为8 nm,较Ni2P/TM41的Ni2P晶粒尺寸(Dc)15 nm小1倍多,这可能是由金属Ti起电子助剂的作用导致[12]。与Ni2P/TiO2催化剂中的TiO2载体一样,TM41载体中的部分Ti4+能被还原为Ti3+,并通过TM41载体的导电带注入Ni的3d电子层,有利于Ni2P活性相的形成,且引入金属Ti有利于活性相更好地分散。催化剂晶粒尺寸的大小和分散相的好坏将影响其HDS反应产物的分布。

图2 Ni2P/M41和Ni2P/TM41的XRD谱
2.1.4 Py-FT-IR分析
众所周知,M41载体的酸性极其弱。然而,Ti4+离子的引入,可能会活化分子筛骨架中的羟基并产生酸性位。吡啶分子可以通过N原子中的长配对电子与L和B酸性位相互作用,在特定FT-IR位置产生特征峰。因此,可以用Py-FT-IR谱来探究载体表面酸的分布和酸量。被吸附的吡啶分子总体上可以分为3类:(1)质子化的吡啶,代表B酸位,在1540和1634 cm-1处出现特征吸收峰;(2)与L酸位配位的吡啶分子,在1440~1460、1575~1580和1600~1620 cm-1处出现特征吸收峰;(3)通过弱氢键使吡啶与羟基发生物理吸附,其特征吸收峰位置在1447和1599 cm-1处[13]。
图3为M41、TM41的Py-FT-IR谱及Ni2P/M41、Ni2P/TM41的原位Py-FT-IR谱。由图3(a)可知,M41的红外吸收峰很微弱,几乎没有任何酸性,而TM41在1446、1578、1597和1634 cm-1处出现了特征吸收峰,其中1446和1634 cm-1处的吸收峰分别归为L酸和B酸位[13-14],表明金属Ti的引入提高了M41的酸性。由图3(b)可知,Ni2P/M41基本没有酸性,而Ni2P/TM41在1447、1490和1548 cm-1处出现了特征吸收峰。其中1447和1548 cm-1处的吸收峰分别归为L酸和B酸位[14],而1490 cm-1处的吸收峰可能与Ni2P活性相有关,因为在负载前载体中并没此特征吸收峰。Duan等[15]将1490 cm-1处的特征吸收峰归为吸附在L酸和B酸位的吡啶共同作用的结果。与Ni2P/M41催化剂对比,金属Ti的引入导致了L酸特征吸收峰的强度变大。另外,与TM41相比,负载Ni2P后的Ni2P/TM41在1447 cm-1处的吸收峰强度均有所下降,且在1548 cm-1处的B酸位代替了原来载体上出现在1634 cm-1处的B酸位。
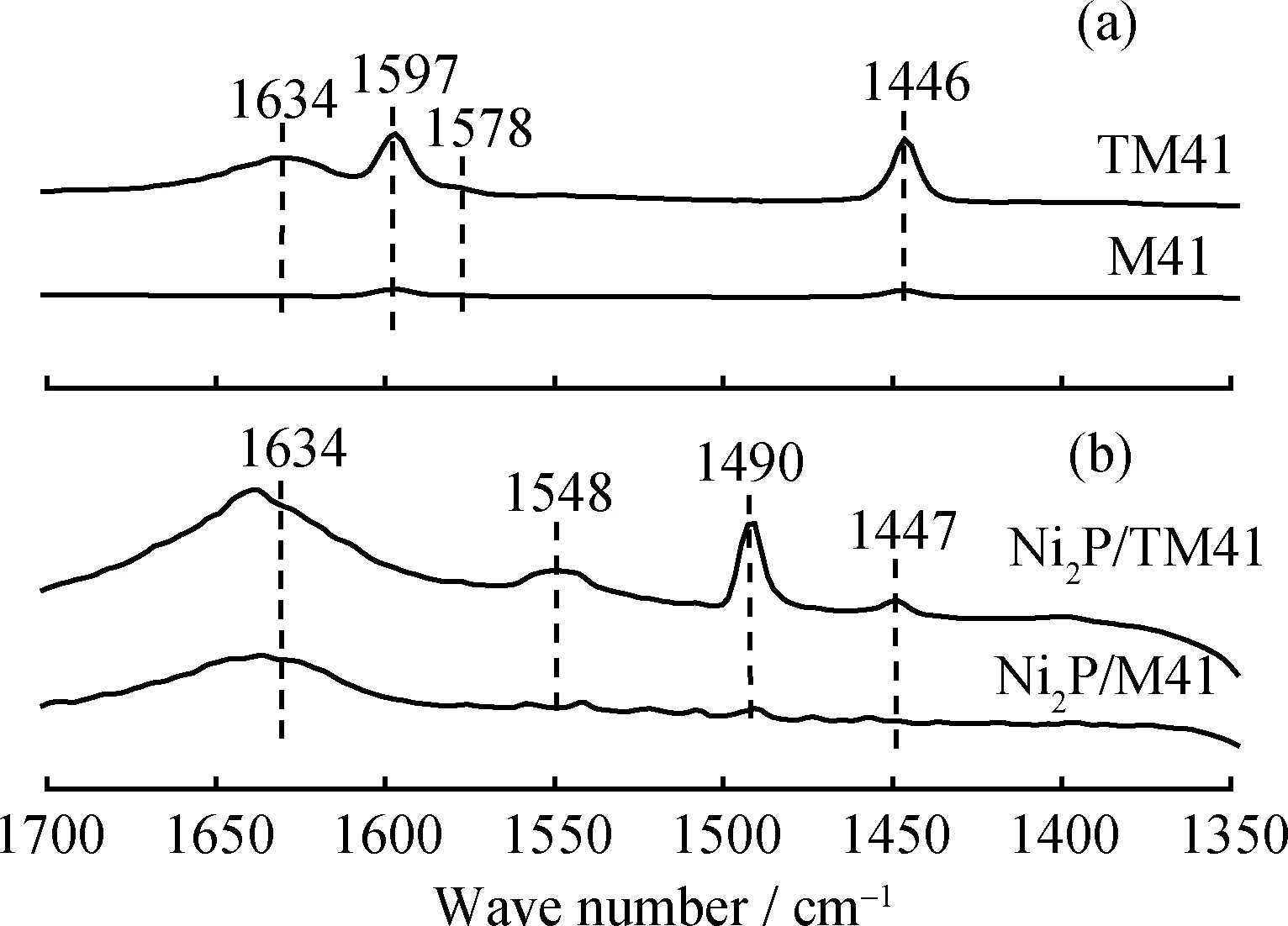
图3 M41 和TM41的Py-FT-IR谱及Ni2P/M41 和Ni2P/TM41的原位Py-FT-IR谱
表2列出了载体和催化剂的B和L酸酸量分布。由表2可见,M41的酸性非常弱,金属Ti的引入提高了载体中B酸和L酸的酸量,与Shu等[16]、Fuks等[17]所得结果一致。与M41和TM41相比,负载Ni2P活性相后的催化剂的B酸和L酸酸量均降低,尤其是Ni2P/TM41的L酸量降低很多,这与负载Ni2P活性相有关。

表2 M41、TM41、 Ni2P/M41和Ni2P/TM41的B和L酸酸量分布
1) Calculated based on the methods reported by Emeis[18]
2.1.5 CO吸附分析
在室温下,可以对催化剂采用CO化学吸附,来确定其表面的金属原子数。假定每个表面的Ni原子吸附1个CO分子(P原子也可能吸附CO分子,但其吸附量与Ni原子的相比非常小,可以忽略不计[19]),可以通过CO吸附量来估算催化剂表面Ni原子的数量及分散性[20-21]。表3为Ni2P/M41 和Ni2P/TM41催化剂的CO吸附量、TOF以及其催化HDS反应的转化率(xDBT)和产物选择性(s)。由表3可知,Ni2P/M41的CO吸附量明显高于Ni2P/TM41的,表明Ni2P/M41上暴露出的Ni原子更多。这与Shu等[16]的结果一致,即载体比表面积大有助于金属Ni的分散性,从而提高CO吸附量。

表3 Ni2P/M41 和Ni2P/TM41的CO吸附量、TOF及其催化DBT HDS反应的转化率(xDBT)和产物选择性(s)
HDS reaction conditions:T=340℃;p=3.0 MPa; MHSV=3.5 h-1;V(H2)/V(Oil)=650
2.2 Ni2P/M41 和Ni2P/TM41的HDS催化活性
由表3可知,金属Ti的引入使催化剂的HDS活性提高了约17百分点。2种催化剂催化DBT HDS的产物主要为环己基苯(CHB)和联苯(BP),分别通过加氢途径(HYD)和直接脱硫(DDS)路径生成;其中BP均占大部分,说明DDS途径为主要脱硫途径,与Houalla[22]和Wang[23]等的结果相吻合。由表3还可知,引入金属Ti后,HYD选择性提高更为明显,表明金属Ti明显促进HYD途径。此外,转化频数TOF也是用来衡量磷化镍催化剂HDS活性的重要指标。Ni2P/TM41的TOF值明显高于Ni2P/M41,表明在Ni2P/TM41催化剂上形成了更高效的Ni2P活性相。
2.3 Ni2P/TM41催化DBT HDS反应机理
引入金属Ti后的Ni2P/TM41催化剂的HDS活性显著提高,可能与其上形成了晶粒更小的活性相Ni2P、金属Ti的电子助剂作用以及其表面酸性有关。如前所述,引入金属Ti后催化剂的CHB选择性提高,因此,引入金属Ti提高催化剂的HDS活性,是HYD途径起决定性作用。Ni2P/TM41具有L酸和B酸中心,而Ni2P/M41几乎没有酸性(见表2),因此,引入金属Ti使催化剂的HDS活性提高可能是由于催化剂的酸中心为HDS反应提供新的反应路径,如图4所示,B酸为DBT提供吸附位[24],L酸促进Ni2P活性相解离出更多的活性氢(Ni2P扮演脱氢酶的角色[18,25])。被解离出的活性氢能够与吸附在B酸中心上的DBT进行加氢反应,通过HYD途径使催化活性提高。Niquille-Röthlisberger等[26]提出,当S原子与被Pt、Pd或Pt-Pd催化剂解离出的活性氢相互作用时,氢溢流现象与C—S键的断裂(即进行HYD途径)会同时发生。Silva-Rodrigo等[27]得到了相似的实验结论。他们在研究NiMo/TM41和NiW/TM41催化噻吩HDS时发现,催化剂适宜的酸强度有利于噻吩转化率的提高。这是因为金属Ti的引入使催化剂表面吸附DBT的酸性位增多,当金属活性位上解离出的活性氢溢流到酸性位时,会与吸附在酸性位上的DBT分子进行加氢反应。总之,由于金属Ti引入载体中,提高了催化剂的L酸和B酸性位,最终通过金属活性位和酸性位协同作用使HYD途径的选择性明显提高。
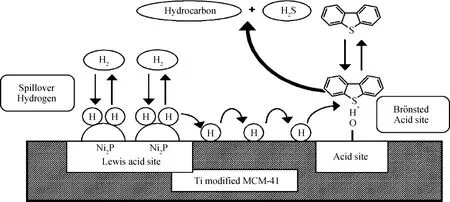
图4 Ni2P/TM41催化DBT HDS可能的新反应路径
3 结 论
结合传统的程序升温还原法和热解次磷酸盐法的各自优点,以Ti-MCM-41介孔分子筛为载体,低温还原法(400℃)制备了Ni2P/Ti-MCM-41催化剂。结果表明,金属Ti可以增强载体和催化剂的B酸和L酸的酸性,有利于更细小颗粒的Ni2P活性相的形成,提高活性相的分散度,从而提高了催化剂的HDS活性。在反应温度280~340℃,反应压力3.0 MPa,V(H2)/V(Oil)=650,质量空速3.5 h-1的条件下,Ni2P/Ti-MCM-41催化DBT HDS的转化率高达99.38%。金属Ti的引入使催化剂的HDS活性提高了约17百分点。
[1] OYAMA S T, GOTT T, ZHAO H Y, et al. Transition metal phosphide hydroprocessing catalysts: A review[J]. Catalysis Today, 2009, 143(1-2):94-107.
[2] 宋华, 代敏, 宋华林. Ni2P加氢脱硫催化剂化学进展[J]. 化学进展, 2012, 24(5):43-47.(SONG Hua, DAI Min, SONG Hualin. Ni2P catalyst for hydrodesulfurization[J]. Progress in Chemistry, 2012, 24(5):43-47.)
[3] SONG H, DAI M, SONG H L, et al. Synthesis of a Ni2P catalyst supported on anatase-TiO2whiskers with high hydrodesulfurization activity, based on triphenylphosphine[J]. Catalysis Communications, 2014, 43:151-154.
[4] SONG H, DAI M, GUO Y T, et al. Preparation of composite TiO2-Al2O3supported nickel phosphide hydrotreating catalysts and catalytic activity for hydrodesulfurization of dibenzothiophene[J]. Fuel Processing Technology, 2012, 96: 228-236.
[5] SONG H, DAI M, SONG H L, et al. A novel synthesis of Ni2P/MCM-41 catalysts by reducing a precursor of ammonium hypophosphite and nickel chloride at low temperature[J]. Applied Catalysis A: General, 2013, 462-463:247-255.
[6] MELENDEZ-ORTIZ H I, GARCIA-CERDA L A, OLIVARES-MALDONADO Y, et al. Preparation of spherical MCM-41 molecular sieve at room temperature: Influence of the synthesis conditions in the structural properties[J]. Ceramics International, 2012, 38(8):6353-6358.
[7] KONG Y, ZHU H Y, YANG G, et al. Investigation of the structure of MCM-41 samples with a high copper content[J]. Advanced Functional Materials, 2004, 14(8):816-820.
[8] SHI Y, WANG S P, MA X B. Microwave preparation of Ti-containing mesoporous materials. Application as catalysts for transesterification[J]. Chemical Engineering Journal, 2011, 166(2):744-750.
[9] KOSSLICK H, LISCHKE G, LANDMESSER H, et al. Acidity and catalytic behavior of substituted MCM-48[J]. Journal of Catalysis, 1998, 176(1):102-114.
[10] WANG X Q, CLARK P, OYAMA S T. Synthesis, characterization, and hydrotreating activity of several iron group transition metal phosphides[J]. Journal of Catalysis, 2002, 208(2):321-331.
[11] OYAMA S T, WANG X Q, LEE Y K, et al. Active phase of Ni2P/SiO2in hydroprocessing reactions[J]. Journal of Catalysis, 2004, 221(2):263-273.
[12] LI X, LU M H, WANG A J, et al. Promoting effect of TiO2on the hydrodenitrogenation performance of nickel phosphide[J]. Journal of Physical Chemistry C, 2008, 112(42):16584-16592.
[13] EIMER G A, CASUSCELLI S G, CHANQUIA C M, et al. The influence of Ti-loading on the acid behavior and on the catalytic efficiency of mesoporous Ti-MCM-41 molecular sieves[J]. Catalysis Today, 2008, 133-135:639-646.
[14] AREAN C O, DELGADO M R, MONTOUILLOUT V, et al. NMR and FTIR spectroscopic studies on the acidity of gallia-silica prepared by a sol-gel route[J]. Microporous and Mesoporous Materials, 2004, 67:259-264.
[15] DUAN X Q, TENG Y, WANG A J, et al. Role of sulfur in hydrotreating catalysis over nickel phosphide[J]. Journal of Catalysis, 2009, 261(2):232-240.
[16] SHU Y Y, LEE Y K, OYAMA S T. Structure-sensitivity of hydrodesulfurization of 4,6-dimethyldibenzothiophene over silica-supported nickel phosphide catalysts[J]. Journal of Catalysis, 2005, 236(1):112-121.
[17] FUKS D, VINGURT D, LANDAU M V, et al. Density functional theory study of sulfur adsorption at the (001) surface of metal-rich nickel phosphides: Effect of the Ni/P ratio[J]. Journal of Physical Chemistry C, 2010, 114(31):13313-13321.
[18] LIU P, RODRIGUEZ J A, ASAKURS T, et al. Desulfurization reactions on Ni2P(001) and α-Mo2C(001) surfaces: Complex role of P and C sites[J]. Journal of Physical Chemistry B, 2005, 109(10):4575-4583.
[19] LAYMAN K A, BUSSELL M E. Infrared spectroscopic investigation of CO adsorption on silica-supported nickel phosphide catalysts[J]. Journal of Physical Chemistry B, 2004, 108(30):10930-10941.
[20] OYAMA S T. Novel catalysts for advanced hydroprocessing: Transition metal phosphides[J]. Journal of Catalysis, 2003, 216(1-2):343-352.
[21]OYAMA S T, WANG X, LEE Y K, et al. Effect of phosphorus content in nickel phosphide catalysts studied by XAFS and other techniques[J]. Journal of Catalysis, 2002, 210(1):207-217.
[22] HOUALLA M, BRODERICK D H, SAPRE A V, et al. Hydrodesulfurization of methyl-substituted dibenzothiophenes catalyzed by sulfided Co-Mo/γ-Al2O3[J]. Journal of Catalysis, 1980, 61(2):523-527.
[23] WANG H M, PRINS R. Hydrodesulfurization of dibenzothiophene and its hydrogenated intermediates over sulfided Mo/γ-Al2O3[J]. Journal of Catalysis, 2008, 258(1):153-164.
[24] KANDA Y, KOBAYASHI T, UEMICHI Y, et al. Effect of aluminum modification on catalytic performance of Pt supported on MCM-41 for thiophene hydrodesulfurization[J]. Applied Catalysis A: General, 2006, 308:111-118.
[25] LIU P, RODRIGUEZ J A. Catalysts for hydrogen evolution from the[NiFe] hydrogenase to the Ni2P (001) surface: The importance of ensemble effect[J]. Journal the American Chemical Society, 2005, 127(42):14871-14878.
[26] NIQUILLE-ROTHLISBERGER A, PRINS R. Hydrodesulfurization of 4,6-dimethyldibenzothiophene over Pt, Pd, and Pt-Pd catalysts supported on amorphous silica-alumina[J]. Catalysis Today, 2007, 123(1-4):198-207.
[27] SILVA-RODRIGO R, CALDERON-SALAS C, MELO-BANDA J A, et al. Synthesis, characterization and comparison of catalytic properties of NiMo- and NiW/Ti-MCM-41 catalysts for HDS of thiophene and HVGO[J]. Catalysis Today, 2004, 98(1-2):123-129.
Hydrodesulfurization Performance of Ni2P/Ti-MCM-41 Catalyst
SONG Hua1,2, WANG Zidong1, SONG Hualin3, WANG Jian1, LI Feng1,2
(1.CollegeofChemistry&ChemicalEngineering,NortheastPetroleumUniversity,Daqing163318,China;2.ProvincialKeyLaboratoryofOil&GasChemicalTechnology,NortheastPetroleumUniversity,Daqing163318,China;3.DepartmentofImageSchool,MudanjiangMedicalUniversity,Mudanjiang157011,China)
Ni2P/MCM-41 and Ni2P/Ti-MCM-41 catalysts were successfully prepared by temperature programmed reduction method at a low reduction temperature(400℃). The obtained catalysts were characterized by XRD, BET, FT-IR, Py-FT-IR, XPS, TEM and CO uptake. The catalytic hydrodesulfurization(HDS) performance of Ni2P/Ti-MCM-41 was investigated on a fixed bed and with dibenzothiophene(DBT) as model compound. The results indicated that the introduction of Ti into MCM-41can modify the acidic nature of supports and catalysts and enhance the Lewis acidity as well as the Brønsted acid intensity of supports, being beneficial to the formation of Ni2P active phase because of the electronic properties of Ti. At the conditions of 340℃, 3.0 MPa, mass hourly space velocity (MHSV) of 3.5 h-1and H2/oil volume ratio of 650, catalyzed by Ni2P/Ti-MCM-41 the conversion of DBT HDS reached 99.38%, 17% higher than that catalyzed by Ni2P/MCM-41 catalyst. The electronic effect of Ti, size of active phase and its dispersion, and the moderate surface acidity of catalyst may be responsible to the enhancement of HDS catalytic activity of the Ti-doped samples.
hydrodesulfurization; nickel phosphide; Ti-MCM-41; dibenzothiophene
2014-09-17
国家自然科学基金项目(21276048)、黑龙江省自然基金项目(ZD201201)资助
宋华,女,教授,博士,从事工业催化和绿色氧化研究;Tel:0459-6503167;E-mail:songhua2004@sina.com
宋华林,男,高级工程师,博士,从事功能材料及仪器分析方面的研究;E-mail:songhualin401@126.com
1001-8719(2015)06-1275-06
O643.31; TE624.4
A
10.3969/j.issn.1001-8719.2015.06.004

