水热法制备ZnWO4及其电化学性能研究
王志涛,张林森,金 恺,谢文菊
(1.武夷学院生态与资源工程学院,福建武夷山354300;2.郑州轻工业学院材料与化学工程学院河南省表界面科学重点实验室,河南郑州450002)
水热法制备ZnWO4及其电化学性能研究
王志涛1,2,张林森2,金 恺2,谢文菊1
(1.武夷学院生态与资源工程学院,福建武夷山354300;2.郑州轻工业学院材料与化学工程学院河南省表界面科学重点实验室,河南郑州450002)
以钨酸钠和乙酸锌为原料,去离子水为溶剂,通过水热法合成前驱物,采用固相烧结制备ZnWO4,探讨不同的pH值和煅烧温度对ZnWO4结构和电化学性能的影响,并通过X射线衍射(XRD)、扫描电子显微镜(SEM)、恒电流充放电和循环伏安测试对其进行表征。结果表明:不同pH下制备的ZnWO4均为表面粗糙的球形颗粒;当pH为7.5、煅烧温度为900℃时,制备得到的黑钨矿型ZnWO4具有良好的电化学性能;在50 mA/g电流密度下,样品的首次充电比容量为710.9 mAh/g,首次放电比容量为419.9 mAh/g。
锂离子电池;ZnWO4;水热法;pH值;煅烧温度
目前,锂离子电池已被广泛应用于各种便携式电子产品和通讯工具。由于其性能优越,锂离子电池也成为潜在的动力电池,并被逐步开发为电动汽车的动力电源。动力电源对电极材料的性能要求非常高,除了要有高比能量和高比功率外,安全性、生产成本及循环性能也需要满足要求。已经商品化的锂离子电池负极材料主要是石墨化碳材料,但作为动力型锂离子电池负极,存在比容量低、安全性较差等问题。2011年Hyun-Woo Shim等[1]发现黑钨矿型结构的ZnWO4材料具有相对于Li/Li+较高的电位和较好的循环性能,其理论比容量为600 mAh/g,低倍率充放电下其实际比容量可以达到420 mAh/g左右,且具有安全无毒等优点,成为极具商业化前景的动力型锂离子电池负极材料。
ZnWO4的制备方法很多,包括固相反应法、溶胶-凝胶法、水热反应法等。其中固相反应法合成周期长,一般需要至少四个步骤,在研磨和烧结过程中有诸多重复。凝胶-凝胶法的优点是前驱体溶液化学均匀性好(可达分子级水平)、凝胶热处理温度低、粉体颗粒粒径小而且分布窄、粉体烧结性能好、反应过程易于控制、设备简单,但是原料成本较高、消耗过多有机试剂(且部分原料对人体健康有害),并且整个溶胶-凝胶过程所需时间一般较长(几天或几周时间),因而可操作性不佳成为这种方法发展的瓶颈。水热法是值得考虑的一种方法[2]。水热法作为一种温和的湿化学合成方法,具有合成条件温和、能以单一步骤完成产物的合成与晶化、流程简单、结晶性好、粒径分布窄、尺寸大小可控、原料成本相对较低等优点,是制备纳米无机材料的理想方法之一。
目前,研究水热法合成ZnWO4并将其应用于锂离子电池负极材料的报道较少[3]。为合成具有高比容量的ZnWO4,本文采用低温水热反应法合成ZnWO4前驱体,经高温煅烧得到ZnWO4材料,探究了不同pH值及煅烧温度对ZnWO4的结构、形貌及电化学性能的影响。
1 实验
1.1 ZnWO4的制备
将钨酸钠和乙酸锌按照物质的量之比1∶1称量,以去离子水做溶剂,准确配置为0.2 mol/L的Na2WO4溶液50 mL及0.2 mol/L的乙酸锌溶液50 mL。室温下,将配置好的乙酸锌溶液逐滴加入Na2WO4溶液中。随着Na2WO4溶液的加入,溶液中逐渐出现白色沉淀,电动搅拌10 min后,用2 mol/L氢氧化钠溶液调节溶液的pH值为7.0~9.0。然后将此白色浆料转入容积为100 mL的聚四氟反应釜中(填充度75%),在80℃下恒温10 h,自然冷却至室温,离心分离后,依次用去离子水和无水乙醇洗涤沉淀多次,以去除可能存在的杂质离子,然后在80℃下干燥,于不同温度下煅烧2 h得到ZnWO4样品。最后将所得产品在玛瑙研钵中研磨2 h备用。
1.2 ZnWO4的表征
本文采用D8-ADVANCE型X射线衍射仪对所得样品进行物相分析,其管压40 kV,管流30 mA,Cu靶Kα射线入射,λ=0.154 2 nm,扫描速度为3(°)/min。采用JSM-6490型SEM-EDXA对样品进行形貌表征。
1.3 电池的组装及电化学性能测试
采用纽扣电池(CR2016)测试ZnWO4的电化学性能,装配过程在高纯氩气(99.999%)保护的手套箱中进行,参比电极和对电极采用金属锂片(纯度99.99%),隔膜采用Celgard 2400,工作电极为ZnWO4电极,电解质为1 mol/L LiPF6/(EC+DMC)(体积比1∶1)。采用恒流方式对电池进行充放电测试,恒流放电电流为50 mA/g,充放电电压范围设置为0.01~3.0 V;采用上海辰华CHI600C型电化学工作站进行循环伏安测试,扫描范围为0.01~3.0 V,扫描速度为0.1 mV/s,扫描方向为负向扫描。
2 结果与讨论
2.1 ZnWO4的结构分析
图1所示为不同pH值ZnWO4样品的X射线衍射(XRD)图谱,水热反应条件为80℃保温10 h。由图1可以看出,在该反应条件下得到的样品峰强度较弱、峰形较宽,无明显的特征峰,说明所得样品为非晶态。对比可知,pH值为7.5所得样品的衍射峰较其他pH条件下的尖锐,说明该pH值下的样品具有一定结晶度。造成上述结果的原因可能是因为材料的合成温度较低或者水热反应时间较短。
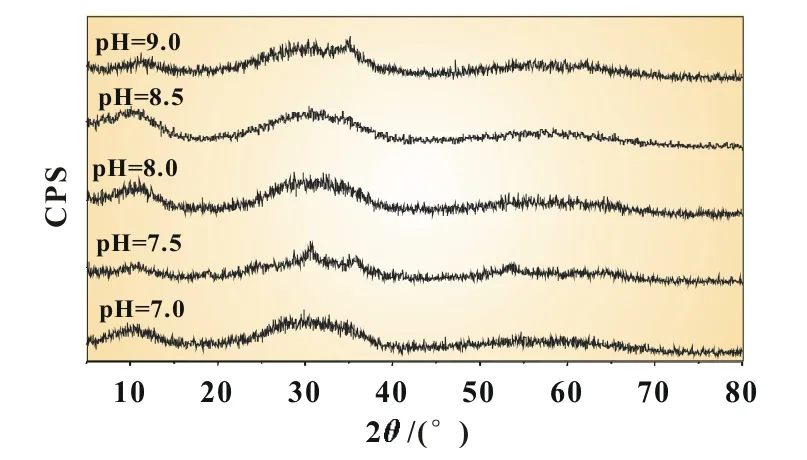
图1 不同pH条件下ZnWO4的XRD图谱
煅烧温度通常直接影响ZnWO4样品的结构及组成。图2为不同煅烧温度制备的ZnWO4的XRD图谱。所有样品的pH值均为7.5。由图2可以看出,未煅烧ZnWO4样品的XRD特征峰不明显,经高温烧结后的粉体谱图中峰形尖锐,可以明显看到所合成ZnWO4的XRD特征峰且强度增加,证明所得产物结晶性变好。不同煅烧温度下所得样品的XRD图均出现与标准卡片PDF15-0774一致的ZnWO4特征衍射峰,说明样品为单斜相黑钨矿结构ZnWO4,相结构单一,证实所得产品为纯相ZnWO4。当煅烧温度为500℃时,ZnWO4粉体的XRD明显特征峰均已出现,峰形也变得较为尖锐;随着煅烧温度从500℃增加到900℃,衍射峰峰位置不变,晶相保持不变,XRD特征峰的半高宽也变得越来越窄,表明随着煅烧温度的升高,晶粒尺寸不断长大,材料的结晶程度逐渐完整。

图2 不同煅烧温度下ZnWO4的XRD图谱
2.2 ZnWO4的形貌分析
由上述XRD图谱可以得出,要制备结晶度良好的Zn-WO4,需要高温煅烧处理。图3所示为在不同pH值所得样品的扫描电镜(SEM)照片,右上角插图为该pH值下的SEM放大图。从图中可以清晰地看到,所得样品为球状结构,表面疏松多孔、不光滑,呈现出无定形态,这与XRD分析结果相吻合。此外,随着pH值的增大,产物的形貌没有明显变化。在放大图中(×10 000倍)可以清晰地看到微米球的表面粗糙,是由很多亚微米级细小颗粒堆积而成。出现上述现象的原因可能是因为在水热合成过程中ZnWO4的成核速率较小,导致晶粒粗大,形成的粉体粒度较大[4]。颗粒粗大及团聚现象可能会导致锂电池循环性能较差,比容量衰减迅速。

图3 80℃不同pH值条件下所得ZnWO4的SEM照片
2.3 ZnWO4的电化学性能分析
2.3.1 ZnWO4的充放电性能测试
在80℃下,不同pH值水热反应10 h制备的ZnWO4的充放电性能对比如图4所示。表1中给出了不同pH所得Zn-WO4材料的首次充放电数据和19次循环后的性能参数。由图4(a)可知,pH值变化对充放电平台电位影响不大;在pH=7.5时电池的首次放电比容量为989.7 mAh/g,充电比容量为208.1 mAh/g;结合表1可知pH=7.5时,样品的首次放电比容量及首次库仑效率最高,循环8次后各样品的容量趋于稳定。综合对比分析,pH=7.5时ZnWO4样品的电化学性能较好,故选pH=7.5为最佳条件。由上述SEM照片可知,在pH=7.5时,部分ZnWO4小颗粒均匀分散在大颗粒之间,既能增加大颗粒之间的接触性能,又能保持其多孔性,从而改善了电极的电子导电性和离子迁移性能,因此电池的性能较好。但是,由于充放电过程中活性物质可能局部发生团聚而导致容量衰减快,容量保持率较低。
图5所示为不同煅烧温度下ZnWO4样品的充放电性能对比。表2中给出了不同煅烧温度所得ZnWO4的首次充放电数据和20次循环后的性能参数。由图5可知,经煅烧后样品的充放电平台电位降低且平台宽度增加,结合表2可见,煅烧温度对材料的首次充放电影响最大,对其后的循环性能影响较小。煅烧温度为900℃时电池的首次充放电比容量最高,但循环20次后其容量保持率很低(16.8%);虽然未煅烧样品的充电比容量最高 (921.1 mAh/g),但其放电比容量较低(233.9 mAh/g)。通过图5可知,经煅烧处理后,材料的首次不可逆容
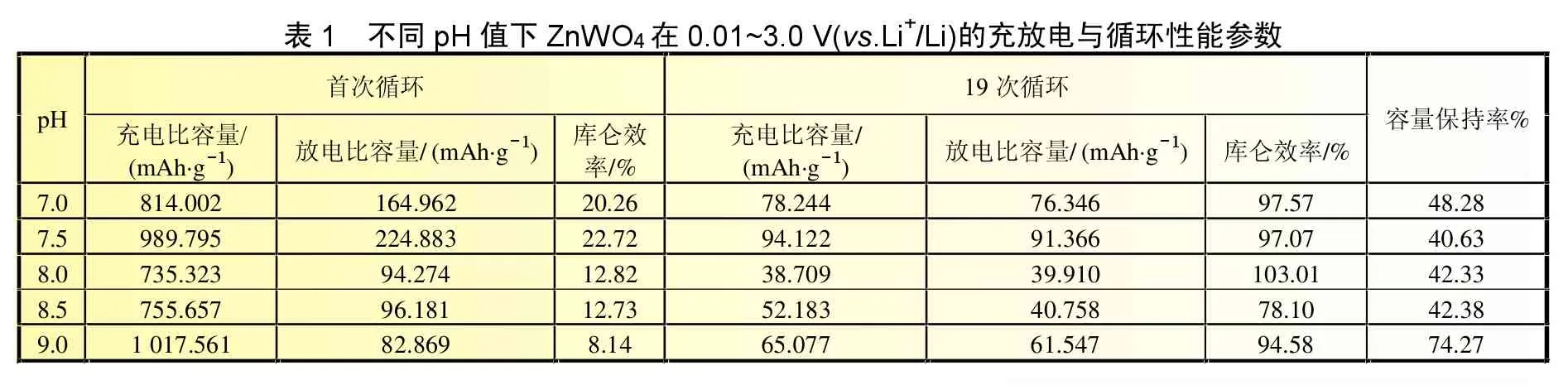
表1 不同p H值下Zn W O在0. 01~3 . 0 V (vs.Li/Li )的充放电与循环性能参数p H 充电比容量/库仑效放电比容量/ ( m A h•g) (mAh•g)首次循环19次循环7 .0 81 4 .0 02 16 4 .96 2 2 0. 26 78 .2 44 7 6. 34 6 97 .5 7 4 8 .28 7 .5 98 9 .7 95 22 4 .88 3 2 2. 72 9 4 .1 22 9 1. 36 6 97 .0 7 4 0 .63率/%充电比容量/放电比容量/ (m A h•g ) 库仑效率/% (m Ah•g) 8 .5 75 5 .6 57 9 6. 18 1 1 2. 73 5 2 .1 83 4 0. 75 8 78 .1 0 4 2 .38 8 .0 73 5 .3 23 9 4. 27 4 1 2. 82 3 8 .7 09 3 9. 91 0 1 0 3. 01 4 2 .33 9 .0 1 0 17 .5 6 1 8 2. 86 9 8 .1 4 6 5 .0 77 6 1. 54 7 94 .5 8 7 4. 27容量保持率%

图4 不同pH值下ZnWO4样品的首次充放电曲线(a)及循环性能曲线(b)

图5 不同煅烧温度下样品的首次充放电曲线(a)及循环性能曲线(b)
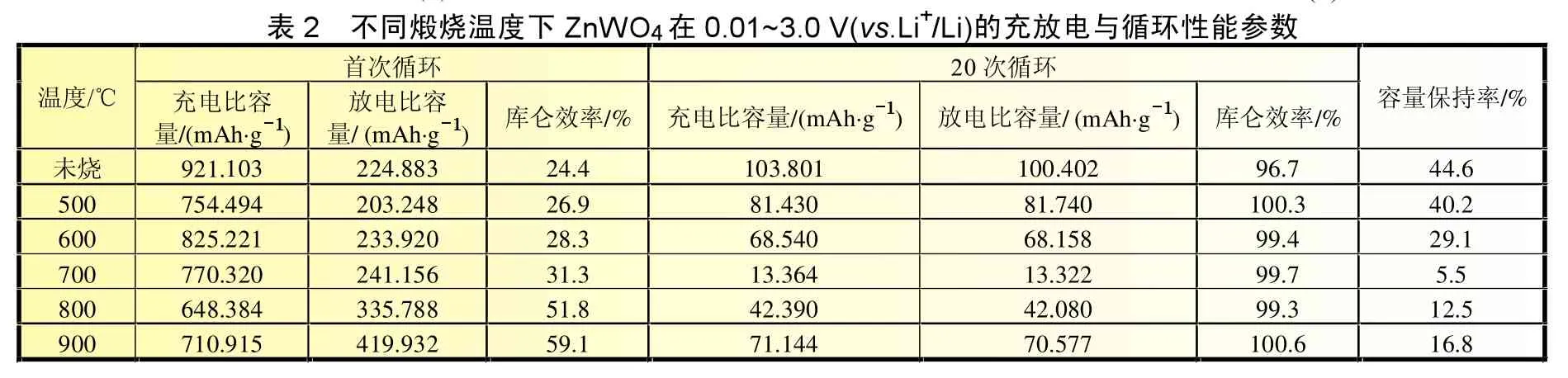
表2 不同锻烧温度下ZnWO在O.O1~3.O V(vs.Li/Li)的充放电与循环性能参数库仑效率/% 充电比容量/(mAh•g) 放电比容量/ (mAh•g) 库仑效率/%容量保持率/%量/ (mAh•g)温度/℃ 充电比容量/(mAh•g)未烧 92 1 .1 03 22 4 .8 83 2 4 .4 1 0 3. 80 1 1 0 0. 40 2 96 .7 4 4 .6首次循环20次循环放电比容6 0 0 82 5 .2 21 23 3 .9 20 2 8 .3 68 .5 4 0 68 .1 5 8 99 .4 2 9 .1 5 0 0 75 4 .4 94 20 3 .2 48 2 6 .9 81.4 3 0 81 .7 4 0 1 00 .3 4 0 .2 9 0 0 71 0 .9 15 41 9 .9 32 5 9 .1 71 .1 4 4 70 .5 7 7 1 00 .6 1 6 .8 7 0 0 77 0 .3 20 24 1 .1 56 3 1 .3 13 .3 6 4 13 .3 2 2 99 .7 5. 5 8 0 0 64 8 .3 84 33 5 .7 88 5 1 .8 42 .3 9 0 42 .0 8 0 99 .3 1 2 .5
量降低,这可能与温度升高使材料结晶度和导电性增大有关。此外,煅烧温度的升高可能使局部团聚现象加剧,将增加锂离子的扩散路径,使充放电时电极极化增加,从而降低材料的循环性能。
2.3.2 ZnWO4的循环伏安测试
为了进一步研究ZnWO4的电化学反应机理,对ZnWO4研究电极进行了三次循环伏安测试,扫描速度为0.1 mV/s,扫描范围为0.01~3.0 V,测试结果如图6所示。由图6可以看出,首次扫描曲线过程明显与其他两次扫描曲线不同,在0.25、0.70和1.28 V出现三个比较明显的阳极峰,与之相对的,在0.10、0.65和1.25 V附近出现三个较弱的阴极峰,但是在第二次扫描过程中,1.25 V附近的阴极峰明显减弱,而0.10 V附近的阴极峰电流明显减弱,这类似于大多数金属氧化物负极材料[5]。首次放电过程即阴极扫描过程显示出明显的不可逆性,不可逆容量可能归因于固体电解质相界面膜(SEI膜)的形成[6-8]。同时,第二次的循环伏安扫描曲线与第三次的吻合较好,说明材料结构趋于稳定,预示电池容量将趋于稳定,这与充放电结果相一致。

图6 ZnWO4的循环伏安曲线
它的氧化还原反应机理如下所示[1]:

3 结论
本文利用水热技术制备了ZnWO4粉体,讨论了不同pH值及煅烧温度对材料结构、形貌及电化学性能的影响。研究结果表明,未经高温处理时,所得材料为非晶态、表面粗糙的颗粒;随着煅烧温度的升高,材料的晶型趋于完整。pH=7.5时制备的样品组装锂离子电池的电化学性能较优,充电比容量为989.7 mAh/g,放电比容量为208.1 mAh/g,循环20次后放电比容量为100.4 mAh/g,充电比容量为103.8 mAh/g;pH=7.5,煅烧温度为 900℃时所得样品的首次放电比容量为 710.9 mAh/g,首次充电比容量为419.9 mAh/g,虽然其可逆比容量及循环性能与现有的碳素材料相比较低,但其作为锂离子电池负极材料是一种较新的材料,研究较少,还需深入的研究。
[1]SHIM H W,CHO I S,HONG K S,et al.Wolframite-type ZnWO4nanorods as new anodes for Li-ion batteries[J].The Journal of Physical Chemistry C,2011,115(32):16228-16233.
[2]施尔畏,夏长泰,王步国,等.水热法的应用与发展[J].无机材料学报,1996,11(2):193-206.
[3]ZHANG L,WANG Z,WANG L,et al.Preparation of ZnWO4/ graphene composites and its electrochemical properties for lithium-ion batteries[J].Mater Lett,2013,108:9-12.
[4]LI W,SHI E,TIAN M,et al.Synthesis of ZnO fibers and nanometer powders by hydrothermal method[J].Science in China Series E: Technological Sciences,1998,41(5):449-459.
[5]SHARMA N,SUBBA RAO G V,CHOWDARI B V R.Electrochemical properties of carbon-coated CaWO4versus Li[J].Electrochim Acta,2005,50(27):5305-5312.
[6]YOGESH S N S,RAO G V S,CHOWDARI B V R.Nanophase ZnCo2O4as a high performance anode material for Li-ionbatteries [J].Adv Funct Mater,2007,17(15):2855-2861.
[7]LARUELLE S,GRUGEON S,POIZOT P,et al.On the origin of the extra electrochemical capacity displayed by MO/Li cells at low potential[J].J Electrochem Soc,2002,149(5):A627.
[8]RONG A,GAO X P,LI G R,et al.Hydrothermal synthesis of Zn2SnO4as anode materials for Li-ion battery[J].J Phys Chem B, 2006,110:14754-14760.
Preparation of ZnWO4by hydrothermal method and its electrochemical properties
WANG Zhi-tao1,2,ZHANG Lin-sen2,JIN Kai2,XIE Wen-ju1
(1.College of Ecology and Resources Engineering,Wuyi University,Wuyishan Fujian 354300,China;2.Key Lab of Surface&Interface Science,Material and Chemical Engineering College,Zhengzhou University of Light Industry,Zhengzhou Henan 450002,China)
ZnWO4was prepared by a hydrothermal method followed by solid state calcination using sodium tungstate and zinc acetate as raw materials as well as deionized water as the solvent.The effects of different pH value and calcination temperature on the structure and electrochemical performance of ZnWO4were investigated by XRD, SEM,constant current charge-discharge and cyclic voltammetry.The results show that the prepared ZnWO4under different pH value are spherical particles with rough surface;when the pH is 7.5 and the calcination temperature is 900℃,the obtained pure phase wolframite type ZnWO4has better electrochemical performance.The initial charge and discharge specific capacity of the sample are as high as 710.9 and 419.9 mAh/g at the current density of 50 mA/g.
Li-ion batteries;ZnWO4;hydrothermal method;pH value;calcining temperature
TM 912
A
1002-087 X(2015)08-1626-03
2015-01-22
河南省科技计划项目(122300410297)
王志涛(1987—),男,河南省人,硕士研究生,主要研究方向为电池材料。
张林森,博士,副教授,E-mail:hnzhanglinsen@163. com

