五酯胶囊对特发性膜性肾病患者环孢素A全血浓度的影响研究
陈揭剑,梅长林
环孢素A(cyclosporine A,CsA)是膜性肾病治疗中可供选择的药物之一,既可以在其他药物治疗无效时使用,也可以作为初始治疗使用[1]。口服CsA的吸收、代谢与肝肠细胞色素P450酶系3A亚家族 (CYP3A)的活性相关[2]。既往研究表明,五酯胶囊可抑制患者体内CYP3A的活性,从而影响一些经CYP3A代谢的药物[3],但关于该药物组合对临床特发性膜性肾病 (idiopathic membranous nephropathy,IMN)患者的影响还罕见报道。本研究对21例接受CsA治疗的IMN患者联合应用五酯胶囊进行治疗,分析五酯胶囊对CsA全血浓度的影响,并探讨其临床应用意义。
1 对象与方法
1.1 研究对象 于2013年1月—2014年3月,选取在第二军医大学附属长征医院肾内科确诊并常规随访治疗的IMN患者48例作为研究对象。IMN诊断标准[4]:经肾穿刺病理活检诊断为膜性肾病,且排除可能存在的感染、肿瘤及药物使用等继发因素。纳入标准:(1)年龄18~70岁;(2)初次发病,之前未接受过任何治疗;(3)尿蛋白定量>3.5 g/24 h,血清蛋白 (ALB)<30 g/L;(4)肾脏病理分期为膜性肾病Ⅱ期。排除标准:(1)有感染、心肺功能不全等合并症;(2)血肌酐(SCr)、尿素、转氨酶、胆红素水平异常。采用随机数字表法,将IMN患者分为2组。对照组27例,其中男15例,女12例,平均年龄为 (52.3±12.9)岁;试验组21例,其中男14例,女7例,平均年龄为 (56.1±10.0)岁。2组患者性别和平均年龄比较,差异无统计学意义 (=0.61,t年龄=1.10,P>0.05)。所有患者均于接受治疗前签署知情同意书。
1.2 治疗方法 (1)对照组采用口服CsA(新赛斯平,中美华东制药有限公司,国药准字H10960122)和泼尼松 (醋酸泼尼松片,上海信谊药厂有限公司,国药准字H31020675)治疗。CsA的起始剂量为2.5~3.0 mg·kg-1·d-1,分2次口服;泼尼松的起始剂量为 0.5 mg·kg-1·d-1,清晨顿服。(2)试验组在对照组治疗的基础上,口服五酯胶囊 (四川禾正制药有限责任公司,国药准字Z10983013,含五味子甲素11.25 mg/粒)。2粒/次,2次/d,与CsA同时服用。
1.3 随访 (1)每个月门诊复查1次,复查内容包括:血常规、尿常规、24 h尿蛋白定量、肝肾功能、血脂、电解质等,并记录随诊时的临床症状;(2)记录2组患者CsA的给药剂量,并根据CsA全血浓度调整给药剂量,使全血浓度维持在0.1~0.2 mg/L;(3)监测患者治疗1周后、治疗1个月后及治疗3个月后的CsA全血浓度。于清晨8:00服药前,空腹抽取患者静脉血2 ml,置于加有乙二胺四乙酸二钠抗凝的试管中待测,检测方法为高效液相色谱法;(4)根据患者具体病情,进行其他必要项目的检测;(5)所有药物根据患者病情变化调整,门诊随访时间>6个月。
1.4 疗效评估 根据尿液检查、ALB及SCr水平分为完全缓解、部分缓解、无效及复发4种情况。(1)完全缓解:治疗后尿蛋白定量<0.3 g/24 h,ALB>35 g/L,SCr水平稳定;(2)部分缓解:治疗后尿蛋白减少>50%,尿蛋白定量0.3~3.5 g/24 h,ALB>35 g/L,SCr水平稳定;(3)未缓解:治疗后未达上述指标;(4)复发:部分或完全缓解至少1个月后,尿蛋白定量再次>3.5 g/24 h。临床治疗有效率=(完全缓解患者数+部分缓解患者数)/该组患者总数。
1.5 统计学方法 采用SPSS 17.0统计软件对数据进行分析。计数资料以率表示,组间比较采用χ2检验;计量资料以 (±s)表示,组间比较采用t检验。以P<0.05为差异有统计学意义。
2 结果
2.1 治疗前、治疗3个月后及治疗6个月后2组患者临床指标比较 (1)治疗前,2组患者间尿蛋白定量、ALB、SCr、丙氨酸氨基转移酶 (ALT)及天冬氨酸氨基转移酶 (AST)比较,差异无统计学意义 (P>0.05);治疗3个月后和治疗6个月后,2组患者间尿蛋白定量、ALB、SCr、ALT及AST比较,差异无统计学意义 (P>0.05)。(2)治疗3个月后和治疗6个月后,2组患者尿蛋白定量和ALB与治疗前比较,差异有统计学意义 (P<0.05);SCr、ALT及AST与治疗前比较,差异无统计学意义 (P>0.05,见表1)。
表1 治疗前、治疗3个月后及治疗6个月后2组患者临床指标比较 (±s)Table 1 Comparison of clinical index between the two groups before treatment,3 months and 6 months after treatment
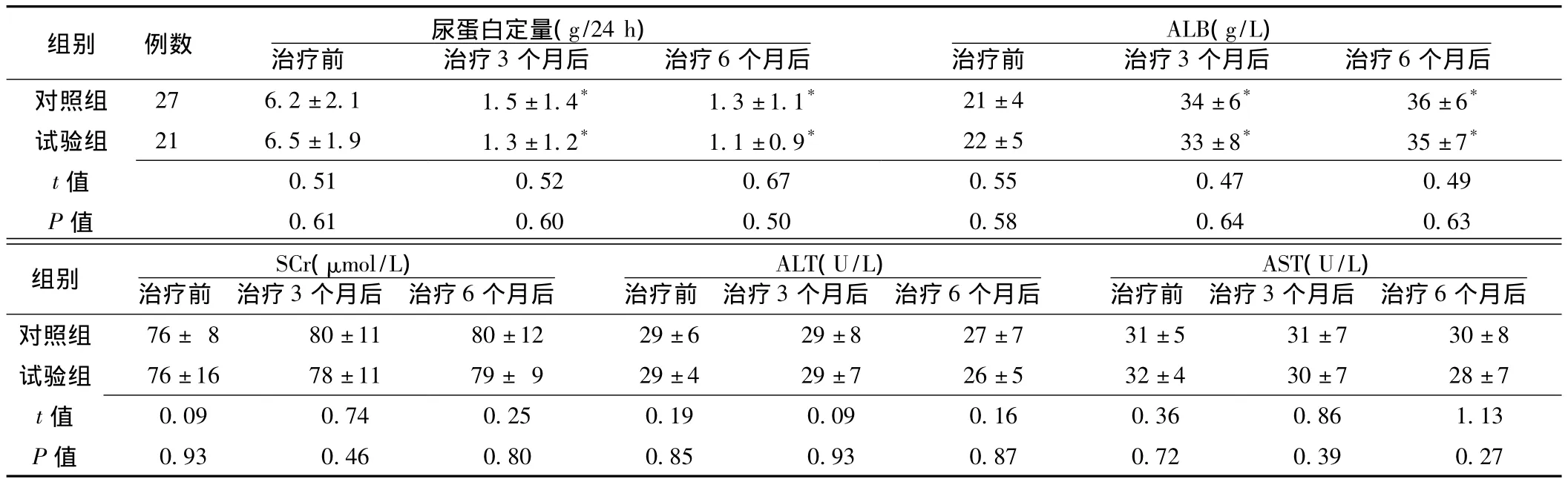
表1 治疗前、治疗3个月后及治疗6个月后2组患者临床指标比较 (±s)Table 1 Comparison of clinical index between the two groups before treatment,3 months and 6 months after treatment
注:与同组治疗前相比,*P<0.05;ALB=血清蛋白,SCr=血肌酐,ALT=丙氨酸氨基转移酶,AST=天冬氨酸氨基转移酶
组别 例数 尿蛋白定量(g/24 h)治疗前 治疗3个月后 治疗6个月后ALB(g/L)治疗前 治疗3个月后 治疗6个月后对照组 27 6.2±2.1 1.5±1.4* 1.3±1.1* 21±4 34±6* 36±6*试验组 21 6.5±1.9 1.3±1.2* 1.1±0.9* 22±5 33±8* 35±7*t 值0.51 0.52 0.67 0.55 0.47 0.49 P值 0.61 0.60 0.50 0.58 0.64 0.63组别 SCr(μmol/L)治疗前 治疗3个月后 治疗6个月后ALT(U/L)治疗前 治疗3个月后 治疗6个月后AST(U/L)治疗前 治疗3个月后 治疗6个月后对照组76± 8 80±11 80±12 29±6 29±8 27±7 31±5 31±7 30±8试验组 76±16 78±11 79± 9 29±4 29±7 26±5 32±4 30±7 28±7 t 值0.09 0.74 0.25 0.19 0.09 0.16 0.36 0.86 1.13 P值0.93 0.46 0.80 0.85 0.93 0.87 0.72 0.39 0.27
表2 治疗1周后、治疗1个月后及治疗3个月后2组患者CsA全血浓度和给药剂量比较 (±s)Table 2 Comparison of dosage and whole blood concentration of CsA between the two groups 1 week,1 months and 3 months after treatment
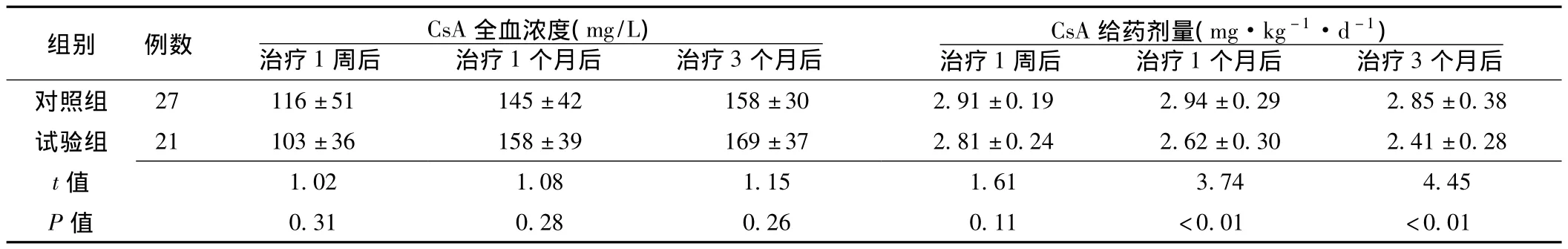
表2 治疗1周后、治疗1个月后及治疗3个月后2组患者CsA全血浓度和给药剂量比较 (±s)Table 2 Comparison of dosage and whole blood concentration of CsA between the two groups 1 week,1 months and 3 months after treatment
注:CsA=环孢素A
组别 例数 CsA全血浓度(mg/L)治疗1周后 治疗1个月后 治疗3个月后CsA 给药剂量(mg·kg-1·d-1)治疗1周后 治疗1个月后 治疗3个月后对照组 27 116±51 145±42 158±30 2.91±0.19 2.94±0.29 2.85±0.38试验组 21 103±36 158±39 169±37 2.81±0.24 2.62±0.30 2.41±0.28 t 值1.02 1.08 1.15 1.61 3.74 4.45 P值0.31 0.28 0.26 0.11 <0.01 <0.01
2.2 治疗1周后、治疗1个月后及治疗3个月后2组患者CsA全血浓度和给药剂量情况 治疗1周后、治疗1个月后及治疗3个月后,2组患者CsA全血浓度比较,差异无统计学意义 (P>0.05)。治疗1周后,2组患者CsA给药剂量比较,差异无统计学意义 (P>0.05);治疗1个月后和治疗3个月后,2组患者CsA给药剂量比较,差异有统计学意义 (P<0.05,见表2)。
2.3 2组患者的临床疗效和不良反应情况 随访6个月后,对照组完全缓解、部分缓解及未缓解的患者比例分别为33.3%(9/27)、37.0%(10/27)及29.6%(8/27);试验组完全缓解、部分缓解及未缓解的患者比例分别为38.1%(8/21)、33.3%(7/21)及28.6%(6/21);2组均无复发患者。2组患者的临床治疗有效率分别为70.3% (19/27)和71.4%(15/21),差异无统计学意义 (χ2=0.01,P>0.05)。随访期间,试验组有1例患者出现多毛症状,对照组有1例患者出现牙龈增生症状,但均未影响治疗。
3 讨论
临床上80%的IMN表现为肾病综合征。临床肾病症状完全缓解,常预示长期肾脏存活率和患者生存率较高,部分缓解也可显著降低终末期肾脏病风险。因此,治疗IMN的首要目的是诱导蛋白尿的持续减少[5]。CsA是由11个氨基酸组成的环形多肽,来源于土壤霉菌,是有选择性的强效免疫抑制剂。1979年起被广泛应用于器官移植和自身免疫性疾病的治疗[6],近年来也被应用于难治性肾病综合征和其他肾脏疾病的治疗。以CsA和他克莫司为主要代表的钙调磷酸酶抑制剂(calcineurin inhibitor,CNI)类药物治疗IMN临床疗效较好,改善全球肾脏病预后组织 (KDIGO)临床实践指南将CNI类药物推荐为IMN的初始治疗替代方案[7]。
CsA的临床疗效较为肯定,仍被用作替代药物的部分原因在于其不良反应,尤其是肝肾毒性。CsA的治疗效果、毒性反应与给药剂量和血药浓度相关,安全范围较窄。临床治疗中,成人CsA给药剂量若达到5 mg·kg-1·d-1,即使血药浓度低于治疗窗,增加CsA的给药剂量也会增加毒性[6]。在应用CsA治疗IMN的过程中,若能既达到有效血药浓度,又可以减少其给药剂量,就可以减少CsA的不良反应,拓宽其应用前景。CsA在肝内通过CYP3A同工酶代谢,因此抑制CYP3A代谢的药物可抑制CsA的代谢,使CsA血药浓度升高[8]。
五酯胶囊由中药华中五味子果实中提取的木脂素衍生物精制而成,主要成分为五味子甲素。国内外研究表明,五味子甲素可抑制 CYP3A 活性[9-12]。Xin 等[13]研究发现,五酯胶囊可提升CNI类药物的血药浓度。任苗苗等[14]应用五酯胶囊联合他克莫司对IMN患者进行治疗,发现五酯胶囊可以减少他克莫司的给药量。Qin等[15]通过研究证实,长期口服五酯胶囊联合泼尼龙对CYP3A酶活性的综合作用表现为抑制效应。刘永光等[16]对肾功能稳定的肾移植患者进行研究,发现五酯胶囊可以提升CsA的血药浓度,减少CsA的给药剂量。本研究结果显示,早晚各服用2粒五酯胶囊能够提升患者CsA的全血浓度,减少患者CsA的使用剂量。随访6个月,2组患者的临床治疗有效率相当,各项肝肾功能的指标比较,差异无统计学意义。说明五酯胶囊可提升IMN患者的CsA全血浓度,减少其CsA服用量。这可能是因为五酯胶囊对CYP3A有抑制作用,延缓了CsA在体内的代谢。五酯胶囊作为护肝药物在临床治疗中被广泛应用,但本研究中2组患者的ALT水平差异无统计学意义,可能是因为CsA导致的肝功能损害发生率较低,且本研究样本量较小,不足以明确应用五酯胶囊是否可以降低CsA对肝功能的损害风险。
综上所述,对IMN患者采用CsA联合五酯胶囊治疗,能明显提升CsA的全血浓度,减少患者CsA给药剂量,减轻患者经济负担。但其长期效果如何,仍需进行大规模的前瞻性研究。本研究的局限性:(1)纳入患者的病理分型均为膜性肾病Ⅱ期,研究结论是否可推广至其他病理分期尚不可知;(2)未能明确CsA联合五酯胶囊治疗,对肾功能异常IMN患者CsA血药浓度、临床疗效和不良反应的影响。
[1]Xia WL,Li MX,Zheng FL.Application of cyclosporin A in different pathological types of primary nephrotic syndrome[J].Chinese Journal of Nephrology,2009,25(3):251-253.(in Chinese)
夏文丽,李明喜,郑法雷.环孢素A在不同病理类型原发性肾病综合征治疗中的应用 [J].中华肾脏病杂志,2009,25(3):251-253.
[2]Wu XC,Xin HW,Yu AR,et al.Cyclosporine A and CYP3A [J].The Chinese Journal of Clinical Pharmacology,2001,17(1):72-75.(in Chinese)
吴笑春,辛华雯,余爱荣,等.环孢素A与CYP3A[J].中国临床药理学杂志,2001,17(1):72-75.
[3]Xin HW,Li Q,Wu XC,et al.Evaluation the effects and cost on the application of tacrolimus combination with Wuzhi-capsule in renal transplanted recipients[J].The Chinese JournalofClinical Pharmacology,2011,27(4):295 -298.(in Chinese)
辛华雯,李罄,吴笑春,等.五酯胶囊与他克莫司合用对肾移植受者的成本与效果评估研究 [J].中国临床药理学杂志,2011,27(4):295-298.
[4]Glassock RJ.Diagnosis and natural course of membranous nephropathy[J].Semin Nephrol,2003,23(4):324 -332.
[5]Beck L,Bomback AS,Choi MJ,et al.KDOQI US commentary on the 2012 KDIGO clinical practice guideline for glomerulonephritis[J].Am J Kidney Dis,2012,62(3):403 -441.
[6]环孢素A在肾内科应用专家协作组.环孢素A治疗肾小球疾病的应用共识 [J].中国血液净化,2007,6(7):393-395.
[7]Hofstra JM,Fervenza FC,Wetzels JF.Treatment of idiopathic membranous nephropathy [J].Nat Rev Nephrol,2013,9(8):443-458.
[8]Li Q,Wu XC,Xin HW,et al.Clinical study on increased blood concentration of cyclosporin A by berberine hydrochloride in renal transplanted recipients [J].Chinese Journal of Organ Transplantation,2001,22(4):209-211.(in Chinese)
李罄,吴笑春,辛华雯,等.盐酸小檗碱对肾移植受者环孢素A血浓度的影响 [J].中华器官移植杂志,2001,22(4):209-211.
[9]Qiangrong P,Wang T,Lu Q,et al.Schisandrin B——a novel inhibitor of P -glycoprotein[J].Biochem Biophys Res Commun,2005,335(2):406-411.
[10]Sun M,Xu X,Lu Q,et al.Schisandrin B:a dual inhibitor of P-glycoprotein and multidrug resistance-associated protein 1[J].Cancer Lett,2007,246(1-2):300-307.
[11]Wan CK,Zhu GY,Shen XL,et al.Gomisin A alters substrate interaction and reverses P-glycoprotein-mediated multidrug resistance in HepG2 - DR cells[J].Biochem Pharmacol,2006,72(7):824-837.
[12]Iwata H, Tezuka Y, Kadota S, et al.Identification and characterization of potent CYP3A4 inhibitors in Schisandra fruit extract[J].DrugMetabDispos,2004,32(12):1351-1358.
[13]Xin HW,Wu XC,Li Q,et al.Effects of Schisandra sphenanthera extract on the pharmacokinetics of tacrolimus in healthy volunteers[J].Br J Clin Pharmacol,2007,64(4):469 -475.
[14]任苗苗,吴琼,杜玄一,等.五酯胶囊联合他克莫司对膜性肾病的疗效[J].中华肾脏病杂志,2013,29(2):141.
[15]Qin XL,Yu T,Li LJ,et al.Effect of long - term co -administration of Wuzhi tablet(Schisandra sphenanthera extract)and prednisone on the pharmacokineticsoftacrolimus [J].Phytomedicine,2013,20(3-4):375-379.
[16]刘永光,郭颖,李留洋,等.五酯胶囊对肾移植受者环孢素全血浓度的影响 [J].广东医学,2010,31(5):641-642.

