气相色谱法同时测定制药企业废气中多种挥发性有机物
冯 媛,吕 溪,姜建彪,宋 玉,任爱玲,杨丽丽
1.石家庄市环境监测中心,河北 石家庄 050022 2.河北科技大学环境科学与工程学院,河北 石家庄 050018
气相色谱法同时测定制药企业废气中多种挥发性有机物
冯 媛1,吕 溪2,姜建彪1,宋 玉2,任爱玲2,杨丽丽1
1.石家庄市环境监测中心,河北 石家庄 050022 2.河北科技大学环境科学与工程学院,河北 石家庄 050018
针对典型制药产品青霉素、阿莫西林、维生素C、对乙酰氨基酚生产过程的挥发性有机物(VOCs)排放特点,建立了吸附-解吸-气相色谱法同时检测制药企业废气中丙酮、乙酸乙酯、异丙醇、苯、甲苯、乙酸丁酯和正丁醇等7种特征VOCs的分析方法。采用活性炭采样管采样-二硫化碳解吸-毛细管色谱柱分离,在解吸时间30 min、柱温35 ℃保持6 min、30 ℃/min速率升温到200 ℃保持2 min的色谱分析条件下,各挥发性有机物可以实现良好的分离;7种物质标准曲线相关系数为0.999 8~0.999 9,相对标准偏差为1.1%~3.2%,检出限为0.004 mg/m3~0.014 mg/m3,7种物质的解吸效率为83.1%~105.1%。结果表明,该方法适用于典型制药企业固定污染源排放废气中特征VOCs的测定。
气相色谱法;制药企业废气;挥发性有机物;吸附;解吸
挥发性有机物(VOCs)是一类有机化合物的统称,通常是指在常压下沸点低于260 ℃或室温时饱和蒸气压大于71 Pa的有机化合物[1]。其危害主要表现在2个方面:一是严重危害人体健康;二是VOCs在一定条件下可产生光化学烟雾,破坏大气臭氧层,导致大气酸性化[2]。制药企业由于在生产过程中经常要使用大量有机溶剂,因此外排尾气中VOCs种类较多,而且溶剂挥发导致在生产的各个环节会产生大量VOCs污染[3],成为大气中VOCs的主要污染源之一。
课题组前期对8家典型的发酵类和化学合成类制药企业的溶剂使用状况进行了调研和监测,初步研究成果表明,青霉素工业盐、维生素C、维生素B12、阿莫西林等典型产品生产过程排放的废气中特征VOCs主要为丙酮、异丙醇、乙酸乙酯、乙酸丁酯、正丁醇、苯、甲苯等。目前我国VOCs污染防治基础较为薄弱,技术标准体系不健全,国内VOCs的相关监测方法尚不能满足同时监测制药企业废气中多种VOCs的要求,如:用于测定环境空气中VOCs(以罐采样/GC-MS法和热脱附/GC-MS法为主)的监测方法[4-5],由于设备昂贵、监测成本高、资金力量相对薄弱的县、市级基层环境监测机构难于普及,不便于常规监测分析,且方法主要适用于环境空气中微量或痕量VOCs的测定,对于高浓度的制药工业废气适用性较差;针对工业废气和工作场所特定VOCs的监测[6-8],以及单项采样、单项分析的国家标准等[9-12],存在对制药企业的针对性不强的问题。
为此,该文建立了使用活性炭采样管采样-二硫化碳解吸-毛细管柱气相色谱法定性定量分析丙酮、乙酸乙酯、异丙醇、苯、甲苯、乙酸丁酯和正丁醇等制药企业废气中特征VOCs的方法。该方法应用于制药企业废气中特征VOCs的测定,具有操作方便快捷、节省时间等优点,取得了满意的效果。
1 实验部分
1.1 仪器与试剂
Agilent 6890N气相色谱仪,配有FID检测器;GH-1型活性炭采样管(6 mm×80 mm,溶剂解吸型,分A、B段,A段100 mg活性炭,B段50mg活性炭);天平;微量注射器(5 μL,10 μL,100 μL);具塞试管(5 mL);LH-1智能空气微尘/气体采样器。
标准品:丙酮(色谱纯)、异丙醇(色谱纯)、乙酸乙酯(色谱纯)、乙酸丁酯(色谱纯)、乙醇(优级纯)、正丁醇(优级纯),二硫化碳中苯(1 000 μg/mL),二硫化碳中甲苯(1 000 μg/mL);二硫化碳(色谱纯);高纯氮气(>99.999%);氢气(>99.999%)。
1.2 标准储备液的配制
标准储备液:10 mL容量瓶中加入5 mL的二硫化碳,在恒温恒湿(25 ℃,相对湿度50%)条件下准确称重后,向其中依次加入丙酮7.78 mg、乙酸乙酯8.80 mg、异丙醇7.81 mg、乙酸丁酯8.78 mg、正丁醇8.10 mg, 用二硫化碳定容至刻度线,得到标准储备液,各物质质量浓度:丙酮778 μg/mL,乙酸乙酯880 μg/mL,异丙醇781 μg/mL,乙酸丁酯878 μg/mL,正丁醇810 μg/mL;另有二硫化碳中苯(1 000 μg/mL)和二硫化碳中甲苯(1 000 μg/mL)的标准物质。
1.3 样品处理
1.3.1 样品采集与保存
采样现场将活性炭采样管两端敲开,用连接管将采样管A段与采样仪器的采样管连接,B段与仪器的流量计量箱和抽气泵连接,以0.2~0.6 L/min的流量采气,采样时长可根据实际情况调整,废气中目标化合物含量越高采样时间越短,一般以10~60 min为宜。采样完毕,将采样管两端快速密封,尽快送回实验室,并于8 h内进行分析[13]。若不能及时分析,应避光密闭、-20 ℃低温保存,保存期限7 d。采集样品的同时采集空白样品。
1.3.2 样品解吸
将活性炭采样管的A段和B段分别取出,放入磨口具塞试管中,再向试管中准确加入1.00 mL二硫化碳,盖紧塞子,振摇1 min,控制解吸时间30 min。摇匀,解吸液转移至气相进样小瓶,准备用气相色谱仪进行测定。
1.4 色谱分析条件
HP-INNOWAX型毛细管色谱柱(30 m×250 μm×0.25 μm)。
柱温:在35 ℃下保持6 min,以30 ℃/min速率升温至200 ℃,保持2 min。柱流量1.0 mL/min,进样口温度250 ℃,检测器温度300 ℃,尾吹气流量25 mL/min,氢气流量30 mL/min,空气流量300 mL/min,进样量1 μL。
2 结果与讨论
2.1 色谱分析条件的选择
制药生产中乙醇被经常使用,实验中发现乙醇会干扰异丙醇和苯的测定。通过改变色谱柱温条件,来消除乙醇的干扰。
图1为柱温条件:50 ℃保持6 min,以30 ℃/min速率升温至200 ℃,保持2 min,其他条件同第1.4节,可见异丙醇、乙醇的分离度较差(1.26),乙醇和苯的分离度为3.57,乙醇对异丙醇存在干扰。调整初始柱温条件为35 ℃,按照第1.4节中的条件进行实验,色谱图如图2所示,异丙醇和乙醇的分离度为1.64,乙醇和苯的分离度为2.03。按照第1.4节的条件,乙醇、异丙醇和苯可以实现良好的分离。

图1 初始柱温50 ℃时的分离情况
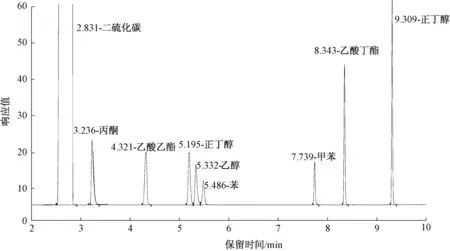
图2 初始柱温35 ℃时的分离情况
2.2 线性关系、检出限和测定下限
分别取标准储备溶液以及苯和甲苯的标准物质10、20、50、100、150、200 μL至10 mL容量瓶中,并用二硫化碳定容至刻度线,得到系列标准溶液进行测定。以峰面积为纵坐标,以各目标挥发性有机物的浓度为横坐标绘制标准曲线,各目标化合物浓度和峰面积的线性关系良好,相关系数均大于0.999,各组分线性回归方程及相关系数见表1。
向活性炭管中加入适量各目标化合物标准物质(以解吸后浓度是预估方法检出限的2~5倍为宜),封闭活性炭管,放置,使其充分吸附。将活性炭采样管的A、B段按第1.3.2节的条件用二硫化碳解吸,再用气相色谱测定。分别进行7次平行测定,计算测定结果的标准偏差,按公式MDL=t(n-1, 0.99)×S计算检出限[14]。计算样品采气量为10 L时的方法检出限,以4倍检出限作为测定下限,具体见表1。
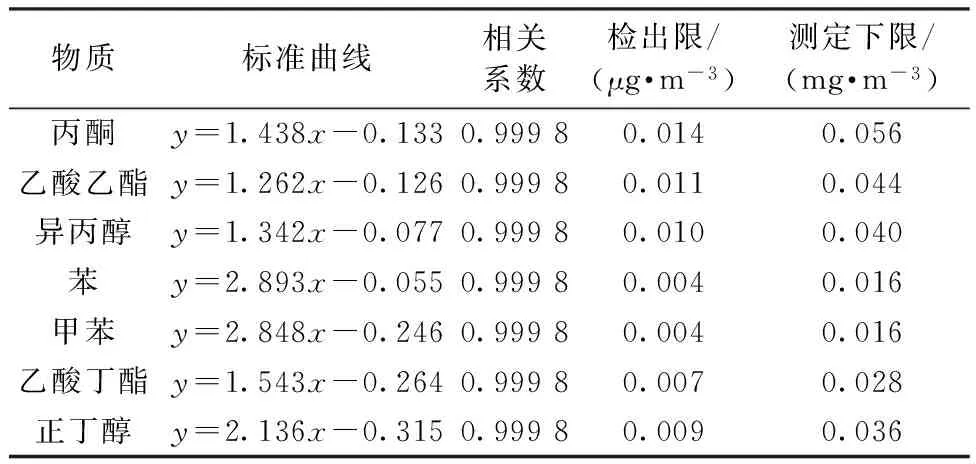
表1 标准曲线及检出限、测定下限
2.3 精密度
在标准系列的测定范围内选择低、中、高3个浓度点,分别进行6次测定,根据测定结果计算相对标准偏差,结果见表2。7种目标化合物的相对标准偏差为1.1%~3.2%,精密度良好。

表2 目标化合物的精密度
2.4 解吸效率
取9支活性炭采样管,每3支一组,分为3组,分别向每组采样管A段中加入低、中、高3个浓度的混合标准储备溶液和苯、甲苯储备溶液,封闭活性炭管,放置过夜,使其充分吸附。分别将上述活性炭采样管的A、B段按第1.3.2节的条件用二硫化碳解吸,再用气相色谱进行分析。以活性炭采样管A段中目标化合物的含量和加标量的比值作为解吸效率。低、中、高浓度样品的解吸效率见表3。各目标化合物的解吸效率均在80%以上,满足测定的需要[15]。

表3 目标化合物的解吸效率
2.5 解吸时间
取12支活性炭采样管,每3支一组,分为4组,分别向每组采样管A段中加入相同浓度的混合标准储备溶液和苯、甲苯储备溶液,封闭活性炭管,放置过夜,使其充分吸附。再分别将上述4组活性炭采样管用1.0 mL二硫化碳解吸10、20、30、60 min,再用气相色谱进行分析。考察不同解吸时间下样品的解吸效率,结果见表4。
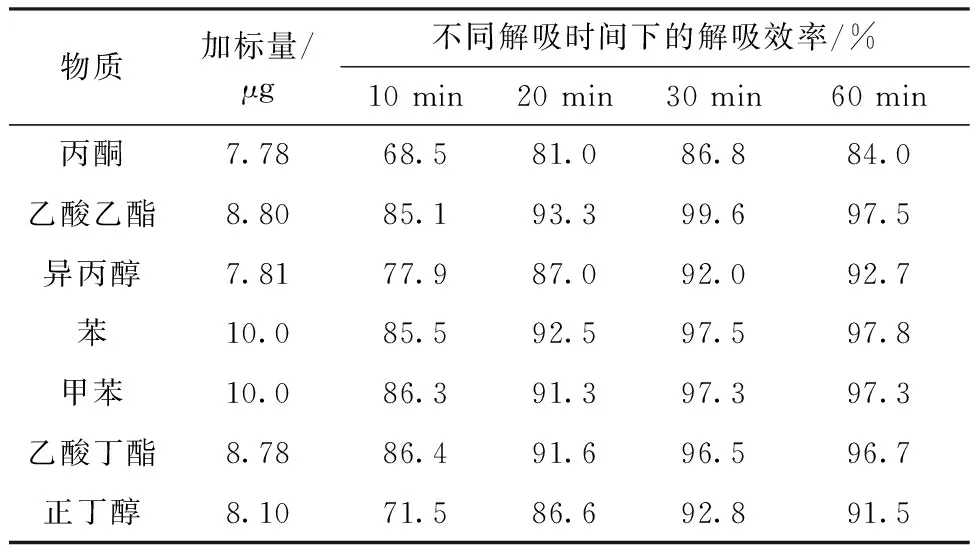
表4 不同解吸时间下目标化合物的解吸效率
由表4可见,当解吸时间从10 min逐渐增至30 min时,解吸效率逐渐提高。解吸时间为30 min和60 min的样品,解吸效率相差很小(均在3%以内),而且由于误差的影响,对于某些物质60 min的解吸效率甚至低于30 min的解吸效率。所以30 min的解吸时间即可满足分析需要,选择30 min为最优解吸时间。
2.6 实际样品测定
应用该方法分析某制药企业青霉素工业盐提纯结晶车间排气筒的废气样品,以0.5 L/min的流量采样20 min。采集样品的同时采集全程序空白样品,同时测定,分析结果见表5。同批次进行空白加标分析,得出解吸效率,见表5。从表5可见,该车间排放的废气中含量最高的是乙酸乙酯,其次是丙酮、乙酸丁酯和正丁醇,苯和甲苯有微量检出,未检出异丙醇。全程序空白样品未检出各目标化合物,同批次的空白加标样品解吸效率均在85%以上。
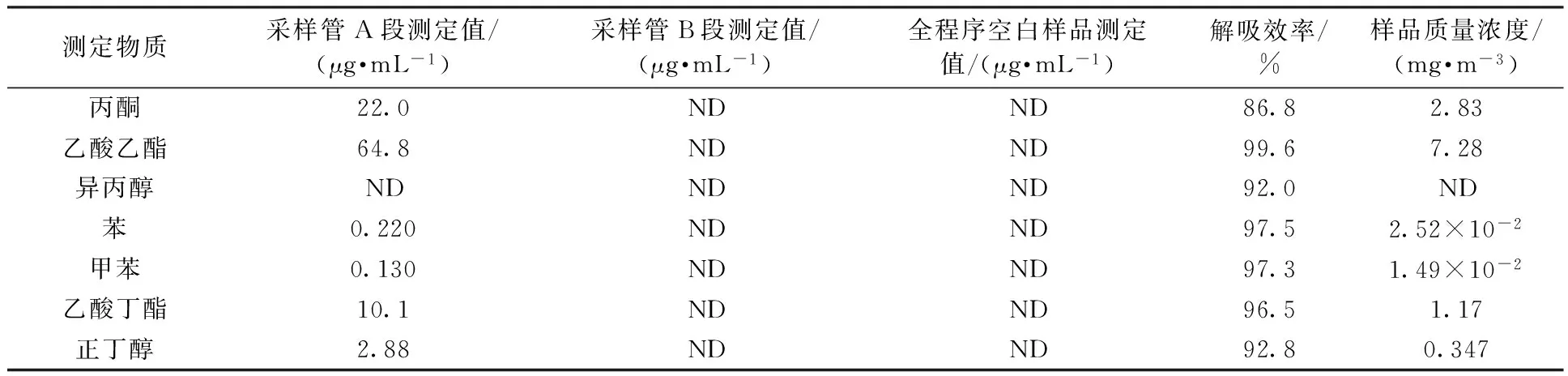
表5 样品分析结果
注:“ND”表示未检测到该物质。
该车间为青霉素工业盐的结晶提纯车间,生产流程:发酵得到的青霉素滤液在酸性条件下用乙酸丁酯进行反复萃取、转移、分离,将青霉素提取到乙酸丁酯中,再经过水洗后进入冷冻脱色罐,并向其中加入活性炭脱色。之后用乙酸丁酯进行碱化萃取,再加入正丁醇进行共沸结晶;得到的结晶液过滤,滤出的晶体用正丁醇洗涤两次,洗后的晶体再用乙酸乙酯结晶提纯后造粒,进入干燥器得到青霉素工业盐。可见该车间的主要VOCs排放物为乙酸乙酯、乙酸丁酯、正丁醇,这与监测结果比较吻合,表明方法准确可靠,满足分析要求,可用于制药企业废气中特征VOCs的测定。
3 结论
活性炭采样管吸附采样,二硫化碳解吸后,用毛细管柱气相色谱法同时测定制药企业废气中的特征VOCs(丙酮、正丁醇、异丙醇、乙酸乙酯、乙酸丁酯、苯和甲苯),方法操作方便简捷,线性响应好,考察了方法的最佳解吸时间,解吸时间30 min即可满足测定要求,可节省一定的分析时间。重点考察了方法的检出限、精密度、解吸效率等性能指标,结果均较为满意。方法可以用于制药企业废气中特征VOCs的测定。
[1] 羌宁.城市空气质量管理与控制[M].北京:科学出版社,2003:201.
[2] 刘亚敏,付智娟.可挥发性有机化合物治理技术及研究进展[J].江西化工,2006(1):23-26.
[3] 沈伯雄,胡国丽,李冬倩,等.我国青霉素钾盐特征VOCs的挥发损失估算[J].中国环境科学,2012,32(12):2 134-2 139.
[4] 魏复盛,滕恩江,池靖,等.空气和废气监测分析方法[M].4版.北京:中国环境科学出版社,2003.
[5] HJ 644—2013 环境空气 挥发性有机物的测定 吸附管采样-热脱附/气相色谱-质谱法[S].
[6] 孟成名,秦文华,张瑞芹.工作场所空气中丙酮、异丙醇、乙酸丁酯、三氯甲烷、乙苯、二甲苯气相色谱同时测定法[J].工业卫生与职业病,2012,38(6):372-374.
[7] 肖学喜,何桂英,雷迅,等.气相色谱法测定工业废气中的异丙醇[J].中国环境监测,2012,28(6):58-61.
[8] 杨丽莉,纪英,胡恩宇.毛细管气相色谱法同时测定空气和废气中多种常见有机污染物[J].现代科学仪器,2006(4):73-75.
[9] GBZ/T 160.55—2007 工作场所空气有毒物质测定脂肪族酮类化合物 丙酮、丁酮和甲基异丁基甲酮的溶剂解吸-气相色谱法[S].
[10] GBZ/T 160.48—2007 工作场所空气有毒物质测定 醇类化合物 甲醇、异丙醇、丁醇、异戊醇、异辛醇、糠醇、二丙酮醇、丙烯醇、乙二醇和氯乙醇的溶剂解吸-气相色谱法[S].
[11] GBZ/T 160.63—2007 工作场所空气有毒物质测定饱和脂肪族酯类化合物 甲酸酯类、乙酸酯类和1、4-丁内酯的溶剂解吸-气相色谱法[S].
[12] HJ 583—2010 环境空气苯系物的测定 固体吸附/热脱附-气相色谱法[S].
[13] HJ 584—2010 环境空气 苯系物的测定 活性炭吸附/二硫化碳解吸-气相色谱法[S].
[14] HJ 168—2010 环境监测 分析方法标准制修订技术导则[S].
[15] GBZ/T 160—2007 工作场所有毒物质测定标准方法[S].
Simultaneous Determination of Multiple VOCs in Waste Gas of Pharmaceutical Industry by Gas Chromatography
FENG Yuan1,LYU Xi2,JIANG Jian-biao1,SONG Yu2,REN Ai-ling2,YANG Li-li1
1.Shijiazhuang Environmental Monitoring Centre,Shijiazhuang 050022,China 2.School of Environmental Science & Engineering Hebei University of Science & Technology,Shijiazhuang 050018,China
Directing at emission characteristics of VOCs in the production process of typical pharmaceutical products such as penicillin, amoxicillin, vitamin C and 4-acetamidophenol, the analytical method for simultaneous determination of seven characteristic VOCs as acetone, ethyl acetate, isopropyl alcohol, benzene, toluene, ethyl acetate and n-butanol in waste gas of pharmaceutical industry by adsorption-desorption-GC method was established. Using activated charcoal adsorption to sample- carbon disulfide to desorb-capillary chromatographic column to separate, under the analytical conditions of maintaining the column temperature at 35 ℃ for 6 minutes and raising the temperature at the rate of 30 ℃ per minute to 200 ℃ and maintaining for 2 minutes, each volatile organic compounds can actualize good separation; the correlation coefficients of the calibration curve were from 0.999 8 to 0.999 9, relative standard deviations were from 1.1% to 3.2%, and detection limits were from 0.004 mg/m3to 0.014 mg/m3, and the desorption efficiency of seven compounds were from 83.1% to 105.1%. The result demonstrated that the method was suitable for the determination of VOCs of the stationary source emission of typical pharmaceutical industry.
Gas Chromatography;waste gas of pharmaceutical industry;VOCs;adsorption;desorption
2013-11-01;
2014-04-10
环境保护公益性行业科研专项“制药行业VOCs与恶臭控制技术政策研究”(201109004)
冯 媛(1982-),女,河北石家庄人,硕士,工程师。
X830.2
A
1002-6002(2015)01- 0104- 05

