HPLC法研究灯盏细辛注射液对水杨酸排泄的影响
戴国梁,李长印,孙冰婷,丁 康,刘史佳,居文政
(1.南京中医药大学附属医院临床药理科,江苏 南京 210029; 2.南京中医药大学药学院,江苏 南京 210029;3.南京中医药大学附属第三医院急诊科,江苏 南京 210001)
◇研究简报◇
HPLC法研究灯盏细辛注射液对水杨酸排泄的影响
戴国梁1,李长印1,孙冰婷2,丁 康3,刘史佳1,居文政1
(1.南京中医药大学附属医院临床药理科,江苏 南京 210029; 2.南京中医药大学药学院,江苏 南京 210029;3.南京中医药大学附属第三医院急诊科,江苏 南京 210001)
近年来,阿司匹林抗血小板聚集活性逐渐成为其临床主要应用领域[1-2],是心血管疾病方面一线药物。临床上,阿司匹林常与灯盏细辛注射液(DI)、脉络宁注射液等中药制剂合用,用于治疗心脑血管疾病,并取得了良好的疗效[3-4]。
研究表明,阿司匹林的消除半衰期短,约为7~12 min,难以测到阿司匹林的体内过程,因此常测定其代谢物水杨酸的浓度变化来研究体内阿司匹林的药动学过程[5-6]。
水杨酸在大鼠体内的排泄研究及DI对水杨酸排泄的影响未见报道。阿司匹林与DI长期合用可能导致体内水杨酸的蓄积,而体内水杨酸浓度升高将导致不良反应[7-8]。
本文以水杨酸为指标,探讨DI对大鼠体内水杨酸排泄的影响,为DI与阿司匹林合用的安全性提供理论支持。
1 材料与方法
1.1 仪器Waters 2695/2487高效液相色谱仪(美国Waters公司);Biofuge PrimoR冷冻高速离心机(德国Heraeus公司);WH-2微型旋涡混合仪(上海沪西分析仪器厂)。
1.2 试剂与药品灯盏细辛注射液(DI)(云南生物谷灯盏花药业有限公司,批号:20120740);阿司匹林肠溶片(沈阳奥吉娜药业有限公司,批号:120502);对照品水杨酸(中国食品药品检定研究院,批号:100106-200303);对照品非那西丁(Sigma公司,批号:048K1586)。
1.3 尿液的收集SD大鼠,♂,12只,体质量250~270 g,由南京中医药大学实验动物中心提供,合格证号:SCXK(浙)2008-0033。给药前禁食12 h,自由饮水。大鼠随机平均分成2组(单独和联合给药组),置于代谢笼中适应5 d,收集尿液作为空白样品。联合给药组先尾静脉注射DI 4 mL·kg-1,后立即灌胃阿司匹林10 mg·kg-1;单独给药组只灌胃阿司匹林10 mg·kg-1。自给药时起,收集0~4、4~8、8~12、12~24、24~48、48~72 h的尿液,并记录体积,-40 ℃保存待测。
1.4 色谱条件Agilent ZORBAX SB-C18色谱柱(4.6 mm×150 mm,5 μm);检测波长237 nm;流速1.0 mL·min-1;柱温40 ℃;流动相为乙腈-0.2%H3PO4=30 ∶70;进样量20 μL。
1.5 对照品溶液的制备精密称取水杨酸对照品10.8 mg于10 mL量瓶中,甲醇定容,得1.08 g·L-1的水杨酸储备液。精密称取非那西丁对照品10.2 mg于10 mL量瓶中,甲醇定容,得1.02 g·L-1的非那西丁储备液。精密移取适量用甲醇稀释成102 mg·L-1的非那西丁内标溶液。
1.6 尿液样品处理取尿样1 mL,加入内标(102 mg·L-1)20 μL,1 mol·L-1盐酸500 μL,旋涡1 min,加入乙酸乙酯4 ml,振荡5 min,4 000 r·min-1离心10 min。吸取上清液,置于离心浓缩仪45 ℃挥干,加100 μL 50%甲醇复溶,旋涡1 min,12 000 r·min-1离心10 min,取上清20 μL进样。
1.7 方法学考察按生物样品分析的相关要求,考察专属性、线性范围、定量限、精密度、准确度、提取回收率和样品稳定性。
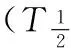
2 结果
2.1 方法学考察上述条件下,水杨酸、内标的保留时间分别约为5.22、4.12 min。各色谱峰峰形良好,无杂峰干扰,基线平稳。
水杨酸在0.42~54 mg·L-1范围内线性良好,定量限为0.42 mg·L-1。
按“1.6”项下制备水杨酸低、中、高3个浓度(尿液浓度为0.84、6.75、27 mg·L-1)的质控样品,进行提取回收率、精密度和准确度、稳定性试验。结果表明,水杨酸低、中、高3个浓度下的回收率分别为82.8%±3.2%、87.3%±5.2%和84.6%±4.5%;其日内、日间准确度分别为95.3%~102.5%(RSD≤6.8%,n=5)和93.1%~108.4%(RSD≤8.8%,n=15);经处理后的尿液样品室温放置24 h后水杨酸尿药浓度的RSD均小于8.83%,-40 ℃保存28 d的RSD均小于9.12%,经过3个冻融周期后的RSD均小于7.39%,以上结果均符合生物样品的测定要求。
2.2 大鼠尿液中水杨酸累积排泄百分率取不同时间段的尿样,按“1.6”项下方法操作,计算水杨酸的排泄量及累积排泄百分率。

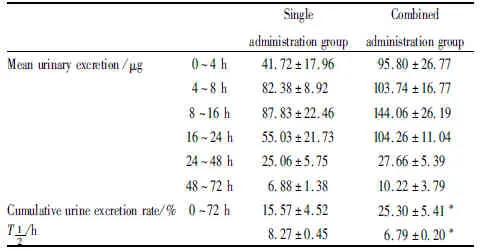
SingleadministrationgroupCombinedadministrationgroupMeanurinaryexcretion/μg0~4h41.72±17.9695.80±26.774~8h82.38±8.92103.74±16.778~16h87.83±22.46144.06±26.1916~24h55.03±21.73104.26±11.0424~48h25.06±5.7527.66±5.3948~72h6.88±1.3810.22±3.79Cumulativeurineexcretionrate/%0~72h15.57±4.5225.30±5.41*T12/h8.27±0.456.79±0.20*
*P<0.05vssingle administration group
3 讨论
水杨酸的蛋白结合率高达80%~90%,而DI中含有咖啡酸、绿原酸等酚酸类成分[9],化学结构与水杨酸相似,故其蛋白结合位点与水杨酸可能相同。大鼠给予DI后,酚酸类化合物可和血液中的血浆蛋白结合,抑制了后续吸收的水杨酸和血浆蛋白的结合,使大鼠体内游离水杨酸增多,加快水杨酸从大鼠体内排出,但确切的作用机制有待进一步研究。
[1] Rafferty M, Walters M R, Dawson J. Anti-platelet therapy and aspirin resistance-clinically and chemically relevant?[J].CurrMedChem, 2010, 17(36): 4578-86.
[2] Fitzgerald R, Pirmohamed M. Aspirin resistance: effect of clinical, biochemical and genetic factors[J].PharmacolTher, 2011, 130(2): 213-25.
[3] 张 凯. 脉络宁合用阿司匹林治疗重症缺血性脑卒中疗效观察[J]. 中华医药杂志, 2003, 3(8): 478-9.
[3] Zhang K. Efficacy of Mailuoning and aspirin in acute ischemic stroke[J].ChinJMed, 2003, 3(8): 478-9.
[4] 李 明, 赵高峰. 灯盏细辛注射液联合拜阿司匹林治疗急性脑梗死50例疗效观察[J]. 中国中医急症, 2010, 19(8): 1314-5.
[4] Li M, Zhao G F. 50 acute cerebral infarction cases treated by Dengzhanxixin injection combined with Bayaspirin[J].JEmergTraditlChinMed, 2010, 19(8): 1314-5.
[5] 周燕文, 陈 丽, 兰聪贤. 人血浆中水杨酸的测定及阿司匹林的人体药物动力学研究[J]. 华西药学杂志, 2008, 23(5): 572-4.
[5] Zhou Y W, Chen L, Lan C X. Determination of salicylic acid in plasma by HPLC- FLU and pharmacokinetics of aspirin in healthy volunteers[J].WestChinJPharSci, 2008, 23(5): 572-4.
[6] 陈卫东, 吕雄文,李 俊, 等. 卡托普利和低剂量阿司匹林在犬体内的药动学相互作用研究[J]. 中国药学杂志, 2005, 40(9): 696-8.
[6] Chen W D, Lü X W, Li J, et al. Pharmacokinetics interaction of captopril and low-dosage aspirin in dog[J].ChinPharmJ, 2005, 40(9): 696-8.
[7] 董素琴. 常量阿斯匹林治疗风湿性疾病致水杨酸中毒[J]. 甘肃医药, 1994, 13(4): 229-30.
[7] Dong S Q. Salicylic acid poisoning of constant aspirin for treating rheumatoid disease[J].GansuMedJ, 1994, 13(4): 229-30.
[8] 滑吉美. 水杨酸中毒的尿液监测方法[J]. 药物分析杂志, 1994, 14(6): 46-7.
[8] Hua J M. Monitoring method for salicylic acid poisoning in urine[J].JPharmAnal, 1994, 14(6): 46-7.
[9] 周 玲, 居文政, 刘子修, 等. 灯盏细辛注射液多成分血浆蛋白结合率测定[J]. 中国药理学通报, 2011, 27(5): 719-22.
[9] Zhou L, Ju W Z, Liu Z X, et al. Determination of plasma protein binding rate of multicomponent in Dengzhanxixin injection[J].ChinPharmacolBull, 2011, 27(5): 719-22.
HPLC studies on effect of Dengzhanxixin injection on excretion of salicylic acid in rats
DAI Guo-liang1, LI Chang-yin1, SUN Bing-ting2, DING Kang3, LIU Shi-jia1, JU Wen-zheng1
(1.DeptofClinicalPharmacology,AffiliatedHospitalofNanjingUniversityofTraditionalChineseMedicine,Nanjing210029,China; 2.CollegeofPharmacy,NanjingUniversityofTraditionalChineseMedicine,Nanjing210029,China; 3.DeptofEmergency,theThirdAffiliatedHospitalofNanjingUniversityofTraditionalChineseMedicine,Nanjing210001,China)
水杨酸;灯盏细辛注射液;阿司匹林;尿排泄;累积排泄率;高效液相色谱;大鼠
salicylic acid; Dengzhanxixin injection; aspirin; urinary excretion; cumulative excretion rate; HPLC; rat
时间:2015-3-16 15:41 网络出版地址:http://www.cnki.net/kcms/detail/34.1086.R.20150316.1541.030.html
2014-11-21,
2015-02-26
国家科技部“重大新药创制”科技重大专项(No 2012ZX09303009-002);江苏省中医药领军人才(No LJ200906);江苏高校优势学科建设工程资助项目(2010)
戴国梁 (1988-),男,硕士,研究方向:中药临床药代动力学, E-mail:daiguoliangdgl@163.com; 居文政 (1965-),男,教授,博士生导师,研究方向:中药临床药代动力学,通讯作者,Tel:025-86617141-60310,E-mail:wzhju333@163.com
10.3969/j.issn.1001-1978.2014.04.030
A
1001-1978(2015)04-0591-02
R-332;R282.71;R446.12;R969.1;R972.7

