碳纳米管在铝基复合材料中的热稳定性研究
马艳霞
(中国船舶重工集团公司 第七二五研究所,河南 洛阳 471000)
0 引言
铝及铝合金具有密度小、耐腐蚀和加工性能好等优点,随着航空航天、汽车制造等现代工业的发展,对这类材料的比强度、比刚度、耐磨性、耐热性和抗疲劳等力学性能提出了更高的要求。碳纳米管具有优异的力学性能和良好的热稳定性[1-4],且为纳米量级,以碳纳米管增强铝基复合材料为铝基复合材料性能的更进一步提高又提供了一个新的途径。碳纳米管的稳定性是决定其能否成功应用于复合材料增强体的关键之一,吕[5]等利用TG-DTA方法研究了碳纳米管在空气中的氧化性能和热稳定性。结果表明碳纳米管在617℃开始氧化。Tao等[6]发现多壁碳纳米管经过4h的振动研磨后,其封闭的两端部分被打开,随着研磨时间的增加,封闭端开口的数量也增加。Pierard等[7]研究发现碳纳米管在振动球磨2h时,能够使碳纳米管长径比显著减小,表面积增大,然而当球磨50h时,碳纳米管的管状结构完全破坏,并形成多层的多聚芳烃聚合物。在利用传统的制备方法制备石墨、碳纤维增强铝基复合材料中,碳与铝容易发生反应,生成脆性的界面反应产物,恶化复合材料的力学性能。碳纳米管是由层片的石墨卷曲面构成的管子,因此碳纳米管具有石墨的一些本征特性。到目前为止,研究碳纳米管与铝反应状况还很少见诸报道。因此系统地研究碳纳米管与铝的反应是有意义的。
1 实验材料及方法
实验所用的多壁碳纳米管由深圳市纳米港有限公司提供,其制备方法是流化床碳氢化合物催化裂解。表1为供给态的多壁碳纳米管的主要参数,基体选用北京有色研究院利用气体雾化成型制备的2024Al合金粉末,其化学成分如表2所示。利用德国耐弛Netzsch公司生产的STA449C差热扫描分析仪研究碳纳米管与铝的反应温度,测试样品尺寸为ø5mm×3mm,坩埚材料为 Al2O3;采用 philips X’pert衍射仪(XRD),利用Cu靶,电压40kV,电流30mA,扫描角 20°~90°,扫描速度 0.5deg/sec,用于碳纳米管复合材料物相鉴定;采用设备为Physical Electronics(PE)PHI-5700系统研究碳纳米管表面和复合材料中碳元素的化学态。复合材料试样采用Philips CM-12型透射电子显微镜(TEM)观察并进行电子衍射分析,加压电压均为120kV。

表1 多壁碳纳米管主要参数

表2 复合材料基体的化学成分/wt%
2 结果与讨论
2.1 碳纳米管与铝反应的热力学与动力学分析
图1为石墨与铝的二元系相图,由图可见在1500℃下,石墨在铝中的溶解度极小(<0.05%),另外当温度高于500℃时,石墨就可能与铝发生化学反应形成铝碳化物(Al4C3相)。由于石墨与铝不润湿,其接触角θ为157°,即使在1000℃时,仍大于90°。石墨与铝反应的化学方程式如式(1)、(2)、(3)所示。
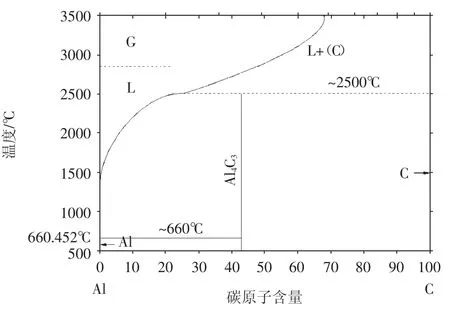
图1 石墨与铝的二元相图[7]

式中:ΔG——吉布斯自由能;
T——绝对温度。
由式(1)、(2)可知,从室温到 2000K 温度范围内,铝与碳反应生成Al4C3的标准生成自由能都为负值,因此,从热力学上讲,碳纳米管与铝从室温到2000K温度范围内均可能发生化学反应生成Al4C3相。然而Al4C3是不稳定化合物,可视为成分要在一定范围内变化的碳在铝中固溶体。铝与碳在低温下开始反应,但反应速度非常缓慢;随着温度的升高,反应越来越剧烈,生成的Al4C3也逐渐增多。
从动力学来说,碳与铝反应的界面反应层厚度满足式(4)关系[8]:
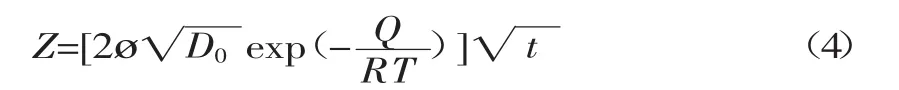
式中:Z——界面反应层厚度;
D0——扩散系数;
Q——反应激活能;
R——气体常数;
T——温度;
t——时间;
ø——依赖于碳在界面浓度的系数。
由式(4)可知,界面反应厚度与反应温度以及反应时间有关。反应温度越高,反应时间越长,则界面反应层就越厚。因此,为了避免碳纳米管与铝基体发生强烈的化学反应,在制备复合材料过程中,应尽量降低制备温度,同时减小高温停留时间。
2.2 碳纳米管与铝反应的状况分析

图2 2024Al和混合粉末的DSC曲线
由于碳为轻量元素,为了便于实验仪器检测碳纳米管的存在,采取在试验中增加碳纳米管的含量。在本文中,DSC混合粉末样品中碳纳米管的含量为10vol%。图2为2024Al粉末与混合粉末的DSC连续升温曲线。由图2可见,2024Al粉末在656.3℃左右出现了一个吸热峰,这个吸热峰为铝的熔化峰。然而在混合粉末中,除了在656.3℃左右出现了一个吸热峰外,还在672.9℃左右出现了一个放热峰。由图2可知,2024Al的初熔温度和熔化结束温度分别为775K和911K,根据式(3)可得在这两个温度下,碳和铝反应的吉布斯自由能分别为-61721.35kJ·mol-1和-59692.849kJ·mol-1,均小于零。因此从热力学上分析,碳纳米管与铝的反应是可能进行的,由于碳与铝的反应为放热反应,故图2中混合粉末中的放热峰可能是碳纳米管与铝反应的放热峰。为了进一步确定反应产物,对DSC试验后的混合粉末进行XRD和TEM分析。图3为不同粉末的XRD图谱,从2024Al粉末图谱上可见,主要的衍射峰是Al和CuAl2,而当10vol%的碳纳米管加入到2024Al粉末后,在衍射图谱中有碳纳米管的衍射峰出现,同时,与2024Al粉末图谱相比,CuAl2的衍射峰变得较强。但是,当混合粉末经过DSC试验后,在衍射图谱中碳纳米管衍射峰消失,相反好几个Al4C3峰出现,此外,CuAl2的衍射峰变得更强。采用气体雾化成型制备的2024Al粉体,由于合金元素的过饱和固溶,2024Al粉末处在亚稳定状态,因此,当粉体被加热时,析出相CuAl2是容易出现的。从图3中可以发现,CuAl2峰变得越来越强,这是由于碳纳米管和2024Al混合粉末在200℃下真空烘干过,而DSC试样加热到800℃,当试样在随后的冷却过程中,析出相是容易出现的。另外,加热温度越高,在随后的冷却时间越长,这就造成析出相CuAl2衍射峰变得越来越强。而试样在DSC试验后碳纳米管的衍射峰消失,一方面碳纳米管与铝发生化学反应将碳纳米管消耗掉,另一方面可能是由于碳纳米管的含量的减少,XRD无法检测到碳纳米管的存在。而Al4C3衍射峰的出现也进一步证实了碳纳米管与铝发生反应。图4为Al4C3相的TEM形貌。从图4a中可以发现Al4C3相均匀分散在铝的晶界处,一部分也位于铝晶粒的内部。针状的Al4C3相平均直径在20nm~40nm,这与原始碳纳米管的直径相似。因此,可以推断当铝液出现后,碳纳米管在铝中是不稳定的,极易与铝液发生反应。

图3 粉末的XRD图谱

图4 Al4C3的TEM形貌
由于TEM观察只是微区的观察,为更进一步弄清碳纳米管与铝的反应状况,DSC试验后的样品通过XPS检测。图5为不同时间Ar离子刻蚀后的DSC试样后的样品表面的XPS图谱,由图可见,样品表面主要是由 O、Al、C、Mg、Ar、N 等元素组成。随着刻蚀时间的增加,样品表面的N1s逐渐减弱,而Ar2p峰逐渐增加。由于N元素是吸附在试样表面,随刻蚀时间的延长,故随之减弱,而样品是在Ar离子的溅射下被刻蚀掉的,所以随着刻蚀时间的延长,Ar2p峰逐渐增加。此外还能看到Al2p峰逐渐增加,这是由于随着刻蚀时间的增加,露出的新鲜的铝基体增多的缘故。对刻蚀8min后样品表面Al和C元素化学状态进行分析并利用高氏-洛仑兹方法对各元素XPS谱进行分离,结果如图6、7所示。由图6可见,Al2p峰主要是由Al2O3、Al4C3和金属态的Al(即零价态,以AlO表示)存在,Al2O3的存在主要是溅射并未完全将样品表面氧化膜溅射掉而造成的。而Al2O3的存在更进一步的证实了碳纳米管与铝发生了反应。而由图7可见,Cls峰主要是由CNTs、Al4C3和C-O组成,CNTs的峰的存在说明在反应过程中碳纳米管并未完全参加反应,而从峰的面积计算可知,反应的碳纳米管占多数。另外,C-O峰的存在是由于部分碳纳米管未参加反应,在这些未反应的碳纳米管表面遗留下来的。
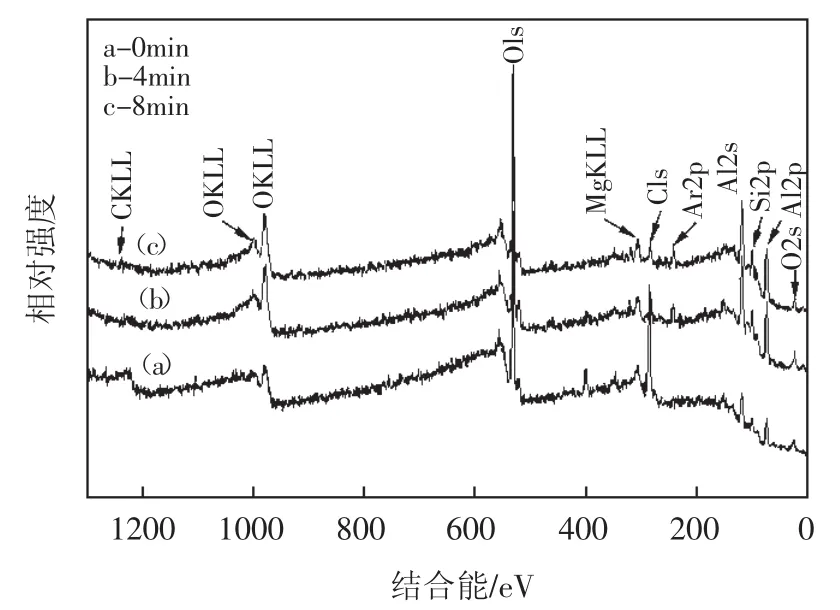
图5 不同时间刻蚀后DSC试验后样品表面XPS谱
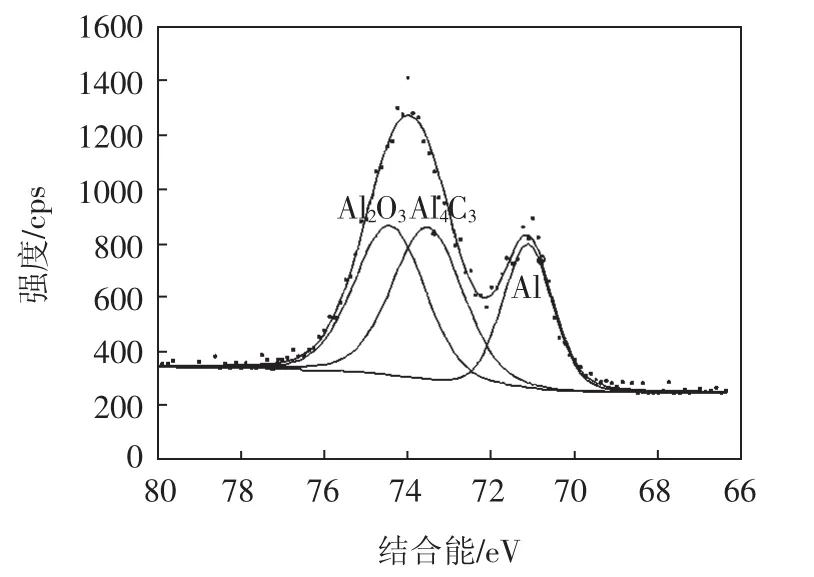
图6 刻蚀8min后粉末表面Al2p XPS谱及其化学状态

图7 刻蚀8min后粉末表面Cls XPS谱及其化学状态
3 结论
(1)从热力学计算看,碳纳米管与铝在从室温到2000K温度范围内均可能发生化学反应生成Al4C3相;从动力学计算看,碳纳米管与铝反应的界面层厚度随反应温度升高和反应时间增长而增加。
(2)当温度超过合金熔点时,碳纳米管在铝中是不稳定的,部分碳纳米管容易与铝发生反应生成Al4C3相。
(3)碳纳米管与铝反应生成的Al4C3相均匀分散在铝的晶界处,一部分也位于铝晶粒的内部,针状的Al4C3相平均直径在20nm~40nm,这与原始碳纳米管的直径相当。
[1]D.B.Miracle.Metal Matrix Composites Form Science to Technological Significance.Composites Science and Technology.2005,65(15~16):2526~2540.
[2]J.L.Sauvajol,E.Anglaret,S.Rols,C.Journet,C.Goze,P.Bernier,W.K.Master,E.Munoz,A.M.Benito,M.T.Martinez.Sturcture and Vibrational Properties of Single Wall Carbon Nanotubes.Synthetic Metals.1999,103(1~3):2537~2539.
[3]O.Zhou,B.Gao,C.Bower,L.Fleming,H.Shimoda.Structure and Electrochemical Properties of Carbon Nanotube Intercalation Compounds.Molecular Crystals and Liquid Crystals Science and Technology,Section A:Molecular Crystals and Liquid Crystals.2000,340:541~546.
[4]M.S.Dresselhaus,G.Dresselhaus,A.Jorio.Unusal Properties and Structure of Carbon Nanotubes.Annual Review of Materials Research.2004,34:247~278.
[5]Z.Tao,H.Geng,K.Yu,Z.Yang,Y.Wang.Effects of High Energy Ball Milling on the Morphology and the Field Emission Property of Multi Walled Carbon Nanotubes.Materials Letters.2004,58:3410~3413.
[6]N.Pierard,A.Fonseca,J.F.Colomer,C.Bossuot,J.M.Benoit,G.V.Tendeloo,J.P.Pirard,J.B.Nagy.Ball Milling Effect on the Structure of Single Wall Carbon Nanotubes.Carbon.2004,42:1691~1697.
[7]B.I.Yakobson,C.J.Bernholc,J.Bernholc.Nanomechanics of Carbon Tubes:Instabilities beyond Linear Response.Physical Review Letters.1996,76(14):2511.
[8]P.C.Hiemenz.Principles of Colloid and Surface Chemistry.Marcel Dekker Inc,1997:109.

