氧化锰纳米管及其超级铝热剂:制备及对环三亚甲基三硝胺热分解的影响
安 亭 赵凤起*, 马海霞 任晓宁 赵宁宁 王 琼 杨 勇
(1西安近代化学研究所燃烧与爆炸技术重点实验室,西安710065)
(2西北大学化工学院,西安710069)
(3清华大学化学系,北京100084)
氧化锰纳米管及其超级铝热剂:制备及对环三亚甲基三硝胺热分解的影响
安 亭1赵凤起*,1马海霞2任晓宁1赵宁宁2王 琼1杨 勇3
(1西安近代化学研究所燃烧与爆炸技术重点实验室,西安710065)
(2西北大学化工学院,西安710069)
(3清华大学化学系,北京100084)
采用水热法制备了MnO2纳米管,以其与纳米铝粉为原料,采用超声分散复合的方法,制备了超级铝热剂Al/MnO2。利用粉末X射线衍射(XRD)、扫描电子显微镜(SEM)及能量散射光谱仪(EDS)对产物的物相、组成、形貌和结构进行分析表征,并运用差示扫描量热法(DSC)研究了MnO2纳米管及其超级铝热剂对环三亚甲基三硝胺热分解特性的影响。结果表明,水热法制备的纳米MnO2呈管状均匀分布,球形纳米Al与管状纳米MnO2相互依附,分散较均匀;MnO2纳米管及其超级铝热剂的加入均改变了环三亚甲基三硝胺的热分解行为及分解历程,使原有占主导的液相分解变为二次的气相反应加剧,使环三亚甲基三硝胺主分解峰形发生了明显的改变。
材料科学;纳米MnO2;超级铝热剂;环三亚甲基三硝胺;水热法;超声分散法;热分解
超级铝热剂(Super Thermite)是一种典型的高反应活性纳米含能材料,通常为纳米级铝粉和氧化性较强的金属/非金属氧化物所组成的复合物。由于其诸多潜在的性能优势,已成为国防科技武器弹药系统研究的热点[1-6]。从目前诸多研究成果来看,超级铝热剂的研究还处于初级阶段、大量的科研工作还只是制备技术和结构性能表征研究[7-21],这一领域非常年轻,其发展正处于从概念认识的形成与完善到探索实践与应用的逐步深入过程中。
超级铝热剂受到热或机械力的引发作用时,能够发生剧烈的氧化还原性的铝热反应,反应过程复杂,燃烧波传播速度快,最终得到氧化铝和单质金属粉或合金并且放出大量的热[21-22]。若选取在推进剂中具有较好催化效果的纳米金属氧化物制备超级铝热剂,可以发挥其应用于推进剂所带来的优异性能,不仅能够提高推进剂燃速,还可以降低压力指数。
材料的性能受其微观结构、形貌和尺寸的影响,近年来纳米材料的尺寸和形貌控制研究引起了人们的广泛关注,并在晶相、晶面及形貌调控方面的研究取得了一些进展[23-30],但大多集中于光电催化以及一些常规条件下的催化氧化反应中,而对于在推进剂中应用、对含能材料热分解反应产生催化作用的相关研究报道则较少。
Al/MnO2发生铝热反应的燃烧热高达6 165 kJ· kg-1,将其应用于推进剂中预计会带来极大的性能优越性。环三亚甲基三硝胺(黑索今,RDX)是硝胺推进剂的主要氧化剂,其热分解特性与推进剂的燃烧性能密切相关,通过考察催化剂对RDX分解的催化作用,可用来预估催化剂对推进剂的催化效果[31-32]。
目前,纳米Al/MnO2复合物对RDX热分解的影响国内外还未见报道,为了研究其催化性能,探索其在固体推进剂中的应用前景,本工作制备了MnO2纳米管及其超级铝热剂,在对产物的微观结构进行表征后,运用差示扫描量热法(DSC)研究了MnO2纳米管及Al/MnO2对环三亚甲基三硝胺热分解特性的影响。
1 实验部分
1.1 试样制备
水热法制备MnO2纳米管:将高锰酸钾溶于去离子水中,缓慢加入盐酸溶液并搅拌均匀,移至水热反应釜中,140℃下于烘箱中反应12 h;反应结束后取出反应釜,自然冷却至室温,经分离、水洗、醇洗、干燥处理后,最终得到黑色粉末状样品。
超声分散复合法制备Al/MnO2复合物:称取一定量的纳米Al粉和水热法制备的MnO2,在超声条件下,分别分散于装有分散剂正己烷的反应容器中,随后置于同一反应容器中,继续超声振动分散,并保持一定温度,直至分散剂蒸发消失,室温下经沉淀老化、干燥处理,最后经玛瑙研钵研磨得产品。
1.2 结构表征
X射线粉末衍射(XRD)测试在日本理学Rigaku D/max-2400型X射线衍射仪上进行,X射线源采用Cu Kα(λ=0.154 18 nm),2θ扫描速率4°·min-1,步长0.02°。采用日本JEOX公司的JEM-2010型透射电子显微镜和荷兰FEI公司Quanta 600型场发射扫描电镜对原料和产物的形貌特征进行观测,30万倍下分辨率1.2 nm;EDS分析则在英国OXFORD公司的INCA Penta FET×3型能谱分析仪上进行,分辨率138 eV。比表面积(BET)由Quantachrome-1比表面测试仪测定。
1.3 试验仪器及条件
将RDX分别与MnO2纳米管及其超级铝热剂以质量比为19∶1、9∶1、5∶1和2∶1的比例混合,采用德国耐驰DSC 204型差示扫描量热仪(DSC)进行实验,压力为0.1 MPa下采用动态纯氮气氛,测试MnO2纳米管和Al/MnO2与RDX混合物的热分解特性,动态流速为100 mL·min-1;温度范围:室温~350℃,升温速率:10℃·min-1;参比物为α-Al2O3,试样量:0.80~1.0 mg;盛放试样的样品池为铝质坩埚。
2 结果与讨论
2.1 XRD分析
将制备的MnO2纳米管及其超级铝热剂进行XRD分析,结果如图1所示,定量估算结果见表1。图1A中,在2θ角为17.96°、28.66°、37.48°、41.86°、49.78°和60.14°附近出现了特征衍射峰,这与标准PDF 44-0141相一致,其分别对应四方晶系结构α-MnO2的(200)、(310)、(211)、(301)、(411)和(521)晶面,其晶胞参数a=0.978 5 nm,c=0.286 3 nm。
XRD图中未出现其他杂峰,表明其为纯的MnO2;图中衍射峰均较尖锐,由此可知本研究中采用水热法制备的MnO2具有较好的结晶性;衍射峰出现宽化现象,说明制备产物晶粒较小。
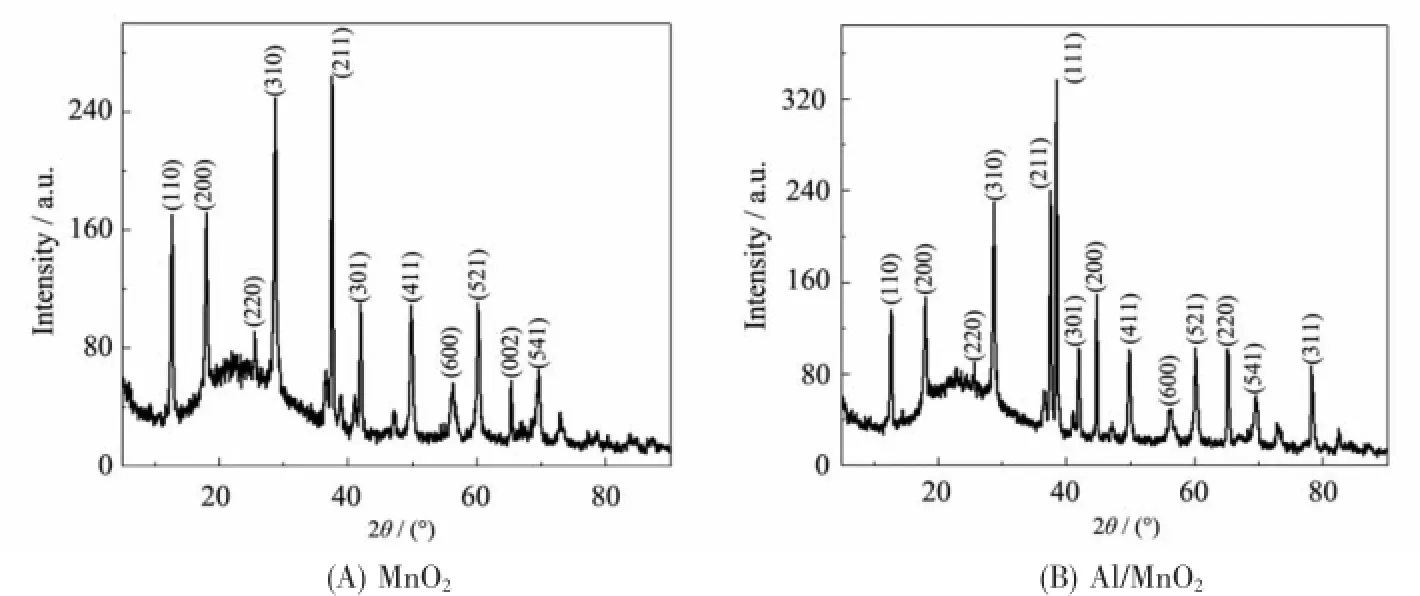
图1 MnO2纳米管及其超级铝热剂Al/MnO2的XRD图Fig.1 XRD patterns of MnO2nanotube and its super thermite Al/MnO2

表1 XRD测试结果的定量估算及纳米铝粉(nano-Al)粒径计算Table1 Quantitative estimation of XRD testing results and size estimation of nano-Al powder
图1B中不仅出现了MnO2四方晶系结构的特征衍射峰,其在2θ角为38.47°、44.90°、65.09°、 78.22°附近还出现了Al的特征衍射峰,分别对应铝面心立方结构的(111)、(200)、(220)和(311)晶面。综上,由定量估算分析结合XRD图可知,超级铝热剂与PDF 04-0787和14-0687一致,即与Al和MnO2的标准图卡片完全吻合,存在两种物质的特征衍射峰,且峰形良好无任何杂峰,这说明复合产物中为纯相的Al和MnO2共存,且二者未发生化学反应,呈现出复合物的特征。
2.2 SEM和EDS表征
采用场发射扫描电镜对制备产物的微观形貌进行分析,MnO2纳米管的SEM照片和EDS微区分析见图2。
由图2可以看出,本研究中采用水热法制备的纳米MnO2表面光滑,长短不一呈管状均匀分布,其管径分布在60~100 nm之间;EDS谱图中仅出现O和Mn两种元素,没有其他杂质,说明产物纯度较高。
纳米颗粒尺寸小,比表面积大和比表面能高,自身团聚现象严重。因此,本工作在制备超级铝热剂过程中,采用超声振荡分散的方法,利用其超声的空化作用,以及在溶液中形成的冲击波和微射流,更大尺度地提高颗粒的分散性。
图3为超级铝热剂Al/MnO2的SEM照片和EDS微区分析,从图中的SEM照片可以看出,球形纳米Al与管状纳米MnO2相互依附在一起形成了复合物,EDS分析表明其中仅含元素O、Mn和Al,未出现其他杂质,说明产物纯度较高。
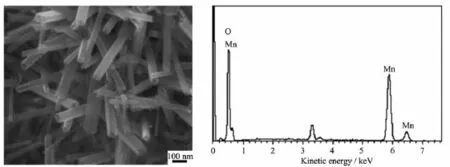
图2 MnO2纳米管的SEM照片和EDS图谱Fig.2 SEM image and EDS spectrum of MnO2nanotube
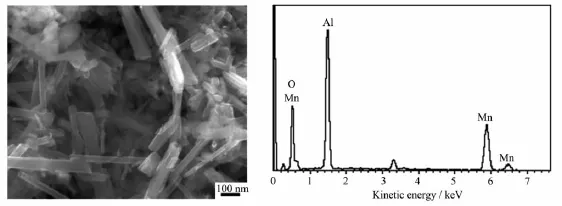
图3 超级铝热剂Al/MnO2的SEM照片和EDS图谱Fig.3 SEM image and EDS spectrum of super thermite Al/MnO2
此外,由比表面测定结果可知,与纯的纳米Al (33 m2·g-1)相比,Al/MnO2超级铝热剂的比表面积(55 m2·g-1)明显增大,这是由于在超声分散作用下,纳米Al与MnO2相互依附,纳米MnO2管状结构的支撑作用减少了球形Al粒子的团聚,使其比表面积增加。此外,纳米MnO2自身大的比表面积(68 m2·g-1)也对复合物较大的比表面积做出了重要贡献。
2.3 对RDX热分解特性的影响
为研究MnO2纳米管及其超级铝热剂Al/MnO2对RDX热分解的影响,分别将其与RDX进行不同含量配比的DSC实验,将获得的DSC曲线示于图4。其中图A为水热法制备的MnO2纳米管含量不同对RDX热分解的影响曲线,图B为超级铝热剂Al/ MnO2含量不同对RDX热分解的影响曲线。
从图4中的DSC曲线可看出,随着混合体系中RDX含量的减少、纳米MnO2及Al/MnO2复合材料的逐渐增多,一次分解(主峰)峰温推后,二次分解(肩峰)峰温提前,主分解峰形发生了明显的改变,由RDX单质的242.0℃处主峰及253.0℃处肩峰的特征逐渐演化为主峰变肩峰及肩峰变主峰的峰形;而当混合体系中MnO2或Al/MnO2加入到一定比例时(如RDX与MnO2或Al/MnO2的比例变化为2∶1),体系二次分解峰形变得尖锐,几乎遮盖了一次分解峰温,二次分解峰温几乎不再变化,即原来归属于RDX的主分解峰消失、肩峰变为主峰,说明MnO2及Al/MnO2的加入改变了RDX的热分解过程,使原有占主导的液相分解变为二次的气相反应加剧。
水热法制备的MnO2纳米管及其超级铝热剂Al/MnO2含量不同时,对RDX热分解行为的影响不同,表2和表3分别为获得的热分解特征量值数据。
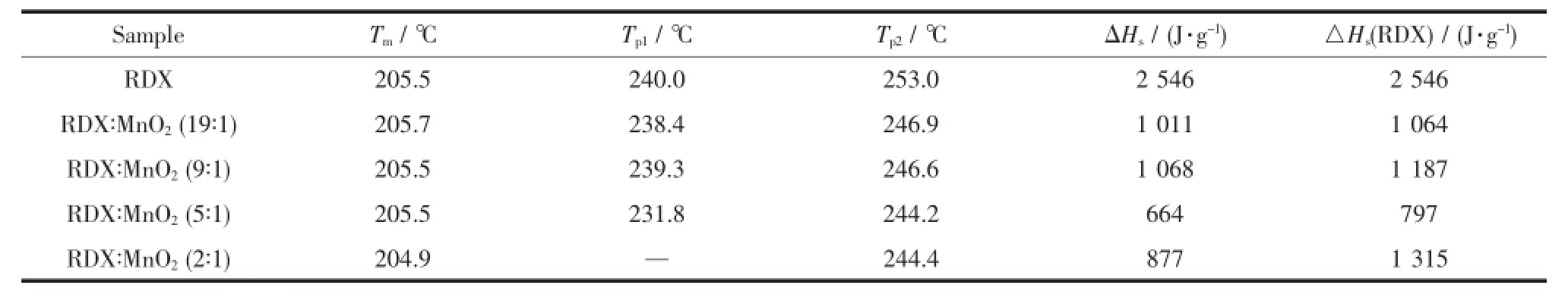
表2 水热法制备MnO2纳米管的含量对RDX热分解的影响Table2 Effect of the content of MnO2nanotube prepared by hydrothermal method on the thermal decomposition of RDX
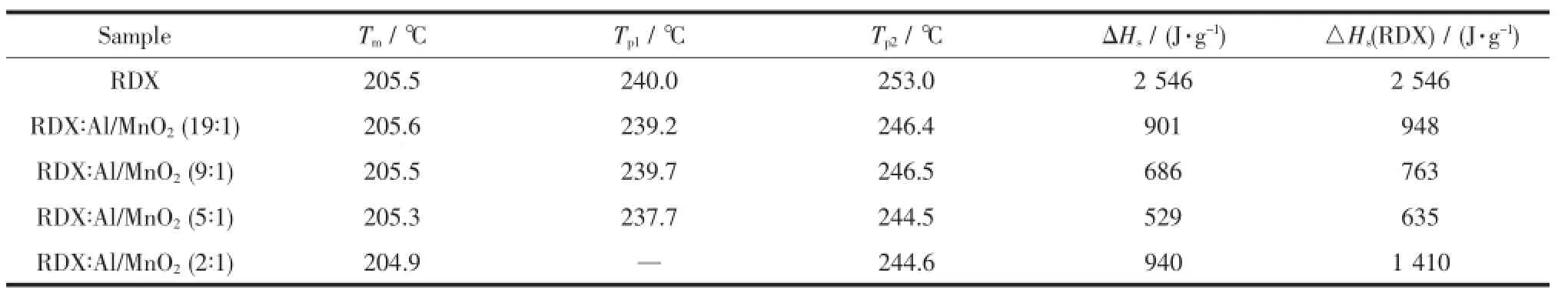
表3 超级铝热剂Al/MnO2的含量对RDX热分解的影响Table3 Effect of the content of super thermite Al/MnO2on the thermal decomposition of RDX
由图4的DSC曲线特征变化及表2、表3的数据可以看出,体系中随着RDX含量的下降、MnO2或 Al/MnO2含量的增多,除发生气相反应占主导之外,RDX的熔点、熔融吸热峰温也均呈现提前的趋势。体系的分解放热量变化规律也出现改变,主要表现为从先前体系中随MnO2或Al/MnO2的增加放热量逐渐降低,出现最小值,再增加MnO2或Al/MnO2则分解热开始增加,但与纯RDX相比,体系的放热量仍是下降的。这主要是因为MnO2或Al/MnO2具有一定导热性,在DSC这种非绝热量热装置中,它们的加入使得整个体系导热系数增加,散热、传热变好,量热时损失的热量增加,热量较纯RDX相比出现下降,且随体系中MnO2或Al/MnO2的逐渐增多分解放热量逐渐下降。但当MnO2或Al/MnO2加入到一定量时(RDX与MnO2或Al/MnO2的质量比为2∶1)整个体系导热系数出现减小,分解放热量开始增加。另外,RDX分解气体产物与MnO2或Al/MnO2在较低温下可能部分发生气固相间的反应,一方面使得RDX分解峰温有所提前,二次分解峰形尖锐。另一方面,该反应会受到二者间比例的影响。
综上分析表明,纳米MnO2及Al/MnO2复合材料的加入均改变了RDX的热分解行为及分解历程,而且随着MnO2及Al/MnO2含量的逐渐增加,RDX热分解的一次分解峰温推后、二次分解峰温提前,体系的分解放热量逐渐降低,而当混合体系中MnO2及Al/MnO2的比例超过某一临界值时,RDX热分解的主分解峰消失,肩峰变为主峰且峰形变得尖锐,体系放热量又开始增加。
3 结论
(1)采用水热法和超声分散复合法,分别制备了纳米MnO2及其超级铝热剂Al/MnO2。形貌和结构分析表明,纳米MnO2呈管状均匀分布,球形纳米Al与管状纳米MnO2相互依附形成了纯相的Al/MnO2复合粉体,体系中的两种材料呈现分子间复合物的特征。
(2)纳米MnO2及Al/MnO2复合材料的加入改变了RDX的主分解峰形,对RDX的高温液相分解产生了明显的影响,随着体系中MnO2或Al/MnO2的相对含量逐渐增多,RDX热分解发生了主峰和肩峰互相转换的现象。
(3)随着RDX含量下降、纳米MnO2及Al/MnO2复合材料含量的增加,体系总的分解放热量逐渐减小,并出现最小值,随后分解热又开始增加,但体系的总放热量仍小于纯RDX的放热量。
(4)MnO2纳米管及Al/MnO2复合材料对RDX热分解的影响主要表现为改变其热分解行为及放热量,且其分解历程会受到二者间比例的影响。
参考文献:
[1]Dreizin E L.Prog.Energy Combust.Sci.,2009(35):141-167
[2]Pamela J,Kaste B.The Amptiac Newsletter,2004,8(4):85-89
[3]Valliappan S,Swiatkiewicz J,Puszynski J A.Powder Technol., 2005(156):164-169
[4]Mei J,Halldeam R D,Xiao P.Scr.Mater.,1999,41(5):541-548
[5]AN Ting(安亭),ZHAO Feng-Qi(赵凤起),XIAO Li-Bai (肖立柏).Chin.J.Explos.Propellants(火炸药学报),2010, 33(3):55-62
[6]AN Ting(安亭),ZHAO Feng-Qi(赵凤起),ZHANG Ping-Fei (张平飞).Nanosci.Technol.(纳米科技),2009,6(36):60-67
[7]Walker J D.Thesis for the Doctorate of Georgia Institute of Technology.2007.
[8]Mei J,Halldeam R D,Xiao P.Scr.Mater.,1999,41(5):541-548
[9]Kim Soo H.Adv.Mater.,2004,16(20):1821-1825
[10]Umbrajkar S M,Schoenitz M,Dreizin E L.Propellants Explos.Pyrotech.,2006,31(5):382-389
[11]Umbrajkar S M,Seshadri S,Schoenitz M,et al.J.Propuls Power,2008,24(2):192-198
[12]Schoenitz M,Umbrajkar S M,Dreizin E L.J.Propuls Power,2007,23(4):683-687
[13]Schoenitz Mirko,Ward Trent S,Dreizin Edward L.Proc. Combust.Inst.,2005(30):2071-2078
[14]Bockmon B S,Pantoya M L,Son S F,et al.J.Appl.Phys., 2005,98(6):064903(7 pages)
[15]Badiola C,Schoenitz M,ZHU Xiao-Ying,et al.J.Alloys Compd.,2009,488:386-391
[16]Valliappan S,Swiatkiewicz J,Puszynski J A.Powder Technol.,2005,156:164-169
[17]Weismiller M R,Malchi J Y,Yetter R A,et al.Proc. Combust.Inst.,2009,32(2):1895-1903
[18]AN Ting(安亭),ZHAO Feng-Qi(赵凤起),YI Jian-Hua (仪建华),et al.Acta Phys.-Chim.Sin.(物理化学学报), 2011,27(2):281-288
[19]AN Ting(安亭),ZHAO Feng-Qi(赵凤起),PEI Qing(裴庆), et al.Chinese J.Inorg.Chem.(无机化学学报),2011,27(2): 231-238
[20]ZHAO Ning-Ning(赵宁宁),HE Cui-Cui(贺翠翠),LIU Jian-Bing(刘健冰),et al.Chin.J.Explos.Propellants(火炸药学报),2012,35(6):32-36
[21]Tillotson T M,Gash A E,Simpson R L,et al.J.Non-Cryst. Solids,2001,285:338-345
[22]Granier J J,Pantoya M L.Combust.Flame,2004,138:373-383
[23]Tian N,Zhou Z Y,Sun S G,et al.Science,2007,316:732
[24]Zhang L F,Zhong S L,Xu A W,et al.Angew.Chem.Int. Ed.,2013,52:645-649
[25]Li L L,Chen X B,Wu Y E,et al.Angew.Chem.Int.Ed., 2013,52:11049-11053
[26]Wu Y E,Cai S F,Wang D S,et al.J.Am.Chem.Soc.,2013, 131:8975-8981
[27]Xie X W,Li Y,Liu Z Q,et al.Nature,2009,458:746
[28]Reid D L,Russo A E,Carro R V,et al.Nano Lett.,2007,7: 2157-2161
[29]FANG Xiao-Sheng(方晓生),ZHANG Li-De(张立德). Chinese J.Inorg.Chem.(无机化学学报),2006,22(9):1555-1567
[30]HAN Yu-Xiang(韩玉香),SHAO Yun(邵云),WAN Hai-Qin (万海勤),et al.Chinese J.Inorg.Chem.(无机化学学报), 2014,30(3):481-486
[31]LIU Zi-Ru(刘子如).Thermal Analyses for Energetic Materials(含能材料热分析).Beijing:National Defense Industry Press,2008.
[32]HU Rong-Zu(胡荣祖),GAO Sheng-Li(高胜利),ZHAO Feng-Qi(赵凤起),et al.Thermal Analysis Kinetics(热分析动力学).Beijing:Science Press,2008.
MnO2Nanotube and Its Super Thermite:Preparation and Their Effect on Thermal Decomposition of Cyclotrimethylene Trinitramine
AN Ting1ZHAO Feng-Qi*,1MA Hai-Xia2REN Xiao-Ning1ZHAO Ning-Ning1WANG Qiong1YANG Yong3
(1Science and Technology on Combustion and Explosion Laboratory,Xi′an Modern Chemistry Research Institute,Xi′an 710065,China)
(2Department of Chemical Engineering,Northwest University,Xi′an 710069,China)
(3Department of Chemistry,Tsinghua University,Beijing 100084,China)
The nano-MnO2was prepared by hydrothermal method,and then super thermite Al/MnO2was prepared by ultrasonic dispersion method using nano-MnO2and Al nanoparticles as raw materials.The physical phase, composition,morphology and structure of products were characterized by X-ray diffraction(XRD)and scanning electron microscope-energy dispersive spectrometer(SEM-EDS).The catalytic effect of MnO2nanotube and the super thermite on the thermal decomposition of cyclotrimethylene trinitramine were investigated by differential scanning colorimetry(DSC).The results indicate that nano-MnO2is in tubular structure,and the globose nano-Al particles are homodispersed on the surface of MnO2nanotube.MnO2nanotube and its super thermite influence the thermal decomposition behavior and decomposition process of cyclotrimethylene trinitramine.They can change the primary decomposition of liquid phase to the reaction of secondary gas phase and can change the shape of main decomposition peak obviously.
material science;nano-MnO2;super thermite;cyclotrimethylene trinitramine;hydrothermal method;ultrasonic dispersion method;thermal decomposition
O611.62;O612.7;O643
A
1001-4861(2015)01-0097-06
10.11862/CJIC.2015.010
2014-07-20。收修改稿日期:2014-09-25。
国家自然科学基金(No.21173163);燃烧与爆炸技术重点实验室基金(No.9140C350302120C3501)资助项目。*
。E-mail:npecc@163.com;Tel:86-29-88291263.;会员登记号:S06N3692M1408。

