MCM-41分子筛负载铁铈催化降解甲基橙
王帅军,董 培,崔爱玲,王 茜,赵朝成
(中国石油大学(华东) 化学工程学院,山东 青岛 266580)
MCM-41分子筛负载铁铈催化降解甲基橙
王帅军,董 培,崔爱玲,王 茜,赵朝成
(中国石油大学(华东) 化学工程学院,山东 青岛 266580)
采用等体积浸渍法制备了负载型有序介孔Fe-Ce/MCM-41催化剂。研究了该催化剂降解甲基橙的适宜工艺条件,并采用XPS,XRD,TEM技术对该催化剂进行了表征。实验结果表明,该催化剂Fenton氧化降解甲基橙的较适宜工艺条件为:溶液pH 5.0、甲基橙溶液初始质量浓度100 mg/L、催化剂加入量2.0 g/L、H2O2浓度20 mmol/L,在此适宜条件下反应120 min时,甲基橙去除率接近100%。表征结果显示:Fe-Ce/MCM-41催化剂主要由铁、铈、氧、碳4种元素组成;铁与铈的摩尔比接近3∶1;铁和铈主要以Fe3O4和CeO2的形态存在于催化剂表面。
铁-铈/ MCM-41催化剂;甲基橙;降解;Fenton氧化;过氧化氢
近年来,随着染料在各行各业中的广泛应用,产生了大量的染料废水[1-2]。染料废水具有毒性大、难生物降解等特点,对生态环境危害极大,因此将染料废水排入水体前需要对其进行处理[3]。传统的染料废水处理方法有物理法、化学法和生物法,但处理后废水很难达到排放要求。Fenton氧化技术反应条件温和,操作过程简单且对环境友好,能快速氧化废水中大部分的有机物[4-6]。但Fenton氧化技术只在酸性条件下具有较高的有机物去除率且铁离子流失严重,限制了其广泛应用[7-8]。为了克服这些缺点,有研究者利用铁离子溶出量较低的零价铁、铁的氧化物及铁负载黏土等来取代Fe2+和Fe3+作为Fenton氧化催化剂处理废水,但由于处理效率较低往往需要借助紫外、可见光或超声进行协同处理,从而增加了废水的处理成本[9-12]。
本工作采用等体积浸渍法将铁和铈的氧化物负载到MCM-41分子筛上,制备得到负载型有序介孔Fe-Ce/MCM-41催化剂,用于降解甲基橙。考察了溶液pH、甲基橙初始质量浓度、催化剂加入量及H2O2浓度等对甲基橙去除率的影响,优化了Fenton氧化反应工艺条件。分别采用XPS,XRD,TEM技术对Fe-Ce/MCM-41催化剂进行了表征,并探讨了Fe-Ce/MCM-41催化剂的Fenton氧化反应机理。
1 实验部分
1.1 材料和试剂
MCM-41分子筛:南开催化剂厂;Fe(NO3)3· 9H2O,Ce(NO3)3·6H2O,H2O2,HCl,NaOH:均为分析纯;甲基橙:化学纯。
1.2 催化剂的制备
首先配制总浓度为2.0 mol/L的Fe(NO3)3和Ce(NO3)3混合溶液,铁与铈的摩尔比为3∶1[13];然后取一定量的MCM-41分子筛置于混合溶液中,在振荡频率为100 kHz的条件下超声反应20 min,取出烘干、焙烧后,得到负载型有序介孔的Fe-Ce/ MCM-41催化剂。
1.3 Fenton氧化反应实验
在500 mL量筒中加入一定量的初始质量浓度为100 mg/L的甲基橙溶液,采用0.1 mol/L的HCl或NaOH溶液调节溶液pH,然后利用吸量管精确加入一定量的H2O2,最后向溶液中加入一定量的Fe-Ce/ MCM-41催化剂。为使催化剂与溶液充分接触,在量筒底部对溶液进行曝气。反应后在波长为510 nm的条件下,采用上海元析仪器有限公司的UV6000-PC型紫外-可见分光光度计测定溶液的吸光度,计算溶液中剩余甲基橙质量浓度,计算甲基橙去除率。
1.4 催化剂的表征
采用英国Kratos公司AXIS Supra型X 射线光电子能谱仪测定催化剂的组成及其表面的化学状态;采用日本JEOL公司201型透射电子显微镜观察催化剂的内部结构;采用荷兰帕纳科公司X’Pert Pro Holland 型多晶粉末 X射线衍射仪测定催化剂的物相。
2 结果与讨论
2.1 Fenton氧化反应工艺条件的优化
2.1.1 溶液pH
在甲基橙初始质量浓度为100 mg/L、催化剂加入量为2.0 g/L、H2O2浓度为20 mmol/L的条件下,溶液pH对甲基橙去除率的影响见图1。由图1可见:当溶液pH为3.0时,甲基橙去除率最高,反应30 min后去除率高达95.4%;当反应时间为120 min时,在溶液pH为3.0~9.0的范围内,甲基橙去除率均高于85.0%。由此可见,在酸性、中性和碱性条件下Fe-Ce/MCM-41催化剂的甲基橙去除率均较高。
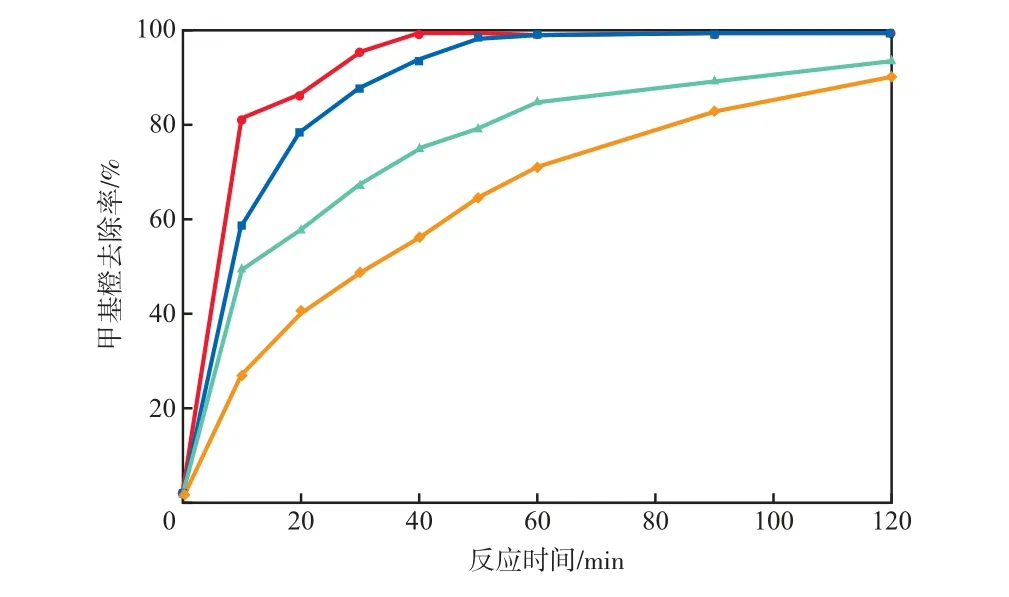
图1 溶液pH对甲基橙去除率的影响
当反应时间为120 min时,溶液pH对溶液中总铁离子质量浓度的影响见图2。由图2可见:随溶液pH的增大,溶液中总铁离子质量浓度先减小后增大;当溶液pH为5.0时,总铁离子质量浓度最低,为7.8 mg/L。故选择溶液pH为5.0较适宜。

图2 溶液pH对溶液中总铁离子质量浓度的影响
2.1.2 甲基橙初始质量浓度
在溶液pH为5.0、催化剂加入量为2.0 g/L、H2O2浓度为20 mmol/L的条件下,甲基橙初始质量浓度对甲基橙去除率的影响见图3。由图3可见:随甲基橙初始质量浓度的增加,甲基橙去除率逐渐降低,这是因为,随溶液中甲基橙质量浓度的增加,染料分子的数量增加,在溶液中Fe-Ce/MCM-41催化剂加入量一定的情况下,产生的·OH数量没有增加,因此造成甲基橙的降解速率下降;当反应时间为120 min时,甲基橙去除率均高于85.0%。甲基橙初始质量浓度过高或过低均不具有代表性,因此后续实验选择甲基橙初始质量浓度为100 mg/L。

图3 甲基橙初始质量浓度对甲基橙去除率的影响
2.1.3 催化剂加入量
在溶液pH为5.0、甲基橙初始质量浓度为100 mg/L、H2O2浓度为20 mmol/L的条件下,催化剂加入量对甲基橙去除率的影响见图4。由图4可见:随催化剂加入量的增加,甲基橙去除率先升高后降低;当催化剂加入量为2.0 g/L时甲基橙去除率最高,反应60 min后甲基橙去除率高于99.4%。这是因为,当催化剂加入量较低时,催化剂表面的铁和铈的氧化物总量也较少,因此生成的·OH数量较少,导致甲基橙去除率较低;当催化剂加入量过高时,催化剂表面的铁氧化物与H2O2反应生成·OH后,进一步发生自身清除反应(Fe2++ • OH→ Fe3++ OH-)。故选择催化剂加入量为2.0 g/L较适宜。
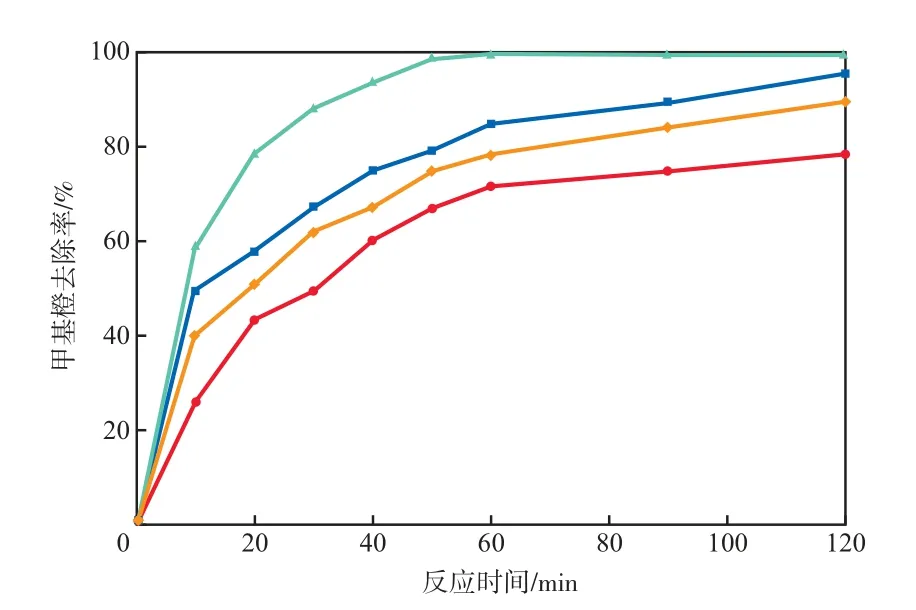
图4 催化剂加入量对甲基橙去除率的影响
2.1.4 H2O2浓度
在溶液pH为5.0、甲基橙初始质量浓度为100 mg/L、催化剂加入量为2.0 g/L的条件下,H2O2浓度对甲基橙去除率的影响见图5。由图5可见:随H2O2浓度的升高,甲基橙去除率先升高后降低;当H2O2浓度为20 mmol/L时甲基橙去除率最高,反应60 min后甲基橙去除率高于99.4%。这是因为,当H2O2浓度较低时,催化剂与H2O2反应不能生成足够的·OH,导致甲基橙去除率较低;当H2O2浓度过高时,生成·OH后,进一步发生自身清除反应。故选择H2O2浓度为20 mmol/L较适宜。

图5 H2O2浓度对甲基橙去除率的影响
2.1.5 小结
在溶液pH为5.0、甲基橙初始质量浓度为100 mg/L、催化剂加入量为2.0 g/L、H2O2浓度为20 mmol/L的适宜条件下,反应时间为120 min时,甲基橙去除率接近100%。
2.2 催化剂的表征结果
2.2.1 XPS分析
Fe-Ce/MCM-41催化剂的XPS谱图见图6。由图6可见,Fe-Ce/MCM-41催化剂主要由铁、铈、氧、碳4种元素组成:其中,氧的含量最高,为85.19%(x);其次是铁,为10.27%(x);再次是铈,为3.42%(x);碳含量最低,为1.22%(x),说明Fe-Ce/MCM-41催化剂中的铁和铈主要以氧化物的形式存在于催化剂的表面。同时铁与铈的摩尔比接近3∶1,与制备过程中Fe(NO3)3与Ce(NO3)3混合溶液的铁与铈的摩尔比为3∶1相吻合,同时说明铁和铈负载到了催化剂的表面。

图6 Fe-Ce/MCM-41催化剂的XPS谱图
Fe-Ce/MCM-41催化剂的Fe 2p谱图见图7。由图7可见,724.6 eV 和 711.3 eV 处的峰分别对应于Fe 2p1/2 轨道和Fe 2p3/2轨道,Fe 2p3/2轨道又可分为 710.8 eV 和 712.9 eV两个峰,分别表明 Fe2+和Fe3+的存在。 因此可以推知,铁主要以Fe3O4的形态存在于催化剂表面。

图7 Fe-Ce/MCM-41催化剂的Fe 2p谱图
Fe-Ce/MCM-41催化剂的Ce 3d谱图见图8。经过分峰处理,可将各峰分为对称的两部分,分别标记为u/v,u′/v′,u"/v",u/v,其中,u和v分别对应于 3d3/2 和 3d5/2自旋轨道状态。 u/v,u"/ v",u/v 属于3d104f0Ce4+形态,而 u′/v′属于3d104f1Ce3+形态。由于Ce4+所占面积远大于Ce3+所占面积,因此可以推知,铈主要以CeO2形态存在于催化剂表面。
2.2.2 XRD分析
MCM-41分子筛和Fe-Ce/MCM-41催化剂的XRD谱图见图9。由图9可见,Fe-Ce/MCM-41催化剂的XRD谱图与MCM-41分子筛基本一致,在2θ为2.30°,3.97°,4.60° 处均出现了明显的衍射峰,分别代表了MCM-41分子筛的(100),(110),(200) 3个晶面,同时也说明分子筛的结构在负载过程中没有受到损坏。

图8 Fe-Ce/MCM-41催化剂的Ce 3d谱图
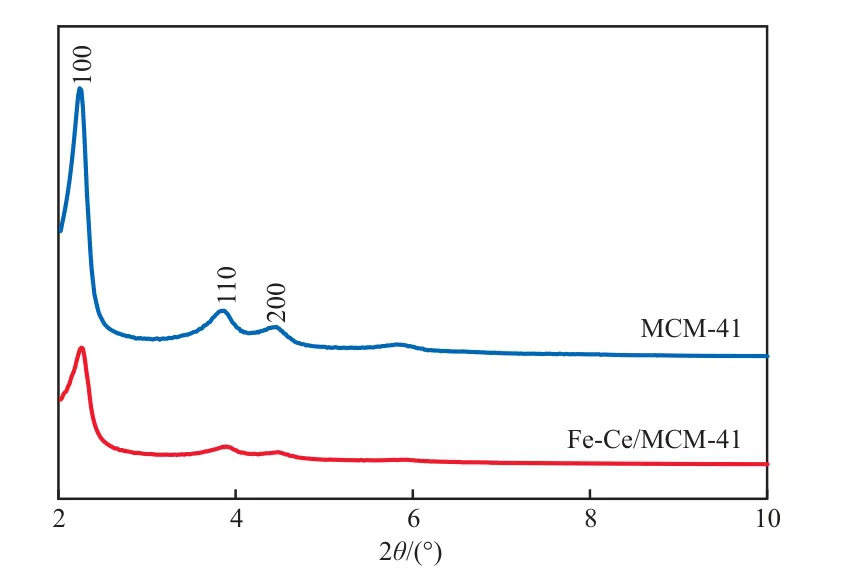
图9 MCM-41分子筛和Fe-Ce/MCM-41催化剂的XRD谱图
2.2.3 TEM表征
MCM-41分子筛和Fe-Ce/MCM-41催化剂的TEM照片见图10。由图10可见,MCM-41分子筛和Fe-Ce/MCM-41催化剂均具有均匀的孔道结构。而图10b中出现颜色较深区域,可能是由于铁和铈的氧化物负载在了催化剂表面。

图10 MCM-41分子筛(a) 和 Fe-Ce/MCM-41催化剂 (b) 的TEM照片
2.3 反应机理
Fe-Ce/MCM-41催化剂Fenton氧化反应可能的反应机理如下。反应首先发生在催化剂表面,≡Fe2+(表面)(≡Fe2+为催化剂表面的Fe2+)与H2O2反应生成·OH(表面),见式(1);≡Fe2+的再生见式(2)和式(3)。Heckert等[14]研究发现,≡Ce3+可以发生类似的反应,见式(4)和式(5)。随着反应的进行,Fe2+进入溶液中进一步发生反应生成·OH(自由),见式(6)~(8)。产生的·OH(表面)和·OH(自由)对有机物进行降解,见式(9)和式(10)。

3 结论
a) 将铁和铈的氧化物负载到MCM-41分子筛上制备得到Fe-Ce/MCM-41催化剂。采用该催化剂催化Fenton氧化反应降解甲基橙的较适宜工艺条件为:溶液pH 5.0,甲基橙溶液初始质量浓度100 mg/ L,催化剂加入量2.0 g/L,H2O2浓度20 mmol/L。在此适宜条件下反应120 min时,甲基橙去除率接近100%。
b) Fe-Ce/MCM-41催化剂主要由铁、铈、氧、碳4种元素组成,铁与铈的摩尔比接近3∶1,铁和铈主要以Fe3O4和CeO2的形态存在于催化剂表面。
[1] Xu Lejin,Wang Jianlong. Magnetic Nanoscaled Fe3O4/ CeO2Composite as an Efficient FentonLike Heterogeneous Catalyst for Degradation of 4-Chlorophenol[J]. Environ Sci Technol,2012,46(18):10145 - 10153.
[2] 林丹丹,赵朝成,王志伟. Co/MCM-41强化零价铁/氧气体系处理炼化企业反渗透浓水研究[J]. 石油炼制与化工,2014,45(2):50 - 54.
[3] 赵彬侠,张小里,王进,等. 焙烧温度对催化剂 Cu-Ni-Ce/SiO2性能的影响[J]. 环境科学学报,2008, 28(11):2305 - 2310.
[4] Lin Shiyang,Chen Chunliang,Chang Dongjang,et al. Catalytic Wet Air Oxidation of Phenol by Various CeO2Catalysts[J]. Water Res,2002,36(12):3009 - 3014.
[5] 张志军,胡涓,陈整生,等. 纳米TiO2-石墨烯光催化剂的水热合成及其光催化性能[J]. 化工环保,2014,34(4):385 - 389.
[6] Lee C,Sedlak D. Enhanced Formation of Oxidants from Bimetallic Nickel-Iron Nanoparticles in the Presence of Oxygen[J]. Environ Sci Technol,2008,42(22):8528 - 8533.
[7] Lai Peng,Zhao Huazhang,Wang Chao,et al. Advanced Treatment of Coking Wastewater by Coagulation and Zero-Valent Iron Processes[J]. J Hazard Mater,2007,147(1):232 - 239.
[8] Wang Xiaojun,Gu Xiaoyang,Lin Dexian,et al. Treatment of Acid Rose Dye Containing Wastewater by Ozonizing-Biological Aerated Filter[J]. Dyes Pigments,2007,74(3):736 - 740.
[9] Ruan Xinchao,Liu Mingyue,Zeng Qingfu,et al. Degradation and Decolorization of Reactive Red X-3B Aqueous Solution by Ozone Integrated with Internal Micro-Electrolysis[J]. Sep Purif Technol, 2010,74(2):195 - 201.
[10] Zhu Xiuping,Ni Jinren,Lai Peng. Advanced Treatment of Biologically Pretreated Coking Wastewater by Electrochemical Oxidation Using Boron-Doped Diamond Electrodes[J]. Water Res,2009,43(17):4347 - 4355.
[12] Chen Yang,Li Gang,Yang Fang,et al. Mn/ZSM-5 Participation in the Degradation of Cellulose Under Phosphoric Acid Media[J]. Polym Degrad Stab,2011,96(5):863 - 869.
[13] 王帅军,董培,赵朝成,等. 分子筛负载铁铈处理甲基橙模拟废水研究[J]. 石油炼制与化工,2015,46(11):88 - 91.
[14] Heckert E,Seal S,Self W. Fenton-Like Reaction Catalyzed by the Rare Earth Inner Transition Metal Cerium[J]. Environ Sci Technol,2008,42(13):5014 - 5019.
(编辑 祖国红)
Catalytic Degradation of Methyl Orange on MCM-41 Zeolite Supported Iron and Cerium
Wang Shuaijun,Dong Pei,Cui Ailing,Wang Qian,Zhao Chaocheng
(School of Chemical Engineering,China University of Petroleum,Qingdao Shandong 266580,China)
The supported ordered mesoporous catalyst Fe-Ce/MCM-41 was prepared by incipient-wetness impregnation method. The suitable conditions for Fenton oxidation and degradation of methyl orange (MO) on the catalyst were studied,and the catalyst was characterized by XPS,XRD,and TEM. The experimental results show that:Under the conditions of solution pH 5.0,initial MO mass concentration 100 mg/L,catalyst dosage 2.0 g/L,H2O2concentration 20 mmol/L and reaction time 120 min,the MO removal rate is nearly 100%. The characterization results show that:The element composition of Fe-Ce/MCM-41 catalyst is mainly Fe,Ce,O,C;the mole ratio of Fe to Ce is about 3∶1;Fe and Ce on the surface of MCM-41 catalyst are in the form of Fe3O4and CeO2.
iron-cerium/MCM-41 catalyst;methyl orange;degradation;Fenton oxidation;hydrogen peroxide
X703
A
1006-1878(2015)06-0651-05
2015 - 07 - 21;
2015 - 08 - 20。
王帅军(1989—),男,河南省商丘市人,硕士生,电话 18325429043,电邮 shuaijunwang@outlook.com。联系人:赵朝成,电话 13506360770,电邮 zhaochch@upc.edu.cn。
中国石油大学(华东)研究生创新工程项目(YCX2015 - 032)。

