天然色素的理化特性及其应用研究进展
王卫国,张仟伟,赵永亮,胡晓伟,林 强,李瑞静,王 卫,管景帅
(河南工业大学 生物工程学院,河南 郑州 450001)
0 前言
天然色素是来源于自然界中带颜色的物质的总称,主要来自于植物的花、叶、果实和种子,还有少部分来自昆虫和微生物.天然色素常用于改善食品的色泽,也广泛用于医药、化妆品和布料的着色.天然色素具有以下特点:大部分从人们日常食用的动植物体中得到,安全无毒且没有副作用;易被人体吸收,对人体健康维护是一种有益的补充;多数天然色素具有生理和药理作用,对某些疾病具有防治功效[1];色彩柔和并具有芳香的气味,会给人带来愉悦的感觉.因此天然色素一直受到人们的喜爱,尤其是在化学合成色素安全事件频发的今天,人们更渴望在日常生活中能真正享用到纯天然的色素.作者综述了天然色素的理化性质、分离纯化及其应用研究进展.
1 天然色素的种类及理化性质
除矿物色素外天然色素根据来源可分为:动物色素、植物色素和微生物色素;根据溶解性质可分为:水溶性色素和脂溶性色素;此外也可按化学结构或颜色系列来分[2],下面主要介绍根据化学结构进行的分类:(1)异戊二烯类色素(脂溶性色素):以异戊二烯为基础单元组成共轭双键长链的色素,如番茄红素、辣椒红素和玉米黄素等;(2)吡咯衍生物类色素:以卟吩(由4 个吡咯环构成)为基础,如叶绿素;(3)酚、酮、醌类色素(醇溶与水溶性):花青素类和单宁类,如天竺葵色素、牵牛花色素等;(4)吲哚类色素:酸枣色素、枣红色素.下面主要介绍几种与人们生产、生活、健康密切相关的天然色素及其理化性质.
1.1 番茄红素
番茄红素主要存在于番茄中(含量随品种和成熟度的变化而变化),此外西瓜、红椒、葡萄柚等果蔬中番茄红素含量也很高.呈明亮红色的针状结晶,属于天然色素中的异戊二烯类,为脂溶性色素,易溶于有机溶剂,难溶于水[3],其结构式见图1.

图1 番茄红素的基本结构Fig.1 Basic structure of lycopene
由图1 可知,番茄红素分子中含多个双键,所以易被氧化而不稳定.光、O2或pH 的改变都会导致番茄红素结构改变和氧化降解[4].
1.2 β-胡萝卜色素
β-胡萝卜色素是自然界中最普遍的天然色素,胡萝卜、菠菜和芒果等果蔬中含量丰富.属于异戊二烯类色素,干品为深红色粉末,不溶于水,易溶于苯、氯仿等.铁离子、光、氧等都可使其褪色,所以β-胡萝卜色素稳定性差[5],其结构式见图2.

图2 β-胡萝卜色素的基本结构Fig.2 Basic structure of β-carrot pigment
由图2 可知,β-胡萝卜色素不饱和度很高,含有很多双键和支链,是较好的单线态氧淬灭剂.共轭双键越多,β-胡萝卜素就会越红[6].
1.3 姜黄色素
姜黄色素是主要存在于姜黄、郁金的块茎中的黄色色素(有芳香味),属于黄酮类化合物,主要包括3 种活性成分:姜黄素、脱甲氧基姜黄素和双脱甲氧基姜黄素.熔点为179~182 ℃,不溶于水,具有亲脂性,易溶于冰醋酸、丙二醇、乙酸乙酯以及碱性溶液和95%乙醇.遇铁离子易变色,对光、热稳定性较差[7],其结构式见图3.
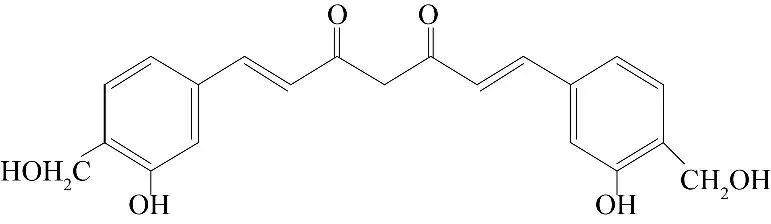
图3 姜黄素的基本结构Fig.3 Basic structure of curcumin
由图3 可知,姜黄色素分子还原性较强(含双键、羟基、羰基),易发生化学反应,着色力较好,尤其对蛋白质着色力较强.朱尽顺等[8]对单体姜黄素的稳定性进行研究:姜黄色素随pH 值的增大由黄色(pH 4)逐渐变成红棕色(pH 10).蔗糖、麦芽糖对姜黄素有增色作用;维生素C、钠离子、钾离子、镁离子对姜黄素无明显影响.
1.4 花青素
花青素(又称花色素)属类黄酮化合物,是水溶性的天然色素,易溶于乙醇,不溶于植物油,是构成花瓣和果实颜色的主要色素之一.主要存在于葡萄、茄子和樱桃的皮中以及草莓、牵牛花等植物的花和果实中.大多偏红、紫色的蔬果都含有花青素[9].花青素的颜色与pH 有关(酸红碱蓝),其结构式见图4.
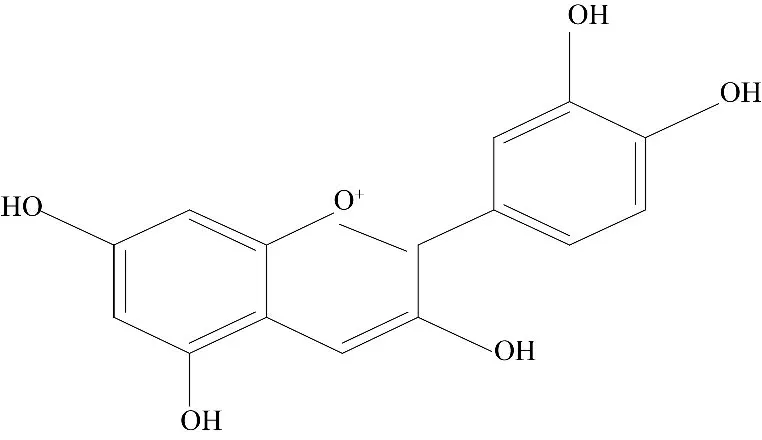
图4 花青素的基本结构Fig.4 Basic structure of anthocyanin
由图4 可知,花青素的基本结构单元是3,5,7-三羟基-2-苯基吡喃型阳离子.花青素结构上羟基数、甲基化和糖基化位置和程度、糖的类别、连接的芳香酸和脂肪酸种类和数量等不同也会使花青素在溶液中呈现不同颜色.现已发现的花青素种类主要有20 多种[10].花青素稳定性差,pH、氧、金属离子等都会影响花青素的稳定性;花色苷和花青素结构中羟基多的稳定性不如甲氧基多的高[11].
1.5 甜菜色素
甜菜色素主要存在于植物的花、果实以及石竹目中大部分科的营养组织中,此外还存在于一些高等真菌中,如毒蝇伞[12],属于吡啶衍生物,是一类水溶性的含氮色素.甜菜色素主要有两种结构:红紫色的甜菜红素和黄色的甜菜黄素.难溶于醋酸、丙二醇,不溶于乙醇、甘油、油脂.目前发现的甜菜色素包括50 多种甜菜红素和20 多种甜菜黄素[13].依据甜菜色素的化学结构可分为甜菜类、苋菜类、千日紫类、脱羧类,其结构式见图5.

图5 甜菜色素的基本结构Fig.5 Basic structure of beet pigment
由图5 可知,甜菜色素的基本基团是醛氨酸,甜菜黄的R 基主要是氨基酸(或胺),而甜菜红素的R 基主要是糖基.甜菜色素易溶于水呈红紫色,在pH 4~7 范围内稳定;pH 小于4 或大于7 时,溶液颜色由红变紫;pH 大于10 时,溶液颜色迅速变黄(甜菜红素就变成甜菜黄素),研究表明甜菜色素与花青色素有互斥性(即不能同时存在于同一植物中)[14].甜菜色素的稳定性与水分活性二者为反比关系.抗坏血酸对甜菜红素具有保护作用[15].
1.6 栀子黄色素
栀子黄色素主要存在于茜草科栀子属栀子的果实中,是天然色素中为数不多的水溶性类胡萝卜素,属于异戊二烯类色素,是一种橙黄色粉末(水溶液为柠檬黄色),主要成分是藏红花素和藏红花酸,易溶于水,溶于乙醇、丙二醇等极性溶剂,难溶于苯、汽油等非极性溶剂,不溶于油脂,其结构式见图6.

图6 栀子黄色素的结构Fig.6 Structre of gardenia yellow pigment
由图6 可知,栀子黄色素分子的母核上含有7个共轭双键,其两端可连接不同数量的葡萄糖(这极大地增加了栀子黄色素的极性),因此栀子黄色素是自然界中少有的水溶性类胡萝卜素.其颜色受环境pH 的影响较小(pH3~9 时保持黄色;pH4~6或pH8~11 时比β-胡萝卜素稳定),在中性或碱性条件下栀子黄色素的耐光和耐热性比在酸性条件下强.此外栀子黄色素易被人体吸收,在人体内可转化为VA,且对蛋白质和淀粉有很强的着色能力,工业上常用于亲水性食品的染色.Cu2+、Fe3+可使其变黑,存放时应避免与之接触.
1.7 叶绿素
叶绿素属于吡咯衍生物类,在光合作用中起催化作用,所以只要进行光合作用的生物基本都含有叶绿素.高等植物中主要有叶绿素a、b 两种,它们的区别就是吡咯环上的一个基团不同:叶绿素a 的吡咯环上是甲基,叶绿素b 的吡咯环上是甲醛基,结构差异导致它们颜色也不相同(叶绿素a呈蓝绿色,叶绿素b 呈黄绿色).难溶于水,易溶于乙醇、乙醚等有机溶剂[16],其结构式见图7.
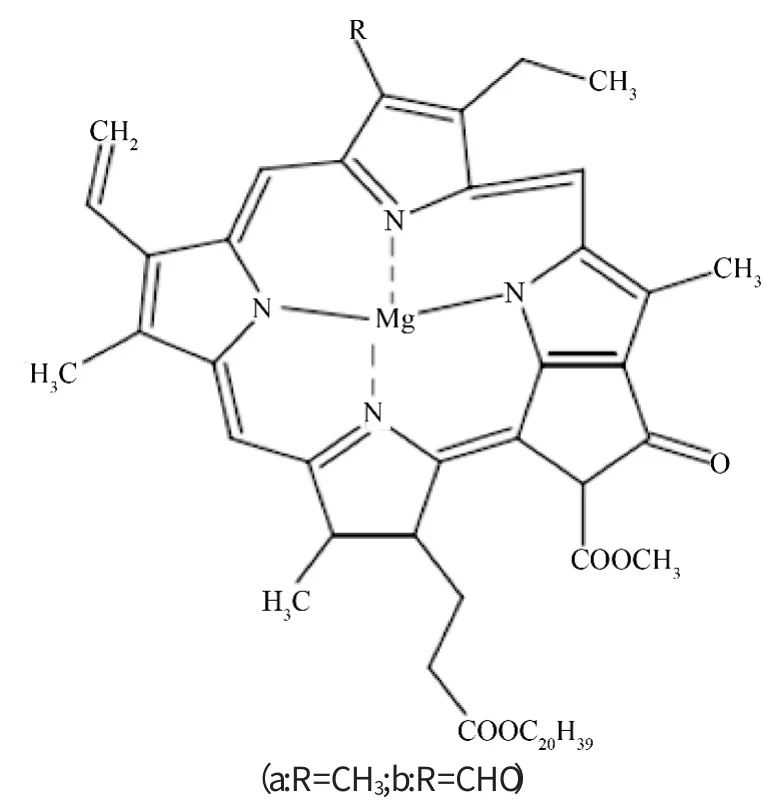
图7 天然色素叶绿素a 和叶绿素b 的结构Fig.7 Structure of natural dye chlorophyll a and b
由图7 可知,4 个吡咯环组成了卟啉环,卟啉环上的R 基要是甲基就是叶绿素a 分子,R 基要是甲醛基就是叶绿素b 分子.叶绿素分子之所以是绿色的就是因为卟啉环中单键和双键形成的共轭体系吸收部分可见光.叶绿素分子自然状态下不稳定性,但是用铜、铁、锌等离子取代叶绿素中的镁离子后,其稳定性就会大大提高[17-18].
1.8 红曲红色素
红曲红色素是红曲霉的一种次级代谢产物,是以大米、黄豆等为原料,利用红曲霉菌发酵制备的天然色素.其化学结构可分为脂肪酸和多聚酮两个部分,熔点为160~192 ℃,可溶于水、乙醚、醋酸、氯仿和正己烷等溶剂中.对光照、温度、酸和碱性溶液的稳定性差、易褪色,其结构式见图8.

图8 红曲红色素的结构Fig.8 Structure of monascus red pigment
由图8 可知,红曲红色素之所以不稳定是因为分子结构中含有高度共扼双键.红曲红色素在中性环境下较稳定,在碱性条件下(pH9~11)的稳定性比酸性环境(pH3~5)强.由于红曲红色素分子中的双键可被Cu2+、Fe3+氧化,其溶液颜色会从亮红色变成红棕色(并产生红褐色沉淀),因此应避免用铁、铜类器皿存放红曲红色素.
1.9 辣椒红色素
辣椒红色素(又叫椒红素或辣椒红),主要来源于茄科的红辣椒果皮,是具有辣椒香味的胭脂红色针状晶体(色泽艳丽、色价高、着色和保色效果好),是类胡萝卜素的一种,属于异戊二烯类色素,其主要成分为辣椒红素和辣椒玉红素.熔点175 ℃左右,不溶于水和甘油,易溶于极性大的有机溶剂,与浓无机酸作用会变为蓝色,其结构式见图9.

图9 辣椒红素的结构Fig.9 Structure of capsanthin
由图9 可知,辣椒红素具有多个不饱和双键,在有氧条件下会加速其氧化分解而褪色.可与Pb3+形成沉淀,Cu2+和Fe3+也能使其褪色(但K+、Ca2+、Na+、Mg2+、Zn2+对其稳定性没有影响,这些金属离子可作为添加剂与辣椒红素一起使用).此外,辣椒红素的耐热(25~70 ℃)、耐酸(pH=3~12)性较强,但耐光性(可见光下稳定,但紫外线易使其褪色)较差.
1.10 其他
除了上述介绍的目前加工业中应用较多的天然色素外,近年来还发现了一些新的天然色素如:从紫苏科的紫苏叶子中提取的紫苏色素;从紫红色甘蓝叶子中提取的红甘蓝色素;由禾本科植物高粱的壳中提取的高梁色素;红米中提取的红米色素.此外还可从动物体内提取到胭脂虫色素、龙虾红色素和蟹壳色素等天然色素[19].
2 天然色素的分离纯化方法
天然色素目前常采用的分离纯化方法主要有:超临界流体萃取法、微波辅助萃取法、分子蒸馏法、溶剂提取法、酶反应法等.
2.1 超临界流体萃取法
超临界流体萃取技术 (Supercritical Fluid Extraction),简称SFE.当处于某个特殊温度或压强(8~50 MPa;35~80 ℃)之上时,气、液相界面消失的状态被称为超临界状态,此状态下的流体叫超临界流体(Super Critical Fluid,SCF),SCF 是兼具气、液两者优点的高密度流体,既具有液体的密度和溶解力又具有气体的低黏度和高渗透力,SCF 的溶解力会随着温度和压力的改变而发生变化从而达到分离提取物的目的.由于CO2超临界温度(31 ℃)接近室温且无毒无污染,不腐蚀设备,常用来做超临界流体[20].不同种类的天然色素的超临界流体萃取的最佳工艺条件有所不同,一般在10~50 MPa、31~80 ℃、3~20 h 的范围内[21-22].
2.2 微波辅助萃取法
微波辅助萃取又叫微波萃取(Microwave Assisted Extraction,简称MAE),是利用偶极子在微波的作用下高速旋转而不断变换正、负极产生涡流和摩擦以及离子传导,在短时间内大量的热量使细胞分子间氢键断裂而引起细胞膜结构破裂,摩擦和碰撞引起的温度上升导致细胞壁破裂,这些都加速了细胞内的天然色素扩散到萃取剂中.微波萃取还具有很好的选择性,对介电性质不同的物质选择性地加热,加热性与介电常数成反比,与极性成正比、微波辅助萃取天然色素的优点是随着微波高频的波动可以加速天然色素溶于萃取剂提高了萃取效率的同时减少了萃取时间,同时微波还具有加热功能,热能在很短的时间内对好几种组分同时进行萃取,并且微波辅助萃取能大大减少萃取溶剂的用量,不仅节约能耗,而且减小了污染,结果还具有可重复性.
2.3 分子蒸馏技术
分子蒸馏法(Molecular Distillation,简称MD)又叫短程蒸馏,是利用不同物质的分子运动平均自由程(一个气体分子相邻两次连续碰撞之间的平均距离)的不同的原理来进行分离的高新技术.首先加热装置对要分离的混合物加热,当分子获得足够能量就会从蒸发面逸出,轻分子的平均自由程比重分子的大,在重分子和轻分子的自由程之间设置一个冷凝面,由于重分子达不到冷凝面而回到蒸发面,保持原有的动态平衡不再逸出,而轻分子能达到冷凝面并不断凝集,破坏了轻分子的动态平衡,使轻分子不断逸出而达到分离目的.天然色素分子蒸馏过程主要分为5 个步骤:(1)天然色素分子从液相主体向蒸发面扩散.(2)天然色素分子从蒸发面上自由蒸发.(3)天然色素分子从蒸发面向冷凝面飞射.(4)天然色素分子在冷凝面上冷凝.(5)收集馏出物和残留物.分子蒸馏法的优点是操作温度低、压力小、分离度高、分离物质不被污染,不仅降低了分离成本,而且保护了天然色素结构不被破坏.
2.4 溶剂提取法
溶剂提取天然色素可分热提法和冷提法两种.根据被提取天然色素的极性、共存杂质的理化特性以及相似相容原理选用对天然色素溶解度大,对不需要溶出成分溶解度小的溶剂,溶剂通过渗透和扩散作用进入样品细胞内,溶解了天然色素和少量杂质后使细胞内外形成浓度差,细胞内的浓溶液不断向外扩散而达到提取天然色素的目的.溶剂提取法的优点是:溶剂便宜、操作简单、提取率高.缺点是:提取天然色素的质量差、纯度低、有异味、有溶剂残留等.
2.5 酶法提取法
天然色素一般存在于植物的细胞内,提取植物中的天然色素时,不仅要穿透细胞膜还要穿过植物的细胞壁,这使天然色素的提取率大大降低,如果能将植物的细胞壁去掉将大幅提高天然色素的提取率,而植物的细胞壁是由纤维素和果胶构成,纤维素酶可以溶解植物细胞壁有利于成分提取.禹华娟等[23]研究表明与水浸分离法相比,酶法提取提高了9.40%~13.35%.天然色素和特定的酶反应产生人们所需要的颜色,如:栀子黄色素的栀子苷在β-葡萄糖苷酶或β-半乳糖苷酶的作用下,可与伯氨基酸(α-氨基酸)发生聚合反应,生成蓝色色素.
分离纯化天然色素的方法很多,但目前的提取率都不太理想.除上述方法外还有:色谱分离法、柱层析法、碱液提取法和膜分离法等[24-26].
3 天然色素的应用概况
3.1 天然色素在食品中的应用
俗话说民以食为天,人们常用“色香味美”来形容一道好菜,人对食物的第一印象就是它的颜色,炒胡萝卜时发现油会变成橙色,而苋菜用热水一烫水就变成红色.天然色素不仅使食品具有诱人的色泽(如彩色饺子、汤圆、小麦、玉米、水果馅月饼、玉米馒头、香芋馒头以及各式蛋糕上色彩斑斓的小动物等),而且营养价值方面也有了质的飞跃,给消费者良好的感官享受和强烈的购买欲.
天然色素虽然使用量不多,但对食品的品质有着重要影响[27-30].天然色素增加食品风味的同时还具有抗菌、抑菌、提高产品保质期的作用.由于不能单独作为食品食用,在食品中主要用于酱油、辣椒酱、泡菜和辣椒油等调味品中,例如:红曲红色素能提高酱油红色指数,用于调味以及烧卤时用的酱油,可使酱油不乌黑;栀子黄色素,可以使酱油的金黄色更明显;萝卜红色素、紫胶红色素用于辣椒酱等酸性产品的着色;红花黄色素可用于甜橙、菠萝、芒果等橙黄色产品的着色;β-胡萝卜素、姜黄色素可用于鸡精的增色和增加营养;辣椒红色素用于饼干喷油与着色;栀子黄色素用于方便面着色;叶绿素铜钠盐和番茄红色素用于蔬菜型挂面的着色;姜黄素用于蛋糕裱装以及月饼馅着色;红米红素用于烘焙食品着色等.
3.2 天然色素在医药保健方面的应用
近年来有关各种癌症、肿瘤高发的报道屡见不鲜,人们谈癌色变的同时也急于寻找出癌症的原因以及预防的措施.众多医学研究及临床试验表明:人体内过剩的自由基(ROS)会在人体内到处抢夺电子,蛋白分子的电子如果被ROS 夺取,那么蛋白质就会与支链连接发生烷基化,蛋白质分子就会发生畸变而导致癌症的发生.研究表明:绝大多数天然色素都具有淬灭人体中的单线态氧、清除自由基和提高人体免疫力,预防癌症发生的功效[31].
叶绿素和它的衍生物具有多方面的医药保健作用,叶绿素分子与人体的血红蛋白分子结构相似,诺贝尔得主Dr.Richand Willstatter 和Dr.Hans Fisher 发现叶绿素有造血功能,产妇和意外失血者饮用叶绿素对其血液恢复会有很大的帮助.叶绿素的衍生物:叶绿素锌、钠盐在临床医学上可有效治疗幼儿缺锌症,皮肤破损以及胃肠溃疡等疾病也可口服叶绿素及其衍生物来帮助愈合,另外例如传染性肝炎、痔疮、白血病也可用叶绿素及其衍生物来辅助治疗.番茄红素含量高低与人的寿命长短有关[32-36],人体自身不能合成,必须通过外界摄入番茄红素,它不仅能调节胆固醇的代谢从而预防心血管疾病,而且还对男性不孕症有特殊的疗效.德国医生做临床对照试验表明:每天补充足够量番茄红素的中老年男子比缺乏番茄红素的群体降低前列腺癌发病率低80%[37],经常补充番茄红素的中老年妇女可大大降低乳腺癌、子宫癌等妇科疾病的发病率,同时对骨质疏松症也有一定的预防作用;β-胡萝卜色素可抑制脂质过氧化、提高免疫力、增强胰岛素敏感性从而能保护视力、降低癌症和糖尿病的发病率[38];姜黄素具有抗炎、抗凝、抗感染和抑制细胞氧化修饰低密度脂蛋白的作用,能够降血脂和预防老年斑及动脉粥状硬化的形成;玉米黄色素在人体内能转化VA,所以有助于保护和恢复视力,还能增强人体的免疫力[39];葡萄皮红色素具有预防冠心病和动脉粥样硬化作用;花青素在具有消炎、抗肿瘤、改善视力的功能同时还能抑制脂蛋白氧化以及血小板凝集的作用,所以能有效预防癌症的发生.紫苏色素具有解毒、散寒、行气和胃的功效.从栀子果实中提取的栀子黄色素具有消炎、解热、利胆和抗氧化的能力[40].
3.3 天然色素在化妆品中的应用
栀子黄色素、β-胡萝卜素、红花黄色素、焦糖、可可色素等多种天然色素具有很强的清除自由基和淬灭单线态氧的能力,常用于防晒品、护肤品等各类化妆品.这是由于清除自由基可有效防止皮肤细胞受到自由基损伤,减少皱纹和雀斑产生;淬灭单线态氧可使皮肤免受紫外线损伤,阻止皮肤光老化,防止诱发皮肤癌.
天然化妆品为皮肤提供健康成分的同时还减轻了皮肤的负担,大大提高了皮肤细胞的呼吸性以及水分的交换率.天然化妆品最大的优点是抗菌、消炎的同时还不刺激皮肤[41-42].例如:焦糖色素的成本很低,但其稳定性很好,在光照、高温等条件下也不变性,对pH 值的变化几乎无反应.焦糖色素不仅色彩鲜艳明亮具有香味,而且很容易上色.紫草红色素从传统中草药紫草根中提取,消斑功效很好;番茄红素不仅红色鲜艳可使化妆品呈现诱人的红色,而且具有很强的抗氧化性能能够延长化妆品的保质期,还可作为着色剂应用于润唇膏和口红等化妆品;可可色素具有耐热、上色性好,可以滋润、保湿皮肤,延缓皮肤衰老.天然色素还能防治各种皮肤病[43-45].随着人们对皮肤新陈代谢的深入了解,天然色素在化妆品中的应用将更广泛.
3.4 天然色素在印染业中的应用
很多合成染料会对皮肤有刺激性,导致皮肤过敏[46].直接染料(直接把纤维等材料染色,不需要其他化学方法辅助染色)、酸性染料(能在酸性介质中染色的染料)和分散染料(一种非离子型染料,水溶性较差)还会导致皮肤病及诱发癌症等.天然色素染料大都来源于动物、植物和微生物,安全性高、无害、无污染、色调独特别致.天然色素在印染领域的使用具有悠久的历史,北宋末年贾思勰所著的《齐民要术》中就有人们从植物中提取天然色素作为染料的记载.由于天然色素染料羟基多(通过范德华力、氢键染上织物)从而亲水性强,而合成纤维的疏水性强,染色时需要用媒染剂(明矾、硫酸铜、重铬酸钾等)来固定颜色,这是因为金属离子可与天然色素染料中的羟基形成络合物同时又能和纤维中的羟基形成络合物,通过金属离子可把染料分子和纤维连结在一起,提高了上染率和染色牢度.姜黄色素通过浸酸、媒染的方法染棉可得到多种颜色,耐洗牢度很高;茶叶中的儿茶素(多酚类天然色素)以硫酸铜作为媒染剂,可把棉、黄麻等织物染成棕色;虫胶、姜黄和洋葱色素可以对涤纶织物染色,在常压下洋葱染料不能对涤纶着色,但是姜黄和虫胶染料可染浅色;叶绿素、可可色素、栀子黄色素等天然色素也可用于纤维素的染色;天然色素可在高温高压条件下通过各种媒染剂(明矾上染率高,硫酸铜耐光牢度好)处理后染涤纶.高压比常压法染色效果好[47-50].
4 天然色素在研发中存在的问题和解决办法
4.1 存在的问题
目前已知的天然色素有80 多种[51].大部分天然色素对人体是无毒的,但是藤黄却有剧毒,因此“天然”并非等同“安全”,所以不能忽视天然色素的安全性.天然色素在研发中还存在一些问题:研究广泛但不深入;毒理学评价滞后;稳定性差;提取率和纯度低;对天然色素的研究成果缺乏比较性.
4.2 解决的办法
针对上述天然色素在应用中存在的问题,可以采取以下解决办法:(1)深入对天然色素的结构、生理以及药理保健方面的研究.(2)对新开发的天然色素进行严格的管理和审批,并对它们的安全性采用综合评价,如:化学结构、稳定性以及动物实验毒性等并建立相对应的ADI 值(人体每日最大允许摄入量)[52].(3)通过不同色素间的结合、离子替换以及加入稳定剂等方法可以大大提高天然色素的稳定性,例如:甜菜红素与茶色素结合在一起后稳定性大大提高,醌类色素用明矾作稳定剂后大大提高了色素的稳定性[53],用铜取代叶绿素中的镁然后制成钠盐或钾盐后绿色素非常稳定.(4)利用愈伤组织以及微生物来生产天然色素不仅扩大了天然色素的来源、提高天然色素的产率,而且减少了环境、季节、物种对天然色素的限制,如:用甜菜的愈伤组织生产甜菜红色素,用葡萄细胞悬浮液培养生产花青素,用藏红花的细胞培养可生产藏红花素[54].(5)将多种不同来源的同一种天然色素进行分离纯化、结构功能和生物学作用等方面进行系统和全面的研究与比较,人们才会对天然色素有更深刻的了解.
5 结论与展望
综上所述,天然色素具有化学合成色素无法比拟的优越性质,在色素行业所占的比重越来越大,随着人们对天然色素研究的深入、环保意识的提高和食品毒理学评价等领域的发展,天然色素将会取代毒副作用较强的化学合成色素成为未来色素行业发展的新方向.然而,目前天然色素研究停滞不前的主要原因是天然色素成分复杂难以完全分离、精制和鉴定,这导致了人们对天然色素成分的结构、性质、生理活性以及安全性认识不足,归根结底还是目前分离提纯技术还不成熟.现阶段应着力于以下几个方面:一是改进提取工艺,研究出高效经济的提取分离技术.二是提高副产品的综合利用率,增加产品的附加值.三是针对天然色素存在的缺点研究出更好的解决方法.四是扩大天然色素的应用领域.相信在不久的将来,天然色素将会在食品、医药保健、印染、化妆品等领域获得更加广泛的应用.
[1]Eleonora M B,Daniel R C,Leif H,et al.Quenching of excited states of red-pigment zinc protoporphyrin IX by hemin and natural Reductors in dry-cured hams[J].European Food Research and Technology,2011,232:343-349.
[2]Caro Y,Anamale L,Fouillaud M,et al.Natural hydroxy anthraqu-inoid pigments as potent food grade colorants:an overview[J].Natural Products and Bioprospecting,2012,2(5):174-193.
[3]Ho K K H Y,Ferruzzi M G,Liceaga A M,et al.Microwave assisted extraction of lycopene in tomato peels:effect of extraction conditions on all-trans and cis-isomer yields[J].LWT-Food Science and Technology,2015,62(1):160 -168.
[4]Kujawska M,Ewertowska M,Adamska T,et al.Antioxidant effect of lycopene -enriched tomato paste on N-nitro-sodiethylamine induced oxidative stress in rats [J].Journal Physiol Biochem,2014,70(4):981-990.
[5]Frengova G I,Beshkova D M.Carotenoids from rhodotorula and phaffia:yeasts of biotechno-logical importance[J].Industrial Microbiol Biotechnol,2009,36(2):163-180.
[6]Yan Ru-Long,Luo Jia,Wang Chuan-Xin,et al.Cu (I) -catalyzed synthesis of polysubstituted pyrroles from dialkylethy lenedicarboxylates and β-Enamino ketones or esters in the presence of O2[J].Journal of Organic Chemistry,2010,75(15):5395-5397.
[7]Subudhi U,Chainy G B.Curcumin and vitamin E modulate hepatic antioxidant gene express -ion in PTU -induced hypothyroid rats[J].Molecular Biolgy Reports,2012,39(11):9849-9861.
[8]朱尽顺,何方.姜黄色素的提取工艺及色素稳定性分析[J].中国纤检,2015(1):86-88.
[9]Hirth M,Preiβ R,Mayer-Miebach E,et al.Influence of HTST extrusion cooking process parameters on the stability of anthocyanins,procyanidins and hydroxycinnamic acids as the main bioactive chokeberry polyphenols[J].LWT -Food Science and Technology,2015,62(1):511-516.
[10]Nems A,Peksa A,Kucharska A Z,et al.Anthocyanin and antioxidant activity of snacks with coloured potato [J].Food Chemistry,2015,172:175-182.
[11]Chandrasekhar J,Madhusudhan M C,Raghavarao K S M S.Extration of anthocyanins from red cabbage and purification using adsorpion[J].Food and Bioproducts Processing,2012,90:615-623.
[12]黄欢,胡慧霞,姜联合,等.植物甜菜色素的研究进展[J].生物学通报,2014,49(8):1-4.
[13]Chauhan S P,Sheth N R,Rathod I S,et al.Analysis of betalains from fruits of opuntia species [J].Phytochemistry Reviews,2013(12):35-45.
[14]Ravichandran K,Saw N M M T,Mohdaly A A A,et al.Impact of processing of red beet on betalain content and antioxidant activity[J].Food Research International,2013,50(2):670-675.
[15]曹机良,曹毅,张成玉,等.甜菜红色素的稳定性探讨[J].染整技术,2014,36(3):28-31.
[16]Liu Weibing,Jiang Huanfeng,Bin Liang.One potsilvercatalyzed and PIDA-mediated seqential reaction:synthesis of poly -substituted pyrroles directly from alkynoates and amines[J].Organic Letters,2010,12(2):312-315.
[17]Sukhendu M,Srijit B,Umasis S J N.Iron(III)-catalyzed four -component coupling reaction of 1,3-dicarb-only-compounds,amines,aldehydes,and nitroalkanes:a simple and direct synthesis of functionalized pyrroles [J].Journal of Organic Chemistry,2010,75(5):1674-1683.
[18]Jessica G G,Sarah J P Y,Nathan R B .Synthesis of unsymmetrical 3,4 -diaryl -3 -pyrrolin-2-ones utilizing pyrrole weinreb amides[J].Journal of Organic Chemistry Chem,2011,76(20):8203-8214.
[19]杨双春,李春雨,潘一.食品工业中微生物色素的研究进展[J].食品研究与开发,2014,35(1):114-117.
[20]张郁松.辣椒红素超临界萃取与有机溶剂萃取的比较[J].中国调味品,2013(4):101-103.
[21]M-Sanchez W D.Supercritical fluid extraction of carotenoids and cholophylla from nannoch loropsis gaditana[J].Journal of Food Engineering,2005,66:245-251.
[22]Liang M T,Yang C H,Li S T,et al.Antibacterial and antioxidant properties of ramulus cinnamomi using supercritical CO2extraction [J].European Food Research and Technology,2008,227(5):1387-1396.
[23]禹华娟,孙智达,谢笔钧.酶辅助提取莲房花青素工艺及氧化活性研究[J].天然产物研究与开发,2010,22(10):154-158.
[24]Suo Q L,He W Z.Micronization of the natural pigment bixin by the SEDS process through prefilming atomization[J].Powder Technology,2005,154:110-115.
[25]Chen Dan,Wu Zanmin.Study on extraction purification process of capsicum red pigment[J].Journal of Agricultural Science,2009,1(20):94-100.
[26]Xin A,Xuefeng L,Zouqing Z,et al.RAPD teachnique used todeter-minthe purity of hybrid hot pepper seeds[J].Hunan Agricultural Science and Technology Newsletter,2000(1):119-123.
[27]Munawar N,Jamil H M T H.The islamic perspective approach on plant pigments as natural food colourants[J].Procedia Social and Behavioral Sciences,2014,121:193-203.
[28]斯波.天然色素在复合调味食品中的应用[J].中国调味品,2011,36(2):97-101.
[29]苗璇.食用天然色素研究应用现状及其发展前景展望[J].化工管理,2013(5):5-7.
[30]Bridle P,Timberlake C F.Anthocyanins as natural food colours selected aspects[J].Food Chemistry,1997,58(2):103-109.
[31]A ssous M T M,Abdel H M M,Medany G M.Evaluation of red pigment extracted from purple carrots and its utilization as antioxidant and natural food colorants[J].Annals of Agricultural Sciences,2014,59(1):1-7.
[32]包华音.番茄红素药理作用的近五年研究进展[J].食品研究开发,2014,35(19):145-147.
[33]Tamilselvan P,Langeswaran K,Vijayaprakash S,et al.Efficiency of lycopene against reproductive and developmental toxicity of bisp -henol a in male sprague dawley rats[J].Biomedicine Preventive Nutrition,2014,4(4):491-498.
[34]Chen W,Lu Y,Wu J,et al.Beta-elemene inhibits melanoma growth and metastasis via suppressing vascular endothelial growth factor mediated angiogenesis [J].Cancer Chemother Pharmacol,2011,67(4):799.
[35]Lopes L B,Vandewall H,Li H T,et al.Topical delivery of lycopene using microemulsions:enhanced skin penetration and tissue anti -oxidant activity[J].Journal of Pharmaceutical Sciences,2010,99(3):1346-1357.
[36]张艳梅,黄泽清,高浩然,等.番茄红素对肺癌患者围术期免疫功能的调节[J].辽宁医学院学报,2011,32(1):35-37.
[37]Chen Liping,He Shuying,Zheng Heng,et al.Effectsand mechanisms of lycopene on the proliferation of vascular smooth muscle cells[J].Chinese Journal of Natural Medicines,2010(3):218-222.
[38]Van P G,Goldbohm R A.Epidemiologic evidence for beta caroteneand cancer prevention[J].The American Journal of Clinical Nutrition,1995,62:1393-1402.
[39]杜泽化,任娇艳.玉米黄色素提取工艺及生物活性研究进展[J].中国食品添加剂,2014(2):214-219.
[40]周坦洋,罗芙蓉,白彬.葡萄籽原花青素生物药理活性的研究进展[J].哈尔滨医科大学学报,2012,46(1):94-96.
[41]Mcardle F,Rhodes L F,Parslew R A G,et al.Effects of oral vitamin E and β -carotene supplementation on ultra viole tradiation -induced oxidative stress in human skin[J].The American Journal of Clinical Nutrition,2004,80:1270-1275.
[42]Wulf H C,Sandby-Moller J,Kobayasi T,et al.Skin aging and natural photoprotection[J].Micron,2004,35(3):185-191.
[43]Yeh S L,Hu M L,Huang C S.Lycopene enhances UVA -induced DNA damage and expression of heme oxygenase -1 in cultured mouse embryo fibroblasts[J].European Journal of Nutrition,2005,44(6):365-370.
[44]Darvin M,Patzelt A,Gehse S,et al.Cutaneous concentration of lycopene correlates significantly with the roughness of the skin [J].European Journal of Pharmaceutics and Biopharmaceutics,2008,69(3):943-947.
[45]Blanch G P,Castillo M L,Mar-Caja M,et al.Stabilization of all-trans lycopene from tomato by encapsulation using cyclo-dextrins[J].Food Chemistry,2007,105(4):1335-1341.
[46]杨建军,崔岩.天然染料的染色技术与媒染方法[J].通化师范学院学报:人文社会科学,2014,35(6):37-43.
[47]Bulut M O,Akar E.Ecological dyeing with some plant pulps on woolen yarn and cationized cotton fabric[J].Journal of Cleaner Production,2012,32:1-9.
[48]Ibrahim N A,El-Gamal A R,Gouda M,et al.A new approach for natural dyeing and functional finishing of cotton cellulose [J].Carbohydrate Polymers,2010,82(4):1205-1211.
[49]Sava V M,Yang S M,Hong M Y,et al.Isolation and characterization of melanic pigments derived from tea and poly phenols[J].Food Chemistry,2001,73(2):177-184.
[50]Kamel M M,El-Shishtawy R M,Yussef B M,et al.Ultrasonic assisted dyeing Ⅲ.dyeing of wool with lac as a natural dye [J].Dyes and Pigments,2005,65(2):103-110.
[51]Caro Y,Anamale L,Fouillaud M,et al.Natural hydroxy anthraquinoid pigments as potent food grade colorants:an overview[J].Natural Products and Bioprospecting,2012,2(5):174-193.
[52]成黎.天然使用色素的特性、应用、安全性评价及安全控制[J].食品科学,2012,33(23):399-404.
[53]Ali N F,El-Mohamedy R S R.Eco-friendly and protective ntaural dye from red prickly pearly pear (Opuntia Lasiacanthapfeiffer) plant[J].Journal of Cleaner Production,2003,11(5):499-509.
[54]Marie -Rose V C,Martine C B,Francois C,et al.Spectroscopic characterization of crocetin derivatives from crocus sativus and gardenia jasminoides[J].JournalAgricultureFood Chemist ry,1997,45:1055-1061.

