离子交换色谱分离-紫外检测法测定吡啶离子液体阳离子
刘元昊 孙晓娇 刘 峰 于 泓邓春娜
(哈尔滨师范大学化学化工学院,哈尔滨150025)
离子交换色谱分离-紫外检测法测定吡啶离子液体阳离子
刘元昊 孙晓娇 刘 峰 于 泓*邓春娜
(哈尔滨师范大学化学化工学院,哈尔滨150025)
建立了用离子交换色谱分离-紫外检测法测定N-乙基吡啶、N-丁基吡啶和N-丁基四甲基吡啶3种吡啶离子液体阳离子的方法。采用磺酸型阳离子交换柱,以乙二胺-柠檬酸-乙腈为流动相,研究了流动相和色谱柱温度对离子保留行为的影响和规律。实验发现,吡啶阳离子的保留过程是放热过程。优化后的色谱条件:流动相为乙二胺(0.2mmol//L)-柠檬酸(0.3mmol//L)-乙腈(0.5%,v/v,pH=4.2),流动相流速为1.0mL/min,色谱柱为Shim-pack IC-C1阳离子交换柱,色谱柱温度为30℃。在此条件下3种吡啶阳离子可以达到基线分离。所测阳离子的检出限(S/N=3)分别为0.01、0.01、0.02mg/L,峰面积的相对标准偏差(n=5)小于0.8%。紫外检测法测定化学实验室合成的吡啶离子液体样品,样品加标后测得的加标回收率在96.3%~104%。方法准确、可靠、快速,具有较好的实用价值。
离子液体;吡啶阳离子;阳离子交换色谱;紫外检测;乙二胺
0 前言
离子液体,又称室温熔融盐或室温离子液体,性质是由组成它的阴、阳离子决定的,其物理化学特性如熔点、粘度、密度、溶解性、热稳定性以及酸碱性等可以通过选择合适的阴、阳离子进行调配,能够在很宽的范围内加以调变;尤其是酸碱性的调变,在用作反应介质和催化剂方面极为有利。此外,其蒸汽压低和不可燃性的特点,使之成为一种环境友好型化学试剂。离子液体的这些特性使其被广泛应用于实验室的有机合成、催化化学、分析化学、电化学等领域[15],并且在工业上已展现很好的应用前景。因此,有关离子液体分离检测方法的研究越来越受到人们的重视。吡啶阳离子是构成离子液体的主要有机阳离子,对离子液体的性能有重要影响,因而对其分析研究很有必要。目前,分离测定离子液体阳离子的方法主要有反相液相色谱法[6]、反相离子对色谱法[7-10]和离子交换色谱法[11-14]等。用离子交换色谱法测定吡啶离子液体阳离子主要采用电导检测方法,尚无用紫外检测方法的研究报道。本文研究了离子交换色谱-紫外检测法分离检测吡啶阳离子的新途径,并成功应用于吡啶离子液体样品的测定,方法准确可靠。
1 实验部分
1.1 试剂
柠檬酸为优级纯试剂,酒石酸、盐酸、乙二胺为分析纯试剂,以上试剂购自天津光复精细化工研究所。乙腈为色谱纯试剂,购自中国迪马科技有限公司。N-丁基-4-甲基吡啶四氟硼酸盐([BMPy][BF4]),N-丁基吡啶三氟甲磺酸盐([BPy][CF3SO3])和碘化N-乙基吡啶([EPy][I])离子液体,纯度99%,购自上海成捷化学有限公司。
1.2 溶液配制与处理
配制溶液均采用电阻率为18.2MΩ·cm的超纯水,由美国Millipore公司Simplicity纯水系统制备。
吡啶阳离子的标准储备溶液(1 000mg/L):准确称取0.158 0g N-丁基-4-甲基吡啶四氟硼酸盐([BMPy][BF4])、0.209 3g N-丁基吡啶三氟甲磺酸盐([BPy][CF3SO3])和0.217 5g碘化N-乙基吡啶([EPy][I])定容于100mL容量瓶中,根据实验需要稀释至色谱进样所需浓度,并用0.22μm滤膜过滤后使用。用超纯水配制实验所用浓度的流动相,用0.22μm滤膜过滤,并进行15min真空脱气后使用。真空脱气采用美国IDEX公司DOA-P504-BN型无油真空泵,测量流动相酸度采用上海精密科学仪器有限公司PHSF-3F型pH计。
1.3 色谱分析
色谱分析采用日本岛津公司LC-20A型液相色谱仪。此色谱仪主要包含SPD-20A型紫外检测器、LC-20AD sp型流动相输液泵、SIL-20A型自动进样器、CTO-20AC型色谱柱温箱和LC Solution Ver 1.1色谱工作站。
色谱分析条件:流动相采用乙二胺(0.2mmol/L)-柠檬酸(0.3mmol/L)-乙腈(0.5%,v/v);色谱柱用日本岛津公司Shim-pack IC-C1型磺酸性阳离子交换柱(150mm×5.0mm i.d.,10μm);流动相流速为1.0mL/min;色谱柱温度为30℃;色谱分析进样体积为20μL;紫外检测波长为254nm。
2 结果与讨论
2.1 检测波长的选择
实验在流动相为乙二胺(0.2mmol/L)-乙腈(2%,v/v,pH=4.0)的条件下,考察了不同检测波长234、244、254、264、274nm对测定的影响。结果发现,当波长为234nm和244nm时,N-丁基-4-甲基吡啶阳离子([BMPy]+)的色谱峰较小;当波长为274nm时,[BMPy]+未被检测出,综合比较[EPy]+、[BPy]+、[BMPy]+三种阳离子的色谱峰形和基线噪音值,在254nm时最佳。
2.2 不同流动相对测定的影响
2.2.1 乙二胺对离子测定的影响
以乙二胺-乙腈(2%)为流动相,色谱柱温度设定为30℃,流速为1.0mL/min,分别考察0.05、0.1、0.2、0.3、0.4mmol/L乙二胺(pH=4.0,用HCl调节)对[EPy]+、[BPy]+、[BMPy]+测定的影响。实验结果表明,吡啶阳离子的保留时间随着乙二胺浓度的增大而缩短。当用乙二胺(0.05mmol/L)时,[BMPy]+的保留时间较长(40min);当浓度为0.3、0.4mmol/L时,[BMPy]+与[BPy]+色谱峰部分重叠,分离效果不好;当浓度为0.2mmol/L时,色谱峰形和分离度较好且优于0.1mmol/L,因此,选择乙二胺浓度为0.2mmol/L。[EPy]+、[BPy]+、[BMPy]+保留因子的对数值(lgk)与乙二胺浓度的对数值(lgE)二者关系曲线方程分别为:[EPy]+,lgk=-0.493 6×lgE-0.463,r=0.993 3;[BPy]+,lgk=-0.614×lgE-0.025 2,r=0.990 9;[BMPy]+,lgk=-0.514 1×lgE-0.333 6,r=0.992 5。由曲线方程可知两者间线性关系良好,[EPy]+、[BPy]+、[BMPy]+的保留模式基本是离子交换[15]。
2.2.2 不同有机酸对离子测定的影响
实验考察了流动相中分别加入柠檬酸、草酸和酒石酸3种有机酸对测定的影响。用乙二胺(0.2mmol/L)和有机酸(0.3mmol/L,柠檬酸或草酸或酒石酸)及乙腈(2%)的混合溶液为流动相,色谱柱温度为30℃,流速为1.0mL/min,对3种阳离子分离测定。结果发现,当流动相中加入酒石酸时,25min内可以分离测定3种阳离子,时间较长;当流动相中加入草酸或柠檬酸时,3种阳离子在15min内即可分离测定,且分析物的色谱峰不受系统峰干扰。由于柠檬酸比草酸更稳定,因此选定乙二胺-柠檬酸-乙腈为流动相。
为达到更好的分离效果,实验固定乙二胺(0.2mmol/L)-乙腈(2%)-柠檬酸为流动相,分别考察浓度0.2、0.3、0.4、0.5、0.6mmol/L柠檬酸对[EPy]+、[BPy]+、[BMPy]+测定的影响。结果表明,3种阳离子的保留时间随着柠檬酸浓度的增加略有缩短,变化不明显;当用0.2mmol/L的柠檬酸时,系统峰干扰[EPy]+的色谱峰。因此流动相中用0.3mmol/L的柠檬酸。
2.2.3 不同乙腈浓度对离子测定的影响
实验设定流动相流速为1.0mL/min,色谱柱温度为30℃,在乙二胺(0.2mmol/L)和柠檬酸(0.3mmol/L)混合溶液流动相中分别加入体积分数为0.3%、0.5%、1%、2%和3%乙腈,考察不同乙腈浓度对吡啶阳离子保留时间的影响。在液相色谱中,流动相中乙腈的体积分数[φ(ACN)]对分析物保留因子(k)的影响存在如下关系:lgk=aφ(ACN)+b。3种吡啶阳离子的lgk与φ(ACN)之间的线性回归方程如下:[EPy]+,lgk=-5.92φ(ACN)-0.002 5,r=0.991 5;[BPy]+,lgk=-12.81φ(ACN)+0.602 4,r=0.990 9;[BMPy]+,lgk=-17.11φ(ACN)+0.936 8,r=0.991 7。由此可知,方程相关系数在0.99以上,且斜率为负值,表明lgk与φ(ACN)之间有较好的线性关系,各离子的保留时间随着乙腈含量的增加均缩短,且按[EPy]+、[BPy]+、[BMPy]+的次序,保留时间缩短程度增大。原因是有机溶剂乙腈减弱了疏水性吡啶阳离子与固定相的吸附作用,促进了分析物的洗脱,导致保留时间缩短。依[EPy]+、[BPy]+、[BMPy]+次序,离子的疏水性增强(即与固定相的吸附作用增强),因此当乙腈浓度增加时,离子保留时间的缩短幅度增大。
随着流动相中乙腈体积分数的增加,各离子的色谱峰形均有所改变,当乙腈含量小于2%时,[EPy]+、[BPy]+、[BMPy]+的色谱峰分离效果较好;为保证同时、快速分离3种阳离子并兼顾各离子的色谱峰形及彼此间的分离度,最终确定乙腈含量为0.5%。
2.3 色谱柱温度对离子保留的影响
分别测试色谱柱温度25、30、35、40、45℃变化对离子保留时间的影响。吡啶阳离子的范特霍夫曲线方程lnk=-ΔH/(RT)+ΔS/R+lnφ(k是保留因子,T是热力学温度,其它项在固定色谱条件下为常数)[16-17]如下:[EPy]+,lnk=807.0×1/T-2.785 8,r=0.997 2;[BPy]+,lnk=1 390.5×1/T-3.429 6,r=0.995 7;[BMPy]+,lnk=1 649.4× 1/T-3.586 5,r=0.995 2。由此可知,曲线斜率均为正值,方程的相关系数接近1,说明吡啶阳离子的保留是放热过程,保留时间随温度的升高而缩短,且阳离子基团越大保留时间缩短的幅度越大。由于在接近室温的30℃,3种阳离子即可达到较好的分离,因此,选择色谱柱温度为30℃。
2.4 检出限、线性和精密度实验
通过以上系列考察,确定最佳的色谱条件见“1.3色谱分析”部分。在此条件下测定吡啶阳离子标准样品的色谱图见图1,[EPy]+、[BPy]+和[BMPy]+在15min内基线分离。以3倍信噪比计算检出限,5次重复测定[EPy]+、[BPy]+和[BMPy]+(20mg/L)混合标准样品计算相对标准偏差(RSD),以峰面积(y)对离子质量浓度(x,mg/L)求得线性回归方程。方法的检出限、精密度和线性范围见表1。表1说明分析三种阳离子的灵敏度较高,精密度较好。
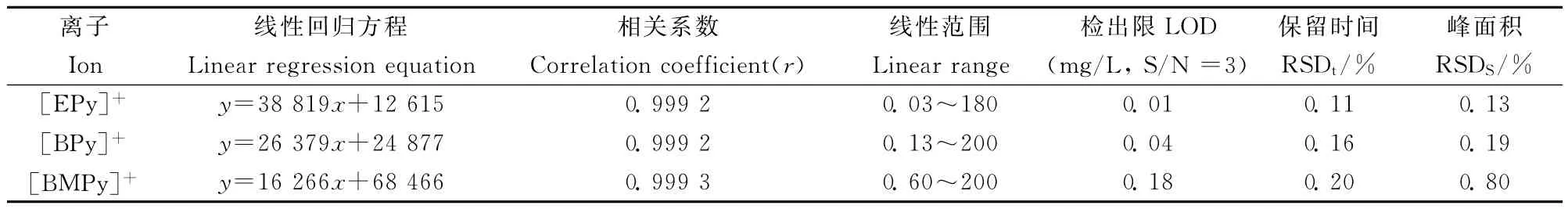
表1 方法的检出限、相对标准偏差和线性范围Table 1 Limits of detection(LODs),relative standard deviations(RSDs)and linear ranges(n=5) /(mg·L-1)

图1 3种吡啶阳离子混合标准溶液的色谱图Figure 1 Chromatogram of three pyridinium cations standard mixture.
2.5 样品分析
采用本方法测定了实验室合成的碘化N-乙基吡啶([EPy][I])、N-丁基吡啶三氟甲磺酸盐([BPy][CF3SO3])和N-丁基-4-甲基吡啶四氟硼酸盐([BMPy][BF4])3种离子液体样品。分别准确称取0.101 3g碘化N-乙基吡啶、0.101 0g N-丁基吡啶三氟甲磺酸盐、0.101 0g N-丁基-4-甲基吡啶四氟硼酸盐离子液体,用超纯水配制成100mL储备溶液。再分别各取1mL储备溶液用超纯水稀释至50mL,稀释液经0.22μm滤膜过滤后,用“1.3”中色谱条件进行分析,样品色谱图和样品分析结果分别见图2和表2。用标准加入法测定了方法的加标回收率,数据亦见表2(其中w=(ρ0×V×N/m)×100%;w—离子液体样品中阳离子的质量分数;ρ0—被测溶液中阳离子的浓度;V—被测溶液的体积;N—稀释倍数;m—样品的质量),其RSD(n=5)均小于1.5%,表明方法能用于离子液体样品中吡啶阳离子的分析。

图2 3种合成离子液体样品的色谱图Figure 2 Chromatograms of three synthesized ionic liquid samples.

3 结论
建立了离子交换色谱分离,用紫外检测法的测定吡啶离子液体阳离子的分析方法。用磺酸性阳离子交换柱,以乙二胺、柠檬酸和乙腈混合液为流动相即可分离吡啶阳离子。可通过调整乙二胺浓度及乙腈含量改善分离。吡啶阳离子主要以离子交换模式被保留,且保留时间随着色谱柱温度的升高而缩短。将此方法应用于测定实验室合成的3种吡啶离子液体样品,能满足离子液体中吡啶阳离子的定量分析要求。
[1]李丹,张欣,于泓 .离子色谱法同时分析离子液体中三氟乙酸根、四氟硼酸根和三氟甲烷磺酸根[J].中国无机分析化学(ChineseJournalofInorganicAnalytical Chemistry),2012,2(3):35-37.
[2]王松,张争艳,常欠欠,等 .离子液体在合成酯反应中的应用[J].化学试剂(ChemicalReagents),2014,36(12):1078-1082.
[3]王慧勇,李志勇,王键吉 .利用双水相分离回收离子液体的研究进展[J].中国科学:化学(ScientiaSinica Chimica),2014,44(6):831-838.
[4]董影杰,于泓,王婧菲,等 .以离子液体为流动相的高效液相色谱-间接紫外检测法分析四甲基铵根离子[J].分析化学(ChineseJournalofAnalyticalChemistry),2011,399(8):1251-1255.
[5]郑秀荣,马亚杰,于泓 .以咪唑离子液体为紫外吸收试剂的高效液相色谱/间接紫外检测法分离测定烷基磺酸盐[J].分析测试学报(JournalofInstrumentalAnalysis),2014,33(9):1026-1031.
[6]孙艺梦 .高效液相色谱-间接紫外检测法分析吗啉离子液体阳离子的研究[D].哈尔滨:哈尔滨师范大学,2013.
[7]高微,于泓,马亚杰 .梯度淋洗离子对色谱法测定咪唑离子液体中的阳离子[J].色谱(ChineseJournalof Chromatography),2010,28(6):556-560.
[8]刘玉珍,于泓,张仁庆 .离子液体的阴离子三氟乙酸根、硫氰酸根、四氟硼酸根和三氟甲磺酸根的离子对色谱-直接电导检测法分析[J].色谱(ChineseJournalofChromatography),2012,30(4):384-390.
[9]Huang X,Yu H,Dong Y J.Rapid and simultaneous determination of imidazolium and Pyridinium ionic liquid cations by ion-pair chromatography using a monolithic column[J].Chin.Chem.Lett.,2012,23(7):843-846.
[10]王淼煜,于泓,李萍,等 .离子对色谱-间接紫外检测法分析哌啶离子液体阳离子[J].色谱(ChineseJournal ofChromatography),2014,32(7):773-778.
[11]刘永强,陈倩,于泓,等 .同系物季铵盐离子液体阳离子的离子交换色谱法分析[J].分析测试学报(Journal ofInstrumentalAnalysis),2014,33(10):1154-1159.
[12]孙晓娇,于泓,张仁庆.离子色谱-直接电导检测法分离测定吗啉离子液体阳离子[J].分析测试学报(Journal ofInstrumentalAnalysis),2013,32(6):705-709.
[13]张仁庆,于泓,刘玉珍.离子色谱-直接电导检测法分析哌啶离子液体阳离子[J].色谱(ChineseJournalof Chromatography),2012,30(7):728-732.
[14]陈倩,于泓,孟令敏,等 .吡啶离子液体阳离子的离子色谱法分析[J].分析测试学报(JournalofInstrumentalAnalysis),2011,30(1):38-42.
[15]Haddad P R,Foley R C.Modeling of cation retention in ion chromatography using fixed-site and dynamically coated ion-exchange columns[J].J.Chromatogr.A,1990,500:301-312.
[16]Yu H,Mou S F.Effect of temperature on the retention of amino acids and carbohydrates in high-performance anion-exchange chromatography[J].Chromatogr:A,2006,1118(1/2):118-124.
[17]Yu H,Li R S.Effect of Column Temperature on the Retention of Inorganic Anions and Organic Acids in Non-Suppressed Anion-Exchange IC[J].Chromatographia,2008,68(7/8):611-616.
Determination of Pyridinium Ionic Liquid Cations by Ion Exchange Chromatography with Ultraviolet Detection
LIU Yuanhao,SUN Xiaojiao,LIU Feng,YU Hong*,DENG Chunna
(CollegeofChemistryandChemicalEngineering,HarbinNormalUniversity,Harbin,Heilongjiang150025,China)
A rapid method for simultaneous determination of three pyridinium ionic liquid cations,such as n-erthyl pyridinium cation([EPy]+),n-butyl pyridinium cation([BPy]+)and n-hexyl pyridinium cation([BMPy]+)by ion exchange chromatography coupled with ultraviolet detection was developed.The effects of mobile phase and column temperature on retention of the cations were investigated with sulfonic acid base cation-exchange column using ethylenediamine-citric acid-acetonitrile as mobile phase.The results indicated that,with the increase of column temperature,the retention times of pyridinium cations were reduced,so the retention process of pyridinium cations is exothermic.The optimum chromatographic conditions were as follows:mobile phase:0.2mmol/L ethylenediamine-0.3mmol/L citrate acid-0.5% acetonitrile(pH=4.2);flow rate:1.0mL/min;column temperature:30℃.Under the optimized conditions,three pyridinium cations were successfully separated.The detection limits(S/N=3)for[EPy]+,[BPy]+,[BMPy]+were 0.01,0.01and 0.02mg/L,respectively.The relative standard deviations(RSDs,n=5)for peak areas were less than 0.8%.The method has been applied to thedetermination of pyridinium ionic liquids synthesized in chemical laboratory with the spiked recoveries of 96.3%to 103.7%.The method is accurate,reliable and rapid,and has good practical value.
ionic liquids;pyridinium cations;ion chromatography;ultraviolet detection;ethylenediamine
O657.32;TH744.12
A
2095-1035(2015)04-0083-05
2015-06-03
2015-09-09
黑龙江省大学生创新创业训练项目(201410231015,B201307)资助
刘元昊,男,学生。E-mail:350830285@qq.com
*通信作者:于泓,男,教授,主要从事离子色谱和高效液相色谱的分析研究。E-mail:yuhonghsd@126.com
10.3969/j.issn.2095-1035.2015.04.019

