双侧肱骨近端骨骼外形一致性的三维CT研究
朱以明 陈辉 姜春岩 李奉龙 李旭 李岳 卓洪武 宋关杨
1 北京积水潭医院(北京100035)
2 中国科学院软件研究所(北京100190)
Hill-Sachs损伤, 即肱骨头后上方的压缩骨折,是复发性肩关节前脱位病人中常见的一类骨性损伤。 现有研究表明, 非常巨大的Hill-Sachs损伤可明显影响Bankart修复术的疗效,导致病人出现术后复发脱位[1-4]。但是,由于难以估计病人肱骨头在出现Hill-Sachs损伤之前正常形态,因而也难以确定其Hill-Sachs损伤的确切深度及体积。既往曾有研究证实,正常人双侧肩盂解剖形态非常接近, 因而可以健侧肩盂作为患侧肩盂的模板,来确定患侧肩盂骨缺损的形态及体积[5]。 我们由此推测, 如能证实正常人双侧肱骨头解剖形态亦十分接近,则有可能以健侧肱骨头作为患侧肱骨头的模板,从而得到Hill-Sachs损伤的精确形态特征。 鉴于此,本项研究通过对肩关节正常的健康人双侧肱骨头三维CT影像进行对比研究, 旨在证实双侧肱骨头解剖形态的一致性。
1 材料和方法
患者行胸部三维CT检查时, 往往需将双侧肩关节一同进行扫描。 我们利用无肩部疾患病史病人的胸部三维CT数据, 研究正常人群双侧肱骨近端解剖结构的一致性。 我们收集了从2012年1月到2012年6月间在我院放射科行胸部三维CT检查的所有患者的CT数据。 根据以下标准选择三维CT数据, 形成健康人双侧肩关节三维CT数据库。
CT数据入选标准:(1) 患者行CT检查时体位为双上肢紧贴体侧或双上肢抱头;(2)CT应包括完整的双侧肱骨头结构;(3)CT扫描条件: 140 KV, 300 mA, 螺距1.0,层厚0.5 mm,矩阵512×512;(4)患者既往无肩关节疾患病史,目前CT显示无明显肩关节骨性损伤。
获得三维CT数据后需对其进行进一步处理。 首先需将骨性结构与周围软组织影分割开来(图1)。

图1
第二步,由于我们仅对骨骼表面轮廓感兴趣,不需要研究髓腔内形态,因此,需对双侧肱骨近端髓腔内结构进行手动填充(图2)。
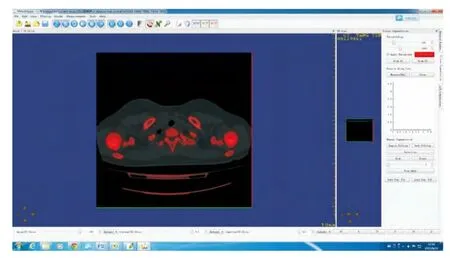
图2
第三步,对分割、填充后的双侧肱骨近端结构进行三维重建, 并选择保留我们所感兴趣的双侧肱骨近端三维重建后影像(图3)。

图3
第四步,由于我们要论证双侧结构互为镜像,因此我们还需要将左侧肱骨近端结构翻转形成镜像后,与右侧互相配准,由软件自动使双侧肱骨近端相互重叠,达到其表面各对应点位置最为接近的配准位置, 得到配准后模型(图4)。

图4
为完成上述各步处理,我们与中国科学院软件研究所合作,开发了专用于本研究的软件——VMedViewer。该软件采用Microsoft Visual C++语言编写,Microsoft Visual Studio 2012 编译运行, 图像绘制使用OSG(OpenSceneGraph)。应用该软件,引入研究对象三维CT的Dicom数据后,可完成上述的分割、填充、三维重建、翻转和配准等步骤, 最终获得两者重合度最佳的重叠模型。
我们将此重叠模型引入VRMesh v8.5 studio软件中, 首先将研究范围限定于肱骨外科颈以上的肱骨头区域(图5)。
然后采用软件中测量对应点距离的功能, 检测两重叠模型中空间位置最为接近的点对点间距离。 软件中, 可自动求得研究范围内两模型上所有对应点间距离,并得出最大距离、平均距离。 同时可在肱骨头模型上找到最大距离的点所在的位置(图6)。
我们以穿过肱骨头关节面中线的平面为切割轴,将肱骨头分为前、后两部分。将肱骨头依据其解剖特点分为肱骨头关节面部、肱骨大结节部、肱骨小结节部、结节间沟部。其中,在肱骨头关节面上和大结节的各点上, 依据其位置与关节面中线平面的相对关系分为前部关节面和后部关节面以及前部大结节和后部大结节。
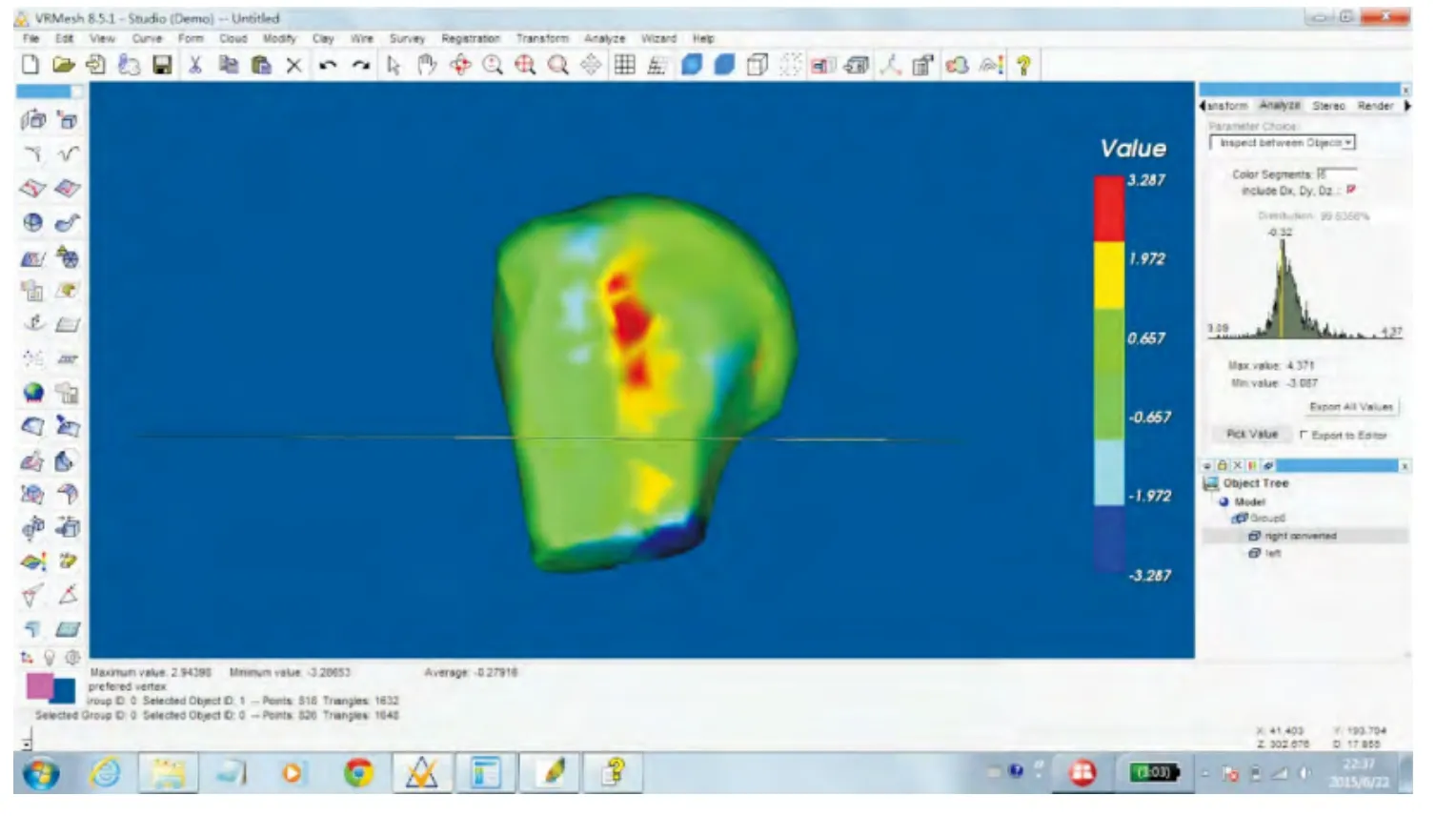
图5
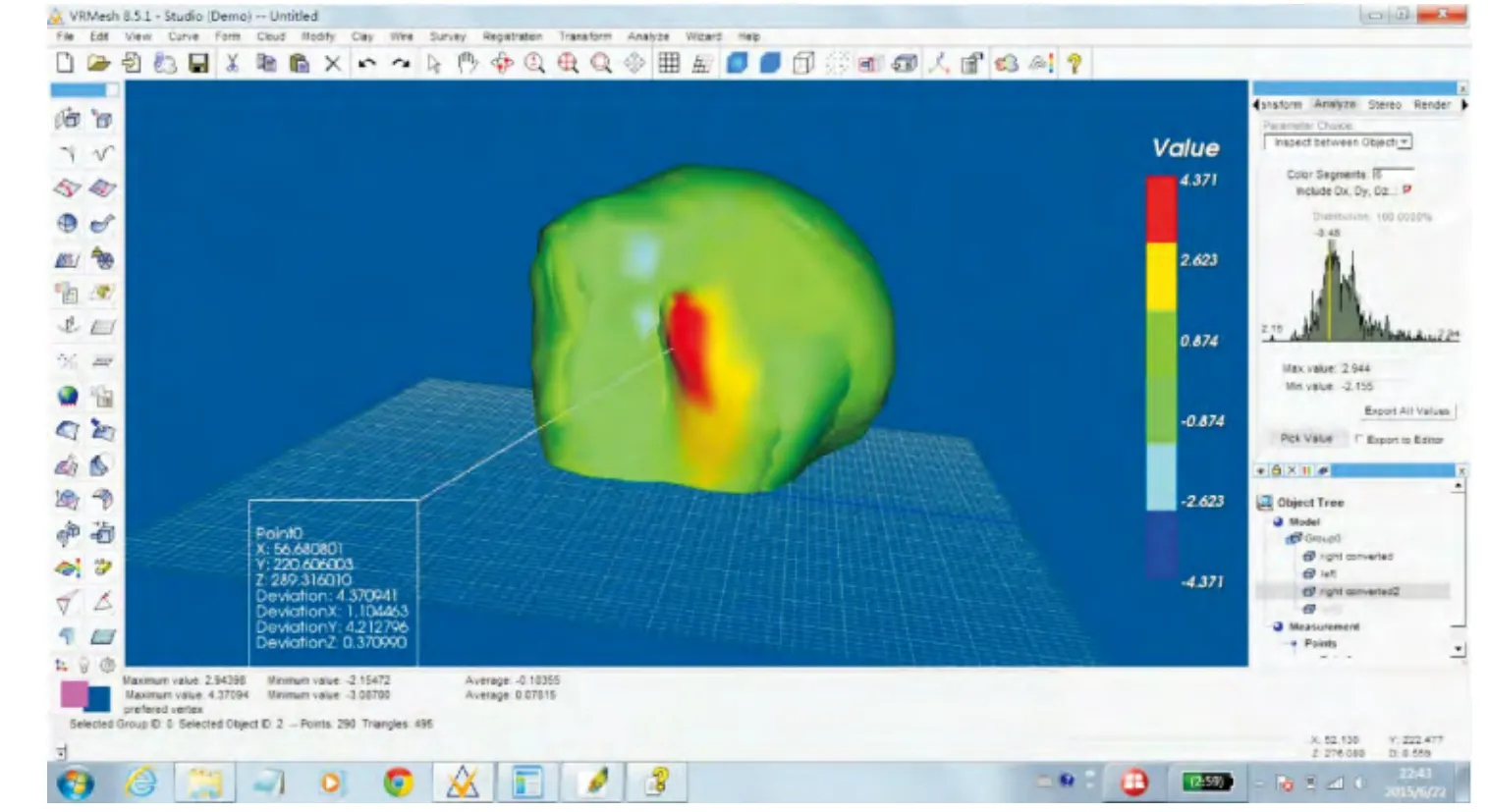
图6
2 结果
从2012年1月到2012年6月间,共收集在我院放射科行胸部CT检查的DICOM数据216套。去除存在双上肢摆放位置不合要求、 双侧肱骨头扫描不全以及合并肩关节骨性损伤等问题的CT数据,共164套DICOM数据符合要求,入选健康人双侧肩关节三维CT数据库。应用本研究方法, 获得配准后双侧肱骨头内任一对应点位置差异数据如下:
配准后双侧肱骨头内各对应点间平均距离为0.16± 0.26 mm;最大点间距离3.27 ± 0.87 mm,其中所有标本中最大点对点距离为5.90 mm; 在各个标本中,相对距离最大对应点分布于后部大结节11例 (11/164=6.70%),后部肱骨头关节面65例(65/164=39.63%),位于结节间沟40例 (40/164=24.39%), 前部大结节13例(13/164=7.93%), 前部肱骨头关节面19例 (19/164=11.59%),小结节16例(16/164=9.76%)。
3 讨论
复发性肩关节前脱位是临床上最常见的关节脱位。目前,关节镜下Bankart修复术是治疗这类损伤的最常用术式。 但是,现有研究发现,关节镜下Bankart修复术仅针对肩关节前方盂肱下韧带止点处前盂唇损伤进行修复,若患者同时存在巨大的肱骨头骨性损伤(Hill-Sachs损伤), 则会明显增加关节镜下Bankart修复术后的复发脱位率[1-4]。 因此有必要在术前对合并的Hill-Sachs损伤进行精确测量,以辅助医生决策是否需在术中对Hill-Sachs损伤进行针对性处理。
许多研究者试图通过术前影像学检查对Hill-Sachs损伤进行评估。Hall等尝试在腋位X线片上测量肱骨头骨缺损累及范围及深度[6];Saito等人试图在横断像的CT上确定肱骨头骨性损伤所处位置及其大小[7]。但由于肱骨头在未损伤时正常形态不得而知, 因而很难估计损伤区域的确切范围及深度。 Iyengar等的研究则在肱骨近端三维CT上,找到骨缺损所在部位,然后在表面覆盖虚拟的、与周边肱骨头关节面最佳匹配的球形,作为发生缺损之前原始肱骨头解剖形态[8],然后据此测量目前骨缺损体积。但是,这一方法所确定的原有肱骨头外形并无相关解剖学依据, 其测量结果是否能代表实际骨缺损体积尚存争议。 这样的问题也发生在肩盂骨缺损的测量中。 为解决肩盂骨缺损精确测量的问题,Diederichs等首先提出了以健侧骨骼形态作为模板来测量患侧骨质缺损的研究思路。在研究中,他们首先通过对健康人双侧肩盂的解剖学研究证实其外形极为近似,因而健侧可作为患侧的镜像。他们进而以病人的健侧肩盂与患侧肩盂相减, 从而得到患侧肩盂前缘骨缺损的形态[5]。 鉴于上述,我们考虑采用类似的数字减影技术,将健侧和患侧肱骨头的影像相减,从而得到肱骨头骨缺损的精确形态,并对其进行测量。如果能够实现这一想法, 则可得到新的对肱骨头骨性损伤的精确测量方法。
但是,要想通过这一方法解决临床问题,首先需要证明正常情况下双侧肱骨头外形是一致的。这方面,既往已有一些初步研究。 DeLude等在尸体标本上测量了双侧肱骨近端骨性结构的11项不同的参数, 结果发现其中10项数值双侧间差异均无显著性,因此,他们认为健侧肱骨头可作为患侧肱骨头的镜像来指导手术[9]。Von Schroeder等人也对双侧肩胛骨尸体标本进行了详细的测量, 结果发现26项解剖学参数双侧均无显著性差异[10]。 Sugaya等人的研究亦证实,健康人的双侧肩盂的形态极为相似[11]。 Diederichs等人对健康人双侧肩盂的三维CT重建后图像进行软件测量得出双侧肩盂的四项重要的解剖学数据, 结果显示双侧值之间无显著性差异[5]。由这些研究的结果,我们可以看到,双侧肩关节的骨骼大体结构是十分近似的。 另一方面,这些已有的研究往往通过测量双侧骨骼的解剖参数并互相对比来论证双侧骨骼解剖形态的一致性。 但解剖参数一致并不能说明骨骼外形完全一致, 而骨骼外形的一致性对于我们采用健侧作为模板, 求出患侧骨缺损的形态及各项体积参数十分重要。
VRmesh studio是一款3D图形处理软件。 它的一项重要功能在于可以将两个三维图形文件引入后测量模型中对应点之间的空间距离。 该项功能目前已被广泛应用于口腔及颌面外科的研究中颅骨及牙齿外形的比对方面[12-15]。
从我们的研究结果看, 研究对象中双侧肱骨近端解剖形态的一致性很高, 平均肱骨近端表面对应点间距离仅为0.16 ± 0.26 mm。 所有数据中最大点间距为5.9 mm。 若以双侧外形轮廓相减的方法求出患侧骨缺损外形参数, 可能由于正常的双侧外形不一致产生最大5.9 mm的误差。
我们的研究发现,各个解剖部位相比,双侧肱骨近端在肱骨头后部关节面及结节间沟区域的形态差异较大。39.63%的研究对象中,解剖差异最大点位于肱骨头后部关节面上; 而在24.39%的研究对象中双侧肱骨近端表面解剖差异最大点位于结节间沟。
本研究所得到的结论亦可作为以健侧肱骨近端作为模板,求出患侧肱骨近端除Hill-Sachs损伤以外的其他部位骨缺损形态及参数的研究方法的理论基础。
本研究的不足之处在于,所引入的病例数量有限,难以根据本研究结果推知人群特点, 因此需继续扩大研究对象数量。
4 总结
健康成年人双侧肱骨近端骨性结构外形近似。 表面各点间平均误差为0.16 ± 0.26 mm, 最大误差为5.9 mm。
[1] Burkhart SS, De Beer JF. Traumatic glenohumeral bone defects and their relationship to failure of arthroscopic Bankart repairs: significance of the inverted-pear glenoid and the humeral engaging Hill -Sachs lesion. Arthroscopy,2000,16(7):677-694.
[2] Cho SH, Cho NS, Rhee YG. Preoperative analysis of the Hill-Sachs lesion in anterior shoulder instability: how to predict engagement of the lesion. Am J Sports Med,2011,39(11):2389-2395.
[3] Purchase RJ, Wolf EM, Hobgood ER, et al. Hill -sachs“remplissage”: an arthroscopic solution for the engaging hillsachs lesion. Arthroscopy, 2008, 24(6):723-726.
[4] Voos JE, Livermore RW, Feeley BT, et al. Prospective evaluation of arthroscopic bankart repairs for anterior instability. Am J Sports Med, 2010, 38(2):302-307.
[5] Diederichs G, Seim H, Meyer H, et al. CT-based patientspecific modeling of glenoid rim defects: a feasibility study.AJR Am J Roentgenol, 2008,191(5):1406-1411.
[6] Hall RH, Isaac F, Booth CR. Dislocations of the shoulder with special reference to accompanying small fractures. J Bone Joint Surg Am, 1959,41-A(3):489-494.
[7] Saito H, Itoi E, Minagawa H, et al. Location of the Hill-Sachs lesion in shoulders with recurrent anterior dislocation. Arch Orthop Trauma Surg, 2009,129(10):1327-1334.
[8] Iyengar JJ, Jiang KN, Kwon D, et al. 3-D Modeling of humeral head defects in glenohumeral instability: Clinical implications of lesion morphology and the glenoid track concept. J Shoulder Elbow Surg, 23(9):e230-e231.
[9] DeLude JA, Bicknell RT, MacKenzie GA, et al. An anthropometric study of the bilateral anatomy of the humerus.J Shoulder Elbow Surg, 2007,16(4):477-483.
[10] von Schroeder HP, Kuiper SD, Botte MJ. Osseous anatomy of the scapula. Clin Orthop Relat Res, 2001,383:131-139.
[11] Sugaya H, Moriishi J, Dohi M, et al. Glenoid rim morphology in recurrent anterior glenohumeral instability. J Bone Joint Surg Am, 2003, 85-A(5):878-884.
[12] Kamburoglu K, Kursun S, Kilic C, et al. Accuracy of virtual models in the assessment of maxillary defects. Imaging Sci Dent, 2015,45(1):23-29.
[13] Almukhtar A, Ju X, Khambay B, et al. Comparison of the accuracy of voxel based registration and surface based registration for 3D assessment of surgical change following orthognathic surgery. PLoS One, 2014,9(4):e93402.
[14] Kurtulmus-Yilmaz S, Ozan O, Ozcelik TB, et al. Digital evaluation of the accuracy of impression techniques and materials in angulated implants. J Dent, 2014, 42 (12):1551-1559.
[15] Naudi KB, Benramadan R, Brocklebank L, et al. The virtual human face: superimposing the simultaneously captured 3D photorealistic skin surface of the face on the untextured skin image of the CBCT scan. Int J Oral Maxillofac Surg, 2013, 42(3):393-400.

