微创技术在脊柱真菌感染中的应用
左明相,龚 进,刘玉武 (.重庆市万州区第一人民医院骨科,重庆40400;.江山市人民医院骨科,浙江 江山3400)
伴随着广谱抗生素、糖皮质激素以及化疗药物的使用,机会性感染率逐渐增加。脊柱的真菌感染并不常见,虽然它也会感染正常人体,但是在免疫抑制的患者身上出现确实罕见。同时因为其临床表现和影像特点不典型,容易误诊和漏诊。微创脊柱外科技术的发展打破了传统治疗手段的局限,为临床治疗脊柱真菌感染提供了新的思路。我们2012 年1 月至2014 年6月对6 例椎间盘真菌感染患者采用了微创脊柱外科治疗,疗效满意。现报告如下。
1 资料与方法
1.1 临床资料
本组患者6 例,女4 例,男2 例,年龄32 ~68 岁,平均46岁。临床症状为腰痛剧烈,3 例有长期糖皮质激素使用病史,1 例有糖尿病史,其余2 例无导致免疫抑制的明显诱因。病变位于L4~L5节段4 例,L5~S1节段2 例,MR 未见明显感染表现(图1a)。入院诊断均考虑为椎间盘感染,不排除椎间盘源性腰痛可能。
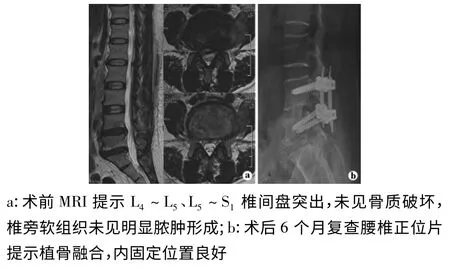
图1 手术前MRI、手术后腰椎正位情况
1.2 治疗方法
入院后行椎间孔镜下髓核摘除活检术,术中未发现明显脓液。术后组织培养结果提示白色念珠菌4 例,曲霉菌2 例,均予抗真菌治疗。由于术后腰部疼痛较前无明显缓解,考虑进一步手术治疗。遂行后路经皮椎弓根螺钉内固定和侧前路小切口下椎间盘病灶清除和取髂骨植骨融合术,术后组织培养再次证实为真菌感染,予规范抗真菌治疗12 周。术后6 个月行X光正侧位检查,观察植骨融合情况。
1.3 统计学分析
采用SPSS 13.0 软件进行分析,手术前后ODI 评分和VAS评分采用Wilcoxon 秩和检验方法。P <0.05 为差异有统计学意义。
2 结果
椎间孔镜手术时间为40 ~75 min,平均(50 ±14)min;前路椎间植骨融合术时间为125 ~170 min,平均(143 ±18)min,总出血量260 ~350 mL,平均(343 ±68)mL,术中无输血。术后平均住院时间(11.8 ±2.4)d。术后1 个月复查ESR 和CRP均降至正常。术后6 个月随访患者腰痛症状消失,复查X 线片均提示植骨融合(图1b)。VAS 评分术前(7.0 ±0.8)分,术后6个月(0.8 ±0.7)分,有显著差异(P=0.026);ODI 评分术前为(56.2 ±7.7)分,术后6 个月为(5.7 ±2.1)分,有统计学差异(P=0.027)。
3 讨论
特发性椎体真菌感染是一种少见的疾病。当患者出现亚急性或者慢性腰背部疼痛但没有发热症状,同时又有静脉置管、免疫抑制或者静脉毒品注射等真菌感染的高危因素时,我们需要高度怀疑椎体真菌感染的可能性。特发性脊柱真菌感染由于症状不典型,其诊断往往被延误,同时,当脊柱破坏在影像学上清晰表现出来的时候,则患者已经处在脊柱畸形不稳甚至脊髓压迫的危险之中了[1]。特发性脊柱的真菌感染常见的病原菌为白色念珠菌、曲霉菌,此外少见的粗球霉菌、皮炎芽生菌感染也有报道[2-3]。目前文献[4-6]报道的真菌感染相关因素包括长期使用抗生素、中心静脉置管、注射毒品、激素和其他免疫抑制剂、恶性肿瘤、糖尿病、酗酒、手术以及尿管的置入。Vinas 等[7]报道发生部位在腰段为53.7%,胸段为46.3%,颈段为2.4%。因为免疫抑制患者数量的增加,真菌感染的发生率总体呈上升趋势[8]。
脊柱真菌感染的诊断往往缺乏特异性指标,容易与其它脊柱疾病混淆,导致误诊和漏诊。Miller 等[1]回顾了59 例脊柱念珠菌感染的病例,发现有87%的患者出现血沉升高,仅18%的患者出现白细胞,同时也只有51%的患者血液培养呈阳性结果。影像学诊断方面,CT 检查没有特异性的表现,而MRI 仅有助于鉴别细菌感染还是真菌感染[9]。但是在疾病早期没有形成典型的影像学改变时,影像学诊断异常困难。患者术前MR 和CT 检查并没有特异性的表现。通常原发性脊柱真菌感染需要跟细菌、结核分枝杆菌以及恶性肿瘤等鉴别。活检和组织培养是明确诊断的金标准,只有在多次CT 引导下细针穿刺活检之后仍没有明确的病原学结果之后,才考虑行开放手术活检。
真菌性椎间盘感染往往容易和椎间盘源性腰痛混淆。我们选择了局部麻醉下椎间孔镜作为进一步明确诊断的手段。如果患者椎间盘源性腰痛,通过椎间孔镜进行椎间盘摘除术即可达到治疗的目的;如果患者是椎间盘感染,那么通过椎间孔镜可以取出椎间盘组织进行病理检查和病原学检查。椎间孔镜手术活检相比细针穿刺活检而言创伤稍大,但是有更高的安全性和直视下取材的准确性,可以提高活检的成功率;另外,相对于开放手术活检而言,手术在局部麻醉下即可完成,对患者的创伤又可以明显减小,同时还不影响活检的准确性。
目前,对于念珠菌性脊柱感染的治疗观点不统一。本例患者进行保守抗真菌治疗同时是否行椎间植骨融合术并没有指南可依据。朱俊锟等[10]报道了2 例早期特发性脊柱真菌感染,保守治疗1 个月后患者背痛和发热症状消失,随访未见背痛复发。当患者仅是轻微腰痛而没有明显的腰椎不稳或者神经受压表现时,单纯的药物治疗就足够了。另一重要原因在于腰椎真菌感染的患者常合并有复杂的内科疾病,身体状况较差,传统开放手术创伤大,患者围手术期死亡的风险大。Kakarla 等[11]回顾了27 例手术治疗的脊柱真菌感染病例,认为手术治疗的指针是耐药、脊髓和神经受压、脊柱不稳和难以控制的疼痛。同时手术治疗的目的在于神经干减压和脊柱的稳定,手术治疗可以预防灾难性的神经损伤。真菌感染患者同时合并的免疫抑制等严重合并症是造成手术效果不佳的首要原因。
本组6 例患者疼痛程度剧烈,同时还有4 例合并导致免疫力低下的内科情况,因此,更倾向于快速和微创的手术治疗。Iwata 等[12]认为在腰椎真菌感染的患者中采用微创的手术方式是最优的方案。Nagata等[13]曾报道1 例白色念珠菌导致椎间盘炎,进行2 次椎间盘镜下抽吸病灶清除术,结果失败了。但是,Iwata 等[12]通过经皮后外侧内镜病灶清除和引流手术成功治疗了4 例脊柱真菌感染。我们认为椎间孔镜技术对于病灶清除的能力较局限,病灶清除不彻底;同时单纯后路的病灶清除术容易使脊柱前柱的感染病灶向后发展,造成感染扩散,甚至脊髓受压或者窦道形成;此外,单纯的清除病灶而不进行植骨融合,容易造成局部的不稳定,不利于感染病灶的治愈且容易形成医源性脊柱不稳。对于治疗效果而言,Vinas 等[7]总结了49例脊柱曲霉菌的感染的病例,70.7%的病例则采用手术联合药物治疗的方式;腰椎感染的病例有21 例,9例保守治疗的病例中5 例出现死亡,12 例采用手术联合药物治疗,其中7 例采用了腰椎融合手术仅1 例死亡,手术的治疗效果更优。
微创手术可以使部分不能耐受开放手术的患者获得手术的机会,从而提高治疗效果。我们选择在椎体感染的治疗中采用微创手术方式:后路经皮椎弓根螺钉内固定术、前路小切口病灶清除、自体髂骨植骨术。后路经皮椎弓根螺钉置入过程较传统后路开放手术置钉方式而言显著减少了术中出血量以及对患者的创伤。同时,由于无需在前路置入内固定的操作,所需要的空间明显减少,手术切口减小至仅需暴露病灶和完成植骨融合操作即可,也降低了前路手术的创伤。此外,该手术方式实现了前后路手术的同期进行,避免了分期手术的诸多不利。
[1]Miller DJ,Mejicano GC.Vertebral Osteomyelitis due to Candida Species:Case Report and Literature Review[J].Clin Infect Dis,2001,33(4):523 -530.
[2]Guler N,Palanduz A,Ones U,et al.Progressive vertebral blastomycosis mimicking tuberculosis[J].Pediatr Infect Dis J,1995,14(9):816-818.
[3]Lagging LM,Breland CM,Kennedy DS,et al.Delayed treatment of pulmonary blastomycosis causing vertebral osteomyelitis,paraspinal abscess,and spinal cord compression[J].Scand J Infect Dis,1994,26(1):111 -115.
[4]Harvey RL,Myers JP.Nosocomial fungemia in a large community teaching hospital[J].Arch Intern Med,1987,147(12):2117 -2120.
[5]Bross J,Talbot GH,Maislin G,et al.Risk factors for nosocomial candidemia:a case-control study in adults without leukemia[J].Am J Med,1989,87(6):614 -620.
[6]LaFont A,Olive A,Gelman M,et al.Candida albicans spondylodiscitis and vertebral osteomyelitis in patients with intravenous heroin drug addiction:report of 3 new cases[J].J Rheumatol,1994,21(5):953-956.
[7]Vinas FC,King PK,Diaz FG.Spinal aspergillus osteomyelitis[J].Clin Infect Dis,1999,28(6):1223 -1229.
[8]Ferra C,Doebbeling BN,Hollis RJ,et al.Candida tropicalis vertebral osteomyelitis:a late sequela of fungemia[J].Clin Infect Dis,1994,19(4):697 -703.
[9]Williams RL,Fukui MB,Meltzer CC,et al.Fungal spinal osteomyelitis in the immunocompromised patient:MR findings in three cases[J].Am J Neuroradiol,1999,20(3):381 -385.
[10]朱俊锟,兰树华,柳育健.特发性脊柱真菌感染两例报告[J].中华骨科杂志,2010,30(9):910 -911.
[11]Kakarla UK,Kalani MY,Sharma GK,et al.Surgical management of coccidioidomycosis of the spine:clinical article[J].J Neurosurg Spine,2011,15(4):441 -446.
[12]Iwata A,Ito M,Abumi K,et al.Fungal spinal infection treated with percutaneous posterolateral endoscopic surgery[J].J Neurol Surg A Cent Eur Neurosurg,2014,75(3):170 -176.
[13]Nagata K,Ohashi T,Ariyoshi M,et al.Percutaneous suction aspiration and drainage for pyogenic spondylitis[J].Spine (Phila Pa 1976),1998,23(14):1600 -1606.

