一种新型螯合树脂固相萃取填料的制备及其吸附性能研究*
郑建华,戴建华
(1.齐齐哈尔大学 分析测试中心,黑龙江 齐齐哈尔161006;2.齐齐哈尔市疾病预防控制中心,黑龙江 齐齐哈尔161000)
近年来,国内外对螯合树脂的研究和制备以及对重金属离子的富集和回收等方面都比较关注[1,2]。螯合树脂是以交联的聚合物为载体,连接具有特殊功能基团的一类功能高分子材料,其功能基一般含有O、N、S、P 等原子,这些原子的孤电子对与金属离子结合形成配位键,从而选择性地螯合吸附金属离子,并且在一定的条件下又可以将所吸附的金属离子释放出来。因而选择性更为优异。此外,因为其骨架是高分子聚合物,不溶于水、酸、碱和有机溶剂,分离操作简便易行,所以在重金属富集、分离和回收方面有着广泛的应用[3,4]。周小华等[5]用聚苯乙烯微球作为反应原料,经硝化、还原、接枝等一系列反应,合成出带有硫脲基团的高分子材料,并且考察该材料对Pd2+的吸附性能。该实验结果表明,合成出的硫脲树脂在混合金属离子体系下,对Pd2+吸附性能良好,As5+、Cd2+、Hg2+、Pb2+分别有少量的吸附。对于水体中某些痕量级重金属离子含量的测定,由于受到基体干扰或低于仪器检测限,而难于直接进行仪器分析定量。因而,对目标物进行分离和预富集就成了样品分析的重要步骤。在已报道的分离和富集水中重金属离子的方法中[5],固相萃取技术[6]是固体吸附剂将液体样品中的目标化合物吸附,然后再用洗脱液解吸附,从而达到分离和富集目标物的目的一种新兴技术。本文以苯乙烯单体为合成聚苯乙烯,然后将聚苯乙烯氯甲基,再与硫代氨基脲反应得到聚苯乙烯硫代氨基脲螯合树脂。该材料作为固相萃取吸附剂富集Mn2+、Cd2+、Hg2+、Pb2+,取得了较为满意的效果。
1 实验部分
1.1 仪器与试剂
S-3400 扫描电子显微镜(日本HITA-CHI 公司),Spectrun one 傅里叶变换红外光谱仪(美国PE公司),X 射线光电子能谱仪(美国Thermo 公司),ICE3500 原子吸收分光光度计(美国赛默飞世尔科技公司)。
锰标液(1000×10-6),镉标液(1000×10-6),汞(二价)标液(1000×10-6),铅标液(1000×10-6),以上标液均为分析专用;无水乙醇,偶氮二异丁腈,四氯化钛,NaOH,聚乙烯吡咯烷酮,苯乙烯,甲醇,三乙醇胺,苯,硫代氨基脲,以上试剂均为分析纯。
1.2 聚苯乙烯硫代氨基脲螯合树脂的制备
向三口瓶中加入一定量的聚乙烯吡咯烷酮、一定比例的乙醇和水;将一定量AIBN 和St 单体放入烧杯中溶解后倒入三口瓶中,在70℃恒温水浴、通N2、200r·min-1机械搅拌下,反应10h 完毕,将产物用无水乙醇洗涤抽滤,于60℃真空干燥箱中干燥24h,得到聚苯乙烯微球。按文献[7]制备氯甲基化试剂和氯甲基化聚苯乙烯。
分别取2g 氯甲基化聚苯乙烯小球和30mL 无水乙醇于三口瓶中,溶胀12h;取6g 硫代氨基脲于小烧杯中,加入50mL 水,超声溶解后倒入三口瓶中,再加30mL 无水乙醇,在55℃恒温水浴、200r·min-1机械搅拌下,反应8h 完毕。用水淋洗产物至流出液呈中性,再用乙醇淋洗抽滤,于60℃真空干燥箱中干燥24h,得到聚苯乙烯硫代氨基脲螯合树脂。
1.3 固相萃取小柱的制备
用筛板将6mL 的柱管末端塞紧,填入0.0600g自制填料,顶端再用筛板将其塞紧并压实。
1.4 柱填料对重金属的吸附
1.4.1 标准曲线的绘制 分别量取锰标液0.2、0.4、0.6、0.8、1.0、1.2mL 于100mL 的容量瓶中,定容至刻度,即得浓度分别为2、4、6、8、10、12mg·L-1的Mn2+标准溶液。同理分别配置Cd2+、Hg2+、Pb2+的标准溶液,待用。采用原子吸收分光光度计测定标准液的吸光度,以浓度C 为横坐标,吸收度A 为纵坐标,绘制标准工作曲线。
1.4.2 树脂吸附性能测定 分别取一定浓度的Mn2+、Cd2+、Hg2+、Pb2+各溶液100mL,分别过固相萃取小柱,流速1.5mL·min-1,再用10mL 浓度为5mol·L-1的硝酸溶液和0.25mL 三乙醇胺的混合液洗脱4 种金属离子,用原子吸收分光光度计测定洗脱液的吸光度,并计算其浓度。
2 结果与讨论
2.1 聚合物的表征与分析
2.1.1 产物的红外光谱表征
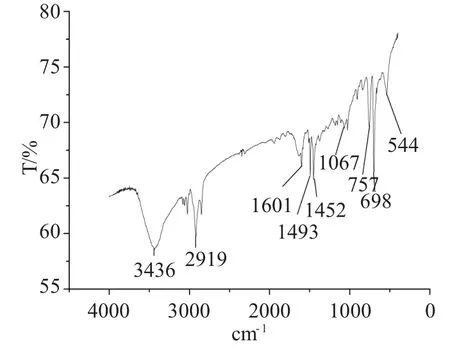
图1 聚苯乙烯硫代氨基脲螯合树脂的红外光谱图Fig.1 FTIR of polystyrene N-aminothiourea chelating resin
由 图1 可 知,2919cm-1:C-H 伸 缩 振 动;1493-1452cm-1:C-H 键弯曲震动;1067cm-1:C=S 伸缩振动;3436cm-1:N-H 伸缩振动;757cm-1:C-N 弯曲振动。
2.1.2 聚苯乙烯微球的扫描电镜分析
图2 是用扫描电子显微镜拍摄的聚苯乙烯微球图片。

图2 聚苯乙烯扫描电镜图Fig.2 SEM of polystyrene microsphere
a 中样品粒子的直径约为3.0μm;b 中样品粒子的直径约为5μm;c 中样品粒子的直径约为5.5 μm;d、中样品粒子的直径约为6μm;
聚苯乙烯微球粒径随着初始单体浓度增加而增大,随着引发剂浓度增而增大,随着稳定剂浓度增加而减小。
2.1.3 氮元素和硫元素的X 射线光电子能谱分析
采用X 射线光电子能谱分析了聚苯乙烯硫代氨基脲螯合树脂表面的化学组成或元素组成。
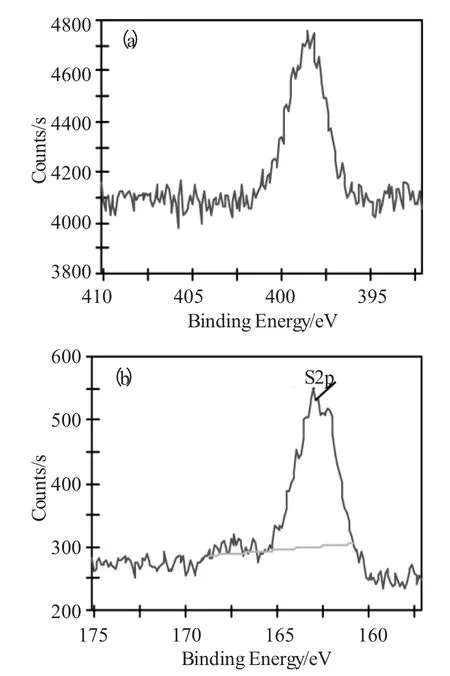
图3 聚苯乙烯硫代氨基脲螯合树脂中N 和S 元素的X 射线光电子能谱Fig.3 XPS of nitrogen and sulfur elements polystyrene of N-aminothiourea chelating resin
在图3 中,a 为氮元素分析,b 为硫元素分析,聚合物表面含有氮、硫元素。

表1 X 射线光电子能谱分析Tab.1 Analysis results of XPS
由表1 可知,碳元素、氮元素与硫元素的原子个数比接近10∶3∶1,聚苯乙烯硫代氨基脲螯合树脂结构相符。
2.2 螯合树脂对重金属吸附性能
2.2.1 吸附容量
树脂吸附容量是指树脂吸附某种离子的能力,吸附容量计算公式:
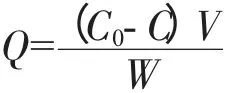
式中 C0:重金属离子的初始浓度;C:吸附后流出液中重金属离子的浓度;V:溶液的体积;W:吸附剂的质量;Q:吸附剂的吸附量。
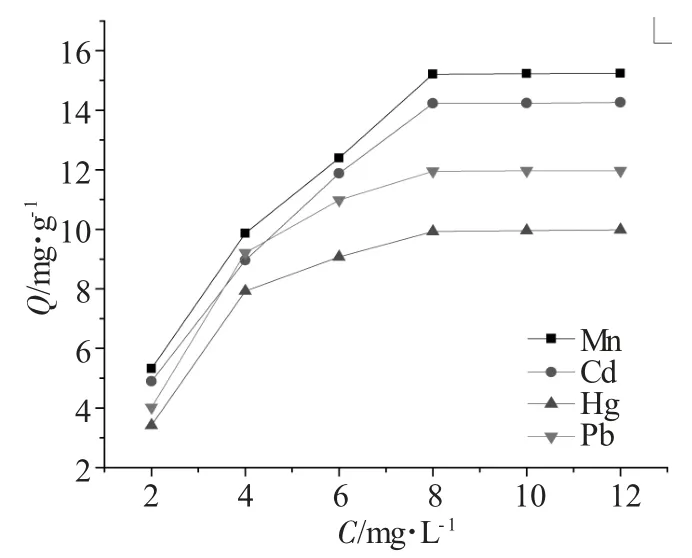
图4 浓度与吸附量的关系曲线Fig.4 Relationship between C and Q
由图4 可知,当4 种金属离子溶液的初始浓度达到8mg·L-1时,聚苯乙烯硫代氨基脲螯合树脂对Mn2+、Cd2+、Hg2+和Pb2+的吸附量达到饱和,分别为16.25、14.23、9.93 和11.95mg·g-1。开始时,吸附量随着初始浓度的增大而增大,浓度达到一定值后,由于树脂的吸附能力有限,当吸附剂的量一定时,随着浓度的继续增大,吸附量基本保持不变。
2.2.2 吸附时间对吸附容量的影响
图5 为吸附量(Q)- 时间(T)的关系曲线。
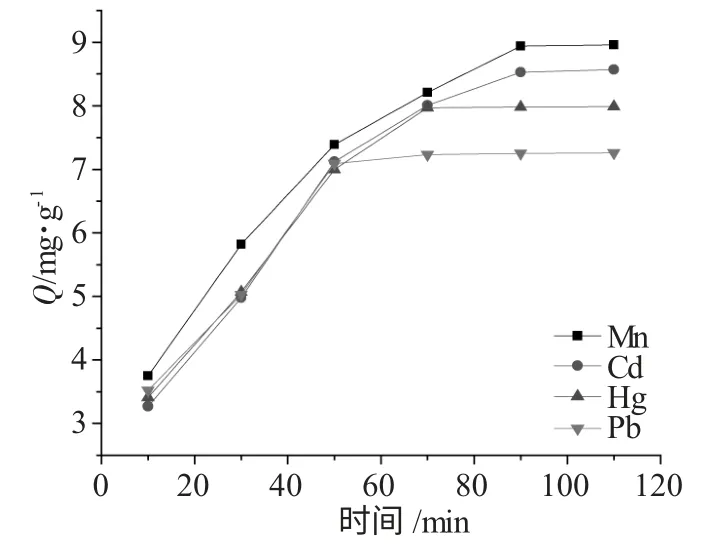
图5 吸附量与时间的关系曲线Fig.5 The relationship of T and Q
由图5 可以看出,当吸附时间达到90min 左右时,树脂对金属离子的吸附量基本不再增加,即吸附达到饱和状态,即为该树脂的吸附容量。在开始阶段,由于溶液金属离子的浓度较大,金属离子很容易被树脂吸附,因此,开始曲线斜率较大,随着时间的推移,溶液金属离子的浓度与树脂之间浓度差逐渐减小,最后达到平衡。
2.2.3 溶液流速对回收率的影响 由流速与回收率的关系图6 可知,在一定流速范围内,随着流速的增加,回收率逐渐增大,当达到某一流速时,继续增大流速,金属离子与树脂就不能被充分吸附,树脂的吸附量逐渐降低。当溶液流速为1.5mL·min-1时,4 种金属离子的回收率最大,此流速为最佳流速。此时,萃取小柱对金属离子Mn2+、Cd2+、Hg2+、Pb2+的回收率分别为93.87%、92.39%、92.42%、93.47%。
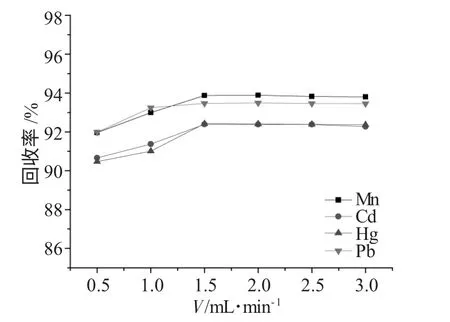
图6 流速对回收率的影响Fig.6 Influence of velocity on recovery rate
3 结论
本文合成了聚苯乙烯硫代氨基脲螯合树脂,并将其作为固相萃取小柱填料,与AAS 联用,测定了金属离子在最佳浓度为8mg·L-1,吸附时间为90min,最佳流速为1.5mL·min-1时,对Mn2+、Cd2+、Hg2+、Pb2+的吸附容量分别为16.25、14.23、9.93 和11.95mg·g-1。
[1] 安富强,代新,王晓华,等.水杨酸型螯合吸附材料对重金属离子的吸附性能[J].化学通报,2012,75(5):446-451.
[2] 王帅.聚酯基硫脲树脂的合成及其对贵金属离子的吸附分离性能[D].湖南长沙:中南大学化学化工学院化学工艺系,2008.
[3] 陈佑宁,高莉,贺茂芳,等.聚乙烯四唑型螯合树脂及其对重金属离子的吸附性能[J]. 高等学校化学学报, 2014, 35(7):1596-1602.
[4] 程永华,李青彬.Amberlite XAD-2000 树脂固相萃取富集- 火焰原子吸收法测定水中痕量铜[J].化学试剂,2010,32(8):718-720;724.
[5] 彭亚勤,钟宏,王帅,等.聚苯乙烯基硫脲螯合树脂的制备及对Au(Ⅲ)吸附性能的研究[J].贵金属,2010,31(1):25-28.
[6] 胡杰,袁新华,曹顺生.分散聚合制备聚苯乙烯微球[J].江苏大学学报,2009,30(4):370-373.
[7] 申艳玲,杨云峰,高保娇,等.制备氯甲基化聚苯乙烯交联微球的新方法[J].高等学校化学学报,2007,28(3):580-583.

