腹腔镜胃转流术治疗2型糖尿病的临床体会(附36例报告)
杨 凯,刘 昶,纪艳超,姜 龙,崔 磊
(哈尔滨医科大学附属第四医院,黑龙江 哈尔滨,150001)
目前全世界已有3 亿人受糖尿病的困扰,且其发病率仍在逐渐增加。糖尿病对患者造成的损害也在逐渐加剧,研究表明糖尿病致残、致死的患者人数正在增加[1]。作为一个系统性、慢性进行性疾病,2型糖尿病具有遗传特性,但也很大程度上受环境的影响。目前的医疗与常规干预不能逆转疾病的进展及其高发病率[2]。一直以来,人们以内科方式治疗糖尿病,近年,手术在其治疗方面取得了较好成果[3]。现将我院为36 例2 型糖尿病患者行腹腔镜胃转流术的结果报道如下。
1 资料与方法
1.1 临床资料 本组36 例患者29~65 岁,平均(35.81 ±15.32)岁;糖尿病病史3~8年,平均(4.3 ±2.3)岁。5 例病变累及眼底;3 例发展为糖尿病肾病,尿检出现蛋白尿;4 例出现皮肤破溃等严重皮肤病变。合并肥胖患者19 例,BMI平均(33.7 ±4.0)kg/m2,高血压9 例,高血脂5 例,伴胆囊炎3 例。本组患者均为原发性2 型糖尿病,且术前控制血糖方案均改为应用胰岛素。术前行C 肽释放试验,证明患者胰岛具有储备功能。出院后嘱患者长期服用铁剂、叶酸及复合维生素,以保证患者的营养摄取。
1.2 手术方法 均采用静吸复合全身麻醉。脐下做约1 cm切口,穿刺成功后,以气腹针注入二氧化碳气体,压力维持在13 mmHg。脐下切口穿刺1 cm Trocar 并置入腹腔镜。分别于右锁骨中线肋下2 cm、5 cm 及左侧腹部穿刺0. 5 cm、1.2 cm、0.5 cm Trocar,分别置入超声刀、抓钳,腹腔镜下将肝脏悬吊于腹壁(图1),充分暴露术野,腹腔探查未见明显异常。剪开肝胃韧带,经口腔置入球囊胃管于胃内,注入30 ml盐水,镜下电凝钩标记剩余容积为30 ml 的胃组织,经胃小弯侧凝切胃后组织至胃底,直线切割闭合器由胃小弯沿剩余胃组织作预切线,向胃底方向切割闭合胃组织(图2)。距十二指肠悬韧带1 m 处切割闭合小肠,远端小肠经结肠前提起,分别于小胃囊及小肠两处各做一小切口,进行保留胃、小肠的侧侧吻合(图3),并连续缝闭吻合残端。距吻合口远端1 m 处,分别于远端及近端空肠做一小切口,对近端空肠与远端空肠进行侧侧吻合(图4),并连续缝合关闭吻合残端。缝合关闭小肠系膜。胃肠吻合口处放置引流管,缝合腹壁穿刺孔,术毕。

图1 肝脏悬吊

图2 向胃底方向切割闭合胃组织

图3 胃空肠吻合
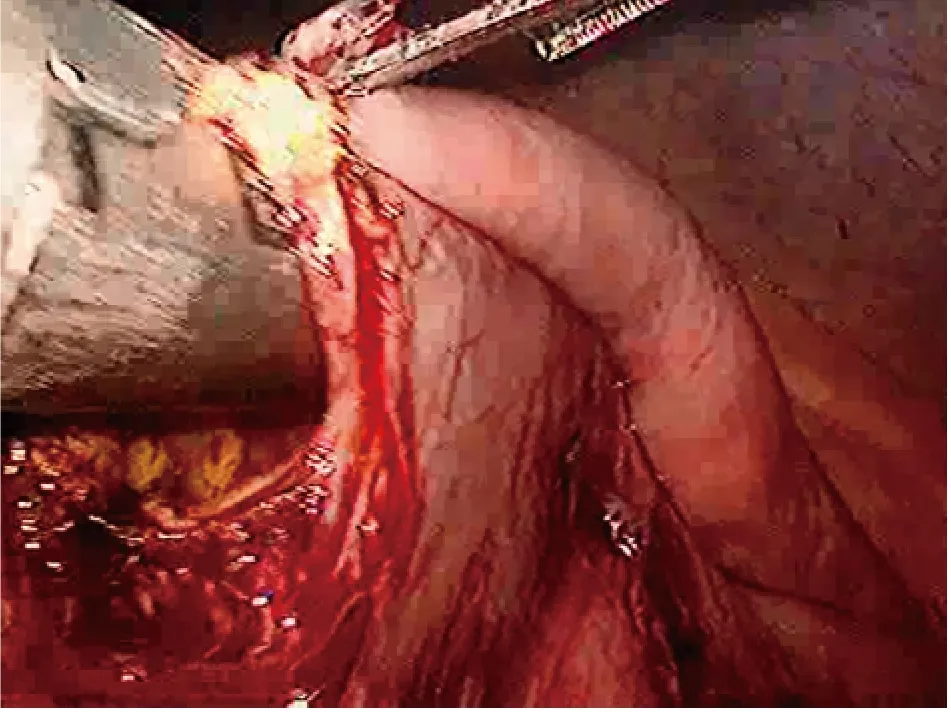
图4 近端空肠与远端空肠吻合
1.3 统计学处理 采用SPSS 19.0 统计学软件进行处理,计量资料以(±s)表示,比较采用t 检验;计数资料采用χ2检验,检验水准α=0.05。P <0.05 为差异有统计学意义。
2 结 果
2.1 一般情况 36 例均成功完成腹腔镜手术,术后无严重并发症发生。手术时间115~203 min,平均(136.4 ±21.3)min;术后可早期下地活动,术后平均住院(14.0 ±3.2)d,出院后约半个月可恢复正常工作生活,术后胃肠道功能恢复较早,患者术后3~6 d 可进流质饮食,平均(4.5 ±1.4)d,1 个月后逐渐过渡为正常饮食。
2.2 对肥胖患者影响 本组有19 例肥胖患者,术后患者各种肥胖指标均明显降低,与术前相比差异有统计学意义(P <0.05)。见表1。
2.3 术后血糖的控制情况 术后患者血糖控制较好,多数术前应用胰岛素患者,术后仅口服降糖药即可较好地控制病情。术前应用降糖药物控制血糖的患者,术后不应用药物,仅靠控制饮食加合理运动即可将血糖控制在理想范围内。术前存在糖尿病并发症的患者,5 例视物模糊患者中3 例症状消失,2 例好转;3 例伴糖尿病肾病患者,临床症状明显缓解,术后尿检蛋白尿转阴;4 例伴糖尿病皮肤溃疡患者,溃疡面均逐渐结痂至愈合。手术前后糖尿病监测指标明显改善,差异有统计学意义(P <0.05)。见表2。
表1 19 例糖尿病伴肥胖患者手术前后体重及BMI 的比较(±s)

表1 19 例糖尿病伴肥胖患者手术前后体重及BMI 的比较(±s)
* P <0.05 vs.术前
?
表2 36 例2 型糖尿病患者手术前后血糖控制情况的比较[(±s),ρ/mmol·L-1]
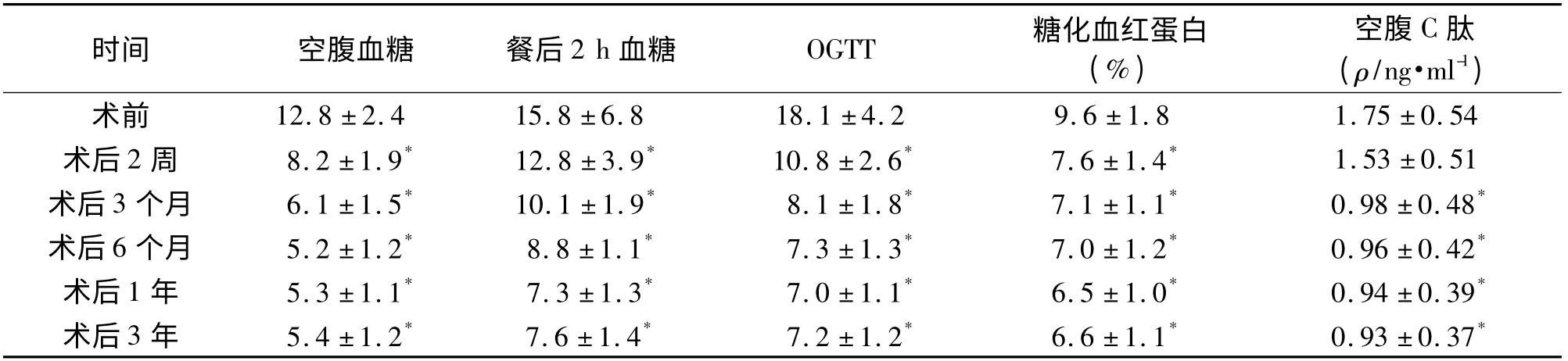
表2 36 例2 型糖尿病患者手术前后血糖控制情况的比较[(±s),ρ/mmol·L-1]
* P <0.05 vs.术前
?
2.4 术后血脂的控制情况 患者术后血脂控制情况较好,各项指标较术前明显改善,差异有统计学意义(P <0.05)。见表3。
表3 2 型糖尿病患者手术前后血脂控制情况的比较[(±s),ρ/mg·dl-1]

表3 2 型糖尿病患者手术前后血脂控制情况的比较[(±s),ρ/mg·dl-1]
* P <0.05 vs.术前
?
2.5 术后血压的控制情况 本组有9 例高血压患者,术后对其进行为期3年的随访,患者血压控制较好。9 例高血压患者中7 例已不再应用降压药物,另2 例患者降压药用量降低且血压控制较理想。见表4。
表4 2 型糖尿病患者手术前后血压控制情况的比较[(±s),p/mmHg]
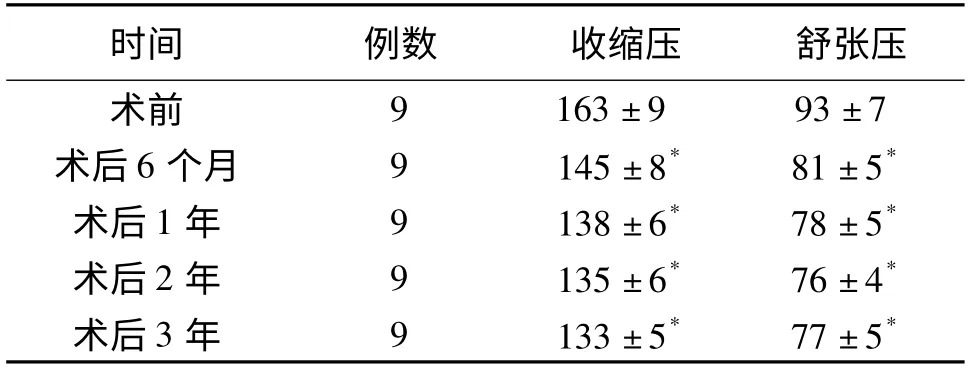
表4 2 型糖尿病患者手术前后血压控制情况的比较[(±s),p/mmHg]
* P <0.05 vs.术前
?
2.6 术后并发症 早期并发症:术后早期1 例患者出现吻合口出血,经及时止血、对症等保守治疗后痊愈;1 例患者腹部切口出现轻微脂肪液化,经短期理疗后情况好转;2 例患者术后出现较重的腹泻症状,经止泻等对症治疗于短期内治愈;1 例患者术后腹胀、排便不畅,立位腹平片提示不全肠梗阻,经禁饮食、灌肠等治疗后治愈。远期并发症:3 例患者出现乏力、面色苍白等贫血表现,经入院检查为缺铁性贫血,给予铁剂、叶酸等改善贫血,同时建议患者进食含铁丰富的食物。6 个月后进行血液复查,贫血情况基本恢复正常。术后随访,患者均未出现倾倒综合征等远期并发症。
3 讨 论
手术治疗2 型糖尿病是近年兴起的治疗方式,《新英格兰医学杂志》最新发表的文章,通过对近期临床实验研究结果进行统计分析得出结论:2 型糖尿病应用手术治疗具有更多的内科治疗无法比拟的优势[4-5],但具有较高的手术风险,因此应严格按照手术适应证的标准选择患者,评估患者病情、全身情况,以决定能否施术。我们选择手术的标准为:(1)<65 岁,2 型糖尿病诊断明确,且病史<15年。(2)术前空腹胰岛素测定值>2/3 参考值下限,空腹C肽检测结果≥1. 0 ng/ml,且糖化血红蛋白>7%。(3)患者心、肺等全身情况可耐受全麻及手术创伤,无严重合并症状及手术禁忌证。
近十年,全世界胃转流手术的数量剧增[6-7]。此手术不仅降低了(BMI)>35 kg/m2患者的死亡率,还改善了2 型糖尿病、高脂血症、高血压患者的病情[8]。关于手术治疗糖尿病的机制主要存在前肠假说与后肠假说两种较主流的观点[9]。前者认为,糖尿病患者自身体内抑胃肽(gastric inhibitory polypeptide,GIP)出现异常分泌,致使患者产生胰岛素抵抗,故血糖控制不佳。术后随着食物对空肠、十二指肠刺激的变化,减少了GIP 的分泌,从而恢复机体糖代谢能力。而后者指出,进入回肠的食物将刺激L 细胞,使肠降血糖素、抑制食欲的激素大量分泌,这些激素可增加胰岛素的分泌及其敏感性,抑制胰高血糖素,从而发挥良好的血糖控制作用,同时可延迟胃排空,这在维持术后体重降低方面也起到至关重要的作用。术后胃底Ghrelin 类生长激素(一种促进食欲的激素)显著降低,也导致热量摄入减少,这将逆转β 细胞功能衰竭、胰岛素抵抗,从而达到控制血糖的效果。此外,术后患者进食量明显减少(限制热量摄入),体重逐渐降低,使胰岛素敏感性增强,从而使患者血糖控制良好。研究表明,BMI 与糖化血红蛋白存在密切的相关性,这也是体重降低在糖尿病病情缓解方面起重要作用的重要证据[10]。这一观点也与最近Dixon 等[11]研究分析得出的结论一致,表明体重下降的程度是2 型糖尿病病情缓解的独立预测指标。本组糖尿病伴肥胖患者术后随访体重明显降低,其血糖控制情况也明显改善。
多项研究表明,对糖尿病患者影响最大、最致命的危害为心血管并发症。而高血压又是其中最常见的并发症,其造成心源性死亡的风险也较大。文献报道,每当糖化血红蛋白发生约1%的下降时,就会减小约15%的心肌梗死发生风险。胃转流术不仅控制血糖,还能改善肥胖伴糖尿病患者的左室功能,在不改变射血分数的情况下降低血脂、血压,从而起到保护心血管系统的作用。本组糖尿病并高血压患者术后血压发生大幅度降低,且差异有统计学意义。本组患者术后血脂也较术前明显改善,且长期控制效果较好,这也有效降低了心血管疾病的发生率。腹腔镜胃转流术尤其适合糖尿病伴其他合并症的患者,患者年龄越小、病程越短,术后糖化血红蛋白降低的幅度越大,相应的血压、血脂控制效果越好,故越早进行手术对患者预后越好。
本组1 例患者发生较轻微的吻合口出血,一方面可能与小血管未能彻底止血有关;另一方面,术后进食较早或食物较硬也会出现此情况。术中操作必须细致,确保止血彻底,视患者病情判断能否进食。脂肪液化的发生应与术后患者血糖控制效果欠佳、致使切口愈合延迟有关。术后严格监控血糖至关重要,但也应防止相对低血糖反应。本组1 例患者发生术后肠梗阻,与胃肠功能恢复不良有关,禁饮食、灌肠等相关治疗后病情缓解。条件允许应鼓励患者下地活动,以促进胃肠蠕动。此外,术后一定依据患者胃肠功能恢复的具体情况指导饮食,我们采取的方案为早期肠外营养,待肠道功能允许后先进无渣肠内营养粉,逐渐过渡为流食,最后恢复正常饮食。Aftab 等[12]发表文献报道,约三分之一的患者术后出现远期并发症,其中包括慢性腹痛不适、胆石症、胃空肠溃疡及贫血。本组3 例患者出现贫血,与胃大部切除后营养吸收障碍有关,经补充铁剂、叶酸等对症治疗后病情缓解。整体而言,此术式并发症较少且较轻微。
本研究证实腹腔镜胃转流术患者创伤小、康复快,整体治疗效果较好。但首例胃转流术至今时间并不足够长,有些远期并发症尚未被充分认识与研究,长期疗效尚需临床、科研不断探索研究,以得出更可靠的佐证。
[1]Yang W,Lu J,Weng J,et al.Prevalence of diabetes among men and women in China[J].N Engl J Med,2010,362(12):1090-1101.
[2]Perreault L,Pan Q,Mather KJ,et al.Effect of regression from prediabetes to normal glucose regulation on long-term reduction in diabetes risk:results from the Diabetes Prevention Program Outcomes Study[J].Lancet,2012,379(9833):2243-2251.
[3]汤礼军,陈涛,崔建峰,等.胃转流术治疗非肥胖型2 型糖尿病的近期疗效[J]. 中华消化外科杂志,2011,10(3):214-216.
[4]Schauer PR,Kashyap SR,Wolski K,et al.Bariatric surgery versus intensive medical therapy in obese patients with diabetes[J].N Engl J Med,2012,366(17):1567-1576.
[5]Mingrone G,Panunzi S,De Gaetano A,et al.Bariatric surgery versus conventional medical therapy for type 2 diabetes[J].N Engl J Med,2012,366(17):1577-1585.
[6]Buchwald H,Oien DM.Metabolic/bariatric surgery worldwide 2011[J].Obes Surg,2013,23(4):427-436.
[7]Burns EM,Naseem H,Bottle A,et al.Introduction of laparoscopic bariatric surgery in England:observational population cohort study[J].BMJ,2010,341:c4296.
[8]Buchwald H,Estok R,Fahrbach K,et al.Weight and type 2 diabetes after bariatric surgery:systematic review and meta-analysis[J].Am J Med,2009,122(3):248-256.e5.
[9]Thomas S,Schauer P.Bariatric surgery and the gut hormone response[J].Nutr Clin Pract,2010,25(2):175-182.
[10]Ngiam KY,Lee WJ,Lee YC,et al.Efficacy of metabolic surgery on Hbalc decrease in type 2 diabetes mellitus patients with BMI<35 kg/m2--a review[J].Obes Surg,2014,24(1):148-158.
[11]Dixon JB,Hur KY,Lee WJ,et al.Gastric bypass in Type 2 diabetes with BMI <30:weight and weight loss have a major influence on outcomes[J].Diabet Med,2013,30(4):e127-134.
[12]Aftab H,Risstad H,Sövik TT,et al.Five-year outcome after gastric bypass for morbid obesity in a Norwegian cohort[J].Surg Obes Relat Dis,2014,10(1):71-78.

