Fe3O4/PPy复合微球的制备及对水中结晶紫的吸附性能
乔永生,沈腊珍,郭 永,李晓琛
(山西大同大学 化学与环境工程学院,山西 大同 037009)
Fe3O4/PPy复合微球的制备及对水中结晶紫的吸附性能
乔永生,沈腊珍,郭 永,李晓琛
(山西大同大学 化学与环境工程学院,山西 大同 037009)
采用化学聚合法将聚吡咯(PPy)原位聚合在Fe3O4纳米粒子表面,制备得到了磁性Fe3O4/PPy复合微球,考察该复合微球对水中结晶紫的吸附性能。用透射电子显微镜、X-射线衍射仪、红外光谱、振动样品磁强计和紫外可见分光光度计对产品进行了表征。结果显示,多个粒径约8 nm的Fe3O4粒子包埋在聚吡咯微球内,形成直径约为130 nm的Fe3O4/PPy复合微球,其比饱和磁化强度为52.2 A·m2/kg,展现出良好的磁响应性能和迅速从液相中分离出来的能力。50 mg的Fe3O4/PPy复合微球在30 min内能够吸附水中97%的结晶紫(30 mg/L,50 mL);70 mg的Fe3O4/PPy复合微球在15 min内能吸附水中95%的结晶紫;在60 min内,50 mg和70 mg的Fe3O4/PPy复合微球均能吸附水中100%的结晶紫,表明制得的Fe3O4/PPy复合微球是一种快速有效的吸附剂,可用于吸附工业废水中的结晶紫。
Fe3O4/PPy;复合微球;结晶紫;吸附;磁性
结晶紫是一种典型的阳离子染料,广泛应用于纺织、造纸、塑料、毛发着色剂和电镀等行业[1-2],大量的结晶紫随着工业废水被排放到自然水体中,造成水环境污染。由于结晶紫带有三苯甲烷基团,很难得到降解和净化,一旦摄入或与皮肤接触,会很容易地进入细胞,对眼睛产生严重的刺激,还会刺激呼吸系统轨道,引起呕吐、腹泻、头痛,甚至癌症[3-4]。因此,含有结晶紫的废水在排放前必须得到净化。煤[5]、水凝胶[6]、绿坡缕石[7]和粘土[1]等都可以从水溶液中除去结晶紫,但这些吸附剂本身却很难从水溶液中分离出来。
磁性纳米四氧化三铁(Fe3O4)有丰富的活性位点,高磁响应灵敏度,在外加磁场的作用下,很容易将其从液相中分离出来。聚吡咯(PPy)具有丰富的-NH官能团和高表面能[8],表现出了优异的吸附性能。将Fe3O4包埋在聚吡咯中,一方面可以提高Fe3O4的分散性和化学稳定性,最主要的是将聚吡咯的-NH官能团包裹在磁性粒子外,使吸附剂具有了磁性,可有效提高分离能力。目前已有关于Fe3O4/PPy复合材料吸附废水中铬(Ⅵ)离子的研究[9,10],但对水中结晶紫的吸附尚属空白。
笔者制备了磁性Fe3O4/PPy纳米复合微球,研究了该复合微球对水中结晶紫的吸附性能。通过透射电子显微镜,X-射线衍射仪,红外光谱,振动样品磁强计和紫外可见分光光度计对所制备的Fe3O4/PPy纳米复合微球的形貌、组成、磁性和吸附特性等进行了表征,考察了吸附剂用量对去除效果的影响。
1 实验部分
1.1 Fe3O4/PPy复合微球的制备
首先,采用共沉淀法制备出Fe3O4纳米粒子,具体步骤是:将5.0 g的FeSO4·7H2O和7.0 gFe2(SO4)3溶解在100 mL蒸馏水中,5.1 g NaOH溶解在50 mL蒸馏水中,将两种溶液混合进行反应,pH值调节至11,反应液在室温下搅拌5 h,得到黑色沉淀,将此黑色沉淀用蒸馏水和乙醇反复洗涤几次,直至pH为中性,然后在20~30 ℃的空气中干燥,得到Fe3O4纳米粒子。接着,将吡咯(PPy)原位聚合在Fe3O4纳米粒子表面,形成聚吡咯包裹的磁性Fe3O4/PPy纳米复合微球。方法为:将0.1 g所制备的Fe3O4纳米粒子和0.005 g十二烷基硫酸钠(SDS)分散在50 mL蒸馏水,超声分散1 h后,将0.5 mL吡咯注入到该溶液中,超声处理30 min,冷却至10 ℃,采用1 mol/L的FeCl3·6H2O水溶液作为氧化剂,然后将10 mL氧化剂溶液逐滴加入上述溶液中进行聚合反应,同时搅拌,1 h后将产品过滤,反复用蒸馏水和乙醇清洗,在50 ℃下干燥,得到Fe3O4/PPy复合微球吸附剂。
1.2 吸附实验
用0.1 mol/L的HCl和NaOH溶液将结晶紫溶液的初始pH调节至8.0,室温下分别将10,20,30,50和70 mg的Fe3O4/PPy纳米复合微球加入到50 mL质量浓度为30 mg/L结晶紫水溶液中,测量0~120 min,在指定的时间间隔范围吸附剂吸附结晶紫的量。溶液中结晶紫的残留浓度利用紫外可见分光光度计于590 nm下进行测定。Fe3O4/PPy复合微球对水中结晶紫的去除率(R)可用下式进行计算:
(1)
式中:c0是结晶紫溶液的初始浓度,mol/L;ct是吸附一定时间t时溶液中剩余的结晶紫浓度,mol/L。
1.3 表征
样品的形貌采用JEOL100CX-Ⅱ透射电子显微镜(TEM)进行观察,加速电压为200 kV .X-射线衍射(XRD)由BDX3300型X-射线衍射仪测定,使用Cu Kα靶,λ=0.154 2 nm .红外光谱(FTIR)采用NEXUS 870傅立叶变换光谱仪进行表征。样品的磁性能测定是由美国LDJ9600-1振动样品磁强计(VSM)完成的。结晶紫的UV-Vis吸收光谱由PerkinElmer Lambda 35紫外可见分光光度计进行测定。
2 结果与讨论
2.1 TEM分析
Fe3O4纳米粒子和Fe3O4/PPy纳米复合微球的TEM图如图1所示。图1-a为Fe3O4纳米粒子的TEM图像,可以看出,Fe3O4纳米粒子的形状接近球形,粒径大小约为8 nm,形貌规整,尺寸均一。图1-b显示多个Fe3O4纳米粒子均匀分散在聚吡咯微球内,形成直径约为130 nm的Fe3O4/PPy复合微球。

a-Fe3O4纳米粒子;b-Fe3O4/PPy复合微球图1 产品的TEM图
2.2 XRD分析
图2为聚吡咯、Fe3O4纳米粒子和Fe3O4/PPy复合微球的XRD图。Fe3O4粒子和Fe3O4/PPy复合微球的衍射图中,在2θ为30.1,35.4,42.9,57.5和62.7处均具有相同的磁铁矿特征衍射峰,而且没有其它杂峰,这表明所合成的Fe3O4纳米粒子具有较高的纯度[11-13],最高衍射峰较尖锐,说明Fe3O4粒子的结晶程度较高。在纯聚吡咯和Fe3O4/PPy复合微球的XRD图中,在较低的2θ范围(15°~30°)内可以观察到一个较宽的峰,这是聚吡咯典型的无定形结构。Fe3O4/PPy复合微球同时显示了Fe3O4和聚吡咯的特征衍射峰,说明复合微球确实包含了Fe3O4和聚吡咯成分。
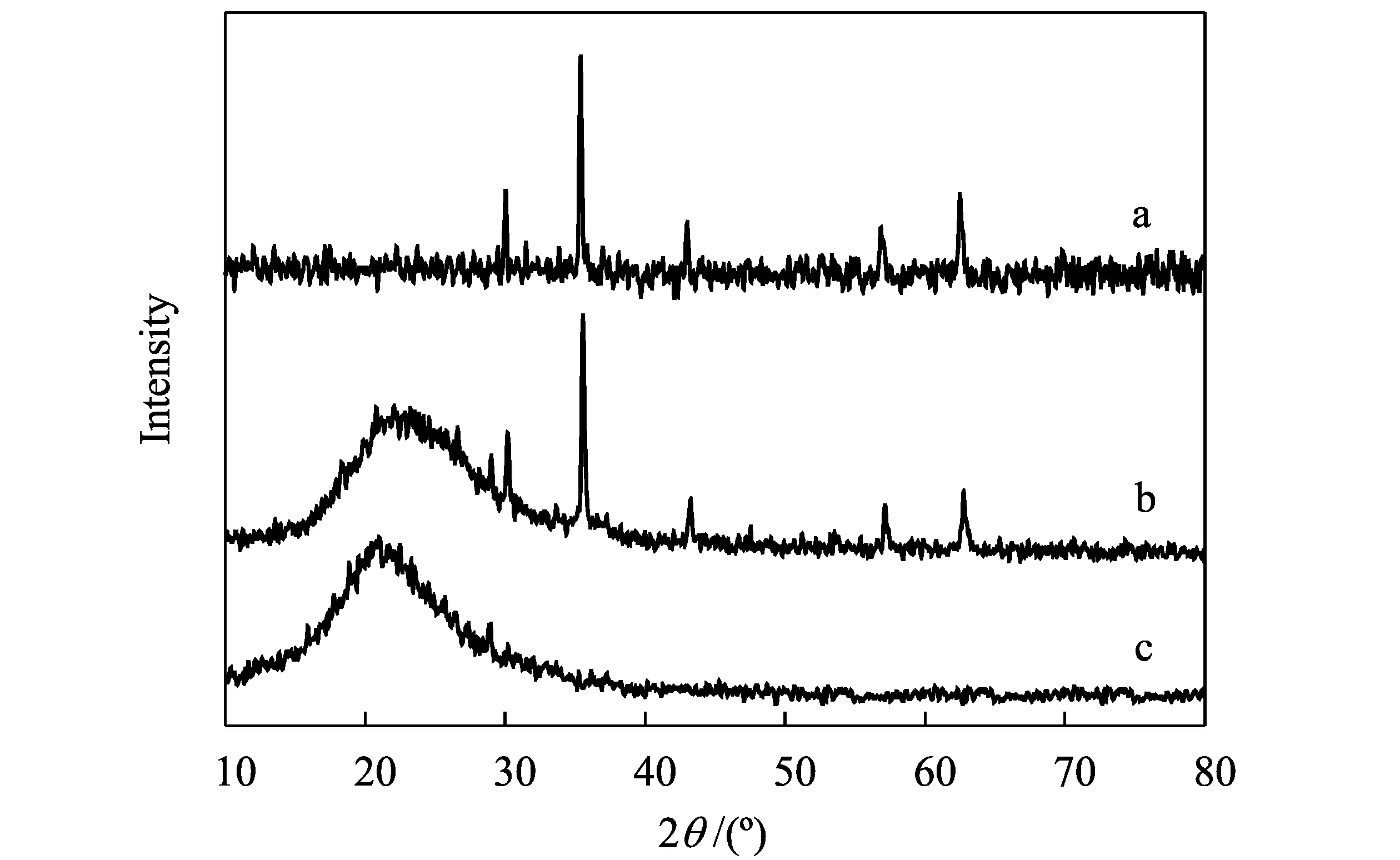
a-Fe3O4纳米粒子;b-Fe3O4/PPy复合微球;c-PPy图2 产品的XRD图谱
2.3 FTIR分析
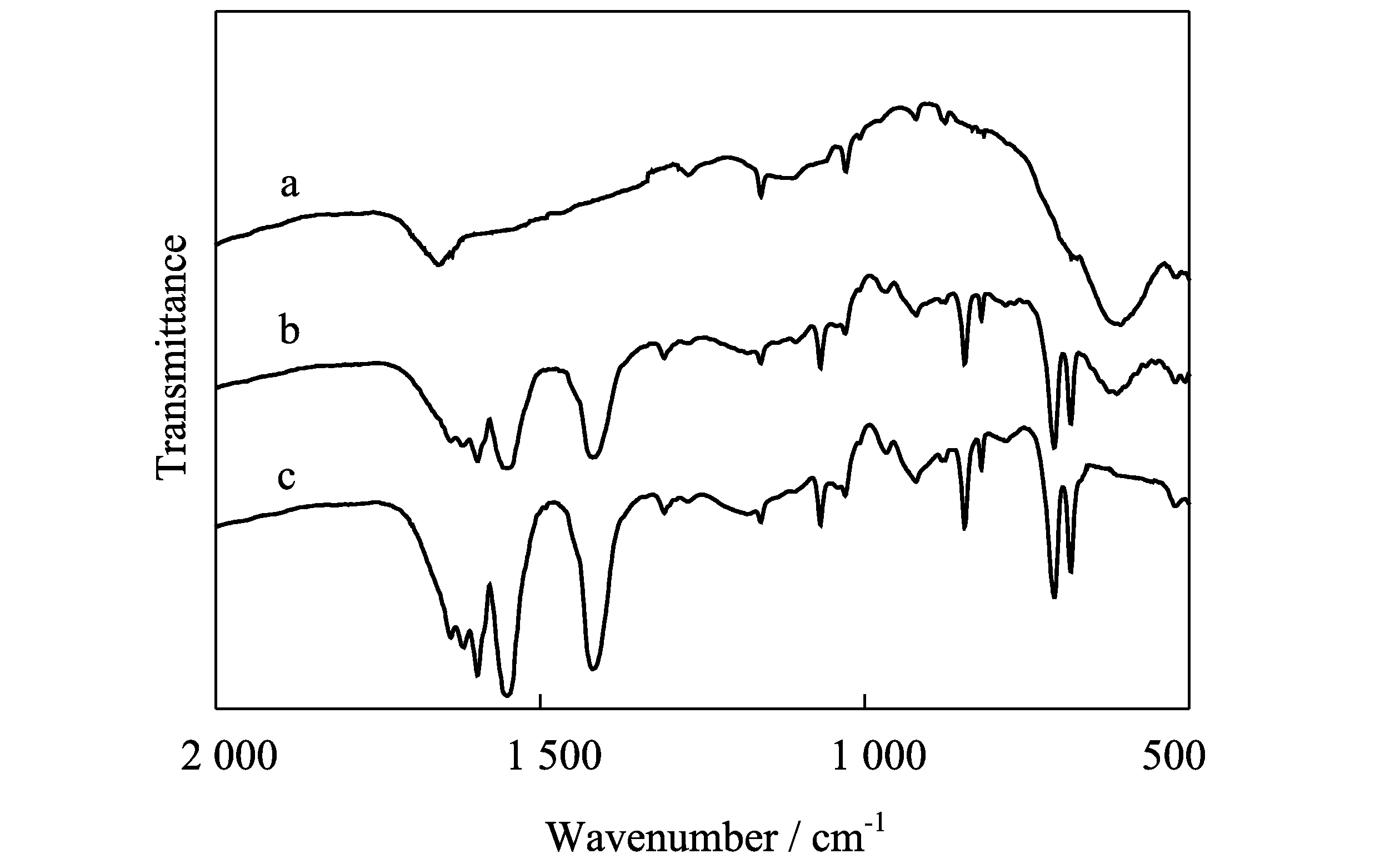
a-Fe3O4纳米粒子;b-Fe3O4/PPy复合微球;c-PPy图3 产品的FTIR谱线
Fe3O4/PPy复合微球的组成由红外吸收光谱进一步证实,FTIR如图3所示。为了便于比较,图3同时也给出了纯聚吡咯以及Fe3O4纳米粒子的FTIR图。Fe3O4的特征吸收峰出现在606 cm-1处,对应于Fe3O4的Fe-O伸缩振动[10]。Fe3O4/PPy复合微球在606 cm-1处出现了一个相对较弱的吸收峰,表明Fe3O4纳米粒子包埋在聚吡咯内。Fe3O4/PPy复合微球的FTIR光谱在1 600 cm-1,1 551 cm-1,1 419 cm-1和1 160 cm-1处出现了类似于纯聚吡咯的吸收峰,它们均为聚吡咯的特征峰[14]。在1 600 cm-1处的吸收峰对应为聚吡咯的C=C伸缩振动,1 551 cm-1和1 419 cm-1处的吸收峰分别为聚吡咯环的非对称伸缩和对称伸缩振动,这表明了聚吡咯的共轭程度[15]。出现在1 309 cm-1位置上的吸收峰为C-N伸缩振动,1 160 cm-1和1 068 cm-1处的吸收峰为=C-H面内振动,920 cm-1位置上为C-H面外弯曲振动,846 cm-1和682 cm-1之间的峰表示聚合物中存在N-H振动。因此,FTIR分析进一步证明了Fe3O4纳米粒子和聚吡咯存在于Fe3O4/PPy复合微球内。
2.4 VSM分析
Fe3O4纳米粒子和Fe3O4/PPy复合微球的室温磁滞回线如图4所示。从图中可以看到,Fe3O4纳米粒子的比饱和磁化强度是82.8 A·m2/kg,接近于块体Fe3O4的理论值(90 A·m2/kg)[16]。Fe3O4/PPy复合微球的比饱和磁化强度比Fe3O4粒子的有所下降,为52.2 A·m2/kg,这是由于Fe3O4纳米粒子包埋在聚吡咯微球内所致。尽管复合微球的磁性降低了,但从图4可以看出,在外加磁铁的作用下,磁性Fe3O4/PPy复合微球仍很容易吸附到磁铁一边,表现出较好的磁响应性能,容易从液相中分离出来,这将有利于吸附剂在废水处理中的回收利用。
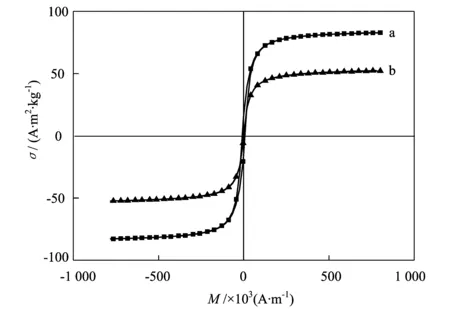
a-Fe3O4纳米粒子;b-Fe3O4/PPy复合微球图4 产品的室温磁滞回线图插图:水中Fe3O4/PPy复合微球被外加磁子吸引
2.5 吸附性能
通过选择不同吸附剂质量(10,20,30,50,70 mg)对相同浓度结晶紫(30 mg/L,50 mL)的吸附效果,考察了Fe3O4/PPy复合微球的吸附能力,图5显示了吸附剂质量对从水溶液中吸附结晶紫效果的影响。可以看出,在吸附进行60 min时,10,20,30,50和70 mg的Fe3O4/PPy复合微球对水中结晶紫的去除率分别为70.1%,81.6%,88.3%,100%,吸附量逐渐提高,且均达到了饱和吸附量。还可以观察到,随着吸附剂质量的增大,吸附速率明显加快,如在吸附进行10 min时,10,20,30,50和70 mg吸附剂可分别吸附31.4%,42.7%,55.3%,71.8%和89.2%的结晶紫。50 mg的Fe3O4/PPy复合微球在30 min内可吸附97%的结晶紫,70 mg吸附剂在15 min内可吸附约95%的结晶紫。结果表明,所制备的Fe3O4/PPy复合微球具有快速和显著吸附结晶紫的能力。
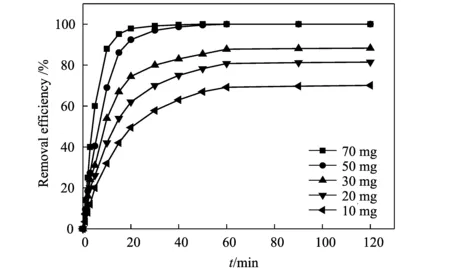
图5 不同质量Fe3O4/PPy复合微球对水中结晶紫的去除率
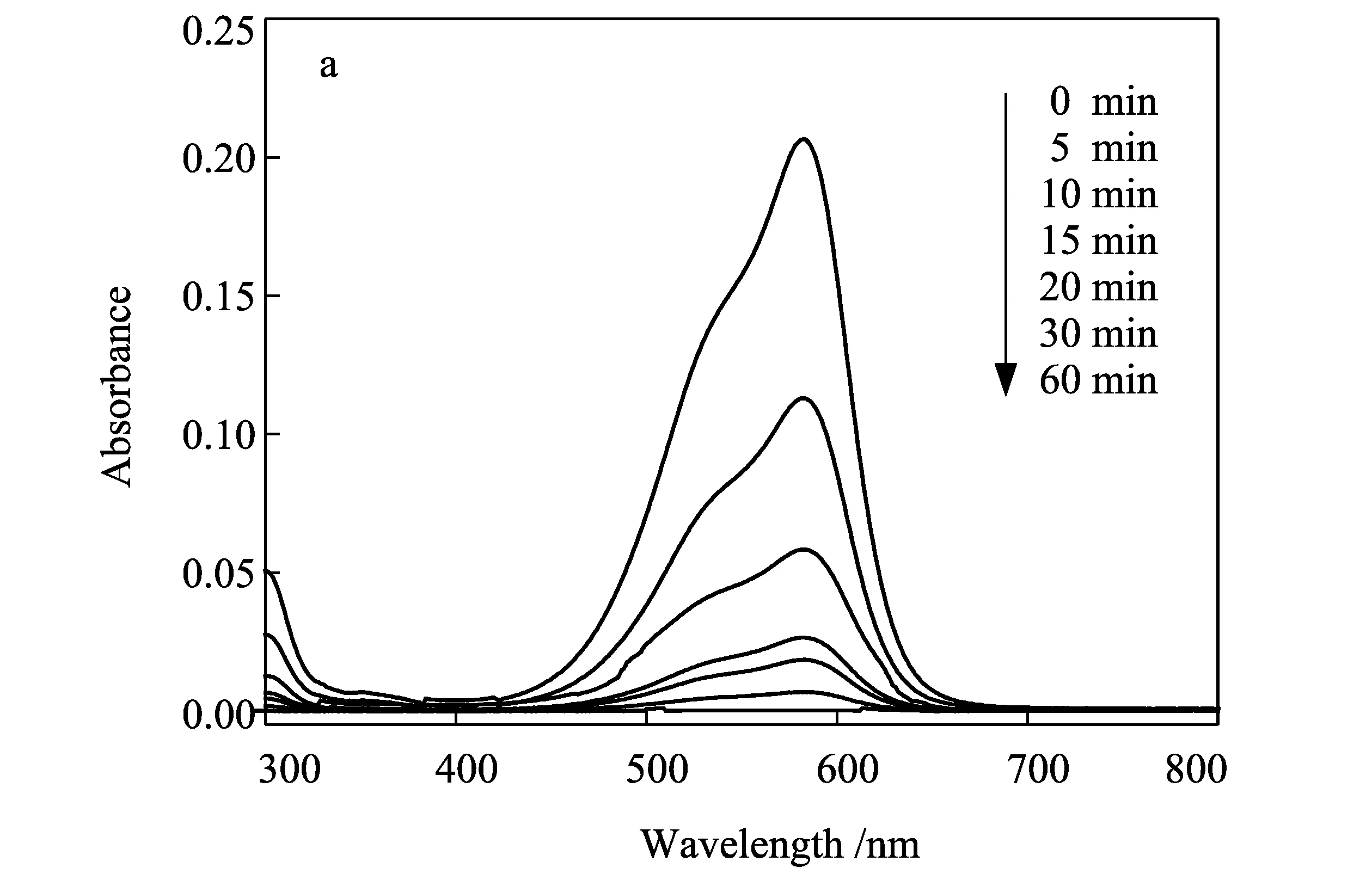

a-UV-Vis吸收光谱;b-结晶紫溶液颜色图6 50 mg Fe3O4/PPy复合微球在不同时间点对结晶紫的吸附
为了考察Fe3O4/PPy复合微球的吸附速率,研究了50 mg吸附剂吸附一定时间后水溶液中剩余的结晶紫浓度,采用紫外可见分光光度计分析不同时间间隔的UV-Vis吸收光谱,如图6-a所示。图6-b为同一时间下的结晶紫水溶液。从图6-a可以看出,结晶紫在590 nm的吸收逐渐减小,且在60 min后完全消失,结合图6-b可以看出,结晶紫溶液的颜色逐渐变浅,在15 min后几乎看不到紫色,60 min后变成无色。这表明所制备的Fe3O4/PPy复合微球对结晶紫具有较快的吸附能力。
3 结论
本文成功制备得到了磁性Fe3O4/PPy纳米复合微球,Fe3O4纳米粒子均匀分散在聚吡咯微球内。采用TEM,XRD,FTIR,VSM和UV-Vis等分析手段对产品进行了表征。结果显示,Fe3O4/PPy复合微球的比饱和磁化强度达52.2 A·m2/kg,显示出了良好的磁响应性能,具有快速从溶液中分离出来的能力。研究了Fe3O4/PPy复合微球对水溶液中结晶紫的吸附性能,包括不同吸附剂用量对吸附速率和吸附容量的影响,以及在不同时间间隔内吸附剂的吸附效率。在15 min内,95%的结晶紫可以被70 mg的Fe3O4/PPy复合微球吸附,60 min时,50 mg吸附剂即可将100%的结晶紫吸附。这表明所制备的Fe3O4/PPy复合微球可以作为一种有效的和快速的吸附剂用于从水溶液中除去结晶紫,Fe3O4/PPy复合微球对结晶紫的显著吸附能力可在印染等行业的污水处理方面做出贡献。
[1] Zhang Q,Zhang T,He T,et al.Removal of crystal violet by clay/PNIPAm nanocomposite hydrogels with various clay contents[J].Appl Clay Sci,2014,90:1-5.
[2] Zhou Y,Zhang M,Wang X,et al.Removal of crystal violet by a novel cellulose-based adsorbent:comparison with native cellulose[J]. Ind Eng Chem Res,2014,53:5498-5506.
[3] Li S.Removal of crystal violet from aqueous solution by sorption into semi-interpenetrated networks hydrogels constituted of poly (acrylic acid-acrylamide-methacrylate) and amylase[J].Bioresour Technol,2010,101:2197-2202.
[4] Singh K P,Gupta S,Singh A K,et al.Optimizing adsorption of crystal violet dye from water by magnetic nanocomposite using response surface modeling approach[J].Hazard Mater,2011,186:1462-1473.
[5] Schoonen M A,Schoonen J M T.Removal of crystal violet from aqueous solutions using coal[J].Colloid Interf Sci, 2014,422:1-8.
[6] Zhao S,Zhou F,Li L,et al.Removal of anionic dyes from aqueous solutions by adsorption of chitosan-based semi-IPN hydrogel composites[J].Compos Part B:Eng,2012,43:1570-1578.
[7] Wang A,Wang W.Nanocomposite of carboxymethyl cellulose and attapulgite as a novel pH-sensitive superabsorbent:Synthesis,characterization and properties[J].Carbohyd Polym,2010,82:83-91.
[8] Hasani T,Eisazadeh H.Removal of Cd (Ⅱ) by using polypyrrole and its nanocomposites[J].Synth Met,2013,175:15-20.
[9] Bhaumik M,Setshedi K,Maity A,et al.Onyango. Chromium(Ⅵ) removal from water using fixed bed column of polypyrrole/Fe3O4nanocomposite[J].Sep Purif Technol,2013,110:11-19.
[10] Wang Y Q,Zou B F,Gao T,et al.Synthesis of orange-like Fe3O4/PPy composite microspheres and their excellent Cr(Ⅵ) ion removal properties[J].Mater Chem,2012,22:9034-9040.
[11] Shen L Z,Qiao Y S,Guo Y,et al.Facile co-precipitation synthesis of shape-controlled magnetite nanoparticles[J].Ceram Int,2014,40:1519-1524.
[12] Jia K,Zhang J,Huang X,et al.Size dependent electromagnetic properties of Fe3O4nanospheres[J].Chem Phys Lett,2014,614:31-35.
[13] Abbas M,Takahashi M,Kim C.Facile sonochemical synthesis of high-moment magnetite (Fe3O4) nanocube[J].Nanopart Res,2013,15:1354-1365.
[14] Soares J C,Brisolari A,Rodrigues da Cruz V,et al.Amperometric urea biosensors based on the entrapment of urease in polypyrrole films[J].React Funct Polym,2012,72:148-152.
[15] Ramesan M T.Synthesis,characterization,and conductivity studies of polypyrrole/copper sulfide nanocomposites[J].Appl Polym Sci,2013,128:1540-1546.
[16] Zhang D E,Zhang X J,Ni X M,et al.Fabrication and characterization of Fe3O4octahedrons via an EDTA-assisted route[J].Cryst Growth Des,2014,7:2117-2119.
(编辑:刘笑达)
Preparation of Fe3O4/PPy Nanocomposites for Removal of Crystal Violet Dye from Aqueous Solutions
QIAO Yongsheng,SHEN Lazhen,GUO Yong,LI Xiaochen
(SchoolofChemistryandEnvironmentalEngineering,ShanxiDatongUniversity,Datong037009,China)
The magnetic Fe3O4/polypyrrole (PPy) nanocomposites were prepared via in situ chemical polymerization of pyrrole on Fe3O4nanorparticles.The adsorption performance of Fe3O4/PPy nanocomposites for crystal violet from aqueous solutions was investigated. The samples were characterized by transmission electron microscopy (TEM),X-ray powder diffraction (XRD),Fourier transform infrared spectroscopy (FTIR), vibrating sample magnetometer (VSM) and UV/Vis spectrometry.The results show that multiple Fe3O4nanoparticles 8 nm in diameter are embedded in PPy spheres to form Fe3O4/PPy nanocomposites with the size of about 130 nm. The as-prepared Fe3O4/PPy nanocomposites exhibit a specific saturation magnetization of 52.2 A·m2/kg,and possess good magnetic response performance and rapid separation capacity from the solution. The 50 mg of Fe3O4/PPy nanocomposites can remove 97% of crystal violet from solution (30 mg/L, 50 mL) at 30 min, and 70 mg of adsorbent can absorb 95% of crystal violet at 15 min, and 100% of crystal violet can be adsorbed in 60 min with the addition of both 50 and 70 mg of adsorbent.This indicates that the as-obtained Fe3O4/PPy nanocomposites can be used as an effective and quick adsorbent for environmental engineering application in removing crystal violet from wastewater.
Fe3O4/PPy; nanocomposites; crystal violet; adsorption; magnetic
1007-9432(2015)05-0532-05
2015-04-15
国家自然科学基金资助项目:Fe3O4/聚吡咯磁性微球的制备及对镉离子的吸附性能研究(21477069);Fe3O4@PPy复合微球的制备及药物控释与靶向性能研究(51303098)
乔永生(1977-),男,山西曲沃人,博士,副教授,主要从事功能纳米材料的研究,(E-mail)dtdxqys@163.com, (Tel)13934123721
沈腊珍,教授,博士,(E-mail)shenlazhen@163.com
O631.2
A
10.16355/j.cnki.issn1007-9432tyut.2015.05.010

