PPARD基因rs2016520位点多态性与那格列奈疗效的关系
宋金方,朱 君,高秋芳,赵懿清*
PPARD基因rs2016520位点多态性与那格列奈疗效的关系
宋金方a,朱 君b,高秋芳a,赵懿清a*
目的 探讨过氧化物酶体增殖物激活受体δ(PPARD)基因rs2016520位点多态性对那格列奈治疗2型糖尿病患者疗效的影响。方法 选取新诊断的2型糖尿病患者60例,接受那格列奈单药治疗8周,治疗前后检测糖脂代谢相关指标。用PCR限制性片段长度多态性(RFLP)法测定基因多态性,根据不同基因型分组比较药效。结果 60例新诊断2型糖尿病患者完成了8周随访,那格列奈治疗后,FPG、PPG、FINS、PINS、HbA1c、TC和TG均显著改善(P<0.05);TT基因型患者PPG降低值高于携带C等位基因的患者(P<0.05)。结论 那格列奈治疗2型糖尿病患者疗效显著;PPARD基因rs2016520位点多态性可影响那格列奈的疗效,那格列奈对TT基因型患者的降糖作用优于携带C等位基因的患者。
2型糖尿病;PPARD;基因多态性;那格列奈
0 引言
口服降糖药物治疗是2型糖尿病患者血糖控制的重要手段,而临床实践发现,应用相同的药物方案治疗不同患者,降糖疗效存在显著的个体差异。那格列奈(Nateglinide)是新型非磺脲类口服降血糖药,通过促进胰岛B细胞分泌胰岛素改善血糖水平,疗效也具有显著的个体差异[1-2]。另有文献报道,那格列奈也具有良好的改善胰岛素抵抗的作用[3-5]。
过氧化物酶体增殖物激活受体-δ(Peroxisome proliferator activated receptor-δ,PPAR-δ)属于过氧化物酶体增殖物激活受体家族(PPARs)成员,由PPARD基因编码,基因定位于染色体6p21.1-p21.2。PPAR-δ分布广泛,在脂代谢相关组织中表达量较高,并且在胰岛B细胞中PPAR-δ是PPARs家族中表达量最高的亚型[6-7]。有研究表明,PPAR-δ影响机体糖脂代谢,PPAR-δ激动剂具有胰岛素增敏作用,可以改善胰岛素抵抗,激活PPAR-δ,改善胰岛功能及其形态[8-9]。药物基因组学研究表明,与胰岛素分泌以及胰岛素敏感性有关基因的多态性如:KCNQ1、SLC30A8和NOS1AP基因的多态性,可能影响T2DM患者对降糖药物的反应性[10-11]。
PPARD基因的生物学功能和那格列奈的治疗作用都主要集中在对胰岛素分泌和胰岛素抵抗的调节上,但PPARD基因多态性是否影响那格列奈的疗效却未见有报道。本研究选取PPARD基因rs2016520位点为遗传标记,探讨PPARD基因多态性对那格列奈治疗T2DM患者疗效的影响。
1 对象与方法
1.1 对象 按照世界卫生组织(WHO)1999年糖尿病分型诊断标准,入选初诊T2DM患者60例,其中男39例,女21例,年龄(49.19±12.19)岁。并且符合以下入选标准:年龄25~70岁;BMI 18.5~30 kg/m2;无胰岛素促泌剂使用史或至少3个月未使用过;排除CYP2C8、CYP3A4及OATP1B1诱导剂或抑制剂使用者;无胰岛素使用史;排除其他家族病史和严重肝肾疾病者;排除不符合CYP2C9*1和SLCO1B1 521TT基因型的患者[12-15]。
1.2 主要试剂与仪器 基因组DNA提取试剂盒(上海赛百盛基因技术有限公司);引物(上海生工生物工程有限公司);dNTPs、buffer、Taq酶(北京全式金生物技术有限公司);限制性内切酶(纽英伦生物技术有限公司);DNA marker(Fermentas公司);QL-866型漩涡混合器(海门市麒麟医用仪器厂);5804R型低温高速离心机(德国Eppendorf公司);Applied Biosystems 2720型PCR仪(ABI公司);Tanon-1600R 型凝胶成像系统(上海天能科技有限公司)。
1.3 方法
1.3.1 临床治疗方案 所有受试者均口服那格列奈(商品名:唐力,北京诺华制药有限公司)120 mg/d,3次/d,餐前15 min口服,连续8周,治疗期间患者饮食、运动习惯保持不变,降压降脂药物使用者剂量维持不变,检测用药前后相关指标。
1.3.2 人体参数及临床指标 记录受试者的姓名、性别、年龄、居住地、民族。对所有受试者在治疗前及治疗8周后,分别测量基本参数,包括身高、体重、腰围、臀围及血压,计算体重指数(BMI)和腰围、臀围比值(WHR)。BMI=体重(kg)/身高(m)2;WHR=腰围/臀围。并且抽取静脉血检测糖脂代谢相关指标。糖代谢:空腹血糖(FPG)、餐后2小时血糖(2hPG)、空腹胰岛素(FINS)、餐后胰岛素(PINS)及糖化血红蛋白(HbA1c)。采用葡萄糖氧化酶法测血糖;用电化学发光法测定胰岛素;用高效液相色谱法测定HbA1c。计算稳态模型胰岛素抵抗指数(HOMA-IR)=FPG(mmol/L)×FINS(mU/L)/22.5。血脂水平:三酰甘油(TG)、总胆固醇(TC)、高密度脂蛋白胆固醇(HDL-c)和低密度脂蛋白胆固醇(LDL-c)。TC、TG、HDL-c、LDL-c用半自动生化分析仪测定。
1.3.3 PPARD基因rs2016520位点多态性检测 用基因组DNA提取试剂盒提取外周血白细胞基因组DNA。用PCR限制性片段长度多态性(RFLP)的方法检测PPARD基因rs2016520位点多态性,条件如下。用引物5′-TGGGAAGGGTGATAGGGCA-3′和5′-CTGGTGAGTGGCAGAGCAGA-3′进行PCR扩增目标片段,片段长度为602 bp。PCR扩增产物用限制性内切酶(FoKI)37 ℃水解6 h,酶切产物在2.0%琼脂糖凝胶中电泳,电压为100 V,电泳35 min,以DNA Maker为分子量标准,应用凝胶成像系统观察分析结果。TT纯合子为410 bp和123 bp两条带,CC纯合子为479 bp和123 bp两条带,TC杂合子为479 bp、410 bp和123 bp三条带。
2 结果
2.1 那格列奈治疗前后临床指标比较 60例T2DM患者那格列奈连续治疗8周后,FPG、PPG、HbA1c、TG和TC水平较治疗前下降,而FINS和PINS水平较治疗前升高,差异有统计学意义(P<0.05),而HOMA-IR、HDL-c和LDL-c用药前后差异无统计学意义(P>0.05)。见表1。
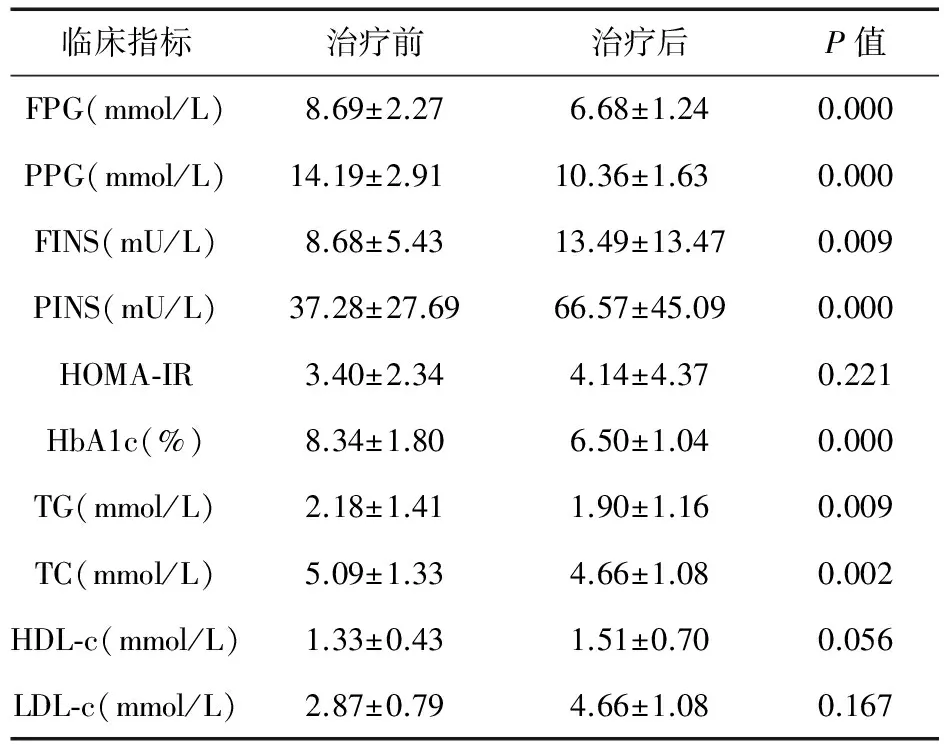
表1 T2DM患者那格列奈治疗前后临床指标
2.2 酶切产物电泳图 TT纯合子为410 bp和123 bp两条带,CC纯合子为479 bp和123 bp两条带,TC杂合子为479 bp、410 bp和123 bp三条带,检测结果见图1。

图1 PPARD rs2016520 PCR扩增产物PCR-RFLP电泳结果
2.3 PPARD基因rs2016520位点变异频率 本研究中,PPARD基因rs2016520位点TT、TC及CC的基因型频率分别为58.33%(35例)、38.33%(23例)及3.33%(2例),T、C等位基因频率分别为77.5%和22.5%;基因型和等位基因频率符合Hardy-Weinberg平衡,样本具有群体代表性,由于CC型患者仅2例,故将TC型和CC型合并为变异组,分析C等位基因携带与那格列奈治疗2型糖尿病疗效的相关性。
2.4 PPARD基因rs2016520位点多态性对那格列奈治疗T2DM患者疗效的影响 比较TT野生型患者与C等位基因携带患者那格列奈的疗效,对那格列奈治疗前后各指标差值进行比较,TT基因型患者PPG降低值高于携带C等位基因的患者(P<0.01)(表2,图2)。
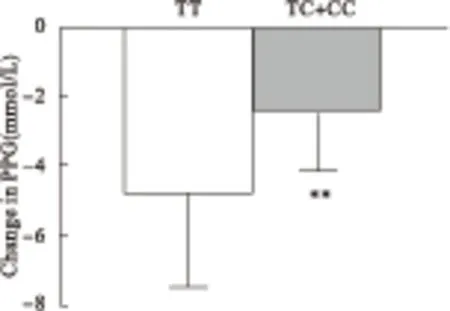
图2 PPARD rs2016520位点不同基因型T2DM患者那格列奈治疗后PPG改善情况
注:与TT型比较,**P<0.01
3 讨论
药物基因组学是近年来新兴的一门学科,可为临床个体化给药提供重要依据。目前,口服降糖药物的药物基因组学研究主要集中于研究经典的磺脲类口服降糖药物、噻唑烷二酮类胰岛素增敏剂和双胍类降糖药物,而格列奈类新型胰岛素促泌剂的药物基因组学研究报道较少,更未见有PPARD基因相关的药物基因组学信息。

表2 T2DM患者PPARD基因 rs2016520位点各基因型
那格列奈是继瑞格列奈后的第2个新型非磺脲类口服降血糖药,临床较为常用,其疗效和不良反应个体差异显著。本研究分析PPARD基因rs2016520位点多态性对那格列奈治疗新诊断2型糖尿病患者疗效的影响。有报道,CYP2C9和SLCO1B1基因多态性可以影响那格列奈的药动学过程,有可能进一步影响那格列奈治疗2型糖尿病患者的药效[12-15],因此,我们选择具有相同CYP2C9*1和SLCO1B1 521TT基因型的患者作为受试者以排除干扰。经过连续8周的那格列奈单药治疗后,患者FPG、PPG、FINS、PINS、HbA1c、TC和TG均显著改善,表明那格列奈对于2型糖尿病患者具有良好的治疗作用。文献报道那格列奈具有改善胰岛素抵抗的作用[3-4],但是本研究并未发现那格列奈治疗后HOMA-IR得到改善,可能是由于药物治疗时间较短,胰岛素增敏作用尚未体现。本研究发现,经过连续8周的那格列奈单药治疗后,TT基因型患者的PPG下降程度显著高于C等位基因携带者,那格列奈对TT基因型患者降糖作用较强(统计功效>85%)。研究结果提示,TT基因型患者对那格列奈具有更好的反应性,同时与C等位基因携带者相比,TT基因型患者发生低血糖的风险也相应增加。近年来,对于PPAR-δ生物学功能的研究取得了很大进展,已经证实了PPAR-δ参与机体糖脂代谢,与胰岛功能和胰岛素抵抗相关[6,8]。由于本研究结果未发现PPARD基因多态性对那格列奈改善胰岛素分泌的作用产生影响,因此,PPARD基因多态性对那格列奈疗效的影响可能是由PPAR-δ在胰岛素敏感性中的作用实现的。PPAR-δ的生物学作用与那格列奈的治疗作用机制具有一定程度的交叉,在一定程度上可以解释PPARD基因多态性影响那格列奈疗效的机制,但确切的分子机制尚有待进一步研究。格列奈类药物属于餐时血糖调节剂,其促胰岛素分泌的特点为快速、短效,降糖作用较弱、安全性好,因此,本研究并未对那格列奈单药治疗时的临床不良事件进行专项研究,也未收到受试者不良事件的相关报告。
综上所述,本研究结果提示,PPARD基因rs2016520位点多态性与那格列奈治疗2型糖尿病的疗效有关,对临床个体化给药具有一定的促进作用。本研究仅为格列奈类药物基因组学研究的探索性试验,还需要开展更大型、更全面的临床研究以及更深入的机制探索来证实其相关性。
[1] 蔡晓凌,罗樱樱,韩学尧,等.那格列奈在亚洲2型糖尿病患者中疗效及安全性的荟萃分析[J].中国糖尿病杂志,2012,21(10):913-917.
[2] 程勇,熊秋香,刘琴,等.那格列奈与阿卡波糖治疗2型糖尿病临床疗效比较研究[J].中国现代药物应用,2010,4:166-167.
[3] Hazama Y,Matsuhisa M,Ohtoshi K,et al.Beneficial effects of nateglinide on insulin resistance in type 2 diabetes[J].Diabetes Res Clin Pract,2006,71(3):251-255.
[4] Shiba T.Improvement of insulin resistance by a new insulin secretagogue,nateglinide-analysis based on the homeostasis model[J].Diabetes Res Clin Pract,2003,62(2):87-94.
[5] Kudo-Fujimaki K,Hirose T,Yoshihara T,et al.Efficacy and safety of nateglinide plus vildagliptin combination therapy compared with switching to vildagliptin in type 2 diabetes patients inadequately controlled with nateglinide[J].J Diabetes Investig,2014,5(4):400-409.
[6] Berger J,Moller DE.The mechanisms of action of PPARs[J].Annu Rev Med,2002,53(1):409-435.
[7] Chen L,Yang G.PPARs Integrate the Mammalian Clock and Energy Metabolism[J].PPAR Res,2014,14:653-617.
[8] Iglesias J,Barg S,Vallois D,et al.PPARβ/δ affects pancreatic β cell mass and insulin secretion in mice[J].J Clin Invest,2012,122(11):4105.
[9] 陈娜,吴英良.PPARδ的结构及其生物学功能与疾病[J].中国药理学通报,2006,22(9):1035-1038.
[10]Schroner Z,Javorsky M,Kozarova M,et al.Pharmacogenetics of oral antidiabetictreatment[J].Bratisl Lek Listy,2011,112(8):441-446.
[11]Chen M,Hu C,Jia W.Pharmacogenomics of glinides[J].Pharmacogenomics,2015,16(1):45-60.
[12]Kirchheiner J,Meineke I,Müller G,et al.Influence of CYP2C9 and CYP2D6 polymorphisms on the pharmacokinetics of nateglinide in genotyped healthy volunteers[J].Clinical Pharmacokinetics,2004,43(4):267-278.
[13]Cheng Y,Wang G,Zhang W,et al.Effect of CYP2C9 and SLCO1B1 polymorphisms on the pharmacokinetics and pharmacodynamics of nateglinide in healthy Chinese male volunteers[J].Eur J Clin Pharmacol,2013,69(3):407-413.
[14]Niemi M,Backman JT,Kajosaari LI,et al.Polymorphic organic anion transporting polypeptide 1B1 is a major determinant of repaglinide pharmacokinetics [J].Clinical Pharmacology & Therapeutics,2005,77(6):468-478.
[15]Izumi S,Nozaki Y,Maeda K,et al.Investigation of the impact of substrate selection on in vitro organic anion transporting polypeptide 1B1 inhibition profiles for the prediction of drug-drug interactions[J].Drug Metab Dispos,2015,43(2):235-247.
Relationship between the PPARD rs2016520 polymorphism and the response to nateglinide treatment
SONG Jin-fanga,ZHU Junb,GAO Qiu-fanga,ZHAO Yi-qinga*
(a.Department of Clinical Pharmacy,b.Department of Internal Medicine,Wuxi Third People′s Hospital,Wuxi 214000,China)
Objective To investigate the effect of peroxisome proliferator-activated receptor δ (PPARD) gene rs2016520 polymorphism on the response to therapy with nateglinide in type 2 diabetic patients.Methods Sixty newly diagnosed type 2 diabetic patients received nateglinide monotherapy fer 8 weeks,the glucose and lipid metabolism related indicators were detected before and after treatment.Gene polymorphism were detected by PCR-restriction fragment length polymorphism (RFLP),the efficacy of different genotypes was compared.Results All the patients with type 2 diabetes accomplished 8 weeks follow-up visits,the FPG,PPG,FINS,PINS,HbA1c,TC and TG were significantly improved (P<0.05)after nateglinide treatment;patients with TT genotype had more decrease in PPG than the patients carrying C allele (P<0.05).Conclusion Nateglinide is effective for type 2 diabetes;PPARD rs2016520 gene polymorphism can affect the efficacy of nateglinide,the patients carrying C allele have poor response to natelinide efficacy as measured by PPG levels than the patients with TT genotype.
Type 2 diabetes;PPARD;Gene polymorphism;Nateglinide
2015-04-15
无锡市第三人民医院a.临床药学科,b.内科,江苏 无锡 214000
*通信作者
10.14053/j.cnki.ppcr.201511007

