他莫昔芬序贯来曲唑与来曲唑单药治疗乳腺癌的临床对比研究
罗 娜
(中南大学湘雅医院乳腺外科,长沙 410008)
他莫昔芬序贯来曲唑与来曲唑单药治疗乳腺癌的临床对比研究
罗娜
(中南大学湘雅医院乳腺外科,长沙 410008)
摘要:目的探讨他莫昔芬序贯来曲唑与来曲唑单药治疗乳腺癌的临床效果。方法选取2008年 2月至2013年4月中南大学湘雅医院收治的90例乳腺癌受体阳性的乳腺癌患者为研究对象,根据随机数字表法分成两组:对照组45例,给予来曲唑2.5 mg治疗,每日1次,连续服用5年;观察组45例,给予他莫昔芬10 mg治疗,每日2次,连续服用2~3年后停用,改来曲唑口服2~3年。观察两组患者治疗后的临床效果。结果观察组患者1~3年复发率明显低于对照组,差异有统计学意义(P<0.05);观察组治疗后潮热、恶心呕吐、阴道出血、高脂血症、血栓栓塞、肌肉关节疼痛、其他的发生率均低于对照组,差异有统计学意义(P<0.05)。结论他莫昔芬序贯来曲唑治疗乳腺癌临床效果显著,安全性高。
关键词:乳腺癌;他莫昔芬;来曲唑;临床效果
乳腺癌是女性常见的恶性肿瘤之一,严重影响广大女性的身心健康。研究表明,所有乳腺癌中有2/3以上属于雌激素依赖性癌组织(约有70%乳腺癌患者为雌激素依赖型)[1]。故在治疗上减少雌激素对肿瘤细胞的刺激是治疗的关键所在。而随着药物制剂学的发展,雌激素受体拮抗剂类药物他莫西芬、芳香化酶抑制剂来曲唑等在降低乳腺癌病死率、复发率和提高生存率上有很好的效果,但在如何运用上存在分歧。本研究对比分析他莫昔芬序贯来曲唑与来曲唑单药治疗乳腺癌的临床疗效,以期寻找最佳的治疗方法,现报道如下。
1资料与方法
1.1临床资料选取2008年2月至2013年4月中南大学湘雅医院收治的90例乳腺癌患者为研究对象。所有患者均经病理证实为非特殊类型浸润性癌患者,免疫组织化学证实为Lumina A型患者,停经时间均超过1年以上。均排除原位癌,未中断标准的化疗、放疗和内分泌治疗患者。采用随机数字表法分为两组:对照组45例,年龄50~69岁,平均(54±4)岁;肿瘤分期:Ⅱ期31例,Ⅲ期14例;手术方式:保乳根治术29例,非保乳根治术16例;病程最短4~26周,平均(10±4)周。观察组45例,年龄52~71岁,平均(54±3)岁;肿瘤分期:Ⅱ期 30例,Ⅲ期15例;手术方式:保乳根治术31例,非保乳根治术14例;病程最短5~28周,平均(10±4)周。两组患者在年龄、手术方式等方面比较差异无统计学意义(P>0.05),具有可比性。
1.2治疗方法两组患者均予手术治疗,术后均予标准的紫杉类+蒽环类联合化疗方案,对照组予以口服来曲唑(江苏恒瑞医药股份有限公司生产,批号:20071204、20120107)2.5 mg,每日1次,连续服用5年。观察组则先口服他莫昔芬(宁波市天衡制药有限公司生产,批号:20080103、20120403)10 mg,每日2次,连续服用2~3年后停用,改来曲唑口服2~3年,口服方法同对照组。
1.3疗效评定标准参考《乳腺癌的临床诊治指导原则》[2]进行临床效果评定,观察两组治疗后在1、3、5年生存率,存活率计算方法为0~1年、>1~3年、>3~5年所存活的患者/随访的总例数的百分比,复发包括局部复发及远处转移复发,对合并有局部和远处转移双重复发的仍计为1种复发,比较两组在0~1年、>1~3年、>3~5年的复发率。计算方法为复发例数/随访的总例数的百分比,比较两组治疗后不良反应情况。
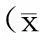
2结果
2.1两组治疗后生存率和复发率比较两组0~1年、>1~3年、>3~5年生存率比较差异无统计学意义(P>0.05),见表1;两组0~1年、>3~5年复发率比较差异无统计学意义(P>0.05),观察组患者>1~3年复发率明显低于对照组,差异有统计学意义(P<0.05),见表2。
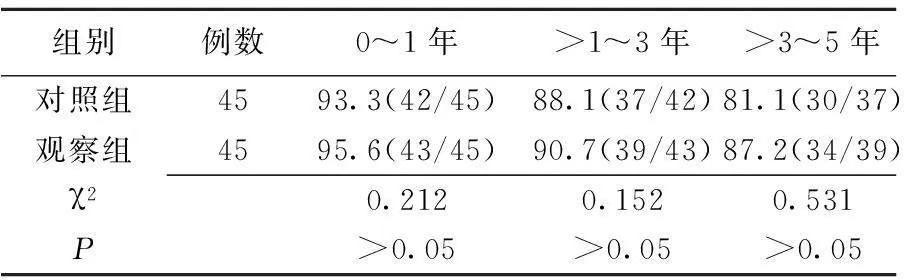
表1 两组乳腺癌患者治疗后生存率比较 (%)
对照组:来曲唑连续服用5年;观察组:他莫昔芬连续服用2~3年后,改来曲唑口服2~3年

表2 两组乳腺癌患者治疗后复发率比较 例(%)
对照组:来曲唑连续服用5年;观察组:他莫昔芬连续服用2~3年后,改来曲唑口服2~3年
2.2两组治疗后不良反应比较观察组治疗后潮热、恶心呕吐、阴道出血、高脂血症、血栓栓塞、肌肉关节疼痛、其他不良反应发生率均低于对照组,差异有统计学意义(P<0.05),见表3。

表3 两组乳腺癌患者治疗后不良反应比较 [例(%)]
对照组:来曲唑连续服用5年;观察组:他莫昔芬连续服用2~3年后,改来曲唑口服2~3年
3讨论
乳腺癌是一种受雌激素和增殖性因素影响的疾病,而雌激素的功能受雌激素α受体传递。总之,细胞生长失调、凋亡缺失是形成乳腺癌发生的必需条件。考虑到乳腺癌是一种全身性疾病,内分泌治疗在治疗乳腺癌中占重要地位,且内分泌治疗不良反应小,不影响患者生活质量,且患者耐受性好[3-4]。
来曲唑是一种传统的芳香化酶抑制剂,其作用机制是通过对芳香化酶的抑制作用,降低绝经后女性体内雌激素水平,以达到抑制雌激素受体阳性乳腺癌细胞的增殖目的。研究表明,来曲唑可通过抑制雄激素向雌激素的转化从而降低雌激素水平,且该药物选择性高,不影响糖皮质激素等功能,具有很好的临床效果[5-6]。但长期应用该药物可能出现多种雌激素相关性不良反应,主要表现为潮热、骨质疏松、肌肉关节疼痛明显等,这在本研究结果中已明确观察到。
他莫昔芬属于新型的抗乳腺癌药物,4-羟基他莫昔芬和乳腺肿瘤细胞内的雌激素受体有很高的亲和力,和天然的雌激素竞争性结合雌激素受体,干扰了雌激素的诱导信号,从而达到抑制细胞增殖和肿瘤细胞增长,诱导细胞凋亡的作用[7]。所以其主要应用在绝经前(他莫昔芬很少用于绝经后患者)的激素受体阳性患者中,加上来曲唑的作用,故在本研究中有很好的效果。但研究表明[8],他莫昔芬序贯来曲唑和来曲唑单药治疗乳腺癌在临床效果上是类似的,虽然两者作用机制不同,来曲唑是芳香化酶抑制剂,他莫昔芬属于雌激素受体拮抗剂,前者能抑制肿瘤细胞增殖,后者可抑制雌激素的水平,但对乳腺癌均有效。而在本研究中是两者联合后的效果显著,这可能与本研究病例较少有关,这点也值得在临床中继续探讨[9]。
本研究结果显示,他莫昔芬联合来曲唑治疗后,相比于单纯运用来曲唑,其不良反应发生率明显下降,说明他莫昔芬联合来曲唑的安全性更高。但即使如此,不良反应的发生率仍较高,分析原因是两种药物均能对循环系统等全身各个系统造成不良反应,其中,他莫昔芬就能通过舒张血管而形成面色潮红、脉搏增快等症状。研究表明,他莫昔芬应用后,患者血栓形成的发生率会增加4%左右,这可能与其会引起血管收缩等有关[10]。而对于内分泌的影响,该药物能引起雌酮、雌二醇、孕酮水平增加。研究指出,来曲唑能抑制小鼠中肝脏三酰甘油和总胆固醇的升高,所以口服来曲唑后患者肝脏分泌功能明显升高,参与了体内蛋白脂肪酶和肝脏三酰甘油脂肪酶的活性,参与了以上成分水解为脂肪酸的过程。文献报道[11],他莫昔芬联合应用来曲唑后,前者可对后者产生抑制,从而降低乳腺癌治疗后的不良反应发生率,而在结果中虽然结论一致,但由于本研究例数较少,故难以评判,有待临床上进一步观察探讨。
综上所述,他莫昔芬和来曲唑对乳腺癌的作用可能是通过肿瘤细胞的分化特性后,在正常乳腺上皮细胞和恶性细胞中有关生长调控的其他信息被肿瘤所干扰的结果。首先要肯定两种药物在治疗乳腺癌上的优势,但也不能忽视其在运用过程中骨质疏松、冠心病、高脂血症等不良反应的情况。
参考文献
[1]何剑芬,陈卓荣,胡红波,等.他莫昔芬和来曲唑对乳腺癌患者子宫内膜影响的对比研究[J].国际医药卫生导报,2012,18(24):3544-3546.
[2]芦珊,周玮.来曲唑在老年乳腺癌新辅助内分泌治疗中的疗效观察[J].实用癌症杂志,2012,27(6):632-634,637.
[3]姚慧韬,吴康康.来曲唑用于绝经后乳腺癌手术前治疗的临床研究[J].中国基层医药,2012,19(3):395-396.
[4]Gjerde J,Geisler J,Lundgren S.Associations between tamoxifen,estrogens,and FSH serum levels during steady state tamoxifen treatment of postmenopausal women with breast cancer[J].BMC Cancer,2010,10(1):774-776.
[5]陈凤舞,金钟奎,陈金平,等.围绝经期乳腺癌患者过渡到绝经期的内分泌治疗策略[J].内蒙古中医药,2011,30(12):29-30.
[6]周文斌, 刘萍.来曲唑和他莫昔芬治疗绝经后妇女早期乳腺癌的疗效比较[J].国外医学:药学分册,2010,33(3):183-185.
[7]张海燕,王建平.第3代芳香化酶抑制药治疗乳腺癌的研究进展[J].医药导报,2010,24(8):705-707.
[8]安富荣,程华丰,张楠森,等.芳香酶抑制剂治疗乳腺癌的研究进展[J].药学服务与研究,2011,1(1):52-56.
[9]Pravin P,Sachin C.Establishment and molecular characterization of breast cancer mesenchymal stem cell line derived from human non-metastasis breast cancer tumor[J].Stem Cell Discovery,2012,1(2):47-49.
[10]徐兵河,孙燕,宋恕平,等.来曲唑治疗绝经后妇女晚期乳腺癌临床研究[J].中国新药杂志,2011,10(10):763-766.
[11]王永霞,张爱玲,张蓉,等.来曲唑与他莫西芬在绝经后乳腺癌新辅助内分泌治疗中的应用[J].南方医科大学学报,2011,28(4):667-668.
Clinical Comparative Study between Sequential Therapy of Tamoxifen and Letrozole with Letrozole Monotherapy for Breast CancerLUONa.(DepartmentofBreastSurgery,XiangyaHospitalofCentralSouthUniversity,Changsha410008,China)
Abstravt:ObjectiveTo investigate the clinical effect of sequential therapy of tamoxifen and letrozole,and letrozole monotherapy for breast cancer.MethodsA total of 90 cases of receptor-positive breast cancer admitted to the Xiangya Hospital of Central South University from Feb. 2008 to Apr. 2013 were randomly divided into control group(45 cases) and observation group(45 cases).Patients in the control group were given letrozole 2.5 mg,one time a day,continuously for five years;patients in the observation group were given tamoxifen for 10 mg,two times a day,continuously for 2-3 years,then switched to oral letrozole for 2-3 years.The clinical effects of the two groups were compared.Results1-3 years recurrence rates of the observation group were lower than the control group,the difference was statistically significant(P<0.05).After treatment,hot flashes,nausea and vomiting,vaginal bleeding,hyperlipemia,thrombosis,muscle and joint pain,and other adverse reaction rates of the observation group were lower than the control group,the differences were statistically significant(P<0.05).ConclusionSequential therapy of tamoxifen and letrozole remarkable clinical effect and high safety for breast cancer.
Key words:Breast cancer; Tamoxifen; Letrozole; Clinical effect
收稿日期:2014-05-19修回日期:2015-01-17编辑:伊姗
doi:10.3969/j.issn.1006-2084.2015.18.055
中图分类号:R453
文献标识码:A
文章编号:1006-2084(2015)18-3410-03

