替吉奥联合奈达铂二线或多线治疗晚期非小细胞肺癌的临床效果研究
马迪,郝学志,邢镨元,李峻岭
替吉奥联合奈达铂二线或多线治疗晚期非小细胞肺癌的临床效果研究
马迪,郝学志,邢镨元,李峻岭
【摘要】目的探讨替吉奥联合奈达铂二线或多线治疗晚期非小细胞肺癌(NSCLC)的临床效果。方法以2013年9月—2014年11月在北京协和医学院中国医学科学院肿瘤医院进行一线化疗失败的17例晚期NSCLC患者为研究对象。所有患者采用替吉奥联合奈达铂进行二线或多线治疗,21 d为1个周期。随访至2015-01-31,观察并记录患者的治疗效果、后续治疗、生存状况及毒副作用情况。结果17例患者中,二线化疗6例(占35.3%),三线及以上化疗11例(占64.7%)。共完成57个化疗周期,疗效评价中获得完全缓解、部分缓解、病情稳定及病情进展的患者数分别为0例、2例(占11.8%)、9例(占52.9%)、6例(35.3%),客观有效率为11.8%(2/17),疾病控制率为64.7%(11/17),中位无进展生存期为3.0个月〔95%CI(0.4,6.1)〕。截至2015-01-31,有3例患者死亡,14例患者生存,中位总生存期为14.0个月〔95% CI(5.1,31.4)〕。出现恶心呕吐、白细胞减少、粒细胞减少、贫血、疲乏的患者数分别为13例(76.5%)、12例(70.6%)、12例(70.6%)、9例(52.9%)、9例(52.9%),且69.2%及以上为Ⅰ~Ⅱ度。除1例患者出现Ⅳ度骨髓抑制外,其他患者的毒副作用均在可耐受范围内,无化疗相关致死事件发生。结论替吉奥联合奈达铂二线或多线治疗晚期NSCLC的疗效较好,生存期较长,且毒副作用较低,应在临床上得到进一步推广和应用。
【关键词】癌,非小细胞肺;替吉奥;奈达铂;放化疗,辅助;治疗结果
马迪,郝学志,邢镨元,等.替吉奥联合奈达铂二线或多线治疗晚期非小细胞肺癌的临床效果研究[J].中国全科医学,2015,18(31):3833-3836,3841.[www.chinagp.net]
Ma D,Hao XZ,Xing PY,et al.Clinical effect of S-1 combined with nedaplatin as second-line or further-line chemotherapy in the treatment of advanced non-small-cell lung cancer[J].Chinese General Practice,2015,18(31):3833-3836,3841.
肺癌是较为常见的恶性肿瘤之一,其中非小细胞肺癌(non-small cell lung cancer,NSCLC)约占所有肺癌的85.0%。近一半的NSCLC患者在确诊时已经处于癌症晚期,而一线含铂化疗方案是目前晚期NSCLC患者的主要治疗策略。对于表皮生长因子受体(EGFR)敏感突变的患者,推荐使用一线酪氨酸激酶抑制剂小分子物质(TKIs)进行化疗,但大多数患者一线化疗后仍会出现病情进展或复发,需要进一步的解救治疗。美国国家综合癌症网络(NCCN)成人癌痛临床实践指南推荐的二线治疗药物包括多西他赛、培美曲塞及厄洛替尼等,但有研究显示,其治疗效果尚不完全如意,客观缓解率(objective response rate,ORR)为10%、中位无进展生存期(median progression free survival,PFS)小于3个月,而毒副作用却有所增加[1-3]。同时,一线化疗失败后的患者机体耐药性升高、体力下降、免疫力低下,导致后续治疗可选择的药物较少。因此,如何选择有效且安全的治疗方案成为NSCLC患者二线和多线化疗中面临的难题。替吉奥是一种5-氟尿嘧啶(5-FU)前体口服药物,已经被广泛应用于多种实体瘤的治疗,2004年日本将其批准为NSCLC化疗用药,而我国对其的报道却较少。本研究回顾性分析了替吉奥联合奈达铂二线或多线化疗晚期NSCLC患者的临床资料,以了解该化疗方案的疗效和安全性,从而为NSCLC的临床治疗提供新的思路和方法。
1 对象与方法
1.1研究对象以2013年9月—2014年11月在北京协和医学院中国医学科学院肿瘤医院进行一线化疗失败的17例晚期NSCLC患者为研究对象。晚期NSCLC诊断标准:经病理学或细胞学检查确诊为NSCLC,根据TNM分期,不管任何大小的肿瘤,存在远处转移的IV期肺癌为晚期[4]。一线治疗失败判断标准:根据实体瘤疗效评价标准(RECIST)[5],疗效评估达到病情进展(PD),表示治疗失败。纳入标准:(1)体力状况(ECOG)评分为0~1分;(2)无严重脏器功能损害,预计生存期>3个月;(3)有可测量的临床、CT片等观察指标;(4)接受过1个及以上方案的治疗,包括化疗和靶向治疗;(5)化疗前各项实验室检查示无化疗禁忌。排除临床资料缺失或失访病例。所有患者或家属均签署化疗知情同意书。
1.2研究方法
1.2.1临床资料收集通过查阅电子病案系统和影像学系统,收集患者的临床资料,包括性别、年龄、病理类型、转移部位、一线治疗方案和疗效、ECOG评分及腹部CT结果等。
1.2.2化疗方案所有患者采用替吉奥联合奈达铂进行二线或多线化疗。替吉奥为口服,连用14 d,剂量按照体表面积而定,体表面积<1.25 m2时,用药剂量为40 mg/次,2次/d;体表面积为1.25~1.5 m2时,用药剂量为50 mg/次,2次/d;体表面积>1.5 m2时,用药剂量为60 mg/次,2次/d。奈达铂为静脉滴注,根据患者体表面积,以75 mg/m2溶入0.9%氯化钠溶液,再稀释至0.9%氯化钠溶液500 ml。21 d为1个周期,每两个周期进行一次胸腹部增强CT扫描,以进行疗效评价。化疗终止指征为病情进展或出现不可耐受的毒副作用。
1.2.3随访方法采用门诊随访和电话随访方式,末次随访时间为2015-01-31。观察并记录患者的治疗效果、后续治疗、生存状况及毒副作用情况。PFS指首次替吉奥联合奈达铂方案化疗到第一次影像学检查发现肿瘤进展的时间;总生存期(overall survival,OS)指首次替吉奥联合奈达铂方案化疗到死亡或最后一次随访的时间。
1.3评价指标(1)疗效评价:根据RECIST,完全缓解(CR)指病灶完全消失;部分缓解(PR)指基线病灶长径总和缩小≥30.0%;病情稳定(SD)指基线病灶长径总和缩小程度不及PR,或增加不达PD;PD指基线病灶长径总和增加≥20%,或出现新病灶。客观有效率(RR)=(CR病例数+ PR病例数)/可评价病例数;疾病控制率(DCR)=(CR病例数+ PR病例数+ SD病例数)/可评价病例数。(2)毒副作用:根据国立癌症研究所毒性判定标准(NCI-CTC 4.0)[6]进行评价,并将患者分为0~4级。
1.4统计学方法采用SPSS 17.0统计软件进行描述性统计学分析,采用Kaplan-Meier法绘制生存曲线。
2 结果
2.1临床资料17例患者中,二线化疗6例(占35.3%),三线及以上化疗11例(占64.7%)。17例患者的具体临床资料见表1。

表1 17例患者临床资料〔n(%)〕Table 1 Clinical data of 17 patients
2.2治疗完成情况17例患者共完成57个化疗周期,平均周期为两个,中位周期为3个。其中1例患者因化疗两个周期后肺部感染,未能继续化疗;1例患者因化疗两个周期后出现Ⅳ度骨髓抑制,终止用药。
2.3疗效评价在可评价的17例患者中,获得CR、PR、SD、PD的患者数分别为0例、2例(占11.8%)、9例(占52.9%)、6例(35.3%)。RR为11.8%(2/17),DCR为64.7%(11/17),中位PFS为3.0个月〔95%CI(0.4,6.1),见图1〕。
2.4后续治疗情况及生存状况截至2015-01-31,有3例患者死亡,14例患者生存,中位OS为14.0个月〔95%CI(5.1,31.4),见图2〕。经替吉奥联合奈达铂化疗后,未出现进展的患者3例,1例死亡;出现进展的患者14例,其中9例采用吉非替尼、厄洛替尼及阿法替尼等靶向治疗,7例维持至今。
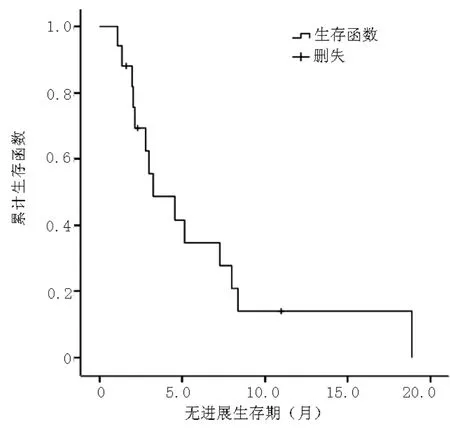
图1 17例患者无进展生存情况Figure 1 Progression free survival of the 17 patients
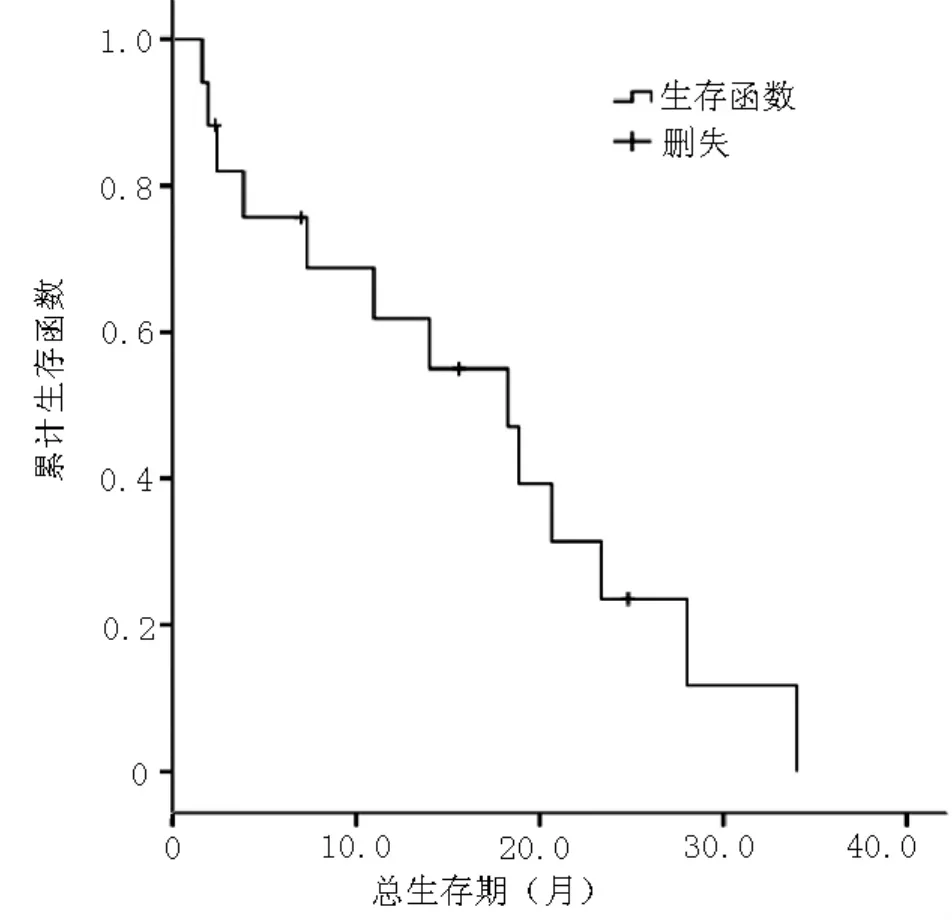
图2 17例患者生存情况Figure 2 Overall survival of the 17 patients
2.5毒副作用出现恶心呕吐、白细胞减少、粒细胞减少、贫血、疲乏的患者数分别为13例(76.5%)、12 例(70.6%)、12例(70.6%)、9例(52.9%)、9例(52.9%),且69.2%及以上为Ⅰ~Ⅱ度。1例(7.7%)患者出现腹泻症状,1例(7.7%)患者出现皮肤色素沉着症状。除1例患者出现Ⅳ度骨髓抑制(粒细胞减少)外,其他患者的毒副作用均在可耐受范围内,无化疗相关致死事件发生。具体毒副作用评价见表2。
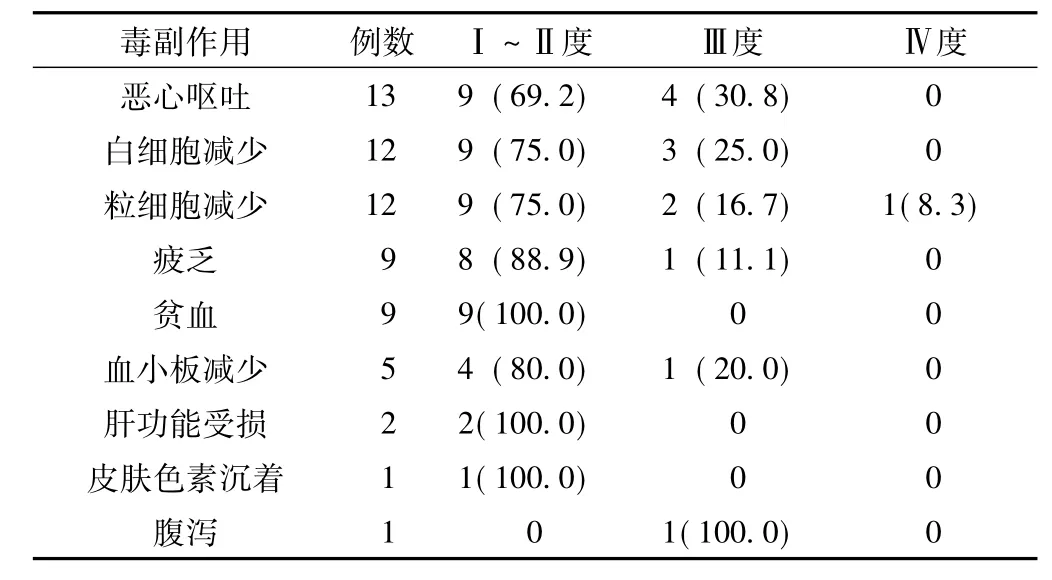
表2 17例患者毒副作用评价〔n(%)〕Table 2 Toxic and side effects of the 17 patients
3 讨论
NSCLC化疗的主要目的为缓解症状、减轻疼痛,提高患者生存质量,延长生存期。以铂类为基础的第三代细胞毒类药物联合方案多为一般状况较好晚期患者的标准一线治疗方案,而靶向治疗也被推荐为敏感突变患者的一线选择。一线方案治疗失败后的二线化疗药物,推荐多西他赛和培美曲塞。随着影像学技术(如磁共振、CT)的进步,许多无症状的转移性肺癌在临床上也开始被发现,经过标准方案治疗后,很多患者还可以接受后续治疗。
有研究显示,晚期肺癌患者生存期的长短,取决于患者接受有效方案的多少[7]。多线治疗后的患者因体力状况较差、外周静脉输注血管情况欠佳及多重耐药性等原因,可选择的治疗药物种类及其用药途径受到一定限制。5-FU具有广谱抗肿瘤作用,被广泛应用于消化道肿瘤的治疗中,但在肺癌治疗中的应用却较少。这主要是因为肺组织中的二氢吡啶脱氢酶(DPD)活性较高,可以参与5-FU的分解代谢,使其在肺内失去抗肿瘤活性。替吉奥是新一代氟尿嘧啶类抗癌药物,为5-FU前体口服复方制剂,由替加氟(FT )、吉美嘧啶(CDHP)、奥替拉西钾(OXO)按照1∶0.4∶1配合而成。其中FT在肝脏及肿瘤组织中可缓慢转变为5-FU;CDHP为DPD的强有力竞争性抑制剂,能够提高肺肿瘤中的5-FU水平,提高其抗肿瘤能力;而OXO能阻断5-FU磷酸化水平引起的胃肠道毒性,从而达到高效低毒的效果[8]。
奈达铂是广谱抗癌药物,属于新一代铂类抗癌药,被广泛应用于多种实体瘤治疗中。其作用机制与顺铂相同,主要是与肿瘤细胞的DNA碱基结合,阻碍DNA复制,从而发挥较广的抗癌作用。与顺铂相比,奈达铂的肾毒性和胃肠道毒性较低,且两者之间无完全交叉耐药性。另外,奈达铂还具有使用方便、较少水化等特点,其剂量限制性是骨髓抑制所致的血小板减少。
多项Ⅰ、Ⅱ期临床研究结果表明,替吉奥无论联合铂类,还是伊立替康、吉西他滨,甚至是联合放疗,其治疗时的毒副作用均可耐受[9-12]。两项Ⅲ期研究表明,替吉奥与卡铂联合应用于NSCLC的一线治疗,其疗效不比标准含铂化疗方案差[13-14]。Totani等[15]报道了替吉奥单药二线治疗晚期NSCLC的Ⅱ期临床试验结果,发现入组的50例患者中,有6例达到了PR,且ORR为12.5%〔95%CI(25.7,53.4%)〕,中位PFS为2.5个月,中位OS为8.2个月,在生存获益的同时,其毒副作用尚可耐受。徐兆国等[16]对一线治疗失败的晚期NSCLC患者进行研究,发现采用替吉奥联合奈达铂治疗患者的1年生存率和PFS均好于采用标准二线化疗方案的患者,且前者的临床获益率为51.3%,中位PFS为99 d。本研究结果显示,采用替吉奥联合奈达铂二线或多线治疗的NSCLC患者的RR为11.8%,DCR为64.7%,PFS为3.0个月,提示该方案的临床获益较好。
本研究结果还显示,替吉奥联合奈达铂二线或多线治疗晚期NSCLC患者的有效率较高,毒副作用较少,主要表现为Ⅰ~Ⅱ度的骨髓抑制和胃肠道反应,大多可耐受且易于处理。另外,该方案给药方便,患者依从性较高,为晚期NSCLC患者的二线或多线化疗提供了一个新方向。但本研究具有一定的局限性,如纳入的病例数较少,观察时间不足;部分进展患者采用了靶向治疗,一定程度上影响了OS的判断;未能统计有效生存期数据,未选择OS为观察终点。因此,该方案的疗效和生存分析仍需进一步的大样本研究来证实。
参考文献
[1]Shepherd FA,Dancey J,Ramlau R,et al.Prospective randomized trial of docetaxel versus best supportive care in patients with nonsmall-cell lung cancer previously treated with platinum-based chemotherapy[J].J Clin Oncol,2000,18(10):2095-2103.
[2]Hanna N,Shepherd FA,Fossella FV,et al.Randomized phaseⅢtrial of pemetrexed versus docetaxel in patients with non-small-cell lung cancer previously treated with chemotherapy[J].Journal of Clinical Oncology,2004,22(9):1589-1597.
[3]Shepherd FA,Rodrigues Pereira J,Ciuleanu T,et al.Erlotinib in previously treated non-small-cell lung cancer[J].N Engl J Med,2005,353(2):123-132.
[4]曹子昂.2014第一版NCCN小细胞肺癌治疗指南解读[J].中国医学前沿杂志:电子版,2013,5(12):79-81.
[5]Yang XN,Wu YL.RECIST-New guidelines to evaluate the response to treatment in solid tumors[J].Journal of Evidence-Based Medicine,2004,4(2):85-90,111.(in Chinese)
杨学宁,吴一龙.实体瘤治疗疗效评价标准-RECIST[J].循证医学,2014,4(2):85-90,111.
[6]Liu YJ,Zhu GP,Guan XY.Comparison of the NCI-CTCAE version 4.0 and version 3.0 in assessing chemoradiation-induced oral mucositis for locally advanced nasopharyngeal carcinoma[J].Oral Oncology,2012,48(6):554-549.
[7]Park SJ,Choi IK,Seo HY,et al.Treatment results including more than third-line chemotherapy for patients with advanced non-small cell lung cancer[J].Oncol Lett,2010,1(1):51-55.
[8]Shirasaka T,Nakano K,Takechi T,et al.Antitumor activity of 1 M tegafur-0.4 M 5-chloro-2,4-dihydroxypyridine-1 M Potassium oxonate(S-1 )against human colon carcinoma orthotopically implanted into nude rats[J].Cancer Res,1996,56(11):2602 -2606.
[9]Kubota K,Sakai H,Yamamoto N,et al.A multi-institution phase Ⅰ/Ⅱtrial of triweekly regimen with S-1 plus cisplatin in patients with advanced non-small cell lung cancer[J].J Thorac Oncol,2010,5(5):702-706.
[10]Ishimoto O,Ishida T,Honda Y,et al.Phase I study of daily S-1 combined with weekly irinotecan in patients with advanced non-small cell lung cancer[J].Int J Clin Oncol,2009,14(1):43-47.
[11]Kaira K,Sunaga N,Yanagitani N,et al.Phase I trial of oral S-l plus gemcitabine in elderly patients with non-small cell lung cancer[J].Anticancer Drugs,2008,19(3):289-294.
[12]Takigawa N,Kiura K,Hotta K,et al.A phase I study of S-1 with concurrent thoracic radiotherapy in elderly patients with localized advanced non-small cell lung cancer[J].Lung Cancer,2011,71(1):60-64.
[13]Okamoto I,Yoshioka H,Morita S,et al.PhaseⅢtrial comparing oral S-1 plus carboplatin with paclitaxel plus carboplatin in chemotherapy-nave patients with advanced non-small-cell lung cancer:results of a west Japan oncology group study[J].J Clin Oncol,2010,28(36):5240-5246.
[14]Katakami N,Gemma A,Sakai H,et al.Randomized phaseⅢtrial of S-1 plus cisplatin versus docetaxel plus cisplatin for advanced non -small-cell lung cancer[J].J Clin Oncol,2012,30:7515.
[15]Totani Y,Saito Y,Hayashi M,et al.A phaseⅡstudy of S-1 monotherapy as second-line treatment for advanced non-small cell lung cancer[J].Cancer Chemother Pharmacol,2009,64(6):1181-1185.
[16]Xu ZG,Zhang XY,Qi XY,et al.Efficacy analysis of S-1 plus nedaplatin versus standard second-line chemotherapy in the treatment of advanced lung adenocarcinoma that failure in the firstline chemotherapy[J].ChineseJournal of Biochemical Pharmaceutics,2014,33(3):78-80.(in Chinese)
徐兆国,张晓晔,齐晓莹,等.替吉奥联合奈达铂对比标准二线化疗用于一线化疗失败的中晚期肺腺癌的疗效分析[J].中国生化药物杂志,2014,33(3):78-80.
(本文编辑:王凤微)
·热点研究·
·论著·
作者单位:100021北京市,北京协和医学院中国医学科学院肿瘤医院内科
Clinical Effect of S-1 Combined With Nedaplatin as Second-line or Further-line Chemotherapy in the Treatment of Advanced Non-small-cell Lung Cancer
MA Di,HAO Xue-zhi,XING Pu-yuan,et al.Department of Internal Medicine, Tumor Hospital,Chinese Academy of Medical Sciences,Peking Union Medical College,Beijing 100021,China
【Abstract】Objective To investigate the clinical effect of S-1 combined with Nedaplatin as second-line or furtherline chemotherapy for patients with advanced non-small-cell lung cancer(NSCLC).Methods We enrolled 17 patients with advanced NSCLC who had unsuccessful first-line chemotherapy in the Tumor Hospital of Chinese Academy of Medical Sciences of Peking Union Medical College from September 2013 to November 2014.All the patients were administrated with S-1 combined with Nedaplatin as second-line or further-line chemotherapy.We took 21 days as a cycle.In the follow-up visits till January,2015,we recorded the therapeutic effect,follow-up treatment,living condition and toxic and side effects.Results Among the 17 patients,6(35.3%)patients were administrated with second-line chemotherapy,11(64.7%)were administrated with three-line or further-line chemotherapy.A total of 57 chemotherapy cycles were completed.In the therapeutic evaluation,the numbers of patients who had complete remission,partial remission,stabilization of the disease and progress of the disease were 0,2,9 and 6,with an objective effective rate of 11.8%(2/17),a disease control rate of 64.7%(11/17)and a median progression-free survival of 3 months〔95%CI(0.4,6.1)〕.By January 31 in 2015,3 patients died,14 patients survived with a median survival of 14.0 months〔95% CI(5.1,31.4)〕.The numbers of patients who had nausea and vomiting,leukopenia,granulocytopenia,anemia and fatigue were 13(76.5%),12(70.6%),12(70.6%),9(52.9%)and 9book=3834,ebook=71(52.9%),and 69.2% or more than 69.2% of the patients with each symptom were atⅠ-Ⅱ°level.Except thatⅣ° myelosuppression occurred in one patient,the toxic and side effects of other patients were all within tolerable range,and no death induced by chemotherapy occurred.ConclusionThe efficacy of S-1 combined with nedaplatin as second-line or further-line chemotherapy is good in the treatment of NSCLC with long survival time and few toxic and side effects,thus the therapy worth further promotion and application.
【Key words】Carcinoma,non-small-cell lung;S-1;Nedaplatin;Chemoradiotherapy,adjuvant;Treatmnet outcome
(收稿日期:2015-06-29;修回日期:2015-09-24)
通信作者:李峻岭,100021北京市,北京协和医学院中国医学科学院肿瘤医院内科;E-mail:drlijunling@ vip.163.com
【中图分类号】R 730.26
【文献标识码】A
doi:10.3969/j.issn.1007-9572.2015.31.014

