CuO纳米线储锂电化学行为与机理的原位透射电镜研究
苏庆梅,杜秀梅,杜高辉,许并社
(太原理工大学 新材料界面科学与工程教育部重点实验室,山西 太原030024)

第一作者:苏庆梅,女,1985年生,博士
CuO纳米线储锂电化学行为与机理的原位透射电镜研究
苏庆梅,杜秀梅,杜高辉,许并社
(太原理工大学 新材料界面科学与工程教育部重点实验室,山西 太原030024)
摘要:过渡金属氧化物是具有前景的锂离子电池负极材料,但是其在电化学反应中的反应行为和反应机制尚不明确。利用原位透射电镜研究了CuO纳米线的首次充放电电化学反应过程。结果表明:放电过程中电化学反应界面沿着CuO纳米线轴向方向移动,且反应的界面始终保持锥形,表明Li+离子的传输是从外向内进行的;且锂化的进行引起了纳米线的径向膨胀和轴向延长及弯曲,径向膨胀~40%,轴向膨胀~43.1%,体积膨胀~185.8%。待首次放电完成后,CuO纳米线转化为Cu纳米晶(2~3 nm),分散在Li2O基体中,而在去锂化后并没有氧化为CuO,而是生成了Cu2O,此不可逆的相转变是造成电池充放电循环中首次不可逆比容量损失的主要原因。
关键词:锂离子电池;电化学行为;CuO纳米线;原位透射电镜
1前言
锂离子电池具有工作电压高、能量密度大、质量轻等优点,在电动汽车和便携式电子设备等领域都得到了广泛的应用,并显示出强劲的发展趋势[1-2]。尽管如此,当前的锂离子电池技术还不能满足人们对高性能电源的需求,从而推动了新型锂离子电池电极材料的研制。过渡金属氧化物以理论容量高、循环性能好、安全性高等优点成为理想的负极材料[3-7]。
CuO是一种最常见的过渡金属氧化物,是目前比较有应用前景的锂离子电池负极材料之一,主要具有以下优势:价格便宜、资源丰富、原料易得、环境友好等。另外CuO具有较高的理论比容量,为670 mAh·g-1(若认为1个CuO分子嵌2个锂离子)[8-9],为石墨负极材料(理论比容量为372 mAh·g-1)的2倍以上。然而,目前CuO负极材料在循环寿命和倍率性能方面还不能满足现代锂离子电池的需求。尤其是,锂离子电池中的电化学反应过程是CuO和Li的氧化还原反应,在电化学反应过程中会有较大的体积膨胀,从而导致电极材料的粉化和微结构的严重破坏而从电极上脱落,使两者之间的接触变差,导致比容量的迅猛衰减[10]。针对这些问题,人们采用各种各样的方法来改进CuO负极材料的电化学性能,如纳米化[11]、构筑特定的纳米结构[12]和引入碳材料(石墨烯和碳纳米管)[13-14]等。纳米材料不仅可以降低储锂过程中的体积膨胀率,还能有效提高大电流充放电能力。如Song等[15]采用原位热氧化法制备了CuO纳米线,电流密度为50 mA·g-1时,100次循环后其可逆比容量仍保持在645 mAh·g-1。文献报道称碳材料的引入不仅能有效缓解充放电循环中较大的体积膨胀产生的应力,还能改善锂在电极材料中的传输,提高了电极的导电性能,从而有效地改善了电极材料CuO的电化学性能。Du等[16]利用微波辅助法制备了CuO/石墨烯复合材料,石墨烯提供了三维网格,有效缓解了CuO放电过程中的体积膨胀,保持了较好的循环稳定性能。尽管CuO作为锂离子电池负极材料时其电化学性能得到了较好的改善,但是还有许多问题并没有得到很好解决。在CuO存储锂机理方面,目前还没有一致的理论,但是较被广泛认同的是在Li嵌入过程中,Li与CuO发生还原反应,生成Li2O,但也包括生成中间相Cu2O等[17]。而在脱锂过程中,Li2O与Cu反应生成Li+和CuO,如下式所示:CuO+2Li++2e-⟺Cu+Li2O,但是这一表达缺乏有力的实验证据。另外,锂离子电池在首次充放电循环中有较大的比容量的损失,主要归因于不可逆的电化学反应过程、SEI膜的生成、电极材料的粉化等[18]。事实上,不可逆电化学反应的本质以及其对转变机理的影响还不明确。最为重要的是CuO作为锂离子电池负极材料的微观转化过程仍然不清楚。
2010年,Huang等[19]利用原位TEM研究了SnO2纳米线的电化学反应过程,开创了锂离子电池电极材料研究的新方法,能保持对电极材料电化学反应的实时监测,近年来此方法得到了广泛的应用。因此我们通过在TEM中建立微电池,其主要组成部分是:以CuO纳米线为工作电极,以锂金属为对电极,以氧化锂为固体电解质,在TEM中对CuO纳米线在电化学反应过程中的形貌变化进行了实时、动态地监控;并通过电子衍射(ED)、高分辨透射电镜(HRTEM)和能量损失谱(EELS)对锂化后CuO电极材料微结构的变化进行了表征,深刻地理解了CuO电极材料的锂化机制。
2实验
2.1CuO纳米线的制备
CuO纳米线是利用热氧化法在铜基底上得到的[20],其主要步骤如下:首先将Cu网在1.0 M的HCl溶液中浸泡30 s,然后用去离子水和无水乙醇反复洗涤3~4次。将上述干燥的Cu网放置在石英舟中,置于管式电阻炉的中央部分,450 ℃下空气气氛中反应3 h。取出石英舟中的黑色粉末即为制备的CuO纳米线。
2.2CuO纳米线的原位电化学反应
CuO纳米线的电化学反应的原位TEM实验是利用Nanofactory公司的STM-TEM样品杆在 JEOL JEM-2100F 透射电镜中完成的。纳米微电池(Nano-LIBs)的建立主要包括3个部分:电极活性物质CuO纳米线、对电极金属锂和固体电解质氧化锂。其主要组装过程如下:首先,用导电胶将样品CuO纳米线粘到金丝的端部,固定在 STM-TEM 样品杆的固定端;接着将 STM-TEM 样品杆放入手套箱内,在手套箱内用剪成的钨丝尖在新鲜的金属锂的表面摩擦几次,以确保针尖上蹭到少许的金属锂。然后将 STM-TEM 样品杆用一个自制的密封袋密封,并取出手套箱快速转移到TEM腔室中,在样品杆转移的过程中会暴露在空气中几秒,这样在锂的表面会快速生成氧化锂层,作为锂离子电池的固体电解质。通过改变STM-TEM样品杆移动端的位置使两电极接触到一起,然后在样品的两端施加一个负电压(-1.0 V)和一个正偏压(+3.0 V)来进行CuO纳米线的锂化和去锂化实验。
3结果与讨论


图1 CuO纳米线的形貌和结构表征:(a)低倍SEM像,(b)高倍SEM像,(c)低倍TEM像,(d)单根CuO纳米线的TEM像,(e)HRTEM图像,(f)ED图像Fig.1 SEM and TEM images of CuO nanowire: (a) SEM image,(b) magnified SEM image of CuO nanowires,(c) TEM image,(d) magnified TEM image of single CuO nanowire, (e) HRTEM image, and (f) ED pattern of CuO nanowire
图2a是TEM中建立的纳米微电池的示意图,包括3个部分:工作电极材料CuO纳米线、金属锂对电极、氧化锂固体电解质。我们在TEM中原位监控了CuO纳米线在锂化反应过程中形貌的变化,利用软件记录下了它们的微观形貌的实时变化。单根CuO纳米线的电化学锂化过程如图2b~g所示,图2b~g是两端所加偏压为-1.0 V时,锂化过程中不同时刻CuO纳米线的TEM像,可以看到随着锂化反应的进行,CuO纳米线发生了轴向的延长和弯曲,CuO纳米线的长度由初始的960 nm延长到1 413 nm;径向也产生了一定的膨胀,纳米线的直径由56 nm增加到78 nm(图3a中对应的A部分),直径膨胀率为39.3%,根据图3可计算出完全锂化后CuO纳米线的体积膨胀为185.8%。
由于在实际的锂离子电池的使用中,电极材料的倍率性能是电池优劣的评价标准之一,因此锂化速率和动力学也很重要,图2h给出了锂化过程中锂化的CuO纳米线长度和时间的关系,可以看出t和L2成正比,表明CuO纳米线的锂化反应属于远程扩散传输类型。图2中箭头所示的是反应界面的位置,表明在锂化的过程中反应界面可以很明显地跟踪到,且反应界面始终保持锥形,表明锂离子的传输是由纳米线的外部向内部进行的。
对CuO纳米线完全锂化后的产物进行了详细的分析研究。图4a是完全锂化的CuO纳米线的TEM像,可以看出CuO纳米线的外部覆盖了一层厚厚的晶体,厚度约为5~7 nm,通过HRTEM和ED图像(图4b,4c)可证明此晶体层为Li2O,即完全锂化后被Li2O层包覆;内部为纳米晶体(尺寸大小为2~3 nm)分散在Li2O基底中。从图4b可以看出,其外层晶体的晶面间距为0.27 nm,对应的是Li2O的(111)面,证明了包覆层Li2O的产生。其内部衬度较深的部分纳米晶(图4b中的白色圆圈)的晶面间距为0.2 nm,对应的是Cu的(111)面,表明完全锂化后CuO被还原成了Cu和Li2O。其完全锂化后电极的ED图像如图4c所示,其衍射环可标定为Cu和Li2O,由此可以看出单晶的CuO发生的电化学反应方程式为:CuO+ 2Li++ 2e-→ Cu + Li2O。图4d是部分锂化的CuO纳米线的形状示意图,可以看出锂化部分的CuO纳米线发生了体积膨胀,且CuO纳米线外面覆盖一层Li2O,其内部的产物为Cu纳米晶分散在Li2O的网格中。

图2 首次锂化过程中CuO纳米线的形貌变化:(a)TEM中构建的纳米微电池的示意图,(b~g)锂化过程中不同时刻CuO纳米线的TEM像,(h)反应界面的位置和锂化时间的关系曲线,(i)反应界面的TEM图像Fig.2 Schematic illustration of the experimental setup for in situ TEM analysis of nano-LIB(a), the electrochemical lithiation of individual CuOnanowire showing obvious volume expansion after lithiation with a potential of -1 V as a function of time (b~g), the reaction front position (arrowed in (b)-(g)) against time(h), and high-magnification TEM image of the reaction front(i)

图3 初始的CuO纳米线的TEM像(a),完全锂化后的纳米线的TEM像(b)Fig.3 TEM images of original (a) and lithiated (b) CuO nanowire
待CuO电极材料完全锂化后,将电极两端的偏压变为+3.0 V 进行去锂化实验,且对去锂化后材料的结构和形貌进行了表征,如图5所示。图5a是去锂化后样品的TEM像,可以看到去锂化后CuO纳米线表面的Li2O层的厚度明显减少,但是仍有一层薄薄的 Li2O。通过图5b的HRTEM 图像可以看到,去锂化后CuO纳米线具有多晶结构,但是细小的纳米晶仍具有较好的单晶结构,部分晶面间距为0.2 nm,对应为Cu2O的(111)晶面,说明在去锂化后有Cu2O纳米晶生成,即去锂化后由Cu转变为了Cu2O而不是CuO,这一结果通过去锂化后电极的ED图像进行了验证,如图5c所示,所有的衍射环均标定为Li2O 和Cu2O,并没有CuO的衍射环出现,这说明去锂化后并没有转变为初始态的CuO。能量损失谱(EELS)可用来判断过渡金属氧化物中金属的化合价,因此我们进一步用 EELS谱对去锂化后样品中铜的价态进行了验证,图5d的EELS 结果对应的正是+1 价的铜[21],这和 HRTEM及ED的结果是相吻合的。通过以上分析,可以确定去锂化后的产物是Cu2O,表明CuO电极材料作为锂离子电池负极材料在首次的充放电循环中发生了不可逆的相转变。另外,去锂化后仍然有Li2O的存在,说明去锂化后仍然有部分锂离子以Li2O的形式存在。曾有文献报道称Li2O是非电化学活性的[3]。而锂化-去锂化循环中Li2O的可逆形成和分解,说明纳米颗粒的特殊电催化效应[3]。在我们的实验中去锂化过程中Li2O的分解可解释为Li2O网格中的Cu纳米晶对其催化作用形成的。

图4 完全锂化后单根CuO纳米线的TEM像(a)、HRTEM像(b)、ED图像(c),部分锂化的CuO纳米线的示意图(d)Fig.4 TEM image(a) , HRTEM image (b) and ED pattern (c) of fully lithiated CuO nanowire,and schematic illustration of partly lithiated CuO nanowire(d)
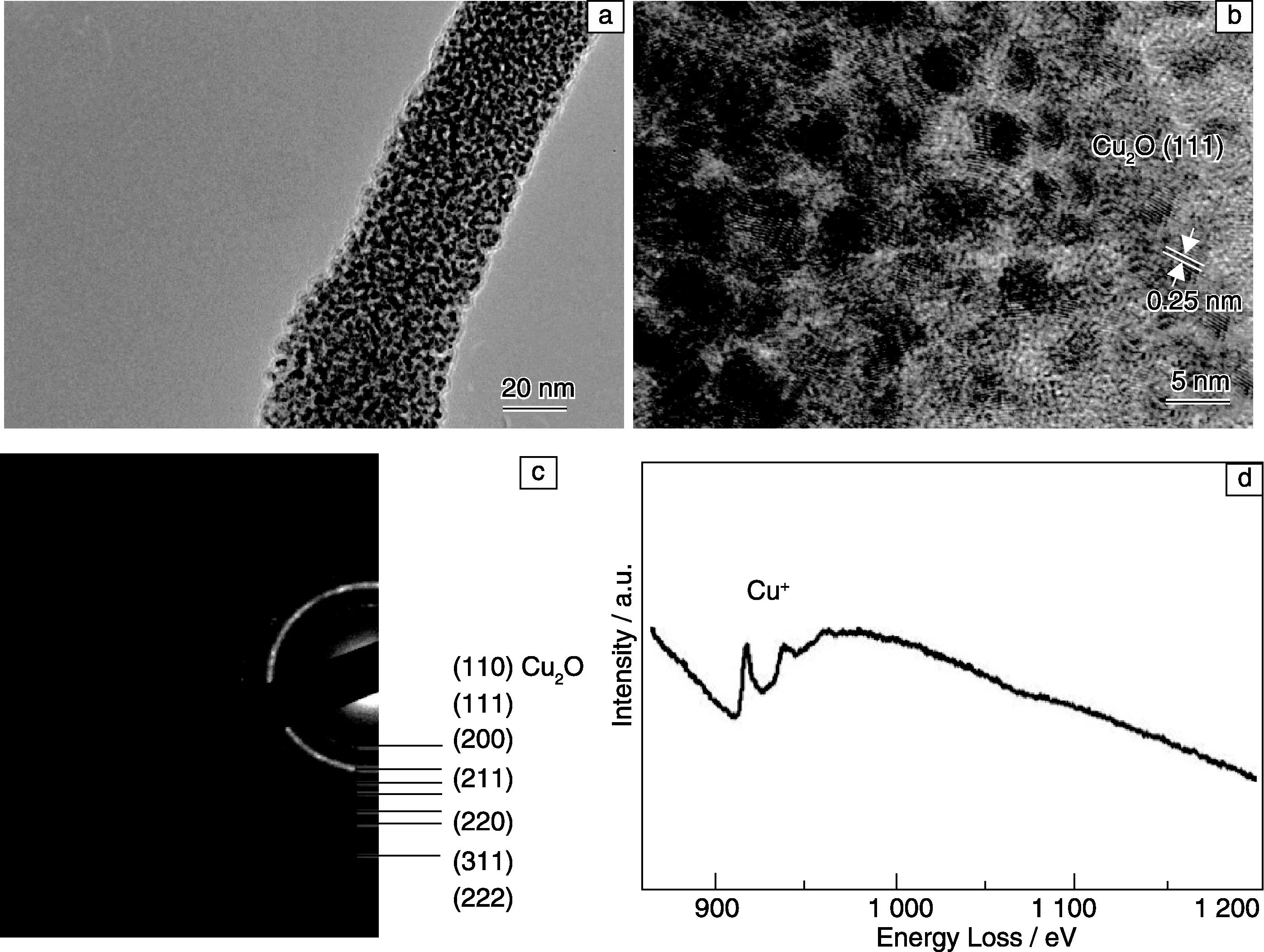
图5 去锂化后CuO纳米线的TEM像(a)、HRTEM像(b)、ED图像(c),去锂化后CuO电极的能量损失谱(EELS)(d)Fig.5 TEM image(a), HRTEM image(b), ED pattern(c) and EELS spectrum (d)of the delithiated CuO nanowire
以CuO纳米线为电极材料构成的微电池,通过原位TEM手段对其首次充放电电化学反应过程进行了实时监控,结合原位 TEM 结果可得到CuO纳米线首次充放电电化学反应过程的反应示意图如图6所示。图6a是CuO纳米线首次锂化过程示意图,初始态的CuO纳米线的直径较均匀,待完全锂化后其发生了径向和轴向的膨胀,体积膨胀达到185.8%,且锂化的CuO纳米线的外表面包覆一层厚厚的Li2O层。根据锂化后产物的HRTEM和ED图可得出首次锂化过程的电化学反应式为:CuO + 2Li++ 2e-→ Cu + Li2O。其首次完全去锂化后,纳米线的体积发生了收缩,且外表面的Li2O层的厚度有所减少,但是仍有一薄层的Li2O存在;且分析结果表明其转化为了Cu2O而不是CuO,因此首次去锂化过程的电化学反应式可表示为:2Cu + Li2O → Cu2O + 2Li++ 2e-。我们周期性地改变所加的偏压,也开展了CuO纳米线的第二个循环的原位观测,其微观结构变化可逆,为如图6b所示。第二次的锂化过程为Cu2O发生体积膨胀,其表面的Li2O层的厚度增加,结构表征仍为Cu纳米晶分散在Li2O的网格中,其电化学反应过程表示为:Cu2O+2Li++2e-→2Cu+Li2O。第二次去锂化过程中膨胀的纳米线体积再次发生收缩,外表面的Li2O层的厚度再次减少,和首次去锂化过程相同产生了Cu2O纳米晶,其电化学反应为:2Cu+Li2O→Cu2O+2Li++2e-。可以看出首次锂化过程是不可逆的,第一次去锂化后发生了Cu和Cu2O之间的可逆的相转变,即为:2Cu + Li2O←→Cu2O + 2Li++ 2e-。

图6 锂嵌入和脱出的过程示意图和相应的电化学反应:(a)首次循环,(b)第2次循环Fig.6 Schematic illustration of Li-insertion and Li-extraction processes, and the corresponding phase transformations at different reaction stages: (a) 1st cycle and (b) 2nd cycle.
4结论
以CuO纳米线为工作电极,以Li金属为对电极,Li2O为固体电解质,利用原位TEM实时监控了在首次充放电过程中CuO纳米线的动态形貌变化,并通过HRTEM、EELS和ED对锂化和去锂化后电极材料的微结构进行了表征,得出以下结论:锂化过程中CuO纳米线发生了径向膨胀和轴向的延长、弯曲,径向膨胀~40%,轴向膨胀~43.1%,体积膨胀~185.8%。待首次锂化完成后,CuO纳米线转变为Cu纳米晶(2~3 nm),分散在Li2O网格中,而完全去锂化后Cu并没有氧化为CuO,而是生成了Cu2O,此不可逆的相转变是造成电池充放电循环中首次不可逆比容量损失的主要原因。原位透射电镜研究手段也可用于其它过渡金属氧(硫、氟)化物电化学反应行为的观测研究,有助于理解其电化学反应机理,为寻找商业化锂离子电池负极材料做深入的探索。
参考文献References
[1]Tarascon J M, Armand M. Issues and Challenges Facing Rechargeable Lithium Batteries[J].Nature, 2001, 414: 359-367.
[2]Lou X W, Archer L A, Yang Z C. Hollow Micro-/Nanostructures: Synthesis and Applications[J].AdvMater, 2008, 20: 3 987-4 019.
[3]Poizot P, Laruelle S, Grugeon S,etal. Nano-Sized Transition-Metal Oxides as Negative Electrode[J].Nature, 2000, 407: 496-499.
[4]Koo B, Xiong H, Slater M D,etal. Hollow Iron Oxide Nanoparticles for Application in Lithium Ion Batteries[J].NanoLett, 2012, 12: 2 429-2 435.
[5]Jiang J, Li Y, Liu J,etal. Recent Advances in Metal Oxide-Based Electrode Architecture Design for Electrochemical Energy Storage[J].AdvMater, 2012, 24(38): 5 166-5 180.
[6]Ding S, Chen J S, Lou X W. One-Dimensional Hierarchical Structures Composed of Novel Metal Oxide Nanosheets on a Carbon Nanotube Backbone and Their Lithium-Storage Properties[J].AdvFuncMater, 2011, 21(21): 4 120-4 125.
[7] Su D, Kim H S, Kim W S,etal. Mesoporous Nickel Oxide Nanowires: Hydrothermal Synthesis, Characterization and Applications for Lithium-Ion Batteries and Supercapacitors with Superior Performance[J].Chemistry-AEuropeanJournal, 2012, 18(26): 8 224-8 229.
[8]Debart A, Dupont L, Poizot P,etal. A Transmission Electron Microscopy Study of the Reactivity Mechanism of Tailor-Made CuO Particles toward Lithium[J].JElectrochemSoc, 2001, 148(11): A1266-A1274.
[9]Sahay R, Suresh Kumar P, Aravindan V,etal. High Aspect Ratio Electrospun CuO Nanofibers as Anode Material for Lithium-Ion Batteries with Superior Cycleability[J].JPhysChemC, 2012, 116(34): 18 087-18 092.
[10] Cabana J, Monconduit L, Larcher D,etal. Beyond Intercalation-Based Li-Ion Batteries: The State of the Art and Challenges of Electrode Materials Reacting through Conversion Reactions[J].AdvMater, 2010, 22(35): E170-E192.
[11]Gao D, Yang G, Li J,etal. Room-Temperature Ferromagnetism of Flowerlike CuO Nanostructure[J].JPhysChemC, 2010, 114(43): 18 347-18 351.
[12]Park J C, Kim J, Kwon H,etal. Gram-Scale Synthesis of Cu(2)O Nanocubes and Subsequent Oxidation to CuO Hollow Nanostructures for Lithium-Ion Batteries Anode Materials[J].AdvMater, 2009, 21(7): 803-807.
[13]Wang B, Wu X L, Shu C Y,etal. Synthesis of CuO/Graphene Nanocomposite as a High-Performance Anode Material for Lithium-Ion Batteries[J].JMaterC, 2010, 20(47): 10 661-10 664.
[14]Zhang S F, Hu J S, Zhong L S,etal. Introducing Dual Functional CNT Networks into CuO Nanomicrospheres toward Superior Electrode Materials for Lithium-Ion Batteries[J].ChemMater, 2008, 20(11): 3 617-3 622.
[15]Li A, Song H H, Wan W B,etal. Copper Oxide Nanowire Arrays Synthesized by In-Situ Thermal Oxidation as an Anode Material for Lithium-Ion Batteries[J].ElectrochiActa, 2014, 132: 42-48.
[16]Zhou X Y, Zhang J, Su Q M,etal. Nanoleaf-on-Sheet CuO/Graphene Composites: Microwave-Assisted Assemble and Excellent Electrochemical Performances for Lithium Ion Batteries[J].ElectrochiActa, 2014, 125: 615-621.
[17]Grugeon S, Laruelle S, Herrera-Urbina R,etal. Particle Size Effects on the Electrochemical Performance of Copper Oxides toward Lithium[J].JElectrochemSoc, 2001, 148(4): A285-A292.
[18]Larcher D, Masquelier C, Bonnin D,etal. Effect of Particle Size on Lithium Intercalation into α-Fe2O3[J].JElectrochemSoc, 2003, 150: A133-A139.
[19]Huang J Y, Zhong L, Wang C M,etal. In Situ Observation of the Electrochemical Lithiation of a Single SnO2Nanowire Electrode[J].Science, 2010, 330(6010): 1 515-1 520.
[20]Jiang X C, Herricks T, Xia Y. CuO Nanowires can be Synthesized by Heating Copper Substrates in Air[J].NanoLett, 2002, 2(12): 1 333-1 338.
[21]Calvert C C, Rainforth W M, Sinclair D C,etal. EELS Characterization of Bulk CaCu3Ti4O12Ceramics[J].Micron, 2006, 37: 412-419.
(编辑惠琼)
In Situ Transmission Electron Microscopy Observation of theElectrochemical Behavior and Mechanism of CuO Nanowires
SU Qingmei, DU Xiumei, DU Gaohui, XU Bingshe
(Key Laboratory of Materials Interface Science and Engineering, Ministry of Education,
Taiyuan University of Technology, Taiyuan 030024, China)
Abstract:Transition metal oxides have been used as one of the most promising candidates as anode materials for lithium ion batteries (LIBs). However, their electrochemical process remains unclear. Here we directly observe the dynamic behaviors and conversion mechanism of CuO nanowire in LIBs by in situ transmission electron microscope. The results show that a reaction front propagates progressively along the nanowire and always keeps a conical shape during the whole process. The conical reaction interface also verifies that lithiation proceeds from the nanowire surface towards its center. After lithiation, the originally straight CuO nanowire becomes heavily distorted and prolonged. The lithiation process causes an axial elongation of 43.1%, a radial expansion of 40%, and the total volume expansion of 185%. Also, single crystalline CuO nanowires are found to transform to multicrystalline nanowires consisting of many Cu nanograins (2~3 nm) embedded in Li2O matrix. The delithiated product is not CuO but Cu2O, accounting for the irreversible electrochemical process and the large capacity fading of the anode material in the first cycle.
Key words:lithium ion battery; electrochemical behavior; CuO nanowire; in situ transmission electron microscope
中图分类号:TB321
文献标识码:A
文章编号:1674-3962(2015)05-0346-07
DOI:10.7502/j.issn.1674-3962.2015.05.03
通讯作者:杜高辉,男,1974年生,博士,研究员,Email:gaohuidu@gmail.com
基金项目:教育部新世纪优秀人才支持计划
收稿日期:2014-10-31

