铁改性活性炭对水中镉的吸附和再生实验研究
李亚如+许智华+张道方

摘 要: 制备了铁改性活性炭,通过快速动态小柱实验研究了活性炭改性前后对镉的吸附性能,同时考察了进水pH、进水流量和初始质量浓度等因素对吸附材料穿透特性的影响,最后对铁改性活性炭再生方法进行了研究.结果表明,铁改性活性炭对镉的吸附量是未改性活性炭的3.7倍,负载的铁氧化物大大提高了改性活性炭对镉的吸附能力,同时铁改性活性炭对镉的吸附受溶液pH、进水流量和初始质量浓度的影响.0.05 mol·L-1的EDTA-2Na溶液能有效再生吸附饱和后的改性活性炭,再生后的改性活性炭可重复使用.
关键词:铁氧化物; 活性炭; 镉; 吸附; 再生
中图分类号: X 703 文献标志码: A
重金属镉是典型的环境污染物,广泛存在于电镀、化工、电子和核工业等领域.镉的毒性较大,虽然在水体中长期以低浓度存在,但是其可通过食物链进入人体,严重危害人体的肝肾等器官[1].
水中镉的去除方法主要有化学沉淀法、离子交换法和吸附法等[2].其中吸附法具有操作简单、使用方便、效率高等特点,是一种有效的处理重金属的方法.活性炭来源广泛,比表面积大,孔隙结构发达,具有丰富的表面官能团,是使用最广泛的一种吸附剂[3-4].然而由于活性炭存在灰分高、微孔分布过宽和选择吸附性能差的缺点,对污染物的去除作用有限,有必要对其进行改性,以增大其吸附容量[5].铁氧化物比表面积较大,表面活性官能团较多,电荷可变性强,对金属离子来说是一种良好的吸附剂[6-8].有研究表明,通过负载铁氧化物改性活性炭去除水中的砷、铬、苯酚和有机染料等污染物,均取得了较好的去除效果[9-12],但目前将其应用于去除水中阳离子重金属的研究较少.
本文利用负载铁氧化物制备一种铁改性活性炭去除水中的Cd(Ⅱ),通过快速动态小柱实验(Rapid smallscale column tests,RSSCTs),比较改性前后活性炭对Cd(Ⅱ)的吸附能力,以及进水pH、流量和初始质量浓度等对吸附性能的影响,同时对再生方法进行探讨.通过对吸附性能和再生方法的系统研究,探讨铁改性活性炭吸附去除水中Cd(Ⅱ)的可行性,为其在水处理中的应用提供一定的参考依据.
1 实验材料和方法
1.1 实验材料
实验中采用的颗粒活性炭为煤质活性炭(碘值为900~1 050 mg·g-1,强度大于等于90,粒度为12~40目).实验使用的药剂均为分析纯,购自国药化学试剂有限公司.
1.2 实验方法
1.2.1 活性炭改性
将颗粒活性炭进行预处理.粉碎后,过100~200目筛,用去离子水洗去活性炭上的杂质,105℃烘干12 h,保存待用.称取10 g预处理后的活性炭,投入到1 000 mL、1 mol·L-1的NaOH溶液中混合均匀,再加入25 g Fe2(SO4)3,磁力搅拌4 h,然后放在40℃的烘箱中密闭干燥48 h,取出用去离子水洗净,烘干待用.未改性活性炭和铁改性活性炭分别用AC和Fe-AC表示.
1.2.2 吸附实验
用3CdSO4·8H2O和去离子水配制含Cd(Ⅱ)模拟废水.吸附实验通过快速动态小柱完成,其材质为有机玻璃,柱高为13.5 cm,内径为0.5 cm,空床体积为2.65 mL,小柱内装有约(1.4±0.1) g活性炭,粒径为100~200目,进水方式为下行式,间隔一定时间取水样进行检测.所有实验均在室温下进行.进水pH分别为4、5、6,进水流量分别为2.0、4.5、9.0 mL·min-1,进水中Cd(Ⅱ)初始质量浓度分别为0.1、0.5、1.0 mg·L-1.考察某一因素时,固定其它两个因素,分别研究进水pH、流量和初始质量浓度对吸附性能的影响.
1.2.3 再生实验
进水pH为6、流量为4.5 mL·min-1、初始质量浓度为1.0 mg·L-1的快速动态小柱吸附饱和后,分别用1 mol·L-1 HCl、1 mol·L-1 HNO3和0.05 mol·L-1 EDTA-2Na溶液对铁改性活性炭进行再生.再生流量为4.5 mL·min-1,进水方式为上行式,再生时间为15 min,再生后用去离子水洗去残余再生液.
1.2.4 分析方法
实验中重金属浓度用TAS-990型火焰原子吸收分光光度仪进行检测.
2 结果与讨论
2.1 吸附Cd(Ⅱ)的影响因素
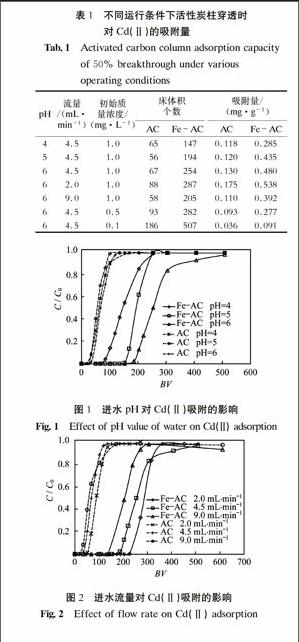
随着溶液流过小柱,溶质逐渐被吸附,在小柱上部的吸附剂达到饱和状态后将不再起吸附作用.当吸附带下沿到达小柱底部后,出水中溶质的浓度迅速上升,当达到允许出水浓度时,此点为吸附穿透点.本文定义动态小柱出水中Cd(Ⅱ)达到初始质量浓度的50%时的点为穿透点[13].在不同运行条件下,改性前后活性炭柱穿透时对Cd(Ⅱ)的吸附量结果如表1所示.
2.1.1 pH的影响
图1为不同pH条件下,改性前后活性炭对Cd(Ⅱ)的吸附穿透曲线.其中,进水Cd(Ⅱ)初始质量浓度为1.0 mg·L-1,流量为4.5 mL·min-1.图中纵坐标为出水质量浓度C与进水初始质量浓度C0的比值,横坐标为进水的床体积个数BV,其为处理水量与活性炭床体积的比值[14].
从图1和表1可知,进水pH分别为4、5、6时,AC的穿透曲线变化不明显,AC床穿透时运行的床体积个数分别为65、56、67,随pH变化较小;而Fe-AC的穿透曲线变化明显,Fe-AC床穿透时运行的床体积个数分别为147、194、254,随pH增加,运行的床体积个数逐渐增加.Fe-AC对Cd(Ⅱ)的吸附量大于AC,且穿透时运行的床体积个数和吸附量随pH增加而增加.当pH为6时,吸附效果最佳,运行的床体积个数和吸附量约为AC的3.8倍,这表明铁改性活性炭对镉的吸附能力有了显著提高.
同时,pH对Fe-AC吸附Cd(Ⅱ)的影响较大,这可能是因为,对于活性炭上一定的活性位点,溶液中的H+和Cd(Ⅱ)存在竞争.pH越小,溶液中H+浓度越高,与Cd(Ⅱ)的竞争越激烈,致使Fe-AC对Cd(Ⅱ)的吸附量减小.此外,当pH为4~6时,均未检测到铁的释出,说明加载在活性炭上的铁非常稳定,未发生脱附现象.
2.1.2 进水流速的影响
图2为不同进水流速下,改性前后活性炭对Cd(Ⅱ)的吸附穿透曲线.其中,进水pH为6,初始质量浓度为1.0 mg·L-1.由表1可知,进水流量分别为2.0、4.5、9.0 mL·min-1时,AC床穿透时运行的床体积个数分别为88、67、58,而Fe-AC床穿透时运行的床体积个数分别为287、254、205.结果表明,AC对Cd(Ⅱ)的吸附能力差,而Fe-AC运行的床体积个数始终是AC的3~4倍,进一步证明铁改性活性炭对Cd(Ⅱ)的吸附能力得到了显著提高.AC和Fe-AC穿透时运行的床体积个数和吸附量均随进水流量的增大而减小,进水流量为2.0 mL·min-1时,吸附效果最佳.随着进水流量增大,吸附带移动速度加快,导致穿透时运行的床体积个数和时间均减少[15].吸附量减小,可能是因为随进水流量的增大吸附质在活性炭床中的停留时间减少,Cd(Ⅱ)不能够及时扩散到活性炭表面.
2.1.3 初始质量浓度的影响
图3为不同进水初始质量浓度下改性前后活性炭吸附Cd(Ⅱ)的穿透曲线.保持进水pH为6,流量为4.5 mL·min-1.由表1可知,进水Cd(Ⅱ)的初始质量浓度分别为0.1、0.5、1.0 mg·L-1时,AC床穿透时运行的床体积个数分别为186、93、67,而Fe-AC床穿透时运行的床体积个数分别为507、282、254,床体积个数均随初始质量浓度的增加而减小,但Fe-AC运行的床体积个数始终大于AC,表明铁改性活性炭对Cd(Ⅱ)的吸附能力得到了提高.
此外,穿透曲线受初始质量浓度的影响较大.随着进水Cd(Ⅱ)初始质量浓度的增加,穿透曲线的斜率增大,运行的床体积个数减小.这表明浓度梯度会影响吸附柱的饱和速率和穿透时间,即扩散过程依赖于浓度.随着进水初始质量浓度增加,重金属的负载率增加,但吸附带长度的传质推动力减小[16].
2.2 再生实验
在进水Cd(Ⅱ)初始质量浓度为1.0 mg·L-1,pH为6,流量为4.5 mL·min-1时吸附饱和后,对Fe-AC进行了再生实验研究,再生液分别为1 mol·L-1 HCl、1 mol·L-1 HNO3和0.05 mol·L-1 EDTA-2Na溶液.采用不同再生液再生前后的Fe-AC对Cd(Ⅱ)的吸附量对比结果如图4所示.
从图4可看出,1 mol·L-1HCl和HNO3的再生效果差,再生后的吸附量分别仅为再生前的15%和13%,而0.05 mol·L-1 EDTA-2Na溶液的再生效果良好,再生后的吸附量约为再生前的76%.因此,本文选用0.05 mol·L-1 EDTA-2Na溶液作为再生溶液进行吸附-再生实验.图5为再生后Fe-AC的吸附穿透曲线.由图5可知,再生后Fe-AC的吸附能力有所降低,每再生一次,穿透时运行的床体积个数约降低13%,这可能是由于再生过程中负载的铁部分流失造成的.但总体而言,经2次再生后运行的床体积个数仍在100以上,对Cd(Ⅱ)仍保持良好的吸附性能.
3 结 论
本文通过快速动态小柱实验,研究负载铁氧化物活性炭对Cd(Ⅱ)的吸附特性.实验结果表明,负载铁氧化物能显著提高活性炭对水中Cd(Ⅱ)的吸附能力.具体结论为:
(1) 在进水pH为6、Cd(Ⅱ)初始质量浓度为1.0 mg·L-1、流量为4.5 mL·min-1时,铁改性活性炭能运行254个床体积后穿透,吸附量达0.480 mg·g-1,而未改性的活性炭仅能运行67个床体积,吸附量仅为0.130 mg·g-1.
(2) 进水pH为4~6时,Fe-AC穿透时运行的床体积个数随着pH增加而增加,且吸附量始终大于AC,实验过程中没有检测到铁的释出,这说明铁在活性炭上的加载非常稳定.同时,Fe-AC对Cd(Ⅱ)的去除还与进水流量和初始质量浓度等因素有关.进水流量越小,穿透时运行的床体积个数越多,吸附量越大.随着进水初始质量浓度的增大,活性炭柱的穿透时间减少,吸附带长度的传质推动力也减小.
(3) 饱和后的Fe-AC可被0.05 mol·L-1的EDTA-2Na溶液有效再生,再生后的Fe-AC吸附性能良好,可重复使用.
参考文献:
[1] 戴世明,吕锡武.镉污染的水处理技术研究进展[J].安全与环境工程,2006,13(3):63-66.
[2] RAO K S,ANAND S,VENKATESWARLU P.Modeling the kinetics of Cd(Ⅱ)adsorption on Syzygium cumini L leaf powder in a fixed bed mini column[J].Journal of Industrial and Engineering Chemistry,2011,17(2):174-181.
[3] JUSOH A,SU S L,ALI N A,et al.A simulation study of the removal efficiency of granular activated carbon on cadmium and lead[J].Desalination,2007,206(1-3):9-16.
[4] ALSLAIBI T M,ABUSTAN I,AHMAD M A,et al.Cadmium removal from aqueous solution using microwaved olive stone activated carbon[J].Journal of Environmental Chemical Engineering,2013,1(3):589-599.
[5] 梁霞,王学江.活性炭改性方法及其在水处理中的应用[J].水处理技术,2011,37(8):1-6.
[6] 刘永红,叶发兵,岳霞丽,等.铁氧化物的合成及其表征[J].化学与生物工程,2006,23(7):10-12.
[7] GRANADOSCORREA F,CORRALCAPULIN N G,OLGUíN M T,et al.Comparison of the Cd(Ⅱ) adsorption processes between boehmite(γAlOOH)and goethite(αFeOOH)[J].Chemical Engineering Journal,2011,171(3):1027-1034.
[8] 丁振华,冯俊明.氧化铁矿物对重金属离子的吸附及其表面特征[J].矿物学报,2000,20(4):349-352.
[9] VITELARODRIGUEZ A V,RANGELMENDEZ J R.Arsenic removal by modified activated carbons with iron hydro(oxide)nanoparticles[J].Journal of Environmental Management,2013,114:225-231.
[10] LIU W F,ZHANG J A,ZHANG C L,et al.Adsorptive removal of Cr(VI)by Femodified activated carbon prepared from Trapa natans husk[J].Chemical Engineering Journal,2010,162(2):677-684.
[11] YANG JK,PARK HJ,LEE HD,et al.Removal of Cu(Ⅱ)by activated carbon impregnated with iron(Ⅲ)[J].Colloids and Surfaces A:Physicochemical and Engineering Aspects[J].2009,337(1-3):154-158.
[12] GONCALVES M,GUERREIRO M C,DE OLIVEIRA L C,et al.A friendly environmental material:Iron oxide dispersed over activated carbon from coffee husk for organic pollutants removal[J].Journal of Environmental Management,2013,127:206-211.
[13] DWIVEDI C P,SAHU J N,MOHANTY C R,et al.Column performance of granular activated carbon packed bed for Pb(Ⅱ) removal[J].Journal of Hazardous Materials,2008,156(1-3):596-603.
[14] NABARLATZ D,DE CELIS J,BONELLI P,et al.Batch and dynamic sorption of Ni(Ⅱ) ions by activated carbon based on a native lignocellulosic precursor[J].Journal of Environmental Management,2012,97:109-115.
[15] MONDAL M K.Removal of Pb(Ⅱ) ions from aqueous solution using activated tea waste:Adsorption on a fixedbed column[J].Journal of Environmental Management,2009,90(11):3266-3271.
[16] GOEL J,KADIRVELU K,RAJAGOPAL C,et al.Removal of lead(Ⅱ) by adsorption using treated granular activated carbon:Batch and column studies[J].Journal of Hazardous Materials,2005,125(1-3):211-220.

