同步放化疗治疗多发脑转移瘤的临床效果
王希龙
[摘要] 目的 观察替莫唑胺联合全脑放射疗法治疗多发脑转移瘤(3~10个病灶)患者的疗效、生存率和不良反应。 方法 全脑放射治疗30 Gy/3 Gy/10 f/2周,同时替莫唑胺75 mg/(m2·d)连续口服14 d,休息4周后继续替莫唑胺150 mg/(m2·d)辅助治疗6个周期。 结果 治疗后93.5%患者神经系统症状改善,对脑转移灶的客观有效率为76.1%(35/46),局部控制率为97.8%(45/46),中位无进展生存时间为8.5个月,中位总生存时间为13.3个月,一年生存率为54.3%(25/46),不良反应主要为Ⅰ~Ⅱ级胃肠道反应、中性粒细胞减少、脱发、疲乏、头痛、焦虑等。 结论 替莫唑胺同步全脑放疗治疗脑转移瘤的有效率和生存率均较高,且安全有效。
[关键词] 全脑放疗;同步化疗;替莫唑胺;脑转移瘤
[中图分类号] R739.41 [文献标识码] A [文章编号] 1674-4721(2014)12(b)-0080-03
脑转移瘤是成人最常见的颅内肿瘤,目前约15%的肿瘤患者会在病程中最终出现脑转移,临床、影像、尸检证实其中约50%为多发脑转移[1-3]。颅外恶性肿瘤在病程中将发生脑转移,常见的原发部位是肺、乳腺、恶性黑色素瘤、消化道及肾脏[4]。一旦发生脑转移就意味着肿瘤已经广泛播散,预后非常差,30%~50%的死亡因为颅内病变未控制或复发。出现脑转移后,如果不进行特殊治疗,中位生存时间仅为4周;全脑放射治疗使中位生存时间延长至4~6个月[4]。本文主要观察替莫唑胺加同步全脑放射疗法(whole brain radiation therapy,WBRT)治疗脑转移瘤的疗效。
1 资料与方法
1.1 一般资料
2008年12月~2012年12月本科收治的多发脑转移瘤患者46例,原发灶已经病理确诊,脑转移灶经脑部CT或MRI证实为3~10个不等,>4个者占23%;转移瘤大小为0.8~5.0 cm,中位大小为2.1 cm;其中男32例,女14例,年龄37~70岁,中位年龄56岁;原发于肺癌的29例,原发于乳腺癌的10例,原发于胃肠道肿瘤的4例,原发于肾脏肿瘤的2例,恶性黑色素瘤1例。治疗前Karnofsky评分≥70分,生存期预计>3个月。
1.2 排除标准
既往脑部有放疗史;1个月内有化疗史,尚未从既往化疗的毒性反应中完全恢复,包括血常规、肝肾功能;合并严重心脏、肝脏、肾脏、血液系统及精神病者;治疗结束后失访的患者。
1.3 治疗方法
1.3.1 化疗 替莫唑胺1次/d,剂量为75 mg/m2,共14 d,同步放化疗结束后休息4周,继续给予6个周期的替莫唑胺辅助治疗,剂量为150 mg/(m2·d),1次/d,共5 d,停药23 d为1个周期。
1.3.2 放疗 化疗第1天接受WBRT,6MV-X DT 30 Gy/3 Gy/10 f,1次/d,5次/周,共2周,在放疗中根据患者脑水肿的轻重适当给予20%甘露醇或地塞米松治疗。
1.4 疗效及毒副反应评价标准
治疗期间每周记录1次体检情况,测定1次血常规及肝、肾功能,放疗前及放疗结束后1个月复查脑部CT或MRI进行疗效评价。采用实体瘤RECIST(1.1版)疗效评价标准[5]:包括完全缓解(CR)、部分缓解(PR)、稳定(SD)和进展(PD),有效=CR+PR,局部控制=CR+PR+SD。生存时间从本方案治疗开始至死亡的时间。毒性反应根据CTCAE 4.0版的标准进行评价:分为Ⅰ~Ⅴ级。Ⅰ级:轻度,无症状或轻度症状,仅临床或诊断发现,无需治疗;Ⅱ级:中度,最小的、局部的或非侵入性治疗指征,年龄相关工具性日常生活活动受限;Ⅲ级:重度或重要医学意义,但不会立即危及生命,住院治疗或延长住院时间指征,致残,自理性日常生活活动受限;Ⅳ级:危及生命,需紧急治疗;Ⅴ级:死亡。
2 结果
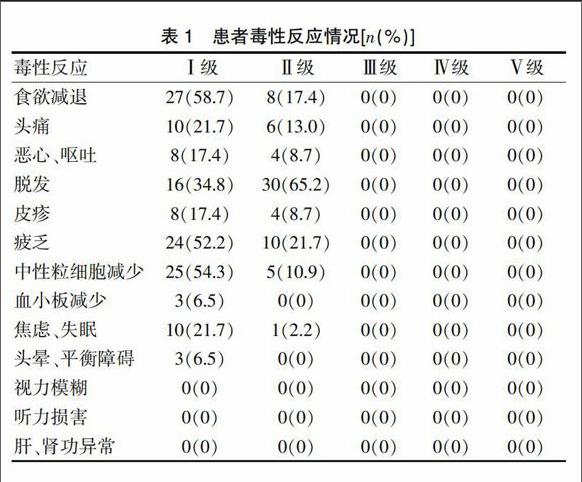
46例患者中43例(93.5%)的脑部症状在治疗后缓解。放化疗结束后1个月复查脑部CT或MRI并与治疗前比较,颅内转移灶CR 8例(17.4%),PR 27例(58.7%),SD 10例(21.7%),PD 1例(2.2%),有效率76.1%(35/46),局部控制率为97.8%(45/46)。中位无进展生存期为8.5个月,中位总生存期为13.3个月,一年生存率为54.3%(25/46)。毒副反应主要是:胃肠道反应、中性粒细胞减少、脱发、疲乏、头痛、焦虑、失眠等,均为Ⅰ~Ⅱ级,无≥Ⅲ级毒性反应,未见视力、听力及肝肾功能损害(表1)。
表1 患者毒性反应情况[n(%)]
3 讨论
脑转移瘤是颅外恶性肿瘤累及脑实质、脑脊膜、脑神经和颅内血管的转移性肿瘤,其中脑实质转移最为多见,随着CT及MRI在临床诊断中的广泛应用及恶性肿瘤疗效的改善,脑转移瘤的发生率呈增加趋势[4]。多发性脑转移瘤的标准治疗是WBRT,在RTOG的随机对照研究中,WBRT近期客观有效率约60%,症状稳定和改善率与此相似,1年生存率为10%~20%。RTOG的Ⅲ期临床试验表明,30 Gy/2周与40 Gy/4周的疗效相似,中位生存时间为3~6个月。脑转移瘤本身与其他部位转移瘤有一样的化疗敏感性,而对化疗药物抗拒的主要原因是血-脑脊液屏障问题,故化疗应选择能通过血-脑脊液屏障的化疗药。由于放疗达到一定剂量后能破坏血-脑脊液屏障使药物到达脑组织内[6],为放化疗联合应用提供了理论基础。替莫唑胺是一种新型的口服烷化剂,能有效通过血-脑脊液屏障,为广谱抗肿瘤药物,到达颅内迅速达到有效药物浓度,多项临床研究均提示替莫唑胺对于来自不同原发肿瘤的脑转移瘤患者均有一定的疗效[7-10],有临床试验证明,替莫唑胺与WBRT联合应用与单纯WBRT相比疗效明显提高,且耐受性较好[11]。endprint
本研究中93.5%的患者头痛、头晕等症状在治疗后均得到改善,脑转移灶客观有效率为76.1%,局部控制率为97.8%,中位无进展生存期为8.5个月,中位总生存期为13.3个月,一年生存率为54.3%,较单纯放疗疗效明显提高。毒副反应主要是:食欲减退、头痛、恶心、呕吐、脱发、皮疹、疲乏、中性粒细胞减少等,均为Ⅰ~Ⅱ级,经对症治疗后均可缓解,因此,替莫唑胺联合同步WBRT治疗多发脑转移瘤是一种较理想的方案。
[参考文献]
[1] Posner JB.Management of brain metastases[J].Rev Neurol(Paris),1992,148(6-7):477-487.
[2] Nussbaum ES,Djalilian HR,Cho KH,et al.Brain metastases.Histology,multiplicity,surgery,and survival[J].Cancer,1996,78(8):1781-1788.
[3] Delattre JY,Krol G,Thaler HT,et al.Distribution of brain metastases[J].Arch Neurol,1988,45(7):741-744.
[4] 殷蔚伯,余子豪,徐国镇,等.肿瘤放射治疗学[M].北京:中国协和医科大学出版社,2008:1200-1201.
[5] Eisenhauer EA,Therasse P,Bogaerts J,et al.New response evaluation criteria in solid tumours:revised RECIST guideline(version 1.1)[J].Eur J Cancer,2009,45(2):228-247.
[6] 伍勇,刘国龙.放疗开放血脑屏障及其对化疗的意义[J].中国神经肿瘤杂志,2007,5(1):63-65.
[7] Abrey LE,Olson JD,Raizer JJ,et al.A phase Ⅱ trial of temozolomide for patients with recurrent or progressive brain metastases[J].J Neurooncol,2001,53(3):259-265.
[8] Christodoulou C,Bafaloukos D,Kosmidis P,et al.Phase Ⅱ study of temozolomide in heavily pretreated cancer patients with brain metastases[J].Ann Oncol,2001,12(2):249-254.
[9] 黄韶华,梁俊君,徐德玲,等.替莫唑胺与司莫司汀治疗恶性脑胶质瘤的疗效分析[J].中国当代医药,2013,20(5):69,71.
[10] 王跃飞,陈谦学,李明昌,等.替莫唑胺联合放疗治疗恶性胶质瘤有效性和安全性的Meta分析[J].中国医药导报,2014,11(23):71,75.
[11] Verger E,Gil M,Yaya R,et al.Temozolomide and concomitant whole brain radiotherapy in patients with brain metastases:a phase Ⅱ randomized trial[J].Int J Radiat Oncol Biol Phys,2005,61(1):185-191.
(收稿日期:2014-09-15 本文编辑:李亚聪)endprint