HPLC-HG-AFS 法分析西藏冬虫夏草中的砷形态化合物
曹晓钢, 王 君, 李建民, 王顺芝
(西藏出入境检验检疫局检验检疫技术中心,西藏拉萨850002)
冬虫夏草是麦角菌科虫草属真菌冬虫夏草菌Cordyceps sinensis 寄生在鳞翅目蝙蝠蛾科蝠蛾属幼虫上所形成的虫生子囊真菌,其中西藏冬虫夏草生长于海拔3 600 米以上,处在昼夜温差大、紫外线强的严寒地带。因此,这造就了其生物活性物质多、药效强、无污染等特点,是虫草中的上品,市场地位和名声很高,有“黄金草”的美誉。
王钢力等[1]考察了17 批青海和西藏(冬虫夏草主产地)产冬虫夏草药材的质量,并采用原子吸收分光光度法测定了其中砷、汞、铜、铅和镉的残留量。结果发现,这些药材中砷的含有量较高,10 批青海产的砷含有量为3.68 ~9.97 mg/kg,而7批西藏产的为1.16 ~4.40 mg/kg,均明显超出《中国药典》2005 年版(一部,2010 年版无)对药材及其制剂的要求(重金属As 残留限量≤2.0 mg/kg)。
目前,人们已发现30 余种砷形态化合物。一般认为,无机砷As (V)和As (Ⅲ)的毒性最大,而有机砷中仅MMA 和DMA 有较小的毒性,其他大多无毒[2-5]。由此可见,以无机砷与有机砷的不同毒性进行综合考察,比用砷的总量来评价其毒性更加科学,因为其总量很可能远大于砷作为有害污染物的限量。本实验将建立西藏冬虫夏草中砷形态化合物As (Ⅲ)、DMA、MMA 和As (Ⅴ)的高效液相色谱-氢化物产生-原子荧光(HPLC-HGAFS)分析方法,用于测定以上4 种成分的含有量。
1 材料
1.1 仪器 BT 224S 电子天平(德国赛多利斯公司);SAP 10-SA 10 HPLC-HG-AFS 联用仪(北京吉天仪器有限公司);KQ300DE 超声波提取仪(昆山超声仪器有限公司);Universal 320R 台式高速离心机(德国Hettich 公司);超纯水系统(去离子水电阻率为18.2 MΩ/cm,美国Millipore 公司)。
1.2 标准溶液和试剂 砷标准溶液(1 000 mg/L,国家标准物质研究中心);亚砷酸根、砷酸根、一甲基砷、二甲基砷标准溶液(以砷计,质量分数分别为75.7 ±1.2、17.5 ±0.4、25.1 ±0.8、52.9±1.8 μg/g,中国计量科学研究院)。甲醇和硝酸分别为色谱纯和优级纯(德国CNW 公司);硼氢化钾、氢氧化钠、硫脲、抗坏血酸均为分析纯(国药集团化学试剂有限公司);盐酸为优级纯(成都市科龙化工试剂厂);其他试剂均为分析纯;实验用水为自制。
1.3 试药 本实验共收集了32 批样品,有29 批在西藏冬虫夏草产区现场采购和市售。其中,21批采自那曲地区(主产区),4 批采自林芝地区,1批采自昌都地区,3 批采自日喀则地区。另外剩余3 批样品采青海和四川省,见表1。
新鲜的冬虫夏草样品取回后,去除泥沙,清洗干净,自然风干至水分含有量在10%以下。然后,将样品粉碎,装入密封袋中,置于冰箱保鲜室储藏备用(除特别说明外,本实验均采用26 号丁青产冬虫夏草作为供试样品)。
2 方法
2.1 仪器参数与色谱条件 原子荧光分光光度计,负高压285 V;灯电流100 mA;辅阴极灯电流45 mA;载气(Ar)体积流量400 mL/min;辅助气(Ar)体积流量600 mL/min。HPLC 色谱柱,保护柱PRP-X100 (25 mm×2.3 mm,12 ~20 μm);阴离子分离柱PRP-X100 (250 mm × 4.1 mm,10 μm);流动相 (NH4)2HPO4溶液 (20 mmol/L,10% 甲酸调节至pH 为6.0);体积流量1.0 mL/min;进样量100 μL;柱温30 ℃。

表1 供试样品列表Tab.1 List of tested samples
2.2 标准溶液的制备 精密称取亚砷酸根、砷酸根、一甲基砷和二甲基砷标准溶液适量,用纯水分别配制成2.0 mg/L 的砷形态单标,4 ℃下保存。然后,将其用水稀释成每1 mL 分别含砷20、40、60、80、100 ng 的混合标准溶液,即得。
2.3 样品的处理 精密称取样品0.5 g,置于50 mL 离心管中,加入纯水10 mL 混匀,超声20 min(功率80%、温度20 ℃),离心10 min (温度10 ℃、转速9 000 r/min),取上清液。然后,再离心10 min (温度10 ℃、转速16 000 r/min),取上清液,过0.22 μm 滤膜,滤液(4 ℃下保存时间不超过48 h)进行HPLC-HG-AFS 分析。
3 结果与讨论
3.1 色谱条件的优化
3.1.1 色谱柱的选择 4 种砷形态化合物As(Ⅲ)、DMA、MMA 和As (Ⅴ)均为中强酸或弱酸性,根据它们在一定介质中能以阴离子形式存在的特点,并参考文献[6-9],本实验采用Hamilton PRP-X100 阴离子分析色谱柱,能较好地分离无机和有机阴离子。
3.1.2 流动相的选择
3.1.2.1 流动相体系[10-13]本实验分别对磷酸氢二钾、磷酸二氢钾、磷酸氢二铵作为流动相进行考察,发现以20 mmol/L K2HPO4和20 mmol/L KH2PO4混合溶液(pH = 6.0)为流动相时,As(Ⅲ)、DMA 和MMA 不能完全分离;以10 mmol/L K2HPO4和10 mmol/L KH2PO4混合液(pH =6.0)为流动相时,4 种砷形态化合物能完全分离,但As(Ⅴ)峰形不理想;以15 mmol/L 磷酸氢二铵(pH=6.0)为流动相时,As (Ⅴ)峰形也不理想,当浓度为25 mmol/L 时,DMA 和MMA 峰灵敏度降低较多,但当浓度为20 mmol/L 时,以上4 种成分能完全分离,而且峰形尖锐,灵敏度高。因此,选择20 mmol/L 磷酸氢二铵作为流动相体系。
3.1.2.2 流 动 相 pH[14]以 20 mmol/L(NH4)2HPO4为流动相,考察了不同pH (5.0、6.0、7.0)下4 种砷形态化合物的分离情况。结果显示,当pH 小于6.0 时,As (Ⅲ)与DMA 不易分离;当pH 大于6.0 时,DMA 与MMA 也难以分离。因此,选择流动相的pH 为6.0。
3.1.2.3 体积流量 流动相的体积流量与分离柱的填料性质、颗粒粒径大小等因素有关,结合柱色谱类型与要求,本实验在0.8 ~1.5 mL/min 之间选择。结果,从谱图的分离效果、峰型等指标来看,当体积流量为1.0 mL/min 时,4 种砷形态的分离效果最好。
3.2 原子荧光条件的优化
3.2.1 KBH4浓度的选择 KBH4可影响氢化物生成和氢火焰质量,对分析结果的影响很大。本实验显示,适宜的KBH4浓度为1.5%。
3.2.2 HCl 浓度的选择 HCl 浓度过高,将生成过量的氢气,易导致信噪比小,重现性低;HCl 浓度过低,三价砷的还原将不完全,同时不能产生有效的火焰。因此,本实验选择HCl 浓度为7%。
3.2.3 蠕动泵转速的确定 蠕动泵转速主要决定KBH4和HCl 的进样浓度,当转速为60 r/min 时,砷形态检测信号达到最佳情况。因此,本实验选择蠕动泵转速为60 r/min。
3.3 前处理条件的优化[15-18]
3.3.1 提取溶剂的选择 砷化合物的提取是定量分析的关键,本实验考察了纯水、磷酸氢二铵-水(0.26%,m/V)、磷酸氢二钾-水(0.5%,m/V)、磷酸-水(2%,V/V)、盐酸-水(2%,V/V)、甲醇-水(20%,V/V)这6 种体系的提取效果。结果显示,采用纯水提取时,提取率较高,而且色谱峰的分离度较好。因此,本实验选择纯水为提取溶剂。
3.3.2 提取参数的选择 通过正交试验优化,本实验确定最佳的提取参数为料液比0.5 g ∶10 mL,超声功率80%,提取时间20 min,提取温度20 ℃。
3.3.3 离心条件的选择 离心条件主要为离心速度、温度和时间。本实验发现,较好的离心条件为离心10 min (温度10 ℃、转速9 000 r/min),取上清液,再离心10 min (温度10 ℃、转速16 000 r/min)。
3.4 方法学考察
3.4.1 线性关系和检出限 0 ~100 μg/L 范围内配制质量浓度为0、20、40、60、80 和100 μg/L的4 种砷形态化合物混合标准溶液,然后以化合物的峰面积为纵坐标(S),相应的质量浓度(μg/L)为横坐标(C),绘制标准工作曲线。结果,在0 ~100 μg/L 范围内,它们均呈良好的线性关系,r均>0.999。再根据仪器3 倍信噪比(3 S/N),计算出砷形态检出限,见表2。
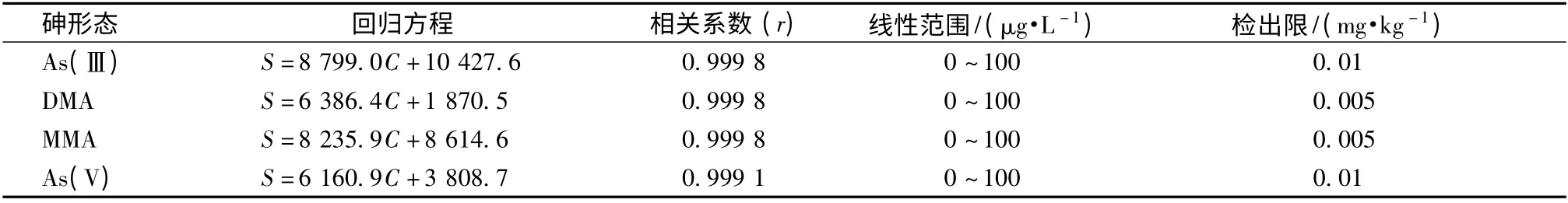
表2 回归方程、相关系数、线性范围及检出限Tab.2 Regression equations,correlation coefficients,linear ranges and limits of detection
3.4.2 回收率及精密度 本实验对同一冬虫夏草样品分别加入高、中、低3 个水平的对照品,每个水平重复6 次,计算回收率及同一水平的RSD 值,结果见表3。由表可知,该方法对冬虫夏草样品的加样回收率在87.0% ~94.0%之间,检测结果间的RSD 值在1.0% ~4.5%之间,显示出良好的回收率和精密度。
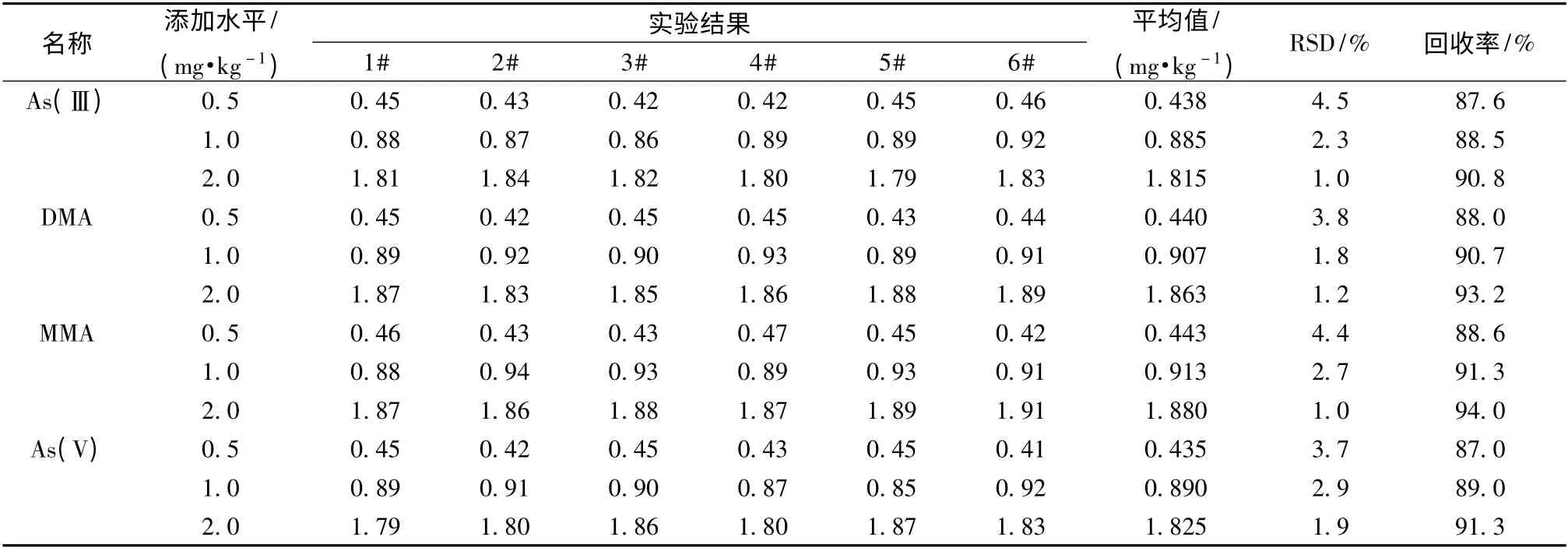
表3 冬虫夏草中砷形态的回收率和精密度(n=6)Tab.3 Recovery rates and precisions of arsenic speciations in Cordyceps sinensis (n=6)
3.4.3 稳定性考察[19]实验中发现,40 ℃下水浴48 h 时,会导致As (Ⅲ)迅速降解,仅有一小部分转化为As (V),而DMA 和MMA 则较为稳定。因此,其前处理方法应简便、快速,经处理后的样品溶液不宜长时间置于室温下,否则很容易造成As (Ⅲ)降解,并且还应尽快上机测定,于4 ℃下保存的时间不宜超过48 h。
3.5 样品测定 为进一步研究样品中的砷形态,本实验采用《GB/T 5009.11-2003 食品中总砷和无机砷的测定》中的方法,测定了32 批样品的总砷、无机砷和有机砷含有量,结果见表4。由表可知,西藏冬虫夏草中总砷的含有量在4.71 ~8.91 mg/kg 之间,明显超出《中国药典》及《药用植物及制剂进出口绿色行业标准》中有害元素砷限量指标≤2.0 mg/kg 的规定。但是,该植物中的无机砷主要以As (Ⅲ)形态存在,含有量较低,在0.01 ~0.06 mg/kg 之间,而且As (V)形态含有量也非常低,仅检出2 批,分别为0.015 和0.020 mg/kg,同时有机砷中的DMA 和MMA 也均未检出。由此说明,西藏冬虫夏草中的总砷主要以其他有机砷形态存在,并且四川和青海产冬虫夏草与西藏产在砷形态含有量方面无明显差异。
4 结论
本实验建立了一种HPLC-HG-AFS 联用技术分析西藏冬虫夏草中砷形态化合物As (Ⅲ)、DMA、MMA、As (V)的方法,并确定了液相色谱、原子荧光以及样品前处理的条件。结果表明,该方法能有效分析测定西藏冬虫夏草中的砷形态化合物,以上4 种成分的加样回收率较高,在87.0% ~94.0%之间,而且分离效果良好,操作简便快速,灵敏度高,重复性好,测定结果准确可靠。
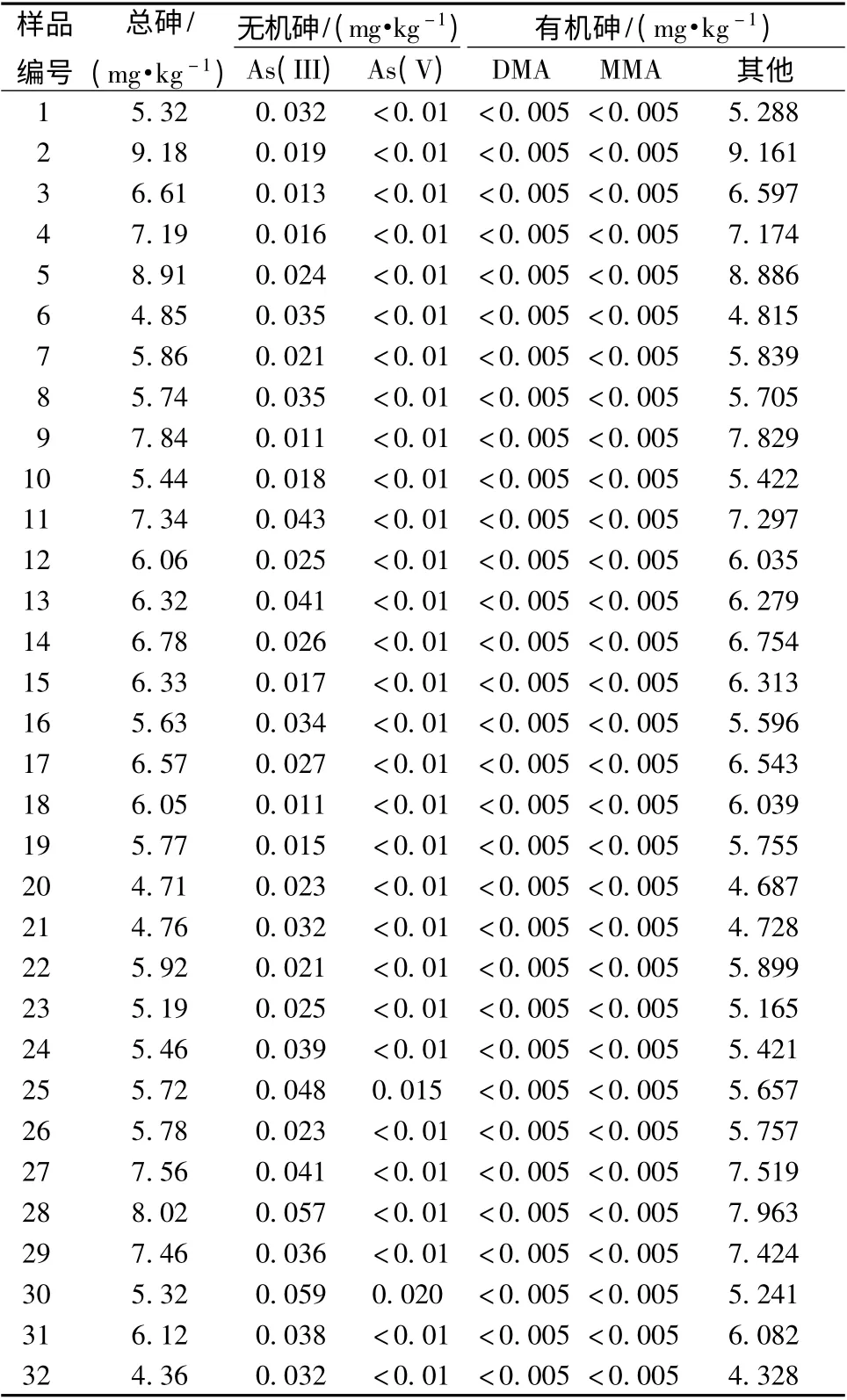
表4 冬虫夏草中砷形态检测结果Tab.4 Determination result of arsenic speciations in Cordyceps sinensis
另外还发现,西藏冬虫夏草中总砷的含有量较高,但毒性较大的无机砷含有量较低,而且毒性较小的DMA 和MMA 也未检出,大部分以其他有机砷形态存在。《GB 2762-2012 食品安全国家标准食品污染物限量》中对无机砷的最高限量为0.1 mg/kg,可见该植物中的无机砷含有量符合最严格的食品安全标准,危害性较小。但是,西藏冬虫夏草中的有机砷是以何种形态存在,其毒性大小如何,还需要进行深入的研究。
[1] 王钢力,金红宇,韩小萍,等. 冬虫夏草药材的质量研究及存在问题[J]. 中草药,2008,39(1):115-118.
[2] Beard H C,Lyerly L A. Separation of arsenic from antimony and bismuth by solvent extraction[J]. Anal Chem,1991,33(12):1781-1782.
[3] Zhang X,Vanderbiesen V,Cubber A D. Accumulation of arsenic species in serum of patients with chronic renaldisease[J].Clin Chem,1996,42(8):1231-1237.
[4] Petrick J S,Ayala-Fierro F,Cullen W R,et al. Monomethylarsonous acid(MMA Ⅲ)is more toxic than arsenite in Chang human hepatocytes[J]. Toxicol Appl Pharmacol,2000,163(2):203-207.
[5] 刘桂华,汪 丽. HPLC-ICP-MS 在紫菜中砷形态分析的应用[J]. 分析测试学报,2002,21(4):88-90.
[6] 熊文明,冯敏玲,李拥军,等. 超声辅助提取-高效液相色谱-电感耦合等离子体质谱法测定南美白对虾中砷形态[J]. 广东农业科学,2013,40(12):122-124,133.
[7] 刘守廷,蒋天成,李健梅,等. HPLC-AFS 联用测定海产品中砷的形态[J]. 化学分析计量,2013,22(1):11-14.
[8] 张国平,刘 虹,刘丛强,等. 离子色谱-等离子体质谱联用测定热泉水样的砷形态[J]. 分析试验室,2007,26(9):17-20.
[9] 郝春莉,王 庚,余晶晶,等. 15 种中药材中砷的形态分析[J]. 分析测试学报,2009,28(8):918-921.
[10] 田 雨,蔡 璇,郑锡波,等. 高效液相色谱-氢化物发生原子荧光光谱法分析桂皮中砷形态化合物的检测方法[J]. 化学工程师,2014,221(2):19-21.
[11] 林燕奎,李 勇,王丙涛,等. 液相色谱-原子荧光光谱联用检测海产品中不同形态砷的研究[J]. 中国卫生检验杂志,2009,19(9):1955-1958.
[12] 沈 黎,陈晓园,路 磊,等. 液相色谱-原子荧光光谱联用检测小龙虾和鱼中不同形态砷的研究[J]. 绿色科技,2013(11):160-162.
[13] 汤 鋆,马冰洁,应 英,等. 原子荧光形态分析仪测定植物类海产品中砷形态化合物[J]. 中国卫生检验杂志,2010,20(11):2729-2731.
[14] 姜 泓,张颖花,丁敬华,等. HPLC-HG-AFS 法测定雄黄中As (Ⅲ)的含量[J]. 化学研究,2008,19(4):67-69.
[15] 徐陆正,解 清,陈玉红,等. HPLC-ICP-MS 联用分析中成药中的可溶性砷形态[J]. 环境化学,2010,29(6):1187-1190.
[16] 孙汉文,李爱红,孙建民. 中草药中微量元素形态分析研究进展[J]. 河北大学学报:自然科学版,2002,22(4):400-403.
[17] 薛 慧,董 宾,宫 博,等. 方便面中砷元素的形态分析[J]. 化学分析计量,2013,22(6):49-51.
[18] 解 楠,徐红斌,曹程明,等. 大米中总砷和不同形态无机砷含量的测定[J]. 食品与发酵工业,2010,36(1):146-148.
[19] 张 磊,吴永宁,赵云峰. 不同形态砷化合物稳定性研究和砷形态分析中样品前处理技术[J]. 国外医学:卫生学分册,2007,34(4):238-244.

