钾离子掺杂对石墨型氮化碳光催化剂能带结构及光催化性能的影响
张 健 王彦娟 胡绍争(辽宁石油化工大学化学化工与环境学部,辽宁抚顺113001)
钾离子掺杂对石墨型氮化碳光催化剂能带结构及光催化性能的影响
张 健 王彦娟 胡绍争*
(辽宁石油化工大学化学化工与环境学部,辽宁抚顺113001)
以双氰胺和氢氧化钾为原料制备了能带可控的钾离子掺杂石墨型氮化碳(g-C3N4)光催化剂,并与碱处理的g-C3N4及g-C3N4/KOH复合催化剂进行了对比.采用X射线衍射(XRD)光谱、紫外-可见(UV-Vis)光谱、傅里叶变换红外(FTIR)光谱、N2吸附、电感耦合等离子体-原子发射光谱(ICP-AES)、荧光(PL)光谱、X光电子能谱(XPS)等分析手段对制备的催化剂进行了表征.结果表明,钾离子含量对氮化碳催化剂的价带及导带位置有显著影响.此外,钾离子的引入抑制了氮化碳晶粒的生长,提高了氮化碳的比表面积以及对可见光的吸收,降低了光生电子-空穴对的复合几率.以染料罗丹明B的降解为探针反应系统研究了钾离子掺杂对g-C3N4在可见光下催化性能的影响,研究了光催化反应机理.结果表明,钾离子掺杂后氮化碳的光催化性能显著提高.制备的钾离子掺杂氮化碳催化剂表现出良好的结构及催化稳定性.
氮化碳;可控能带;钾离子掺杂;稳定性;可见光
1 引言
目前,由于能源和环境危机的日益严重,寻找新的清洁能源变得越来越紧迫.太阳能是无污染的可再生能源.以太阳能代替传统化石能源是解决目前能源与环境危机的最佳方案之一.然而,较低的能量转换效率大大限制了太阳能的实际应用.最近,非金属石墨相氮化碳(g-C3N4)作为可见光光催化剂在光解水制氢气、1降解有机物2及有机合成3等方面被证实有巨大的应用前景.这归功于其适中的带隙宽度、优越的化学和热稳定性以及独特的电子性质.然而,g-C3N4有一个明显的缺点,那就是光生载流子寿命短、易复合,导致量子效率较低.4,5
©Editorial office ofActa Physico-Chimica Sinica
发展g-C3N4基异质结光催化剂是解决量子效率问题的有效途径之一.光生电荷能通过异质结实现快速有效的转移,对提高光催化性能有显著影响.众所周知,两种半导体催化剂的能级匹配是形成异质结的关键所在.因此,如能实现g-C3N4的能级可控合成,将对两半导体间的能级匹配及异质结的形成起到事半功倍的作用.掺杂是实现能级调控的最为简单有效的方法之一.掺杂后,掺杂剂的原子轨道与g-C3N4原有的分子轨道发生轨道杂化,引起电子结构的改变,进而导致g-C3N4价带与导带能级位置的变化.
由于活泼的化学性质,碱金属被广泛地应用于催化反应中,例如酯交换反应、丙烯环氧化、N2O还原、甲苯氧化等.6-9然而,碱金属的引入对光催化性能的促进作用却很少有人报道.10,11Grzechulska等10制备了一系列碱金属改性的TiO2催化剂,并用于光催化降解有机物反应.结果表明碱金属的引入提高了催化性能,活性顺序为:TiO2/KOH>TiO2/Ca(OH)2>TiO2/Ba(OH)2>TiO2(锐钛矿).Chen等11采用溶胶-凝胶法制备了K+掺杂的TiO2催化剂.结果表明,焙烧过程导致形成K4-4xTixO2,其中x对光催化性能有显著影响.此外,K+掺杂提高了界面电荷转移能力及催化剂对反应底物的吸附能力.
本文以双氰胺和氢氧化钾为原料制备了能带可控的K+掺杂g-C3N4光催化剂,并与碱处理的g-C3N4及g-C3N4/KOH复合催化剂进行了对比.采用X射线衍射(XRD)光谱、紫外-可见(UV-Vis)光谱、红外傅里叶变换(FTIR)光谱、N2吸附、荧光(PL)光谱、X光电子能谱(XPS)等对制备的催化剂进行表征,考察了K+的引入对催化剂物理性质、光学性质及结构性质等的影响.以染料罗丹明B的降解为探针反应考察了催化剂的光催化活性及稳定性.本文不仅提供了一种能级可控的g-C3N4的制备方法,还为g-C3N4基异质结光催化剂的制备打开了方便之门.
2 实验部分
2.1 K+掺杂g-C3N4的制备
采用双氰胺为前驱体制备g-C3N4.12称取2 g双氰胺分散在10 mL去离子水中,加入10 mL的KOH溶液(0.02,0.05,0.07,0.09 mol·L-1).将得到的悬浊液加热至水分蒸干,放入烘箱中,80°C干燥.将干燥后的固体研磨后放入坩埚中,550°C下焙烧2 h,升温速率5°C·min-1,待坩埚冷却后取出.得到一系列K+掺杂g-C3N4催化剂,记为K(x)-CN,其中x为KOH的浓度.重复上述制备过程,将10 mL去离子水或10 mL的NH4OH(0.05 mol·L-1)取代KOH溶液,得到的催化剂命名为g-C3N4和OH(0.05)-CN.将制备的g-C3N4分散在10 mL的KOH(0.05 mol·L-1)溶液中,得到的悬浊液搅拌10 h,加热蒸干水分,得到的固体命名为g-C3N4/KOH.
2.2 结构表征
XRD光谱采用日本岛津公司的X射线衍射仪(XRD-7000)进行测定,以Cu靶Kα1作为辐射电源,工作电压40 kV,工作电流30 mA.FTIR光谱使用美国NICOLET公司的傅里叶变换红外光谱仪(FTIR,Nicolet360)进行测定.氮气吸附等温线均是采用Micrometrics ASAP 2010物理吸附仪在-196°C下测得.测定前,样品首先于350°C下真空脱气处理10 h,样品的比表面积是通过Brunauer-Emmett-Teller (BET)方法求得.UV-Vis光谱采用日本JASCA公司的紫外-可见光谱仪(UV-550)进行测定.电感耦合等离子体(ICP)质谱采用美国Perkin Elmer公司的Elan6100DRC型ICP-MS.X光电子能谱(XPS)使用赛默飞世尔科技有限公司的Thermo ESCALAB 250光电子能谱仪进行测定.PL光谱使用FP-6300荧光分光光度计,Xe灯为激发光源进行测定.
2.3 活性评价
以250 W高压钠灯(主波长400-800 nm)为可见光光源,以亚硝酸钠溶液为循环水除去其中紫外光.以染料罗丹明B为降解物评价催化剂的光催化活性.0.05 g催化剂加入到200 mL浓度为10 mg·L-1的罗丹明B中,搅拌0.5 h达到催化剂对反应底物的吸附平衡.搅拌下将溶液放在光源下进行照射,同时鼓入空气(30°C,标准大气压).每0.5 h取一个样品置于离心管中,在转速为3000 r·min-1的条件下离心5 min后取上层清液,用紫外-可见分光光度计于550 nm测定吸光度.
3 结果和讨论
3.1 XRD表征
图1为g-C3N4、K(x)-CN,OH(0.05)-CN和g-C3N4/KOH的XRD图谱.图中有两个特征峰,分别位于2θ为13.1°和27.5°处.其中27.5°处的衍射峰最强,为芳香物层间堆积特征峰,晶面指数标记为(002),对应层间距d=0.33 nm,说明g-C3N4具有和石墨类似的层状结构.13.1°处的衍射峰是melon类物质的特征峰,晶面指数标记为(100),对应3-s-三嗪结构中氮孔间距d=0.67 nm.13图1(a)显示,随着K+含量的提高,衍射峰强度逐渐降低,说明K+的引入抑制了氮化碳催化剂晶粒的生长.依照Debye-Scherrer公式计算得出,g-C3N4、K(0.02)-CN、K(0.05)-CN、K(0.07)-CN和K(0.09)-CN的粒径分别为65、53、48、33和27 nm.在谱图中没有发现K物种相应的特征峰,然而随着K+含量的提高,衍射峰角度出现明显向低角度偏移的现象.这可能是由于K+掺入了g-C3N4的平面晶格结构,由于K+半径较大,导致扩大了层间距.图1(b)显示,制备的OH(0.05)-CN和g-C3N4/KOH催化剂的衍射峰强度和位置与g-C3N4催化剂无明显差别.这说明一方面,K+在g-C3N4/KOH和K(x)-CN中的存在形式是不同的;另一方面,图1(a)所示中K(x)-CN发生的晶格扭曲现象不是由于碱处理引起的,而是由于K+的掺杂作用.
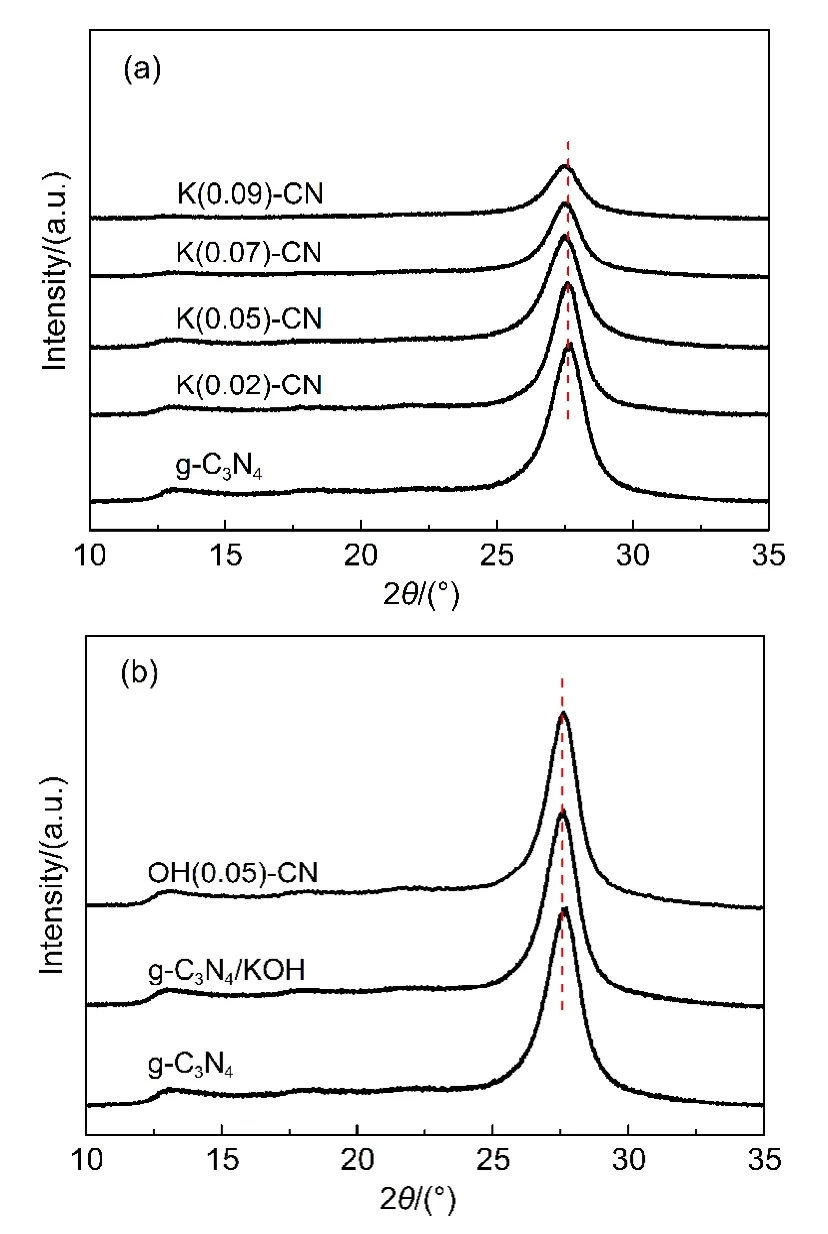
图1 g-C3N4,K(x)-CN,OH(0.05)-CN和g-C3N4/KOH的XRD图谱Fig.1 XRD patterns of g-C3N4,K(x)-CN, OH(0.05)-CN,and g-C3N4/KOH
3.2 N2吸附
图2为g-C3N4和K(0.05)-CN的N2吸附-脱附等温线.可以看出,两个催化剂都呈现出典型的IV型等温线,表明两者均具有介孔结构.g-C3N4、K(0.02)-CN、K(0.05)-CN、K(0.07)-CN和K(0.09)-CN样品的比表面积(SBET)分别为8.9、18.8、26.9、29.2和30.8 m2· g-1.可以看出,K+掺杂后催化剂的SBET显著提高.这可能是由于K+掺杂抑制了g-C3N4晶粒的生长,导致生成了更多的g-C3N4小晶粒.这些g-C3N4小晶粒相互堆积,形成了更多的次级孔.催化剂比表面积的提高可以促进反应物的吸附及产物的扩散,因此有利于催化性能的改善.
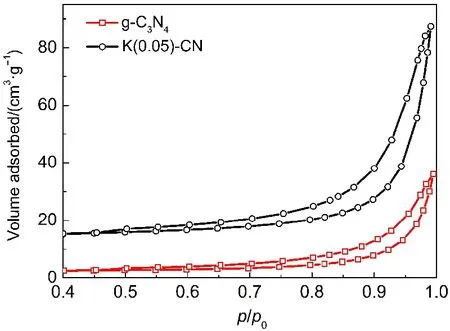
图2 g-C3N4和K(0.05)-CN的N2吸附-脱附等温线Fig.2 N2adsorption-desorption isotherms of g-C3N4and K(0.05)-CN
3.3 UV-Vis表征
图3为制备催化剂的UV-Vis谱图.图3(a)显示, g-C3N4的吸收边界为460 nm,利用公式Eg=1240/λg(Eg为禁带宽度,λg为吸收波长阈值)计算出其带隙能为2.65 eV.K(x)-CN系列催化剂表现出明显的吸收边界红移的现象.K(x)-CN系列催化剂的颜色如图3 (a)中所示,随着K+含量的增加而逐渐加深.根据公式计算得出,K(0.02)-CN、K(0.05)-CN、K(0.07)-CN和K(0.09)-CN的带隙能分别为2.60、2.57、2.55和2.52 eV.这说明K+含量对制备的g-C3N4催化剂的光学性质及能带结构有显著影响.Ma等14利用第一性原理计算了P掺杂g-C3N4催化剂的电子结构.他们发现一个独立的P 3p轨道存在于g-C3N4的导带底端的下方.K+与P3-有相似的电子结构,因此K+掺杂后,也可能有相应的掺杂剂轨道存在于带隙之中,或掺杂剂轨道与g-C3N4的原有分子轨道发生了轨道杂化,使g-C3N4的价带与导带位置发生了改变,因此表现出带隙能的变化.图3(b)显示,g-C3N4、OH(0.05)-CN和g-C3N4/KOH的UV-Vis图谱没有明显差异.此结果再次说明,一方面,K+在g-C3N4/KOH和K(x)-CN中的存在形式是不同的;另一方面,光学性质及能带结构的变化不是由于碱处理引起的,而是由于K+的掺杂作用.

图3 g-C3N4和K(x)-CN(a)及g-C3N4,OH(0.05)-CN和g-C3N4/KOH(b)的UV-Vis漫反射图谱Fig.3 UV-Vis diffuse reflection spectra of g-C3N4and K(x)-CN(a);g-C3N4,OH(0.05)-CN,and g-C3N4/KOH(b)
3.4 XPS结果
X射线光电子能谱是表征元素在催化剂表面的状态的有效手段.图4为制备催化剂的N 1s,C 1s和K 2p能级的XPS图谱以及价带(VB)XPS图谱.如图4(a)所示,g-C3N4的N 1s能级可分为三个峰,分别位于398.2、399.3和400.3 eV处.其中,398.2 eV的峰归属为sp2杂化的N原子(C―N=C),399.3 eV附近峰应归属为连接环状结构的N原子(N―(C)3,括号外的数字代表连接的原子个数,下同)或者层状结构边缘的氨基中的N原子((C)2―N―H),400.3 eV处的峰则归属为芳香环中连接三个C原子的N原子.15图4 (b)中g-C3N4的C 1s图谱可分为三个峰,其中284.6 eV处的峰归属为环状结构中sp2杂化的C原子(N―C=N),285.8 eV的峰归属为sp3杂化的C原子(C―(N)3),287.9 eV处的峰则归属为石墨型结构中C―N键中的C原子.16,17与g-C3N4相比,K(0.05)-CN催化剂样品中N 1s轨道的出峰位置向低结合能方向发生明显偏移,而C 1s轨道的出峰位置却未发现此现象(图4(a,b)).这可能是由于N元素有较高的电负性,与掺杂的K形成了较强的相互作用.K元素上的电子转移至N元素,导致N元素电子密度提高,原子核对核外电子的束缚能力降低,因此结合能降低.
如图4(c)的K 2p轨道所示,g-C3N4/KOH的结合能位于292.7 eV,此峰归属于K―O键.18,19对于K(0.05)-CN催化剂,K 2p轨道的出峰位置向低结合能方向发生明显偏移(约0.2 eV).此外,根据XPS相关数据计算得出,K(0.05)-CN催化剂中K含量为1.46%(质量分数,下同),与ICP测试结果接近(1.35%).而对于g-C3N4/KOH,XPS计算结果为K含量3.3%,远远高于ICP的测试结果(1.39%).这可能是由于K物种在两个催化剂中不同的存在形式导致的.在g-C3N4/KOH中,K物种主要存在于表面.而对于K(0.05)-CN,K物种在缩聚过程中以K―N键的形式掺入了g-C3N4晶格,因此均匀地分散在了K(0.05)-CN的体相中.而且,由于N的电负性比O弱,K在K―N键中的电子密度要高于在K―O键中的电子密度,因此导致结合能的差异.此外,K离子的半径明显大于C和N的半径.因此在此催化剂中, K不可能取代C或N元素发生取代掺杂.然而如图4 (c)中插图所示,g-C3N4的结构单元中晶格间隙的最大平面距离约为0.71 nm,14完全能容纳K离子.因此可能的掺杂方式为间隙掺杂,具体掺杂位置如图4 (c)中插图所示.XPS结果还检测出少量的O元素,约为2.4%.因此K离子的电荷可能被少量的O平衡.图4(d)为g-C3N4和K(0.05)-CN的VB XPS图谱.与g-C3N4相比,K(0.05)-CN的价带位置发生了明显的位移,约为0.48 eV.g-C3N4和K(0.05)-CN的价带电势分别为+1.56和+2.04 eV.结合UV-Vis结果,g-C3N4和K(0.05)-CN的导带电势分别为-1.09和-0.53 eV.众所周知,g-C3N4中N原子的孤对电子对电子密度分布有显著影响,进而影响g-C3N4的电子结构.20K+掺杂改变了N原子的电子密度,因此对g-C3N4的电子结构及能带位置产生了影响.类似的方法计算出,K(0.02)-CN,K(0.07)-CN和K(0.09)-CN的价带和导带电势分别为+1.78和-0.82 eV,+2.13和-0.42 eV,+2.21和-0.31 eV.此结果说明K+掺杂量对g-C3N4能带位置有显著影响.这种可调变的能级位置有利于与多种半导体形成异质结催化剂,可以满足不同应用的需求.
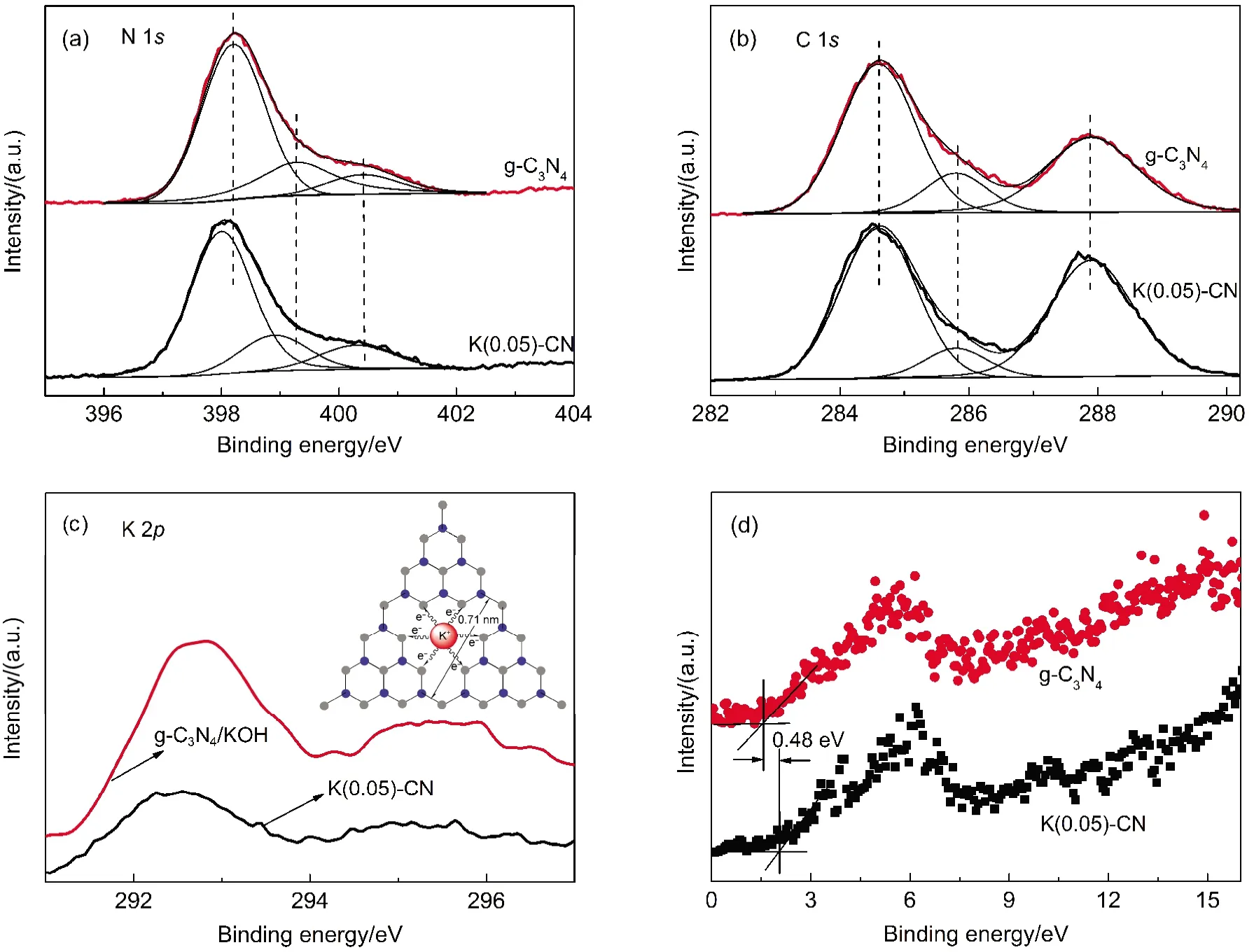
图4 制备催化剂的N 1s(a),C 1s(b)和K 2p(c)能级的XPS图谱以及价带(VB)XPS(d)图谱Fig.4 XPS spectra of as-prepared catalysts in the region of N 1s(a),C 1s(b),K 2p(c),and valence band(VB)XPS(d)
3.5 PL图谱结果
光生电荷的分离-复合对催化剂的性能十分重要,电子-空穴对的高分离效率可以保证光催化反应的有效进行.21图5为制备催化剂的PL图谱,激发光源波长为380 nm.g-C3N4在460 nm附近有很强的荧光发射峰,与UV-Vis谱图中g-C3N4的吸收边界一致.22K(x)-CN系列样品的荧光光谱谱图形状与g-C3N4基本一致,然而强度发生明显的猝灭现象,并且随着K+含量的增加,K(x)-CN样品的PL信号强度逐渐减弱.此结果说明K+掺杂后催化剂的电子-空穴分离效率显著提高.g-C3N4/KOH和OH(0.05)-CN的PL光谱谱图与g-C3N4相比没有明显区别,再次证明了一方面,K+在g-C3N4/KOH和K(x)-CN中的存在形式是不同的;另一方面,电子-空穴分离效率的提高不是由于碱处理引起的,而是由于K+的掺杂作用.

图5 制备催化剂的PL发射图谱Fig.5 Photoluminescence(PL)emission spectra of as-prepared catalysts
3.6 光催化活性评价
g-C3N4和K(x)-CN系列催化剂在可见光下对罗丹明B的降解反应结果如图6(a)所示.光照之前,K(x)-CN系列催化剂对罗丹明B的吸附能力明显强于g-C3N4.这可能是由于K(x)-CN系列催化剂具有较大比表面积导致的.光照后,g-C3N4在120 min内对RhB的降解率为18%.K+掺杂后,K(0.02)-CN、K(0.05)-CN、K(0.07)-CN和K(0.09)-CN在120 min内的降解率分别提高到57%、70.6%、69%和32%.这可能是由于K+掺杂后提高了催化剂的比表面积,降低了带隙能,并且有效抑制了光生电子-空穴的复合.K(0.05)-CN表现出最佳的活性,当K+含量大于0.05 mol·L-1时,催化剂活性显著降低,说明K+含量对催化剂光催化性能有显著影响.理论上讲,g-C3N4的导带(CB)和VB的能级分别位于-1.12和+1.57 V,·OH/OH-和的氧化还原电位分别为+1.99 V和-0.33 V.23,24g-C3N4的CB比的氧化还原电位更负,因此导带电子可以将O2还原成然而g-C3N4的VB电位高于·OH/OH-的氧化还原电位,价带空穴(h+VB)不能将OH-氧化为·OH,因此反应体系的活性物种应该是对于K(0.05)-CN体系,其CB和VB的能级位置发生了显著变化(-0.53和+2.04 V),g-C3N4的VB电位低于·OH/OH-的氧化还原电位.因此,K(0.05)-CN体系中的活性物种为和·OH,使其光催化性能显著提高.而K(0.09)-CN体系的CB和VB的能级位置分别位于-0.31和+2.21 V,其CB能级低于的氧化还原电位,因此该体系不能生成物种,因此其光催化活性明显降低.通常情况下,光降解反应遵循一级反应动力学,动力学方程为:-ln(C/C0)=kt,其中C和C0分别代表任意时刻和初始时刻罗丹明B的浓度,由直线的斜率可得到速率常数k.25如图6(a)所示,g-C3N4的速率常数k为0.0017 min-1.K+掺杂后,K(0.02)-CN、K(0.05)-CN、K(0.07)-CN和K(0.09)-CN的速率常数k分别提高到0.0074、0.0110、0.0100和0.0037 min-1. K(0.05)-CN表现出最大的速率常数,是g-C3N4的6.4倍.如图6(b)所示,g-C3N4/KOH和OH(0.05)-CN的光催化性能与g-C3N4相比没有明显区别,进一步证实了上述表征结果所得出的结论.
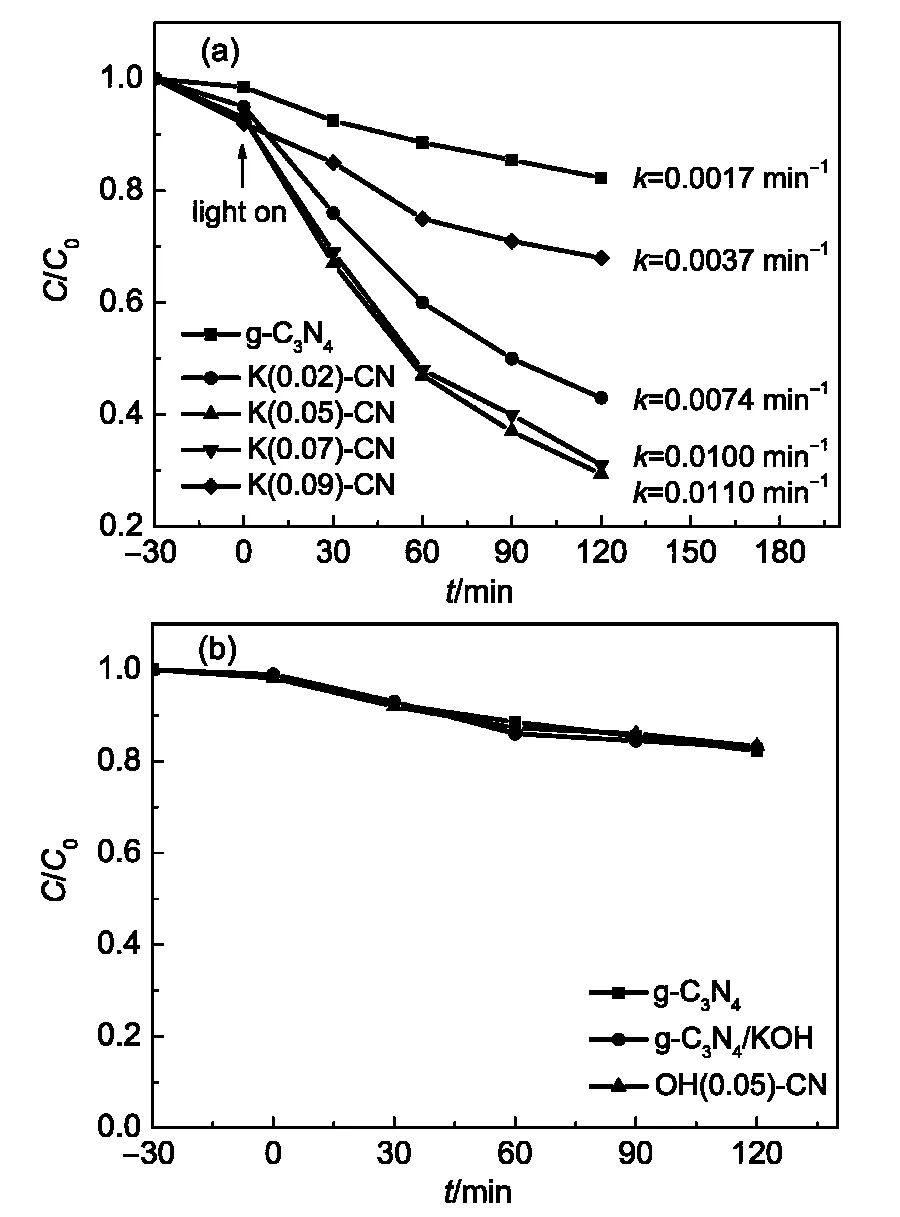
图6 制备催化剂在可见光下的光催化性能Fig.6 Photocatalytic performance of as-prepared catalysts under visible light irradiation
3.7 光催化稳定性评价
K(0.05)-CN的催化稳定性评价结果如图7所示.催化剂在三次循环使用后,活性没有明显的降低,说明K(0.05)-CN具有优越的催化稳定性.此外, ICP结果显示,重复使用三次后,K(0.05)-CN中K的含量为1.33%(质量分数),与新鲜催化剂中K含量相近(1.35%).为了对比,对g-C3N4/KOH催化剂反应后的K含量也做了测试.ICP结果显示,反应后K含量为0.44%,大大低于新鲜催化剂的K含量(1.39%).这可能是由于部分KOH溶于反应溶液中导致的.为了证实这一结论,本实验采用pH计测试了反应后罗丹明B溶液的pH值.结果显示,K(0.05)-CN体系反应液的pH值为7.17,几乎为中性.而g-C3N4/KOH体系反应液的pH值为9.25,呈明显的弱碱性.因此可以得出结论,制备的K(x)-CN系列催化剂在结构上和催化性能上都具有优越的稳定性.
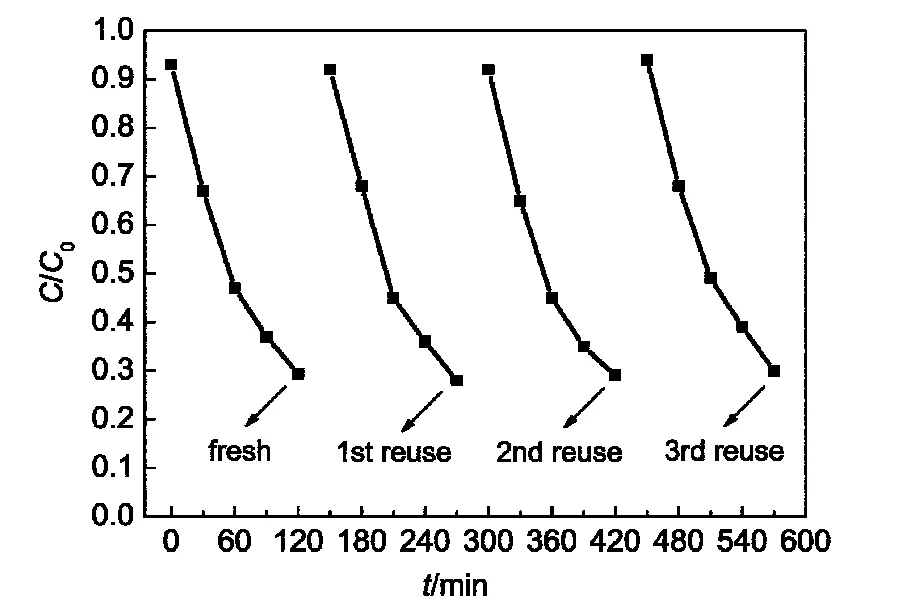
图7 K(0.05)-CN催化剂光催化稳定性Fig.7 Photocatalytic stability of K(0.05)-CN catalyst
4 结论
以双氰胺和氢氧化钾为原料制备了能带可控的钾离子掺杂g-C3N4光催化剂.钾离子的引入抑制了氮化碳晶粒的生长,提高了氮化碳的比表面积及对可见光的吸收,降低了光生电子-空穴对的复合几率.钾离子含量对氮化碳催化剂的价带及导带位置有显著影响.钾离子掺杂后,g-C3N4催化剂在可见光下对染料罗丹明B的降解性能显著提高.K(0.05)-CN表现出最大的速率常数,是g-C3N4的6.4倍. K(x)-CN系列催化剂在结构上和催化性能上都具有优越的稳定性.不仅如此,K(x)-CN系列催化剂具有可调变的能带结构,能与具有不同能级位置的多种半导体形成异质结催化剂,可以满足不同应用的需求.
(1) Zhang,J.S.;Zhang,G.G.;Chen,X.F.;Lin,S.;Möhlmann,L.; Lipner,G.;Antonietti,M.;Blechert,S.;Wang,X.C.Angew. Chem.Int.Edit.2012,51,3183.doi:10.1002/anie.v51.13
(2) Bu,Y.Y.;Chen,Z.Y.;Li,W.B.Appl.Catal.B:Environ.2014,144,622.doi:10.1016/j.apcatb.2013.07.066
(3) Xu,J.;Wu,H.T.;Wang,X.;Xue,B.;Li,Y.X.;Cao,Y.Phys. Chem.Chem.Phys.2013,15,4510.doi:10.1039/c3cp44402c
(4) Sridharan,K.;Jang,E.;Park,T.J.Appl.Catal.B:Environ.2013,142-143,718.
(5) Niu,P.;Zhang,L.;Liu,G.;Cheng,H.Adv.Funct.Mater.2012,22,4763.doi:10.1002/adfm.v22.22
(6) Salinas,D.;Araya,P.;Guerrero,S.Appl.Catal.B:Environ.2012,117-118,260.
(7) Chu,H.;Yang,L.J.;Zhang,Q.H.;Wang,Y.J.Catal.2006,241,225.doi:10.1016/j.jcat.2006.04.028
(8) Pekridis,G.;Kaklidis,N.;Konsolakis,M.;Athanasiou,C.; Yentekakis,I.V.;Marnellos,G.E.Solid State Ionics2011,192, 653.doi:10.1016/j.ssi.2010.03.024
(9) Qu,Z.P.;Bu,Y.B.;Qin,Y.;Wang,Y.;Fu,Q.Chem.Eng.J.2012,209,163.doi:10.1016/j.cej.2012.07.138
(10) Grzechulska,J.;Hamerski,M.;Morawski,A.W.Water Res.2000,34,1638.doi:10.1016/S0043-1354(99)00275-4
(11) Chen,L.C.;Huang,M.;Tsai,F.R.J.Mol.Catal.A:Chem.2007,265,133.doi:10.1016/j.molcata.2006.10.011
(12) Bojdys,M.J.;Müller,J.O.;Antonietti,M.;Thomas,A.Chem. Eur.J.2008,14,8177.doi:10.1002/chem.v14:27
(13) Wang,Y.;Wang,X.C.;Antonietti,M.Angew.Chem.Int.Edit.2012,51,68.doi:10.1002/anie.201101182
(14) Ma,X.G.;Lv,Y.H.;Xu,J.;Liu,Y.F.;Zhang,R.Q.;Zhu,Y.F.J.Phys.Chem.C2012,116,23485.doi:10.1021/jp308334x
(15) Zhang,Y.W.;Liu,J.H.;Wu,G.;Chen,W.Nanoscale2012,4, 5300.doi:10.1039/c2nr30948c
(16) Khabashesku,V.N.;Zimmerman,J.L.;Margrave,J.L.Chem. Mater.2000,12,3264.doi:10.1021/cm000328r
(17) Lei,W.;Portehault,D.;Dimova,R.;Antoniettit,M.J.Am. Chem.Soc.2011,133,7121.doi:10.1021/ja200838c
(18) Miyakoshi,A.;Ueno,A.;Ichikawa,M.Appl.Catal.A:Gen.2001,219,249.doi:10.1016/S0926-860X(01)00697-4
(19) Muhler,M.;Schlogl,R.;Ertl,G.J.Catal.1992,138,413.doi: 10.1016/0021-9517(92)90295-S
(20) Dong,G.P.;Zhang,Y.H.;Pan,Q.W.;Qiu,J.R.J.Photochem. Photobiol.C:Photochem.Rev.2014,20,33.doi:10.1016/j. jphotochemrev.2014.04.002
(21) Jin,R.R.;You,J.G.;Zhang,Q.;Liu,D.;Hu,S.Z.;Gui,J.Z.Acta Phys.-Chim.Sin.2014,30,1706. [金瑞瑞,游继光,张倩,刘 丹,胡绍争,桂建舟.物理化学学报,2014,30,1706.] doi:10.3866/PKU.WHXB201406272
(22) Ge,L.;Han,C.Appl.Catal.B:Environ.2012,117-118,268.
(23) Wang,X.C.;Maeda,K.;Thomas,A.;Takanabe,K.;Xin,G.; Domen,K.;Antonietti,M.Nat.Mater.,2009,8,76.doi: 10.1038/nmat2317
(24) Liu,G.;Niu,P.;Yin,L.C.;Cheng,H.M.J.Am.Chem.Soc.2012,134,9070.doi:10.1021/ja302897b
(25) Li,X.Y.;Wang,D.S.;Cheng,G.X.;Luo,Q.Z.;An,J.;Wang, Y.H.Appl.Catal.B:Environ.2008,81,267.doi:10.1016/j. apcatb.2007.12.022
Effect of K+Doping on the Band Structure and Photocatalytic Performance of Graphitic Carbon Nitride Photocatalysts
ZHANG Jian WANG Yan-Juan HU Shao-Zheng*
(Division of Chemistry,Chemical Engineering and Environment,Liaoning Shihua University, Fushun 113001,Liaoning Province,P.R.China)
Aseries of band gap-tunable K+doped graphitic carbon nitride(g-C3N4)photocatalysts have been prepared using potassium hydrate and melamine as precursors,and fully characterized by X-ray diffraction (XRD),UV-Vis spectroscopy,inductively coupled plasma-atomic emission spectroscopy(ICP-AES),Fourier transform infrared(FTIR)spectroscopy,N2adsorption,photoluminescence(PL),and X-ray photoelectron spectroscopy(XPS).The results of these analyses indicated that the positions of the valence and conduction bands were obviously changed as the concentration of K+increased.The K+ions were found to be embedded in the structural units of the g-C3N4,which inhibited the growth of the graphitic carbon nitride crystals,enhanced the surface area,and increased the separation rate of the photogenerated electrons and holes.The activity of K+doped g-C3N4catalysts was tested towards the photocatalytic degradation of rhodamine B(RhB)under visible light irradiation.The result indicated that the activity improved significantly after K+doping.Furthermore,the K+doped g-C3N4catalysts exhibited outstanding structural and catalytic stability.
Graphitic carbon nitride;Tunable band;K+doping;Stability;Visible light
The project was supported by the Education Department of Liaoning Province,China(L2013150).
辽宁教育厅一般项目(L2013150)资助
O643;O641;O649
10.3866/PKU.WHXB201411201www.whxb.pku.edu.cn
Received:September 24,2014;Revised:November 20,2014;Published on Web:November 20,2014.∗

