Ni,Cr掺杂对LiFePO4/C电化学性能的影响
肖志平,王 英,唐仁衡,肖方明
广东省工业技术研究院(广州有色金属研究院),广东 广州 510650
橄榄石型LiFePO4因其具有成本低廉、安全环保及循环性能好等优点,成为最具实际应用价值的正极材料之一[1],在各种移动电源尤其在动力电池领域有着较好的市场前景.但未经改性处理的LiFePO4本身电导率低,难以满足大电流充放电的实际应用要求[2].针对这一缺陷,目前主要是采取表面包覆碳[3]和颗粒纳米化[4]等途径来改善电极材料的性能,这些方法虽然在一定程度上改善了材料的倍率性能,但对于降低晶格内部价带能隙没有实质性作用;于是有研究者引入金属离子进行取代掺杂,改变能带结构进而提高本征电子导电率,获得了较好的效果[5].然而,作为动力电池材料还必须具有优良的倍率循环稳定性和安全性.对于作为动力电池材料的LiFePO4而言,如仅对其进行颗粒表面包覆或金属离子内部掺杂等单一的改性处理,较难满足高功率型电极材料的要求.
本文作者在材料颗粒表面包覆碳的同时引入了与Fe元素在同一周期的过渡金属Ni,Cr进行晶格内部离子掺杂,着重分析了Ni,Cr掺杂对LiFePO4的物相结构、颗粒形貌及电化学性能的影响.
1 实验部分
1.1 材料制备
按化学计量比Li∶Fe∶(Ni/Cr)∶P=1.0∶0.98∶0.02∶1称取Li2CO3(广州产,AR),FeC2O4·2H2O(深圳产,AR),Ni(OH)2·H2O/Cr2O3(阿拉丁,AR),NH4H2PO4(广州产,AR),同时加入碳含量占理论生成物质量分数8.0%的葡萄糖(广州产,AR)作为碳源,以无水乙醇(广州产,AR)为介质,将上述混合物在Pulverisette 5型行星式球磨机(德国产)中以300r/min的转速球磨(球料比8∶1)3h,将获得的前驱体置于通有高纯氮气的管式炉(合肥产)中,先以5℃/min速率升温到500℃,保温5h,再以10℃/min速率升温到750℃,保温10h,反应完毕后,随炉冷却至室温,轻度研磨,最终得到Ni,Cr掺杂 的 LiFePO4/C 复 合 材 料,分 别 记 为LiFe0.98-Ni0.02PO4/C 和 LiFe0.98Cr0.02PO4/C,碳的添加是为了在颗粒之间形成导电网络.为便于比较,以相同的工艺合成了未掺杂样品LiFePO4/C.
1.2 制备电极和模拟电池组装
将活性物质、聚偏氟乙烯(上海产,电池级),导电碳黑(上海产,电池级)按质量比8∶1∶1混匀,以N-甲基-2-吡咯烷酮(天津产,电池级)为溶剂制成浆料,涂覆于直径14mm,厚25μm的Al箔(深圳产,电池级)圆片上,再在60℃下烘至半干,以20MPa的压力压实,在120℃下真空(-0.1MPa)干燥12 h,即制得约含4.5mg活性物质的工作电极.
以金属锂片(天津产,电池级)为对电极,Celgard 2400膜(美国产)为隔膜,1mol/L LiPF6/EC+DEC(体积比1∶1,广州产,电池级)为电解液,在充满氩气的手套箱内组装CR2032型扣式电池.电池静置24h后进行电性能测试.
1.3 性能测试
用RINT-1100型X射线衍射仪(日本产)对样品物相及结构进行分析,仪器测定条件设置为:CuKα,λ=0.15406nm,管压40kV,管流40mA,扫描速率0.02°/s;用JSM-5910型扫描电子显微镜(日本产)观察样品颗粒形貌.
用2000型电池测试系统(武汉产)进行恒流充放电测试,电压范围为2.5~4.2V;用Parstat 2273电化学工作站(美国产)测试循环伏安曲线,扫描速度0.2mV/s,扫描电压区间2.0~4.5V.
2 结果与讨论
2.1 结构和形貌
样 品 LiFePO4/C,LiFe0.98Ni0.02PO4/C 及LiFe0.98Cr0.02PO4/C的 XRD 谱如图1所示.
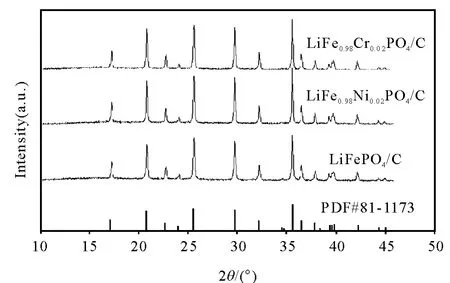
图1 样 品 LiFePO4/C,LiFe0.98Ni0.02PO4/C 和LiFe0.98Cr0.02-PO4/C的 XRD图Fig.1 XRD patterns of samples LiFePO4/C,LiFe0.98Ni0.02-PO4/C and LiFe0.98Cr0.02PO4/C
由图1可见,三种样品均有尖锐的衍射峰,几乎没有其它明显杂质相,与正交晶系的标准卡片(PDF#81-1173)相一致,说明所制备的材料能形成结晶度较高的单相固溶体.合成Ni3+,Cr3+掺杂的LiFe-PO4样品,是按化学计量比来称取原料的,如果掺杂离子未取代晶格内部其它原子的位置,必然会造成某种元素过量而产生第二相,但在图1中并没有检测出杂相,且掺杂后的样品均保持了LiFePO4橄榄石晶型结构,属于Pnma空间群.这证明掺杂样品中掺杂原子进入了晶格内部,并占据了部分格位,但与LiFePO4/C相比,两种掺杂样品的衍射峰的强度有微小的变化,主要是由于橄榄石结构的LiFePO4中的部分格位分别被 Ni2+,Cr3+取代所致[6].此外,没有检测到碳的衍射峰,说明碳以无定型的形式存在.
利用XRD测试的数据,运用三点抛物线法先分别确定6个强峰的峰位,再根据柯亨(M.U.Choen)最小二乘法[7]计算样品的晶胞参数,结果列于表1.
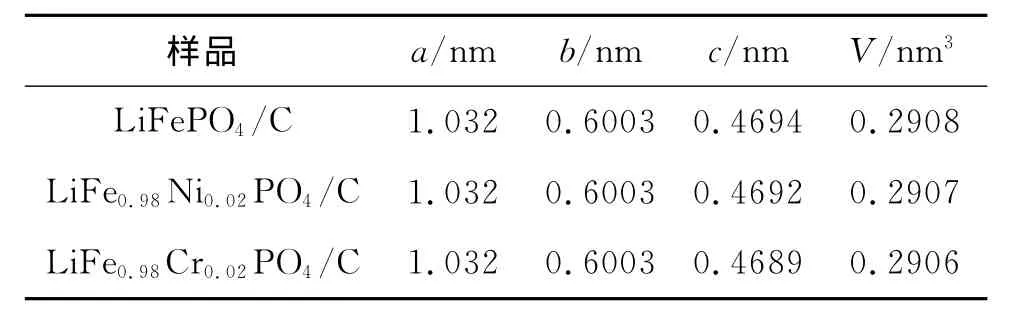
表1 三种LiFePO4样品的晶胞参数Table 1 Crystal cell parameters of three samples of LiFePO4
从表1可以看出,掺杂后晶胞体积略有变小,主要表现在掺杂后晶胞在c轴方向上有不同程度的压缩,而在a,b轴方向三种样品没有明显的区别.由于Ni2+,Cr3+的半径均小于 Fe2+(0.078nm),掺杂Ni2+,Cr3+可以占据LiFePO4中的 M1(Li)位置,或者 M2(Fe)位置,据Chung所提出的掺杂机理[8],上述掺杂离子倾向于占据M1的位置,即可能替代Li+位置,而Li在LiFePO4中是平行于c轴呈线形排列的,所以掺杂后晶胞参数c会缩小.至于掺杂离子在橄榄石结构中的具体占位情况,还有待进一步研究.
样 品 LiFePO4/C,LiFe0.98Ni0.02PO4/C 及LiFe0.98Cr0.02PO4/C的SEM 图见图2.从图2可知,掺杂后样品的颗粒形貌差别不大,但颗粒度均有所下降,平均粒径约为200nm,颗粒间的结合较松散,孔隙率增加,多为表面光滑的球形或类球形颗粒,而未掺杂样品团聚相对严重,颗粒分布不均匀.这说明掺杂Ni2+和Cr3+不仅降低了颗粒度,对产物形貌也产生了积极影响.较小的颗粒通常具有较大的比表面积,这意味着活性物质与电解液的接触面积增大,可加快锂离子在颗粒内部的动力学过程;粒度分布越均匀,电极各部位的电阻、电流密度及反应状态越稳定,有利于材料的循环性能发挥.

图2 样品的SEM图(a)LiFePO4/C;(b)LiFe0.98Ni0.02PO4/C;(c)LiFe0.98Cr0.02PO4/CFig.2 SEM photographs of samples

图3 样品的首次充放电曲线(a)LiFePO4/C;(b)LiFe0.98Ni0.02PO4/C;(c)LiFe0.98Cr0.02PO4/CFig.3 First charge-discharge curves of samples
2.2 电化学性能
样 品 LiFePO4/C,LiFe0.98Ni0.02PO4/C 及LiFe0.98Cr0.02PO4/C 在0.2C 倍率下的首次充放电曲线如图3所示.从图3可知,各样品在充放电过程中均具有宽而平坦的充放电电压平台,表现出明显的两相共存特征,在3.45V附近的平台容量占总容量的90%以上,掺杂后各样品的首次放电比容量比未掺杂的样品有明显增加,分别达到145.5mA·h/g(LiFe0.98Ni0.02PO4/C)和 146.7mA · h/g(LiFe0.98Cr0.02PO4/C),而未掺杂的样品仅为136.7 mA·h/g,掺杂后样品的首次充放电效率也有所提高,分别为99.4%和99.7%.这可能与掺杂后样品的颗粒形貌有关,细小而均匀的颗粒有利于缩短Li+在嵌脱过程中的扩散路径,参与电化学反应的活性物质利用得更为充分,不可逆容量损失降低.
样 品 LiFePO4/C,LiFe0.98Ni0.02PO4/C 及LiFe0.98Cr0.02PO4/C以0.2C 倍率循环50次,循环性能结果见图4.从图4可知,与未掺杂样品相比,掺杂 样 品 的 循 环 性 能 得 到 了 改 善,LiFe0.98Ni0.02-PO4/C和LiFe0.98Cr0.02PO4/C在第50次循环时,容量保持率分别为98%和99.7%,而未掺杂样品仅为95.8%.电极材料良好的循环性能除与LiFePO4本身骨架结构稳定及良好的结晶度有关外,颗粒度和材料导电性也是影响容量衰减的重要因素.细小颗粒往往具有较大的比表面积,比表面积的增加可以扩展电解液与电极材料颗粒的接触范围,这样,在短时间内将有更多的锂离子同时参与两相界面反应,从而降低电极极化;更重要的是,Ni2+,Cr3+部分取代Fe2+之后在材料内部将产生缺陷,缺陷的产生导致材料的电子结构,包括带隙、半导体类型、杂质带的产生及共价性等发生明显变化,对材料的导电率起到实质性的改善.在Fe位掺杂少量Ni2+后,系统的能量低于掺杂前,说明掺杂后体系更加稳定,材料的充放电循环性能变好[9],图4的结果也印证了这一点,LiFe0.98Cr0.02PO4/C 比 LiFe0.98Ni0.02PO4/C的循环性能优异,这主要是由于掺杂少量Cr之后,Cr的3d4s轨道与Fe的3d4s轨道共同作用,提供电子形成了新的杂质导带,带隙变窄,使电子跃迁变得容易,从而提高了材料的电子导电能力[10],此外,Cr3+取代Fe2+会导致材料内部空穴数量增多,有利于锂离子的快速迁移.
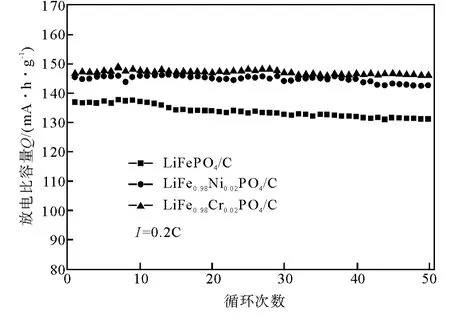
图4 样 品 LiFePO4/C,LiFe0.98Ni0.02PO4/C 和LiFe0.98Cr0.02-PO4/C的循环性能Fig.4 Cycle performance of samples LiFePO4/C,LiFe0.98-Ni0.02PO4/C and LiFe0.98Cr0.02PO4/C
样品 LiFePO4/C,LiFe0.98Ni0.02PO4/C 及LiFe0.98Cr0.02-PO4/C在不同倍率下循环充放电测试的结果见图5.从图5可以看出,在电流条件为1C倍率时,样品LiFePO4/C,LiFe0.98Ni0.02PO4/C 及 LiFe0.98Cr0.02PO4/C均具有较高的首次放电比容量,它们分别为128.4,134和139.9mA·h/g,三者相差不大.随着放电倍率的增加,掺杂与否倍率容量的差别越来越明显,在2C,5C,10C倍率,未掺杂样品LiFePO4/C的首次放电比容量分别为120.2,109.0,94.9mA·h/g,其中10C容量保持率(10C/1C)仅为1C的73.9%,下降较快,而掺杂样品在各倍率的首次放电比容量下降相对缓慢,样品LiFe0.98Cr0.02PO4/C在2C,5C和10C倍率的首次放电比容量分别为133.9,142.4和116.3 mA·h/g,10C 容 量 保 持 率 可 达 1C 的 82.9%.LiFe0.98Ni0.02PO4/C的 10C 容 量 保 持 率 略 低,为78.3%.同时,我们还发现,掺杂与否,样品的倍率循环稳定性也存在一定的差异,尤其是在高倍率条件下.比如,在10C时,未掺杂样品经过10次循环后放电比容量下降了3.4%,而掺杂样品的容量基本没有衰减.在充放电过程中,Li+和电子不断通过形成新的两相界面维持有效电流,尤其在大电流条件下,如果Li+扩散速率或电子跃迁能力有限,随着两相界面的不断缩小,Li+扩散量或电子传导不足以维持有效电流,充放电将提前停止,这样颗粒内核部分的活性物质不能被充分利用,造成容量损失;其次,Li+在LiFe-PO4中的脱嵌是两相共存反应,但FePO4和LiFePO4几乎均为绝缘相,这给Li+和电子共参与的界面电荷传递带来挑战.因此,为了获得优异的高倍率性能,电极材料不仅应具有较高的离子导电性,还应是电子的良好导体或半导体.在LiFePO4体相晶格中引入Ni2+可以改变Fe2+/Fe3+比例,在禁带中产生新杂质导带,提高电子的跃迁能力,而掺杂Cr3+不仅可以改善材料内部的电子结构,而且能产生晶格缺陷如空穴等增加材料无序化程度,为Li+扩散提供顺畅的通道.此外,掺杂后获得更为细小的颗粒度,缩短锂离子的扩散路径,有利于材料高倍率性能的发挥.

图5 样 品 LiFePO4/C,LiFe0.98Ni0.02PO4/C 和LiFe0.98Cr0.02-PO4/C在不同倍率下的循环性能Fig.5 Cycle performance of samples LiFePO4/C,LiFe0.98-Ni0.02PO4/C and LiFe0.98Cr0.02PO4/C at different rates
为了进一步研究掺杂与否各样品电性能的差别,进行了循环伏安测试,结果见图6.从图6可知,各样品的循环伏安曲线均只有一对明显的氧化还原峰,且对称性较好,它们分别对应着Li+从LiFePO4脱出与嵌入,但掺杂后的峰更为尖锐,说明掺杂加快了电极动力学过程.从图6中还可以看出,未掺杂样品的氧化还原峰的电位差值ΔE=0.169V,而掺杂Ni2+,Cr3+的样品分别减小到0.139,0.128V,极化程度降低,意味着在充放电循环过程中,Li+在掺杂样品电极中脱嵌可逆性更好.这主要与掺杂后获得细小而均匀的颗粒有关,掺杂不仅有利于材料与电解液的充分接触,而且可明显缩短Li+的扩散路径;另一重要原因就是掺杂Ni2+,Cr3+改善了材料内部的电子本征导电率和离子扩散通道.因此,在宏观和微观的共同作用下,使掺杂材料获得了较好的电化学性能.
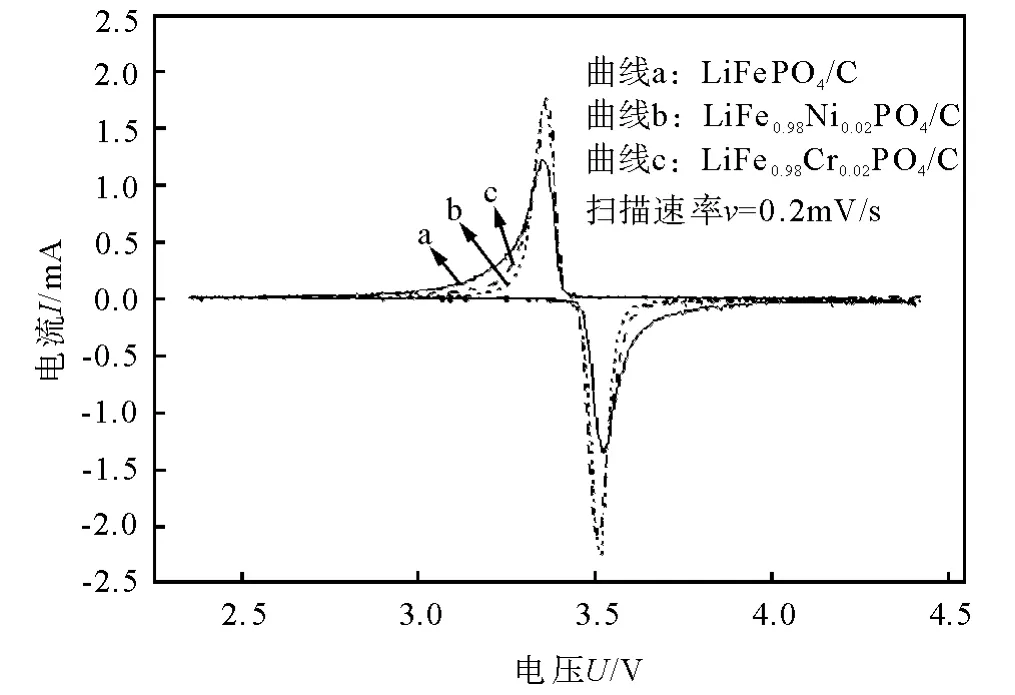
图6 样 品 LiFePO4/C,LiFe0.98Ni0.02PO4/C 和LiFe0.98Cr0.02-PO4/C的循环伏安曲线Fig.6 Cyclic voltammograms of samples LiFePO4/C,LiFe0.98Ni0.02PO4/C and LiFe0.98Cr0.02PO4/C
3 结 论
采用二步固相反应在惰性气氛下合成了橄榄石型LiFe0.98M0.02PO4/C(M=Ni,Cr)复合正极材料.在Fe位进行少量Ni2+,Cr3+掺杂不会引起晶体结构和物相成分的改变,对材料颗粒形貌能起到改善作用,粒径可下降到200nm左右,在一定程度上增强了材料的本征电导率,能获得比LiFePO4/C更好的电性能.循环伏安测试结果表明,掺杂Cr3+比Ni2+具有更高的可逆性,LiFe0.98Cr0.02PO4/C 材料的0.2C首次放电比容量为146.7mA·h·g-1,循环50次的容量保持率为98.1%,10C放电比容量可达116.3mA·h·g-1.
[1]FISHER C A J,HART P V M,ISLAM M S.Lithium battery materials LiMPO4(M=Mn,Fe,Co,and Ni):Insights into defect association,transport mechanisms,and doping behavior[J].Chem Mater,2008,20:5907-5915.
[2]PROSINI P P,LISI M,ZANE D,et al.Determination of the chemical diffusion coefficient of lithium in LiFe-PO4[J].Solid State Ionics,2002,148(1/2):45-51.
[3]LV Y J,SU J,LONG Y F,et al.Effects of ball to powder weight ratio on the performance of LiFePO4/C prepared by wet-milling assisted carbothermal reduction[J].J Power Sources,2014,253:467-473.
[4]HUANG G L,LI W,SUN H Z,et al.Polyvinylpyrrolidone(pvp)assisted synthesized nano-LiFePO4/C composite with enhanced low temperature performance[J].Electrochim Acta,2013,97:92-98.
[5]WANG Y F,ZHANG D,YU X,et al.Mechanoactivation-assisted synthesis and electrochemical characterization of manganese lightly doped LiFePO4[J].J Alloys Compd,2010,492(1/2):675-680.
[6]夏继才,王殿龙,张若昕,等.Ni2+掺杂LiFePO4正极材料电化学性能的影响[J].稀有金属快报,2008,27(11):23-26.
[7]李树棠.晶体X射线衍射学基础[M].北京:冶金工业出版社,1990.
[8]CHUANG S.Y,BLOKING J T,CHIANG Y M.Electronically conductive phosphor-olivines as lithium storage electrodes[J].Nature Mater,2002,2:123-128.
[9]张冬云,张培新,宋申华,等.镍镁掺杂LiFePO4的电子结构[J].中国有色金属学报,2012,22(8):2318-2325.
[10]李学良,陈洁洁.Cr掺杂LiFePO4导电性能的第一原理研究[J].金属功能材料,2011,18(1):44-48.

