柏大蚜蜜露中可培养细菌的季节变化动态
王鸿艳,南小宁,王云果,魏 琮,贺 虹*
(1.西北农林科技大学林学院,陕西杨陵 712100;2.西北农林科技大学植物保护学院,陕西杨陵 712100)
蚜虫是典型的植食性昆虫,是农林业主要的刺吸性害虫之一,它不仅通过吸食树木的汁液影响其生长,而且其排泄的蜜露可诱发煤污病和其他林木病害,对农作物和林木的生长环境造成很大的危害。同时,蚜虫分泌的蜜露中含有丰富的糖类、氨基酸等碳水化合物,是自然界中蚂蚁的重要食物资源 (Buckley,1987;Fischer et al.,2002),也被一些天敌昆虫如瓢虫、小蜂等利用进行补充营养,并成为这些天敌昆虫搜寻寄主的信息物质(陆宴辉等,2005)。Leroy et al.(2011)的研究进一步发现蜜露中特殊的微生物挥发出的信息物质能引诱和增加天敌昆虫对蚜虫的寄生效率。此外,蚜虫体内普遍存在内共生细菌Buchnera和次级内共生菌(secondary symbionts) (Douglas,1998;Haynes et al.,2003;Baumann,2005),这些细菌是否也有可能存在于蜜露中,然后随之传播到其他取食蜜露的昆虫体内?因此,为了了解蚜虫蜜露中微生物的分布情况,作者以柏大蚜Cinara tujafilina (del Guercio)为例,连续收集了7个月的蜜露样品,采用微生物分离培养与16S rRNA 基因片段测序相结合的手段,进行了柏大蚜蜜露中细菌的种类组成和多样性研究,并初步探讨了这些细菌可能的来源和功能。
1 材料与方法
1.1 柏大蚜蜜露的采集
分别于2011年7-10月和2012年4-6月,于陕西杨凌西北农林科技大学校园内侧柏林中,利用高枝剪剪取侧柏枝条,检查其上柏大蚜的分布状况,并将感染有柏大蚜的侧柏枝条带回室内养虫室。首先,利用毛笔先将枝条上的柏大蚜移入灭菌的培养皿中;然后将侧柏枝条先用自来水冲洗,然后再浸于灭菌水中冲洗三遍,尽量清洗干净枝条上的灰尘,晾干水分后将侧柏枝条插入盛有无菌水的三角瓶中,重新将柏大蚜接于枝条上;三角瓶口外围套上20 cm×20 cm的灭菌铝箔纸,使蜜露掉落其上,然后用灭菌的大头针和小枪头吸取蜜露置于1.5 mL 离心管中(预先称重),根据蜜露量连续收集2-3 d,称重后直接稀释用于细菌培养。养虫室提前经过消毒处理,减少室内空气中微生物的影响。
1.2 实验方法
1.2.1 蜜露细菌的分离培养及纯化
每月将收集的0.05 g 新鲜蜜露用500μL 无菌水稀释成原液,并按几何梯度稀释至10-8。取原液、不同梯度稀释液各100μL 涂布接种于LB 培养基平板上,各梯度分别做3个重复,用无菌水涂布3个平板,作为阴性对照。同时每天将3个干净的LB 培养基平板置于收集蚜虫蜜露样品处,暴露于空气中5 min,作为阳性对照以检测实验室空气中存在的细菌。将所有接种和空气对照的平板倒置于恒温培养箱(28℃±1℃)中,培养48 h,选取菌落数在30-300个之间、无蔓延菌落生长的平板进行菌落计数。通过肉眼观察比较菌落形态特征(包括菌落形状、大小、色泽、光泽、湿润度、透明度、隆起状况、边缘状况、表面状况等),初步确定不同的细菌种类后,进行划线培养,分离纯化。使用固体斜面培养基对不同菌种进行划线培养,置于4℃保存。
1.2.2 菌落PCR
分别挑取分离纯化的细菌单菌落,用10μL的无菌水稀释成菌悬液作为模板,以16S rRNA 基因通用引物27F (5'-AGAGTTTGATCMTGGCTCAG-3')和1492R (5'-ATGGGYTACCTTGTTACG ACTT-3')进 行PCR 扩 增 (Weisburg et al.,1991)。PCR 反应体系包括:TaKaRa Taq DNA 聚合酶(5 U/μL)0.5μL,10×PCR 反应液(Mg2+free)2.5μL,dNTP 混合液 (2.5 mM)2μL,MgCl2(25 mM)1.5μL,引物(10μM)各1μL,模板2μL,用灭菌ddH2O 补足25μL。反应程序包括:94℃预变性2 min;94℃变性30 s,55℃退火45 s,72℃延伸1 min,进行25个循环;最后72℃延伸7 min。PCR 产物经1.5%琼脂糖凝胶电泳检测,当达到测序的浓度和纯度后送上海生工生物工程股份有限公司进行双向测序。每种形态的菌落至少挑取2个进行测序分析。
对于不能扩增出PCR 产物以及PCR 产物无法满足测序要求的菌株,通过尝试以下3 种方法进行多次试验至获得可用的PCR 产物:(1)将菌悬液煮沸后作为模板进行PCR 扩增;(2)多次划线培养,挑取单菌落重新制成菌悬液作为模板,进行PCR 扩增;(3)挑取单菌落置于LB 液体培养基中,28℃、220 rpm 振荡培养过夜,菌液经3-5次反复冻融后,用细菌基因组DNA 试剂盒提取DNA,作为模板进行PCR 扩增。扩增体系和反应程序如上所述。
1.3 数据处理及分析
1.3.1 序列的处理及系统发育分析
利用软件ChromasPro 1.5 和Lasergene 7 对原始序列进行拼接和校对,并切除首尾乱序。将校对后的序列在GenBank NCBI 数据库中进行Blast比对并下载同源性最高的序列,整理后的序列在ClustalX 2.1 软件(Larkin et al.,2007)中进行多重比对,比对结果在MEGA 5.05 (Tamura et al.,2011)中检测出最理想的建树模型,然后构建最大似然系统发育树(Maxium Likelihood),并结合Ribosomal Database Project 数据库 (http://rdp.cme.msu.edu/)确定细菌的分类地位,依据细菌97%的序列相似性作为判定种类的标准。本研究分离得到的细菌16S rRNA 基因序列已经全部上传 GenBank,序列号分别为 KC170346-KC170365 (7月份蜜露样品)和KC810822-KC810841 (其他月份)。
1.3.2 细菌群落结构分析
采用α 多样性指数(Hill et al.,2003)分析柏大蚜蜜露中可培养细菌的群落结构。
Shannon-Wiener 指数的计算公式为:

式中:S为一个样品中可培养细菌属水平上的总数;ni为第i个属的细菌菌落数;N为可培养细菌菌落总数。
Simpson 指数的计算公式为:
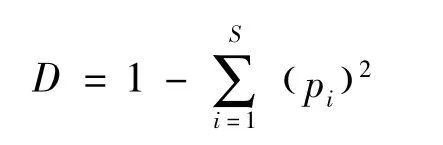
均匀度(Evenness)指数的计算公式为:

Margalef 物种丰富度指数的计算公式为:
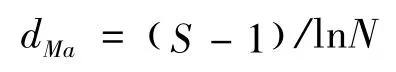
2 结果与分析
2.1 柏大蚜蜜露样品中可培养细菌的数量变化
柏大蚜蜜露样品中可培养细菌数量及变化趋势如图1 所示。采用稀释平板法计算出蜜露样品中可培养细菌数量变化范围为7.9× 102-4.9×105CFU/g,跨3个数量级,变化幅度较大,平均值为9.04×104CFU/g。蜜露样品中的细菌数量在2011年7月达到最大值,8月蜜露样品中的细菌数量大幅降低,9月又出现一个小高峰;2012年4-6月蜜露样品中的细菌数量整体处于较低水平,6月数量最低。

图1 不同月份柏大蚜蜜露样品中可培养细菌的数量变化Fig.1 Quantity change of culturable bacteria in honeydew samples of Cinara tujafilina
2.2 柏大蚜蜜露中可培养细菌的种类组成
从7个月的蜜露样品中,共分离到73个菌落表型差异的菌株,对其16S rRNA 基因序列的NCBI比对结果显示这些菌株隶属于4 门25 属的细菌(表1)。其中,21.9% (16/73)的菌株为芽孢杆菌属Bacillus 细菌,13.7% (10/73)菌株为不动杆菌属Acinetobacter。此外,2011年8月的蜜露样品中细菌种类最多,包括10个属的细菌,2012年5月的蜜露样品中细菌种类最少,仅包括3个属的细菌。其中在柏大蚜蜜露样品中发现的库克菌属Kocuria、壤球菌 属 Agrococcus、微球菌 属Micrococcus 和短小杆菌属Curtobacterium 在空气对照中也检测到。
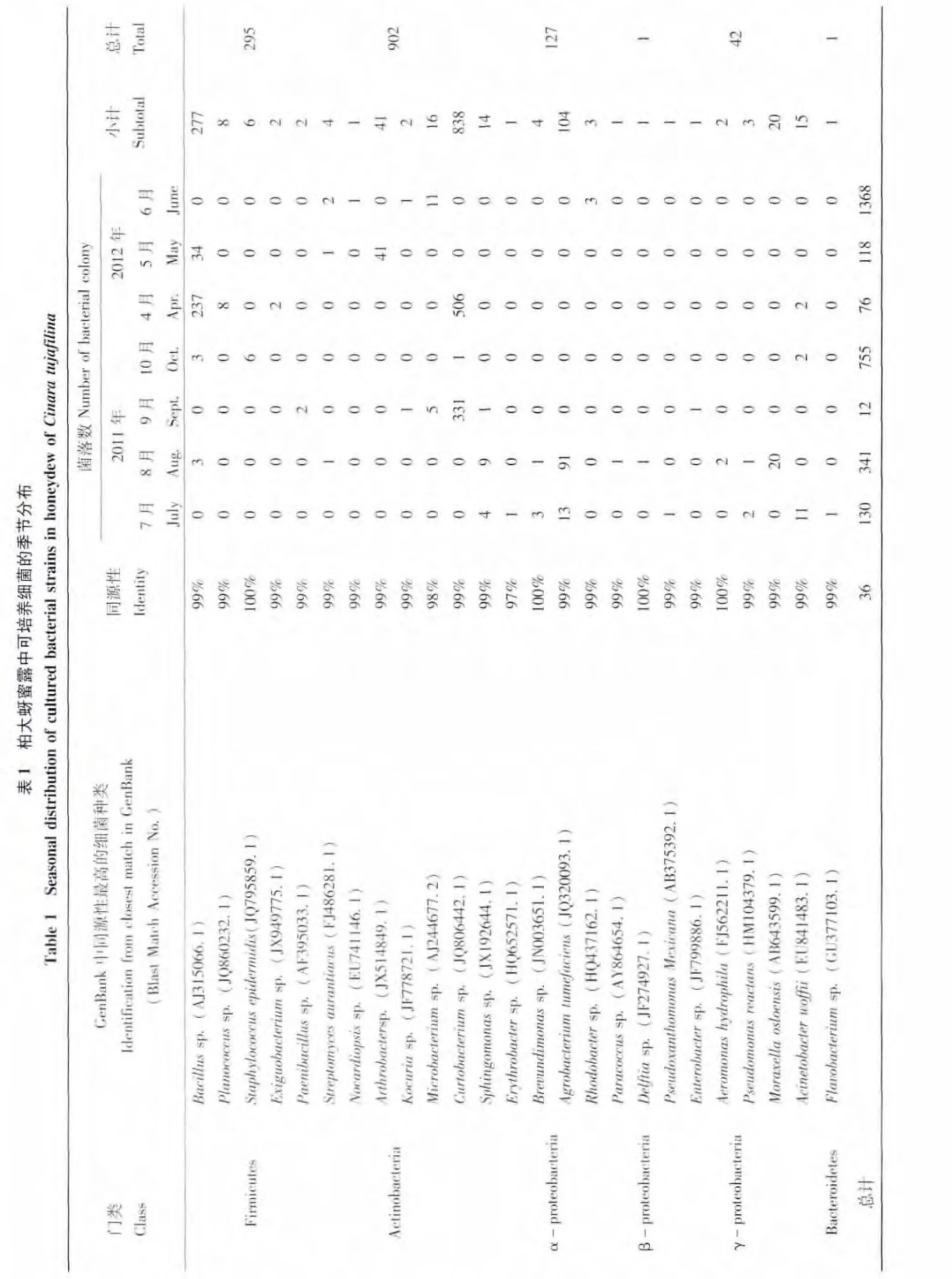
就菌落数量而言,柏大蚜蜜露中可培养细菌的优势菌群随着蜜露采集季节的变化而发生变化(表1)。2011年7月,优势菌群为土壤杆菌Agrobacterium 和不动杆菌Acinetobacter,分别占该月 总菌落数的 36.1% (13/36) 和 30.6%(11/36);8月为土壤杆菌Agrobacterium 和莫拉氏菌Moraxella,分别占70% (91/130)和15.4%(20/130);9月为短小杆菌Curtobacterium,占97.1%(331/341);10月为葡萄球菌Staphylococcus,占50% (6/12);2012年4月,优势菌群为短小杆菌Curtobacterium 和芽孢杆菌Bacillus,分别占67% (506/755)和31.4% (237/755);5月为节细菌Arthrobacter 和芽孢杆菌Bacillus,分别占53.9% (41/76)和44.7%(34/76);6月为细杆菌Microbacterium,占61.1% (11/18)。其中,土壤杆菌Agrobacterium、短小杆菌Curtobacterium 和芽孢杆菌Bacillus的细菌在不同月份的蜜露样品中都表现出明显的数量优势。说明柏大蚜蜜露样品中细菌种类随着时间和外界的条件而发生变化。
就各属细菌在不同蜜露样品中的分布而言,芽孢杆菌属Bacillus 细菌在蜜露样品中最常出现,在4个月的样品中都有发现;其次为链霉菌Streptomyces、短小杆菌Curtobacterium、鞘氨醇单胞菌Sphingomonas 和不动杆菌Acinetobacter 在3个月的样品中都有发现。
2.3 柏大蚜蜜露样品中可培养细菌的多样性分析
不同月份柏大蚜蜜露样品中可培养细菌的多样性指数见表2。Shannon-Wiener 指数(H')大小为7月>10月>6月>8月>5月>4月>9月,Simpson 指数(D)大小为7月>10月>6月>5月>8月>4月>9月,表明2011年7月、10月和6月的蜜露样品中的可培养细菌多样性较高,2012年4月和2011年9月的可培养细菌多样性较低。从Evenness 指数(E)指数可以看出,10月>7月>6月>5月>8月>4月>9月,表明2011年10月蜜露样品中的可培养细菌种类分布最均匀。就Margalef 物种丰富度(dMa)来看,7月>8月>6月>10月>9月>4月>5月,2011年7月蜜露样品中的细菌种群类多,物种最丰富。
总之,由丰富度和细菌种类的不均匀性共同导致多样性的高低起伏变化。2011年夏秋季节蜜露样品中可培养细菌多样性变化的规律性不明显而且波动幅度较大,多样性指数H' 和D的大小分别为:7月>10月>8月>9月。2012年采集的3个样品(4月、5月和6月)中细菌多样性指数波动幅度相对较小,多样性水平随时间的推移而逐渐升高。

表2 柏大蚜蜜露样品中可培养细菌的物种多样性Table 2 Species diversity of bacterial strains in honeydew samples of Cinara tujafilina
2.4 柏大蚜蜜露样品中可培养细菌的系统发育分析
从7个月的蜜露样品中,共分离到73个菌落表型差异的菌株,序列相似性比对结果表明这些菌株分属于25个属的细菌。选取代表菌株的序列和从Genbank 中下载的与其最相似的序列构建了最大似然ML 系统发育树(图3)。从ML 系统树中可以看出,所有菌株构成6个分支。变形菌门Proteobacteria的细菌比重最大,占 71.2%(52/73),又分为3个分支:其中α-变形菌纲Alphaproteobacteria 和 γ-变形菌 纲Gammaproteobacteria 分别占23.3% (17/73),各含6个属,β-变形菌纲Betaproteobacteria 分支中仅包含代尔夫特菌属Delftia的1 株细菌。变形菌门的细菌主要集中在2011年7月和8月收集的蜜露样品中,占变形菌门所有细菌的86.5%(45/52)。厚壁菌门Firmicutes 占27.4%(20/73),包括5个属。放线菌门Actinobacteria 分支占23.3%(17/73),包含6个属。此外,拟杆菌门Bacteroidetes的黄杆菌Flavobacterium 形成一个单独分支。

图3 柏大蚜蜜露样品可培养细菌的系统发育分析Fig.3 Phylogenetic analysis for 16S rRNA sequences of cultured bacteria in honeydew samples of Cinara tujafilina
3 结论与讨论
蚜虫蜜露中细菌数量在不同月份表现出明显差异,这可能与蚜虫及其寄主植物所处的温湿度条件有关(表3)。蜜露样品中细菌数量在2011年7月达到最大值,可能是由于当时气温较高、湿度较大,蚜虫营养条件适合,同时也适合细菌的繁殖;8月高温干旱,来源于植物内生菌的数量可能降低;进入10月,温度降低,不适合于细菌繁殖;2012年6月与2011年8月气候条件相似,高温干旱可能导致植物内生菌的数量降低,从而间接影响了蜜露细菌的数量。
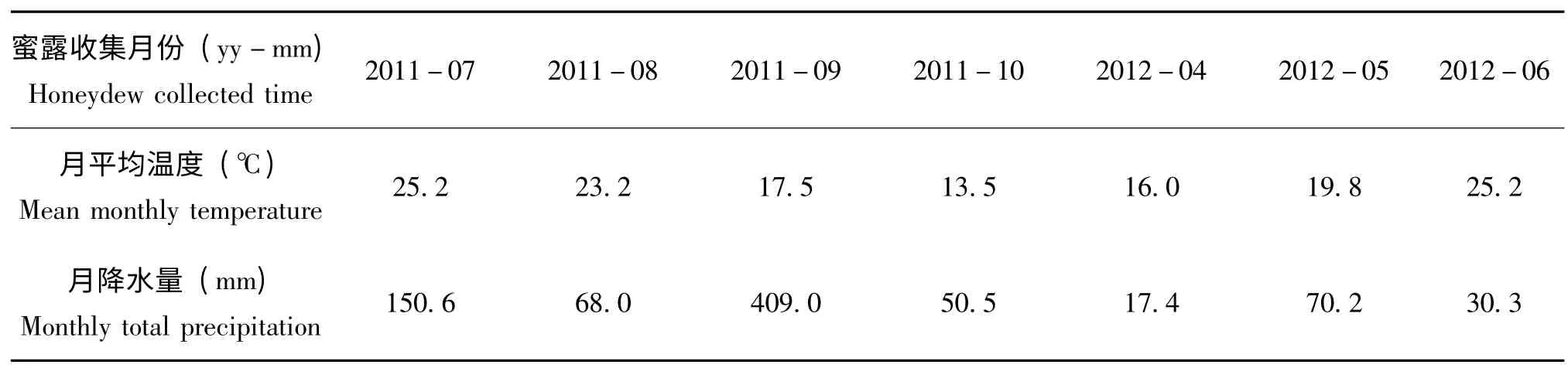
表3 蜜露收集月份的气象统计数据Table 3 Weather statistics of honeydew collected months
柏大蚜蜜露样品中可培养细菌的多样性变化动态也与采样季节密切相关,总体来说,由于2011年夏秋蜜露样品中细菌的多样性变化的规律性不明显而且波动幅度大,多样性指数为7月>10月>8月>9月;在2012年春季4月、5月和6月收集的3个蜜露样品中,细菌多样性指数变化幅度也相对较小,且随时间的推移而逐渐升高。
本研究从2011年7-10月和2012年4-6月共7个月所收集的柏大蚜蜜露样品中共分离出25个属的细菌。对于柏大蚜蜜露细菌种类的组成而言,不同月份收集的蜜露样品中细菌种类、优势菌种、群落结构都有很大差异。
无论在菌落数量、还是菌株数量季节分布来看,芽孢杆菌Bacillus 都是柏大蚜蜜露样品中可培养细菌的优势类群。芽孢杆菌是一类好氧或兼性厌氧生活的革兰氏阳性细菌,营养要求不高,生活能力强,该菌在不利的环境中可以形成芽孢将自己保护起来,复活率高,因而在自然界中广泛分布于土壤、空气等环境(于雅琼等,2007)。此外,芽孢杆菌属的细菌也是马尾松(欧阳革成和张润杰,2005)、鹅掌楸(夏杰等,2009)、银杏(朱士茂,2011)等多种植物的内生菌,并在多种昆虫体内也发现有该属细菌的存在,如桑肩星天牛 Apriona germari (张伟等,2004)、黄粉虫Tenebrio molitor (张丽等,2006)、豆天蛾Clanis bilineata tsingtauica 幼虫(吕飞等,2009)、甘薯粉虱Bemesia tabaci (Ateyyat et al.,2010)、桔二叉蚜Toxoptera aurantii (Sevim et al.,2012)等,但尚未有报道指出芽孢杆菌属的细菌存在于侧柏或柏大蚜体内。芽孢杆菌能够分泌脂肪酶、淀粉酶和蛋白酶等多种微生物酶,因而能够降解甘油三酯、淀粉、蛋白质、木聚糖、果胶等高分子物质,尤其对植物性的碳水化合物具有较强的降解能力(于雅琼等,2007)。柏大蚜取食的是侧柏枝条韧皮部和木质部中的汁液,它会将植物汁液中多余的碳水化合物排出体外而形成蜜露,该属细菌对蜜露中的碳水化合物可能同样具有降解作用。
短小杆菌属Curtobacterium的细菌在2011年9月、10月及2012年4月的柏大蚜蜜露样品中均有发现,并且在9月和4月的蜜露样品中该属细菌在菌落数量上都占有较大优势(表1),其菌落数加起来占所有可培养细菌菌落总数的61.3%(838/1368)。短小杆菌常出现于植物、土壤和油田,其中萎蔫短小杆菌C.flaccumfaciens 是常见的植物致病菌(车秀珠和蔡妙英,2001)。短小杆菌属在柑橘罹病植株(李颜方等,2011)、黄瓜初花期叶片(孙占斌等,2012)中都是优势的内生菌群。在黑粉虫Tenebrio obscurus 和黄粉虫T.molitor(张丽等,2006)、六斑异瓢虫Aiolocaria mirabilis(孟祥杰等,2008)、东亚飞蝗Locusta migratoria manilensis (贺新华等,2010)的肠道中也有发现。本次分离到的短小杆菌属细菌可能源于侧柏或蚜虫体内。
不动杆菌Acinetobacter 在2011年7月、10月及2012年4月的柏大蚜蜜露样品中都有发现,且是7月蜜露样品中的优势菌之一。该属中的乙酸钙不动杆菌 A.calcoaceticus 曾在豌豆蚜Acyythosiphon pisum 蜜露中分离到(Leroy et al.,2011)。蜜露中的其他细菌在自然界中也很普遍,如,根癌土壤杆菌Agrobacterium tumefaciens 被列为十大细菌性植物病原菌之一,它能引起冠瘿病(Mansfield et al.,2012);鞘氨醇单胞菌Sphingomonas 也在自然界中广泛分布,已经从多种水陆环境中得到分离,并在昆虫肠道中也有发现(Wenzel et al.,2002)。总之,这些从蜜露中分离到的细菌是否广泛存在于其他蚜虫蜜露中,对于蜜露的降解以及其他生物尤其是天敌昆虫的影响有待于进一步的研究。
在野外收集蜜露比较困难,因此我们选择在室内进行蜜露收集。在蜜露收集过程中进行实验室消毒、采集工具高压灭菌处理,对于蚜虫所取食的侧柏枝条也用无菌水多次冲洗,尽量排除实验室人为污染。同时,作者认为蚜虫寄主植物微生物对蜜露的组成所构成的“污染”也是蜜露细菌组成的一个合理部分,因为在野外蚜虫蜜露也会受到来源于空气、蚜虫寄主植物及蚜虫体表微生物的污染。此外,也不能排除来源于植物或者空气中的某些细菌在蜜露中大量富集,而对蚜虫天敌产生影响的可能性。Stavrinides 等(2009)证明了豌豆蚜取食被附生细菌侵占的植物时,顺带也摄取到细菌,细菌在其消化系统内寄生和大量繁殖,并通过蚜虫蜜露排出体外,结果导致接种的叶片上附生细菌的数量急剧上升。
在本次试验中我们没有检测到蚜虫中普遍存在的内共生菌,这可能是因为昆虫的内共生菌分离需要更为严格的培养要求。此外,在本实验中为了便于菌落计数和初步了解蜜露中细菌的组成情况,我们仅仅选择了细菌常用的LB 培养基进行了分析,而不同的培养基和不同的培养条件会分离到更多的细菌种类,这都有待于进一步的深入研究。
References)
Ateyyat MA,Shatnawi M,Al-Mazra'aw M.Isolation and identification of culturable forms of bacteria from the sweet potato whitely Bemesia tabaci Genn (Homoptera:Aleyrodidae)in Jordan [J].Turkish Journal of Agriculture and Forestry,2010,34 (3):225-234.
Baumann PL.Biology of bacteriocyte-associated endosymbionts of plant sap-sucking insects[J].Annual Review of Microbio1ogy,2005,59:155-189.
Buckley RC.Interactions involving plants,Homoptera,and ants[J].Annual Review of Ecology Systematics,1987,18:111-113.
Dong XZ,Cai MY.Common Bacterial System Identification Manual[M].Beijing:Science and Technology Press,2001,275.[东秀珠,蔡妙英.常见细菌系统鉴定手册[M].北京:科学技术出版社,2001,275]
Douglas AE.Nutritional interactions in insect-microbial symbioses:aphids and their symbiotic bacteria Buchnera[J].Annual Review of Entomology,1998,43:17-37.
Fischer MK,Vlkl W,Schopf R,et al.Agespecific patterns in honeydew production and honeydew composition in the aphid Metopeurum fuscoviride:implications for ant-attendance [J].Insect Physiology,2002,48 (3):319-326.
Haynes S,Darby AC,Daniell TJ,et al.Diversity of bacteria associated with natural aphid populations [J].Applied and Environmental Microbiology,2003,69 (12):7216-7223.
He XH,Liu YS,Zheng JF.Effects of different feeding plants on the intestinal bacteria of Locusta migratoria manilensis [J].Chinese Journal of Microecology,2010,22 (6):492-497.[贺新华,刘玉升,郑继法.不同食料植物对东亚飞蝗肠道细菌状况的影响[J].中国微生态学杂志,2010,22 (6):492-497]
Hill TCJ,Walsh KA,Harris JA,et al.Using ecological diversity measures with bacterial communities [J].FEMS Microbiology Ecology,2003,43:1-11.
Larkin MA,Blackshields G,Brown NP,et al.Clustal W and Clustal X version 2.0[J].Bioinformatics,2007,23:2947-2948.
Leroy PD,Sabri A,Heuskin S,et al.Microorganisms from aphid honeydew attract and enhance the efficacy of natural enemies[J].Nature communications,2011,DOI:10.1038/ncomms1347:1-7.
Li YF,Yin YP,Wang YX,et al.Isolation of facultative anaerobic entophytic bacterial companioned Ca Las infected citrus tissues and evaluation of dominant bacterial populations [J].Microbiology China,2011,38 (9):1362-1370.[李颜方,殷幼平,王玉玺,等.亚洲韧皮杆菌兼性厌氧型伴生细菌鉴定及优势菌群分析[J].微生物学通报,2011,38 (9):1362-1370]
Lu YH,Shi XL,Zhong CX,et al.Impacts of honeydew on the growth,fecundity and foraging behavior of natural enemies [J].Chinese Bulletin of Entomology,2005,42 (4):379-389.[陆宴辉,史晓利,仲崇翔,等.蜜露对天敌昆虫生长繁殖及搜寻行为的影响[J].昆虫知识,2005,42 (4):379-385]
Lv F,Liu YS,Wang ZP,et al.Pilot study on intestinal bacteria of Clanis bilineata tsingtauica[J].Chinese Journal of Microecology,2009,21 (1):36-39.[吕飞,刘玉升,王振鹏,等.豆天蛾幼虫肠道细菌的初步研究[J].中国微生态学杂志,2009,21(1):36-39]
Mansfield J,Genin S,Magori S,et al.Top 10 plant pathogenic bacteria in molecular plant pathology [J].Molecular Plant Pathology,2012,13:614-629.
Meng XJ,Liu YS,Cui J,et al.Isolation and identification of bacteria from gastrointestinal tract of Aiolocaria mirabilis (motschulsky)[J].Chinese Journal of Microecology,2008,20 (2):120-121,125.[孟祥杰,刘玉升,崔俊,等.六斑异瓢虫成虫肠道细菌分离及鉴定研究[J].中国微生态学杂志,2008,20 (2):120-121,125]
Ouyang GC,Zhang RJ.The occurrence of pine wilt disease caused by Bursaphelenchus xylophilus related to endophyte [J].Acta Scientiarum Naturalium Universitatis Sunyatseni,2005,44 (2):82-85.[欧阳革成,张润杰.植物内生菌Bacillus spp.与松材线虫病的关系研究[J].中山大学学报 (自然科学版),2005,44 (2):82-85]
Sevim E,Celebi O,Sevim A.Determination of the bacterial flora as a microbial control agent of Toxoptera aurantii (Homoptera:Aphididae)[J].Biologia,2012,67 (2):397-404.
Stavrinides J,McCloskey JK,Ochman H.Pea aphid as both host and vector for the phytopathogenic bacterium Pseudomonas syringae[J].Applied and Environmental Microbiology,2009,75 (7):2230-2235.
Sun ZB,Yuan XF,Wang YX et al.Diversity of culturable entophytic bacteria in cucumber leaves at blossoming and fruiting stages[J].Microbiology China,2012,39 (6):764-772.[孙占斌,袁行方,王音娴,等.黄瓜初花期与结瓜期叶片可培养内生细菌多样性研究[J].微生物学通报,2012,39 (6):764-772]
Tamura K,Peterson D,Peterson N,et al.MEGA5:Molecular evolutionary genetics analysis using maximum likelihood,evolutionary distance,and maximum parsimony methods [J].Molecular Biology and Evolution,2011,doi:10.1093/molbev/msr121.
Wenzel M,Schönig I,Berchtold M,et al.Aerobic and facultatively anaerobic cellulolytic bacteria from the gut of the termite Zootermopsis angusticollis [J].Journal of Applied Microbiology,2002,92:32-40.
Xia J,Fang F,Zhao HN,et al.Preliminary study on the isolation and anti-bacterial activity of Liriodendron chinense Endophyte [J].Modern Agricultural Sciences,2009,16 (6):10-11.[夏杰,方芳,赵会娜,等.鹅掌楸内生菌分离纯化及其抗菌活性初步研究[J].现代农业科学,2009,16 (6):10-11]
Yu YQ,Chen HY,Li PL,et al.Isolation,identification and antibiotic susceptibility of Bacillus from different stuffs[J].Food Science,2007,28 (7):324-330.[于雅琼,陈红艳,李平兰,等.不同生境中芽孢杆菌的分离鉴定及药敏性检测[J].食品科学,2007,28 (7):324-330]
Zhang W,He ZB,Deng XP,et al.Variety and distribution of intestinal flora of Apriona germari (Hope)lervae[J].Journal of Southwest Agricultural University (Natural Science),2004,26 (2):169-172.[张伟,何正波,邓新平,等.桑粒肩天牛幼虫肠道菌群的种类及分布[J].西南农业大学学报(自然科学版),2004,26 (2):169-172]
Zhang L,Liu YS,Liu DW,et al.Comparison of bacteria isolated from gastrointestinal tact of Tenebrio obscurus and T.molitor [J].Entomological Journal of East China,2006,15 (1):17-21.[张丽,刘玉升,刘大伟,等.黑粉虫与黄粉虫幼虫肠道细菌的比较[J].华东昆虫学报,2006,15 (1):17-21]
Zhu SM.Isolation and identification of endophytes in Ginkgo biloba L[J].Journal of the Graduates Sun Yat-sen University (Natural sciences,medicine),2011,32 (4):64-74.[朱士茂.银杏内生菌的分离与鉴定[J].中山大学研究生学刊(自然科学、医学版),2011,32 (4):64-74]

