急性等容血液稀释联合不同效应室浓度舒芬太尼靶控输注的安全性及术中血液保护作用
王 庚 何锡强
北京积水潭医院麻醉科,北京 100035
血液稀释使血管内容量中细胞成分相对或绝对减少,从而减少手术失血和输血量[1],是节约用血的技术方法之一。双侧髋关节置换手术由于手术区域血供丰富,无法应用止血带,骨膜及髓腔内无法止血,加上手术部位深、手术时间长,因而术中出血量较多。由于目前血源紧张及传染乙、丙型肝炎、梅毒、艾滋病的可能性存在,该类手术实施血液保护十分重要。舒芬太尼是芬太尼的N-4噻吩基衍生物,脂溶性高,与阿片受体亲和力强,具有起效快、心血管系统功能稳定、无组胺释放、呼吸抑制轻等优点[2],在骨科手术麻醉维持中广泛应用。
本次研究的目的为观察七氟烷与不同效应室浓度(Cet)舒芬太尼靶控输注(TCI)维持麻醉时,急性等容血液稀释(ANH)是否会对血流动力学指标及脑电双谱指数(BIS)值产生影响,以及ANH是否可以减少术中出血及异体输血的发生。
1 资料与方法
1.1 一般资料
本次研究为随机、对照研究,经北京积水潭医院医学伦理委员会通过。选取2011年3月~2013年1月择期于北京积水潭医院全麻下行双侧髋关节置换手术患者84例。入选标准:预计术中失血量>800 mL,美国麻醉医师协会(ASA)健康分级Ⅰ级或Ⅱ级,年龄18~65 岁,体重指数(BMI)为 16~32 kg/m2。所有患者心肺功能均未见异常,无神经、精神疾病史,无长期应用镇静催眠类药物及酗酒史。排除标准:妊娠或哺乳,血细胞比容(HCT)<33%,有器官器质性病变,低蛋白血症,凝血机制障碍。所有患者术前均知情并签署同意书。患者随机分为4组,每组各21例,分别给予TCI舒芬太尼至 Cet为 0.2 ng/mL (S1组),0.4 ng/mL(S2组及 C 组),0.6 ng/mL(S3组)。
所有患者均完成研究设计。各组患者性别比例、年龄、身高、体重、ASA分级及术前HCT、基础心率(HR)、基础动脉血压(MAP)、基础 BIS值等基础资料比较,差异均无统计学意义(P>0.05),具有可比性。见表 1、2。
1.2 麻醉方法
1.2.1 麻醉准备 所有患者均于麻醉前30 min肌注阿托品0.5 mg。入室后开放上肢静脉通路,输注乳酸钠林格液500 mL补充术前禁食水损失量。连接Datex Ohmeda System 5(Datex公司,芬兰)多功能监测系统连续监测心电图、血压、脉搏血氧饱和度、呼气末二氧化碳分压(PetCO2)。局部浸润麻醉下行与静脉通路不同侧上肢桡动脉穿刺置管,监测MAP。若预计术中失血量>全身总血容量(EBV)的25%,行颈内静脉穿刺置入双腔中心静脉导管,以连续监测中心静脉压力(CVP)及补液需要。Aspect A-2000系统连接标准四电极传感(Aspect Medical Systems公司,美国)监测BIS。
表1 各组患者一般情况比较(±s)
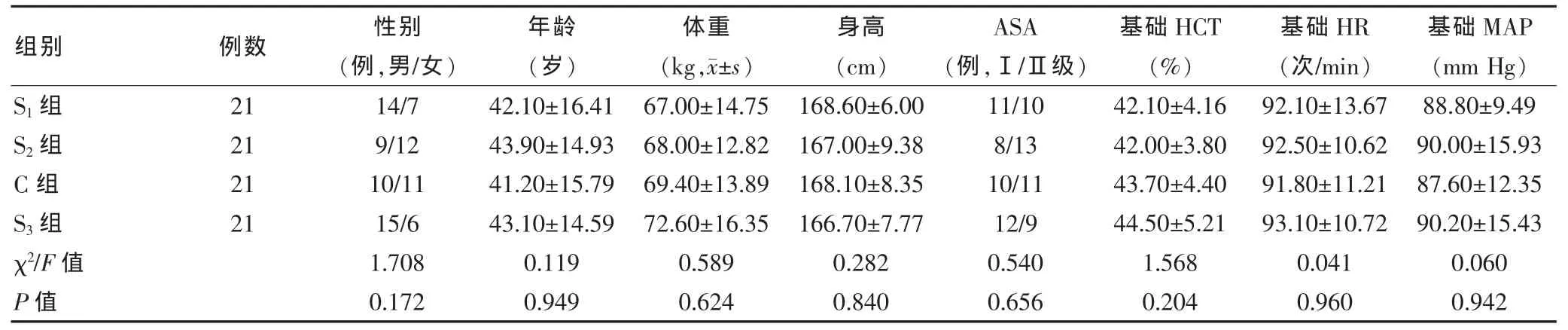
表1 各组患者一般情况比较(±s)
注:HCT:红细胞压积;ASA:美国麻醉医师协会;HR:心率;MAP:动脉血压;1 mm Hg=0.133 kPa;基础HCT为入院时检查所得;基础HR为病房测量HR的平均数、手术日晨起HR及入室时HR 3次数据平均值;基础MAP为病房测量MAP的平均数、手术日晨起MAP及入室时MAP 3次数据平均值
组别 例数 性别(例,男/女)年龄(岁)体重(kg,±s)身高(cm)ASA(例,Ⅰ/Ⅱ级)基础HCT(%)基础HR(次/min)基础MAP(mm Hg)S1组S2组C组S3组χ2/F值P值21 21 21 21 14/7 9/12 10/11 15/6 1.708 0.172 42.10±16.41 43.90±14.93 41.20±15.79 43.10±14.59 67.00±14.75 68.00±12.82 69.40±13.89 72.60±16.35 168.60±6.00 167.00±9.38 168.10±8.35 166.70±7.77 42.10±4.16 42.00±3.80 43.70±4.40 44.50±5.21 92.10±13.67 92.50±10.62 91.80±11.21 93.10±10.72 88.80±9.49 90.00±15.93 87.60±12.35 90.20±15.43 0.119 0.949 0.589 0.624 0.282 0.840 11/10 8/13 10/11 12/9 0.540 0.656 1.568 0.204 0.041 0.960 0.060 0.942
1.2.2 麻醉诱导 TCI丙泊酚 (规格500 mg/50 mL,Corden Pharma S.P.A.,Caponago,意大利)使用 Graseby3500(Graseby公司,英国)注射泵,内置 Mash药代动力学模型,预设Cet为3 μg/mL,待患者意识丧失,BIS值降至75以下时,静脉注射维库溴铵0.7 mg/kg,手控辅助通气,并吸入流量为6 L/min的纯氧,观察BIS值变化。待丙泊酚达预设Cet后,开启靶控输注泵(思路高,北京,内置Bovil药代动力学模型),TCI舒芬太尼 (规格 50 μg/mL,Impfstoffwerk Dessau-TornauGmbh公司,德国,用生理盐水稀释至 1 μg/mL),使四组患者舒芬太尼Cet分别至预定值,TCI过程中继续手控辅助通气,吸入6 L/min纯氧。当舒芬太尼达目标Cet时停止泵注丙泊酚,即刻进行气管插管。气管插管后连接Ohmeda-Datex型麻醉机 (Datex公司,芬兰)行机械通气,吸入氧气与空气混合气(氧浓度40%),流量2 L/min,调节潮气量和呼吸频率维持PetCO2在 30~40 mm Hg(1 mm Hg=0.133 kPa)。
1.2.3 麻醉维持 开启七氟烷挥发罐,调节呼气末七氟烷浓度,在5 min内达到并维持于1.0×最低肺泡有效浓度(MAC),各组按预设舒芬太尼Cet持续泵注。在给药过程中若出现收缩压(SBP)<80 mm Hg,予扩容或麻黄碱6~12 mg,使SBP维持于80 mm Hg以上;若出现HR<45次/min,予阿托品0.5 mg使HR维持于45次/min以上。手术均于ANH完成后开始,术中按预设舒芬太尼Cet持续泵注;调节七氟烷浓度,使BIS维持于40~60,维持血压低于基础值0~20%,若高于基础值则根据病情使用血管活性药物对症处理。术中根据Aspect A-2000监测系统显示肌电图(EMG)情况追加肌松。
1.3 血液稀释
S1、S2及S3组患者于七氟烷呼气末浓度达到1.0 MAC,且丙泊酚效应室浓度为0后开始ANH,目标HCT为0.28,经桡动脉放血,采血速度由三通控制,20~40 mL/min,采血量按如下公式计算:V=EBV(H0-H1)/H(V:采血量;EBV:全身总血容量,以 70 mL/kg估计;H0: 初始 HCT;H1: 目标 HCT,0.28;H:H0与 H1的均值)[3]。采集血液置于预先含有CPDA-1抗凝剂的血袋中(每100毫升血需14 mL的CPDA-1抗凝剂),血袋置于地板平面,在采血过程中手动摇匀以使血液与抗凝剂充分混合。采血均于40 min内完成。血袋采满后封闭管路,并于室温下置于手术间内。采血同时,以等速率等量输入万汶(Fresenius Kabi公司,德国)。采血过程中,若出现SBP<80 mm Hg,则停止采血,予万汶扩容,必要时予麻黄碱 6~12 mg,维持 SBP>80 mm Hg。所有输入液体均放入恒温箱内加温至37℃备用,监测鼻咽温度并维持体温于35.5℃以上。在ANH过程中禁止体位变化,以避免手术刺激及体位变化对血液循环力学及BIS产生影响。
所有采集自体血及回吸收洗涤后自体血均于手术结束前回输。血液制品输注顺序为自体采血,回吸收洗涤后自体血,而后是异体血。异体输血指征为前两者输完后血气分析检测显示血色素(Hb)≤70 g/L。
C组患者作为对照组术中不进行ANH。
1.4 监测指标
记录入室时及诱导前、TCI舒芬太尼前、舒芬太尼达 Cet时、采血前(T0)、采血 5 min(T1)、10 min(T2)、15 min(T3)、20 min(T4)、25 min(T5)、30 min(T6)、35 min(T7)、40 min(T8)时HR、MAP及BIS值(T0~T8)。 Aspect A-2000监测系统每秒测定并记录1次BIS值,并可自动计算最小时间间隔为1 min内的BIS平均值,T1~T88个时间点的BIS值分别为每5分钟时间间隔内,5次系统自动计算出的1 min内BIS平均值平均数;T0为采血开始前的BIS值。记录入院后、采血前及采血完成后HCT(均为动脉血血气分析显示数据)。记录术中出血量(为回吸收洗涤后自体血量×3)及异体输血情况。
记录术中特殊情况,如失血明显增多、凝血功能障碍、DIC等。记录有无严重低血压、术后恶心、呕吐等不良反应发生。术后随访并记录有无术中知晓。
表2 4组患者丙泊酚及舒芬太尼使用量及给药前后HR、MAP及BIS值比较(±s)
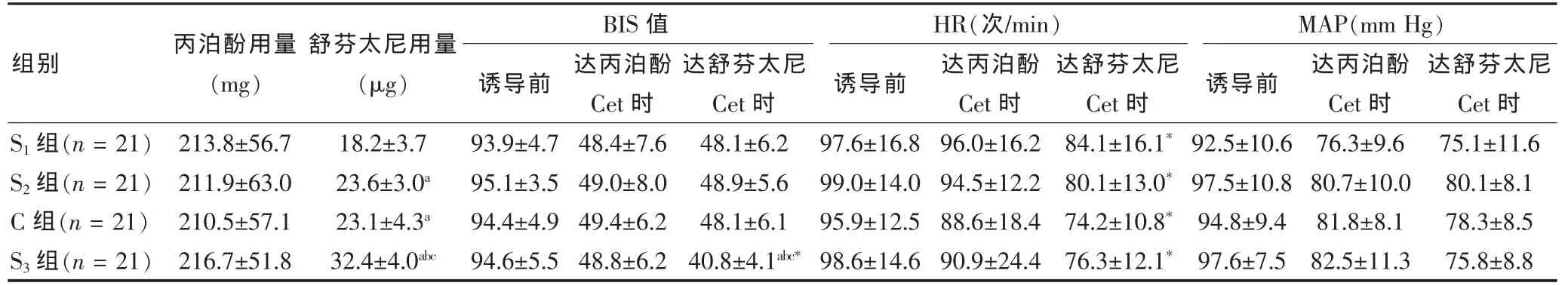
表2 4组患者丙泊酚及舒芬太尼使用量及给药前后HR、MAP及BIS值比较(±s)
注:与 S1组比较,aP < 0.01;与 S2组比较,bP < 0.01;与 C 组比较,cP < 0.01;与组内达丙泊酚 Cet时比较,*P < 0.05;HR:心率;MAP:动脉血压;BIS:脑电双谱指数;1 mm Hg=0.133 kPa
组别 丙泊酚用量(mg)舒芬太尼用量(μg)BIS值诱导前 达丙泊酚Cet时达舒芬太尼Cet时HR(次/min)诱导前 达丙泊酚Cet时达舒芬太尼Cet时MAP(mm Hg)诱导前 达丙泊酚Cet时达舒芬太尼Cet时S1组(n=21)S2组(n=21)C 组(n=21)S3组(n=21)213.8±56.7 211.9±63.0 210.5±57.1 216.7±51.8 18.2±3.7 23.6±3.0a 23.1±4.3a 32.4±4.0abc 93.9±4.7 95.1±3.5 94.4±4.9 94.6±5.5 48.4±7.6 49.0±8.0 49.4±6.2 48.8±6.2 48.1±6.2 48.9±5.6 48.1±6.1 40.8±4.1abc*97.6±16.8 99.0±14.0 95.9±12.5 98.6±14.6 96.0±16.2 94.5±12.2 88.6±18.4 90.9±24.4 84.1±16.1*80.1±13.0*74.2±10.8*76.3±12.1*92.5±10.6 97.5±10.8 94.8±9.4 97.6±7.5 76.3±9.6 80.7±10.0 81.8±8.1 82.5±11.3 75.1±11.6 80.1±8.1 78.3±8.5 75.8±8.8
表3 S1、S2、S3组患者稀释指标及不同稀释时点BIS值比较(±s)
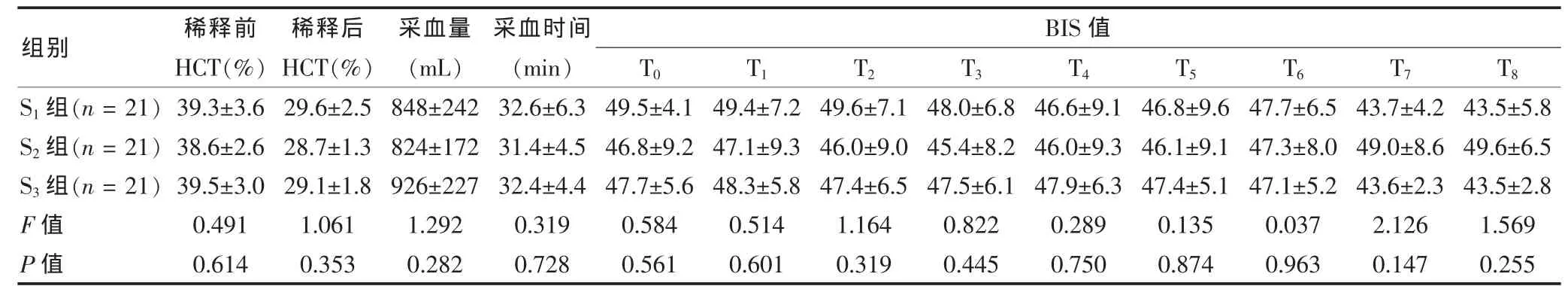
表3 S1、S2、S3组患者稀释指标及不同稀释时点BIS值比较(±s)
注:HCT:红细胞压积;BIS:脑电双谱指数
组别 稀释前HCT(%)稀释后HCT(%)采血量(mL)采血时间(min)BIS值T0 T1 T2 T3 T4 T5 T6 T7 T8 S1组(n=21)S2组(n=21)S3组(n=21)F值P值39.3±3.6 38.6±2.6 39.5±3.0 0.491 0.614 29.6±2.5 28.7±1.3 29.1±1.8 1.061 0.353 848±242 824±172 926±227 1.292 0.282 32.6±6.3 31.4±4.5 32.4±4.4 0.319 0.728 49.5±4.1 46.8±9.2 47.7±5.6 0.584 0.561 49.4±7.2 47.1±9.3 48.3±5.8 0.514 0.601 49.6±7.1 46.0±9.0 47.4±6.5 1.164 0.319 48.0±6.8 45.4±8.2 47.5±6.1 0.822 0.445 46.6±9.1 46.0±9.3 47.9±6.3 0.289 0.750 46.8±9.6 46.1±9.1 47.4±5.1 0.135 0.874 47.7±6.5 47.3±8.0 47.1±5.2 0.037 0.963 43.7±4.2 49.0±8.6 43.6±2.3 2.126 0.147 43.5±5.8 49.6±6.5 43.5±2.8 1.569 0.255
1.5 统计学方法
采用统计软件SPSS 13.0对数据进行分析,计量资料以均数±标准差(±s)表示,多组间比较采用方差分析,两两比较采用LSD-t检验。非正态分布的计量资料用中位数(M)及四分位数(P25,P75)表示,采用秩和检验。计数资料以率表示,采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 各组患者不同给药时间点HR、MAP及BIS值比较
4组患者诱导前HR、MAP、BIS值及达丙泊酚Cet时 (即舒芬太尼给药前)HR、MAP、BIS值差异无统计学意义(P>0.05)。4组患者达舒芬太尼Cet时HR值均较达丙泊酚Cet时显著下降,差异有统计学意义(P<0.05);4组患者舒芬太尼给药前、后MAP差异均无统计学意义(P>0.05),每组患者均未发生舒芬太尼给药后MAP的明显下降。S3组患者达舒芬太尼Cet时BIS值显著低于S1、S2及C组患者,差异有高度统计学意义(P<0.01),且较达丙泊酚Cet时显著降低(P<0.05),而S1、S2及C组患者未发现BIS值的显著变化。见表2。
2.2 S1、S2、S3组患者稀释指标及不同采血时点BIS值比较
S1、S2、S3组患者稀释前 HCT、稀释后 HCT 及采血量、采血时间比较差异无统计学意义(P>0.05);S1、S2、S3组患者不同采血时间点BIS比较差异无统计学意义(P>0.05)。 见表 3。
2.3 S1、S2、S3组患者不同采血时点循环指标及BIS值比较
S1、S2、S3组患者分别进行组内比较,T0~T8时间点其HR、MAP及BIS值比较差异均无统计学意义(P>0.05)。 见表 4。
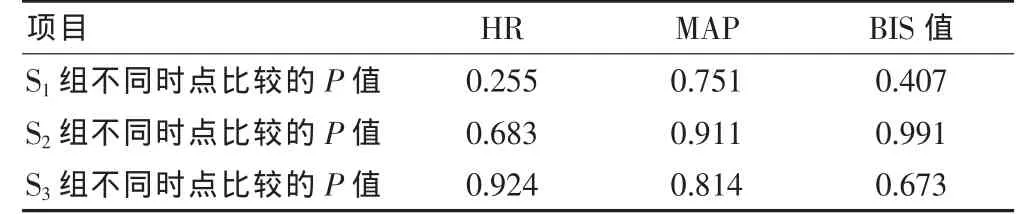
表4 S1、S2、S3组患者组内不同时点HR、MAP及BIS值比较的统计值
2.4 各组患者术中失血量及异体输血情况比较
与S1、S2及S3组患者比较,C组患者术中出血量明显增多(P=0.001);C组患者异体输血量明显多于S1、S2及 S3组患者(P=0.022);但四组比较异体输血比例差异无统计学意义(P=0.085)。 S1、S2及 S3组患者之间出血量、异体输血量及输血比例差异无统计学意义(P > 0.05)。 见表 5。

表5 各组患者术中出血量、输血量及输血比例情况比较[M(P25,P75)]
2.5 不良反应
所有患者术中均无不良反应发生。术后随访无不良事件及术中知晓发生。
3 讨论
BIS是监测麻醉深度非常有效的措施,能直观地反映麻醉深度和大脑皮质功能状态,从而指导临床合理用药,防止术中知晓的发生,同时对于患者的临床转归也有一定意义。Monk等[4]研究发现,在大的非心脏手术中,BIS值<45的累积时间过长,会成为术后一年内死亡率增加的一个独立危险因素。因此BIS监测已成为现代麻醉监测中一个重要的安全性指标。
舒芬太尼是芬太尼家族中效力最强的μ-受体激动剂。许多研究表明,当舒芬太尼和丙泊酚联合应用时,两者之间存在着协同作用[5-7]。但有些学者的研究认为,临床常用剂量的阿片类药物不会对BIS值产生影响[8-9]。本次研究表明,S3组患者达舒芬太尼Cet时BIS值显著低于S1、S2及C组患者,且较舒芬太尼给药前显著下降,而S1及S2、C组患者未发现BIS值的显著降低。
为明确S3组患者的BIS值改变是源于其本身的镇静作用还是由于影响了丙泊酚的药效学特性,笔者在之后的研究中停止丙泊酚TCI,改用七氟烷维持麻醉,观察不同Cet的舒芬太尼维持麻醉是否会导致BIS值的差异。其后进一步进行ANH并观察BIS值,以明确ANH是否会对舒芬太尼的镇静作用产生影响。
以往研究发现,血液稀释对药物的血浆浓度有影响,血浆蛋白浓度随血液稀释而下降,药物的血浆蛋白结合率也会随着血液稀释而下降[10],药效也会发生改变,主要表现为血液稀释后药效加强[11]。但是本次研究发现当七氟烷呼气末浓度相同时,不同Cet舒芬太尼TCI时BIS值差异无统计学意义(P=0.561),同时在血液稀释进程中的不同时点(T1~T8),进行ANH的三组患者比较BIS值变化无统计学意义 (P>0.05)。三组患者进行组内比较发现,每组患者在血液稀释过程中的不同时点BIS值变化均无统计学意义(P>0.05)。由此推论舒芬太尼并不会引起BIS值明显改变,大剂量舒芬太尼与丙泊酚联合应用时会因为协同作用而加强丙泊酚的镇静效能,从而出现BIS值下降。每组患者在稀释过程中,各时点(T1~T8)HR及MAP的变化无统计学意义(P>0.05),因此复合使用七氟烷及舒芬太尼维持麻醉时,ANH不会造成血流动力学不稳定及BIS值的改变。
研究发现无论何种剂量舒芬太尼TCI均会发生HR下降(表2),分析原因为:①抑制交感系统及应激反应,减少儿茶酚胺释放;②兴奋迷走神经减慢HR。而不论何种浓度舒芬太尼均对MAP均无影响。宋永生等[12]的研究也证实舒芬太尼与丙泊酚联合应用更易引起HR下降,因此需加强监护。
与S1、S2及S3组患者比较,C组患者术中出血量及异体输血量明显增多。黎玉辉等[13]对ANH研究进行Meta分析,并对纳入研究进行整体分析及按手术种类或不同血液稀释程度进行亚组分析显示,中度ANH对于骨科大手术可减少术中出血量,这与本次研究中的发现一致。许多研究表明ANH是一项安全有效的血液保护措施[14-15],可减少术中异体输血量。本次研究中四组比较异体输血比例差异无统计学意义(P=0.085),而Meta分析显示ANH能减少异体输血率至少达70%,这可能是由于本次关于双侧全髋置换术的研究中常规应用伤口出血洗涤自体回吸收技术,可以明显减少术中异体输血的比例[13];此外,由于研究的样本量较小,有可能无法发现这一差异,今后需进行进一步研究以明确ANH对减少术中异体输血发生情况的影响[14-15]。S1、S2及S3组患者之间出血量、异体输血量及输血比例差异无统计学意义。
以上结果说明,复合使用七氟烷及舒芬太尼维持麻醉时,ANH不会造成血流动力学不稳定及BIS值的改变;同时ANH可以减少术中出血及异体输血量,因此是一项安全可行的血液保护措施。但是由于大剂量舒芬太尼与丙泊酚联合应用时会出现HR及BIS值下降,即使单纯使用舒芬太尼时并不会引起BIS值变化,麻醉中仍需选择适宜浓度的舒芬太尼以确保患者安全。
[1]何满,高峰,田玉科,等.急性非等容性血液稀释对靶控输注丙泊酚镇静深度的影响[J].临床麻醉学杂志,2012,28(9):837-840.
[2]Hemgen E,Houfani M,Billard V,et al.Propofol-sufentanil anesthesiafor thymid surgery:optimal concentrations for hemodynamic andelectroencephalogram stability,and recovery features[J].Anesth Analg,2002,95(3):597-605.
[3]Cross JB.Estimating allowable blood loss:corrected for dilution[J].Anesthesiology,1983,58(3):277-280.
[4]Monk TG,Saini V,Weldon BC,et al.Anesthetic management and one-year mortality after noncardiac surgery[J].Anesth Analg,2005,100(1):4-10.
[5]Ropcke H,Konen-Bergmann M,Cuhls M,et al.Propofol and remifentanil pharmacodynamic interaction during orthopedic surgical procedures as measured by effects on bispectral index[J].J Clin Anesth,2001,13(3):198-207.
[6]谢国柱,王荣宁,卞丽玉,等.丙泊酚与舒芬太尼相互作用的药效学关系[J].临床麻醉学杂志,2010,26(10):840-842.
[7]吴书平,张春艳.舒芬太尼与芬太尼用于全麻诱导对血流动力学及BIS的影响[J].中国现代药物应用,2012,6(13):77-78.
[8]杨宁,左明章.不同靶浓度舒芬太尼对异丙酚全麻患者脑电双频谱指数的影响[J].中华麻醉学杂志,2008,28(10):869-872.
[9]刘远辉,张伟红.BIS监控下舒芬太尼对老年人全麻诱导插管期间心血管反应的影响[J].国际医药卫生导报,2011,17(23):2846-2849.
[10]郑宏,王江,曹兴华,等.急性超容血液稀释对靶控输注异丙酚血药浓度及系统性能的影响[J].中华麻醉学杂志,2004,24(4):418-421.
[11]王江,郑宏,宣燕,等.急性等容血液稀释对靶控输注异丙酚血药浓度及系统性能的影响[J].中华麻醉学杂志,2007,27(3):244-246.
[12]宋永生,张野,胡宪文,等.舒芬太尼复合七氟醚或丙泊酚在全麻诱导中的应用[J].临床麻醉学杂志,2011,27(6):552-554.
[13]黎玉辉,郭新峰,王心田,等.急性等容血液稀释血液保护的 Meta 分析[J].中华麻醉学杂志,2006,26(8):703-706.
[14]Bennett J,Haynes S,Torella F,et al.Acute normovolemi chemodilution in moderate blood loss surgery:a randomized controlled trial[J].Transfusion,2006,46(7):1097-1103.
[15]邵雪泉,余功敏,许小峰.急性等容血液稀释联合控制性降压对颅脑肿瘤术中血液保护的临床观察[J].浙江实用医学,2011,16(1):37-39.

