一种多头基有机硅季铵盐的合成及其性能
丁寒卫,薛永强,崔子祥,郭文涛
(太原理工大学应用化学系,山西 太原 030024)
有机硅季铵盐除了具有一般季铵盐表面活性剂的优点外,还因其具有有机硅基团,可水解成硅羟基,硅羟基可与羟基、酰胺基、硅官能基团等反应。另外,有机硅季铵盐类表面活性剂降低表面张力的能力大于其他表面活性剂,还具有优良的润湿性、消泡性以及生理惰性。而且,有机硅季铵盐具有优越的安全性能。目前,有机硅季铵盐类表面活性剂的应用越来越广泛,受到了广泛的关注[1-8]。
多头基季铵盐表面活性剂同传统的单头表面活性剂相比,具有更高的电荷密度,在水溶液中表现出不同于传统表面活性剂的聚集状态,具有更高的表面活性、更好的水溶性、油溶性和缓蚀性能[9]。Tomokazu等[10]的工作揭示了分子中季铵盐基团的个数显著影响季铵盐表面活性剂的克拉夫特点、临界胶束浓度和在水中的溶解度。在国际上,多头基季铵盐受到特别关注,许多多头基季铵盐被合成出来。Keisuke等[11]合成了一种双头基季铵盐,并研究了季铵盐基团的增加对表面特性和胶束形成的影响。Lorena等[12]用六亚甲基四胺和γ-氯丙基三甲氧基硅烷合成了一种含有单个支链的有机硅季铵盐,并且用于二氧化硅的表面改性,进而用于芳胺类化合物的固相萃取。
另外,Garacia-Rsao等[13]研究认为,含多个季铵盐基团的季铵盐对微生物具有较强的吸附和抑杀作用。含有多个季铵盐基团的有机硅季铵盐,国内外尚未见有文献报道。
本文用六亚甲基四胺和 γ-氯丙基三甲氧基硅烷合成了一种多头基有机硅季铵盐,对其合成工艺进行了优化,并测定了该产物的物化性能及抑菌性能。
1 实验部分
1.1 合成
合成反应如图1。
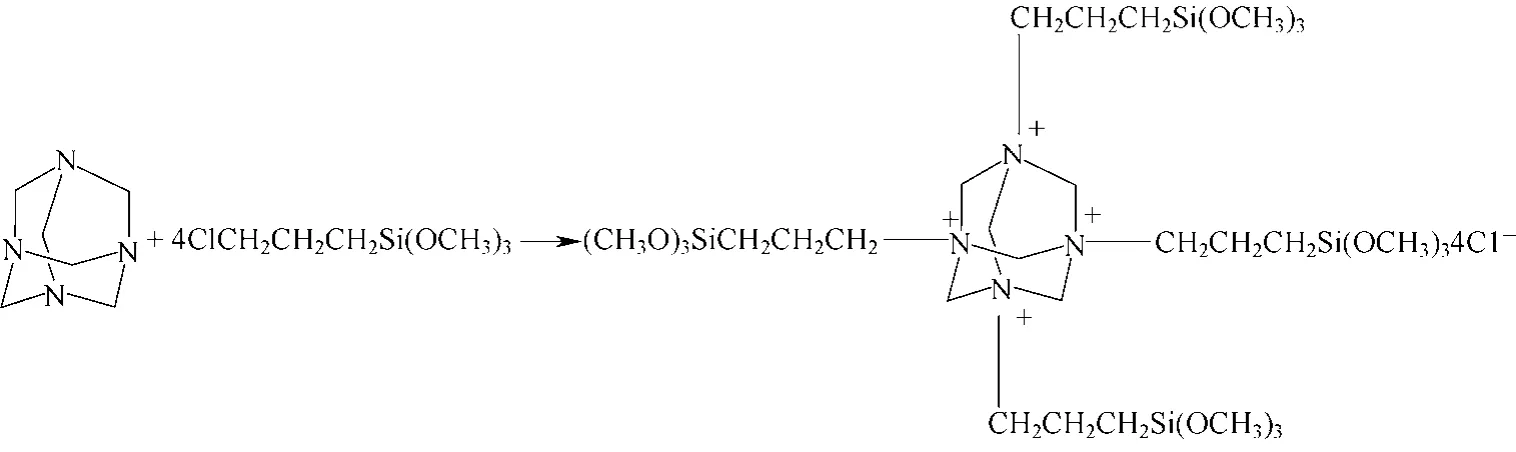
图1 目标产物合成路线
本文所用的试剂六亚甲基四胺、γ-氯丙基三甲氧基硅烷、四氢呋喃、二氧六环、乙腈等,试剂均为分析纯。
合成步骤:称取一定量的六亚甲基四胺,完全溶解于溶剂中,加热到一定温度,接着加入一定量的γ-氯丙基三甲氧基硅烷,连续回流反应50 h。 然后,蒸出甲醇溶剂和未反应的γ-氯丙基三甲氧基硅烷,得到黄色黏稠物,再加入到丙酮中进行重结晶,得到白色片状固体产物。本文根据 GB/T 5174—2004 阳离子表面活性物含量测定法(溴化底米鎓法),对产物进行定量分析。
1.2 微波辅助合成
由于该反应用油浴或者水浴等常规加热方式,反应过慢,所以将微波技术应用于该反应中,反应步骤如下:在三颈瓶中,加入 30 mL吡啶,称取1.26 g六亚甲基四胺,使其完全溶解于吡啶中,接着滴加2.14 g的γ-氯丙基三甲氧基硅烷,将三口瓶转入一个顶部带有冷凝装置的 MCR-3型微波化学反应器(巩义市予华仪器有限责任公司)中,调节功率为560 W(07档),调节温度为110 ℃,开启微波加热,连续回流反应2~10 h。反应结束后,将三颈瓶放在低温的地方,静置48 h,瓶底有大量粗大的白色晶体颗粒生成,最后用丙酮进行重结晶。
1.3 合成产物的表征
采用 KBr 压片法,用 FTIR-1730型红外光谱仪(美国铂金埃尔默公司),测定了产物的红外光谱,扫描范围为4000~500 cm−1,并在Bruker AdvanceⅢ 300 NMR 核磁共振仪(德国布鲁克公司)上获取了产物的1H NMR谱图。
1.4 产物性能测试
本文采用TDGC2-05型显微熔点测定仪(北京调微仪器厂),测定目标产物的熔点;采用最大气泡法测定表面张力,所用仪器型号为 DMPY-2C(南京大学应用物理研究所);采用电导率法测定其临界胶束浓度,仪器为 PXSJ-216型离子分析仪(上海精密科学仪器有限公司)。
杀菌试验:采用抑菌环直径测定法,评价目标产物及对比样品(十六烷基三甲基溴化铵)对大肠杆菌的杀菌效果。实验步骤如下:在 50 ℃的无菌条件下,分别在5个培养皿中倒入琼脂液,并且要求其在直径9 cm的面积内含琼脂液15 mL;然后再室温下冷却,固化;然后,分别把5份0.2 mL的105个/mL的大肠杆菌菌液涂于上述5个培养皿的琼脂培养基表面;再取5份10 mg的样品分别放在5个培养皿中;在36~37 ℃下培养48 h;测量并记录抑菌环的直径。
2 结果与讨论
2.1 产物的结构分析结果
目标产物的红外光谱图见图2。从图2中可以看出,在 1100~1000 cm−1有两个明显的吸收峰,这是 Si—O键的伸缩振动红外特征吸收峰,690~900 cm−1的3个明显吸收峰是Si—C键的伸缩振动红外特征吸收峰。927~972 cm−1两个吸收峰为季铵盐的特征吸收峰。季铵盐基团的存在也可由下面的核磁共振谱图所印证。
目标产物的核磁共振谱图见图3。图3中,经过计算可知,化学位移为7.427~7.558 ppm的氢原子数与化学位移为 4.454 ppm的氢原子数的比为5.11∶17.24,而化学位移为7.427~7.558 ppm的氢原子是与氮原子相连的亚甲基上的氢原子,化学位移为4.454 ppm的氢原子为γ-氯丙基三甲氧基硅烷上除γ碳以外其他碳原子上的氢原子。因此,实验产物的结构中含3个有机硅基团,即为三头基有机硅季铵盐。
此外,还采用GB/T 5174—2004的方法对合成产物中的阳离子活性物含量测定,计算结果也表明,实验产物的结构中平均含有3个有机硅基团。
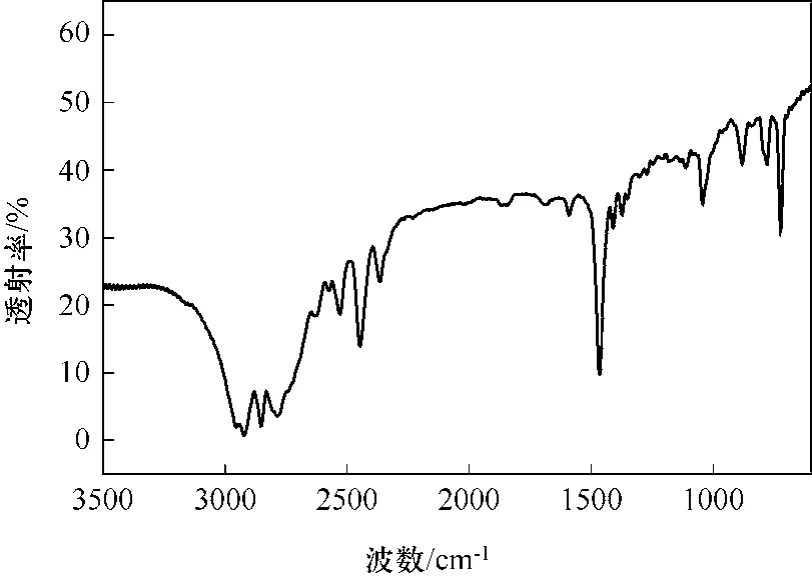
图2 产物的红外光谱图
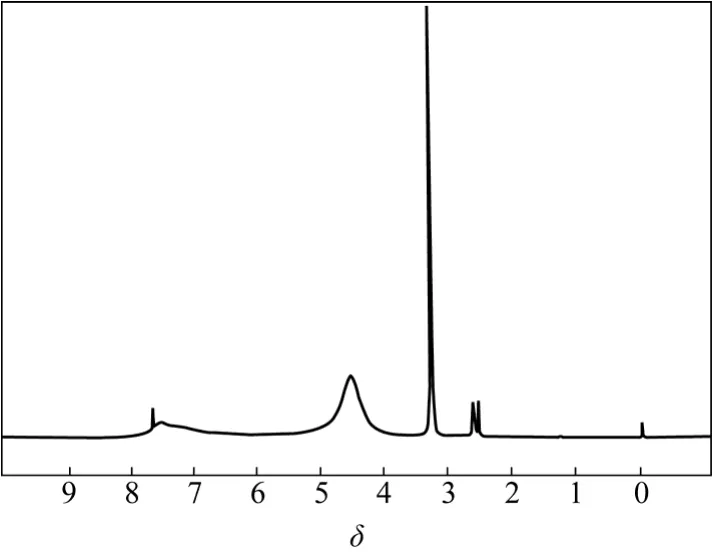
图3 产物的1H NMR谱图
2.2 工艺优化结果
在合成目标产物的过程中,对几个影响实验产率的因素进行了一定的研究,并做了正交试验,见表1。
由表1可见,所做实验得出结论,反应时间、原料配比和所用溶剂对实验产率的影响依次减小。较佳的工艺条件为:溶剂选择二氧六环,六亚甲基四胺与γ-氯丙基甲氧基硅烷的摩尔比选择1.0∶1.2,反应时间选择60 h。
2.3 微波辅助合成实验结果
微波辅助合成实验中,考察了反应时间对产率的影响,实验结果见图4。
由图4以及表1的结果对比可知,微波技术的运用明显提高了反应速率和产率,这可能归结于微波对极性物质的选择性加热,即微波致热效应加速了该有机反应[14],或者是微波降低了该反应的活化能,使得反应速率得到提高[15]。另外,反应进行8 h之后,反应的产率开始下降,可能是反应时间太长造成了部分产物的分解。
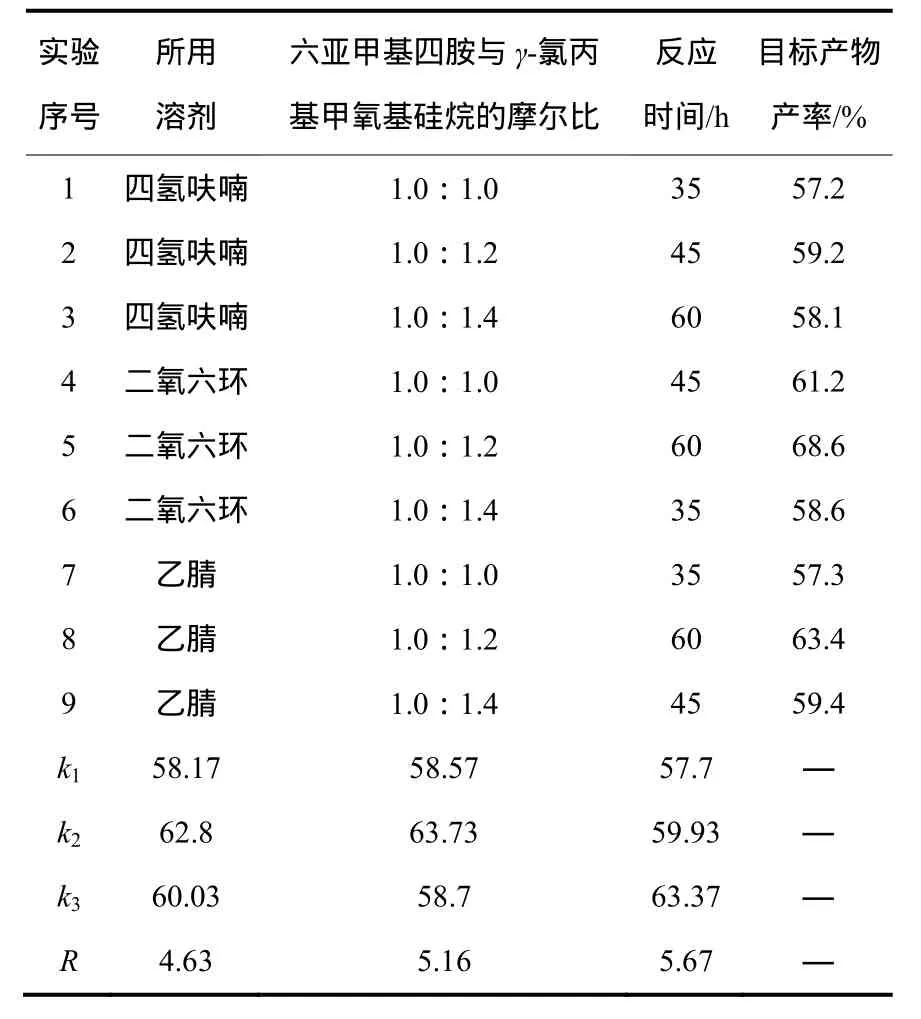
表1 合成产物的正交试验表
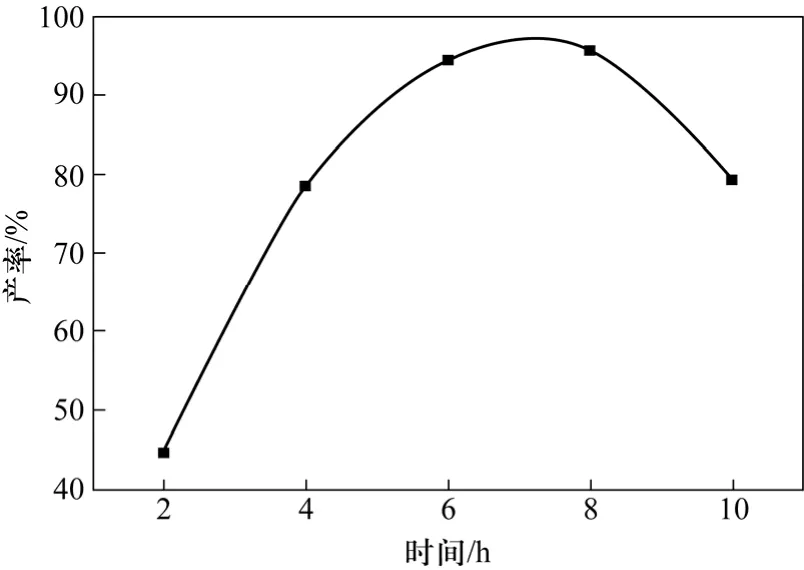
图4 微波辅助合成实验结果
2.4 性能的测定结果
产物的熔点为116.3~118.8 ℃;γCMC为46.30 mN/m,临界胶束浓度CMC 为0.19 g/L;产物对大肠杆菌的抑菌环直径可达27.4 cm。可见,本文所合成的多头基有机硅季铵盐杀菌剂具有优良的综合性能。
3 结 论
以六亚甲基四胺和γ-氯丙基三甲氧基硅烷为原料,可以合成出一种多头基(平均为三头基)有机硅季铵盐的合成。较佳的工艺条件为:溶剂为二氧六环,六亚甲基四胺与γ-氯丙基甲氧基硅烷的摩尔比为1.0∶1.2,反应时间为60 h。该合成反应中微波技术的运用明显提高了反应的速率和产率,仅用8 h就使产率达到 95.6%;所合成产物的熔点为116.3~118.8 ℃,γCMC为46.30 mN/m,临界胶束浓度CMC 为0.19 g/L,对大肠杆菌的抑菌环直径可达27.4 cm。
[1]幸松民,王一璐. 有机硅合成工艺及产品应用[M]. 北京:化学工业出版社,2000:169-171.
[2]李俊英,冯圣玉,李天铎. 聚硅氧烷季铵盐抗菌整理剂的合成及应用[J]. 日用化学工业,2003,33(4):249-251.
[3]谢瑜,张昌辉,徐旋. 有机硅季铵盐抗菌剂的研究进展[J]. 化工技术与开发,2008,37(4):25-28.
[4]王绪荣. 有机硅卫生整理剂的合成、性能与应用[J]. 染整科技,2000(1):32-38.
[5]王友国,王佩维,姚晨之,等. 织物柔软剂酯基季铵盐生物降解性的研究[J]. 化工新型材料,2005(7):19-21.
[6]徐群,曹明丽,邢凤兰,等. 含酯基不对称双季铵盐表面活性剂的合成[J]. 精细化工,2004(12):903-905.
[7]吕艳萍,李临生,安秋凤. 织物抗菌整理剂有机硅季铵盐 ASQA的合成及应用[J]. 印染助剂,2005,22(1):20-23.
[8]河合博. 道康宁5700抗微生物处理剂[J]. 印染,1996,22(3):38-42.
[9]Tae-Seong Kim,Toshiyuki Kida,Yohji Nakatsuji,et al. Preparation and properties of multiple ammonium salts quaternized by epichlo-rhydrin[J]. Langmuir,1996,12(26):6304-6308.
[10]Tomokazu Yoshimura,Nagisa Chiba,Keisuke Matsuoka. Supra-long chain surfactants with double or triple quaternary ammonium headgroups[J]. Journal of Colloid and Interface Science,2012,374:157-163.
[11]Keisuke Matsuoka,Nagisa Chiba,Tomokazu Yoshimura,et al. Effect of double quaternary ammonium groups on micelle formation of partially fluorinated surfactant[J]. Journal of Colloid and Interface Science,2011,356 :624-629.
[12]Lorena Vidala,Orlane Robina,Jevgeni Parshintseva,et al. Quaternary ammonium-functionalized silica sorbents for the solid-phase extraction of aromatic amines[J]. Journal of Chromatography A,2013,1285:7-14.
[13]Garacia-Rsao A,et al. A study of structure-activity relationship of quaternary ammonium salts[J]. Anales de Quimica,Serie C:Quimica Organicay Bioquimica,1981,77(1):12-18.
[14]Edwin G E Jahngen,Ronald R Lentz,Peter S Pesheck, et al.Hydrolysis of adenosine triphosphate by conventional or microwave heating[J]. The Journal of Organic Chemistry,1990,55(10):3406-3409.
[15]Ipsita Roy,Munishwar N Gupta. Non-thermal effects of microwaves on protease-catalyzed esterification and transesterification[J].Tetrahedron,2003,59(29):5431-5436.

