晚期胃癌的腹腔热灌注联合全身静脉化疗临床疗效的观察
何思略,张玉新 (广州军区广州总医院:.南方医科大学临床学院研究生队;.普通外科,广州 5050)
胃癌5年生存率不高,且20%会发生腹膜转移[1-3],若单纯行保守治疗,发生腹膜转移的患者生存期只有6~8个月[4-6]。晚期胃癌患者由于腹膜转移,血浆腹膜屏障的存在,传统的全身静脉化疗效果不理想[7]。腹腔热灌注治疗,不仅可有效治疗胃癌患者的恶性腹水,而且,在腹腔热灌注化疗后,胃癌腹膜转移患者最高生存期可延长达35个月[8]。然而,大部分胃癌腹膜转移患者,其肿瘤转移并不局限于腹腔。有部分患者出现腹膜转移时已经合并肺、骨和脑等脏器转移,这些患者单纯行腹腔热灌注化疗并不能获益。本研究对胃癌腹膜转移合并其它脏器转移的患者,行腹腔热灌注化疗联合全身静脉化疗和仅行全身静脉化疗的临床疗效进行了回顾性分析研究,以探讨腹腔热灌注化疗联合全身静脉化疗的临床效果。
1 资料与方法
1.1 临床资料
收集2011年9月至2013年9月收治的23例晚期胃癌患者,其中男10例,女13例;5例患者年龄超过65岁;13例患者伴有腹膜合并单脏器转移,10例伴有腹膜合并多脏器转移。所有患者的临床诊断均经术后病理证实,并排除多发肿瘤或伴有较重基础疾病可影响研究结果的情况,2组患者的一般资料比较差异无统计学意义。按照治疗方法的不同将患者分为2组,均行常规的胃癌根治术,实验组10例,术中和术后接受腹腔热灌注化疗联合术后全身静脉化疗;对照组13例,仅接受术后单纯静脉化疗。
1.2 治疗方法
23例患者均经病理确诊为胃癌,经CT或者PET/CT证实伴有腹膜合并多脏器转移。治疗组术中在腹腔左右侧膈下和盆腔2侧,放置4条腹腔热灌注管,分别作为进、出水管。把循环器套管按要求安装于体腔热灌注机上(BR-TRG-I型体腔热灌注治疗系统),并将生理盐水3 000~4 000 mL作为灌注液(根据患者腹腔容量确定),设定治疗温度为43℃,灌注速度为400 mL/min,术中灌注1次,术后每日灌注1次,每次灌注时间为60 min,根据患者对腹腔热灌注的反应情况,可连续灌注3~5次。2组患者均采用行全身静脉化疗(按照美国国家癌症综合网推荐方案进行化疗,选用多西他赛加顺铂加5-氟尿嘧啶化疗方案)。
1.3 观察指标
术后每月复查CEA、AFP等,必要时加做MRI或CT。定期复查血常规和肝肾功能等,按WHO抗癌药物不良反应评价标准,将不良反应分为0~Ⅳ度。以治疗过程中出现的最严重不良反应及并发症进行分度,生存质量应用KPS评分。
1.4 随访和生存分析
2组患者进行常规随访,患者死亡时随访终止。末次随访时间为2013年9月1日随访期间定期按上述化疗方案化疗。计算总生存期(overall survival,OS)、不良反应及并发症情况、生存质量。KPS评分较治疗前评分增多10分以上,即定为KPS评分较前改善。KPS评分减少、不变或增多在10分以下,定为病情无改善。
1.5 统计学方法
应用SPSS 13.0软件进行统计学分析。2组之间计数资料的比较采用Fisher精确检验和秩和检验;采用Kaplan-Meier法进行生存分析。P<0.05为差异有统计学意义。
2 结果
2.1 生存情况的比较
中位随访时间为8个月,随访期内2组患者有不同程度的疾病进展。截至随访结束,2组生存率为0%。实验组较对照组总生存期较对照组延长,P=0.003,差异有统计学意义(图1)。
2.2 患者不良反应和并发症的比较
2组患者的主要不良反应为骨髓抑制和消化系统反应(见表1)。实验组3例患者发生不完全性肠梗阻,均自行缓解;对照组1例患者出现药物热,1例患者发生再生障碍性贫血。2组之间的不良反应和并发症发生率差异无统计学意义。
2.3 患者生存质量KPS评分的比较
实验组6例KPS评分较前改善,对照组5例KPS评分较前改善,2组生存质量KPS评分没有统计学差异(P=0.835)。
3 讨论
胃癌严重威胁着人类健康,全球每年约有876 000例新发病例和647 000例肿瘤相关死亡病例[1],其发病率和病死率都很高,即使施行了手术治疗,术后5年生存率仍然较低[7]。晚期胃癌患者的生存质量较差,若再合并有癌肿腹膜和肝脑等脏器转移,不仅其生存质量会更加低下,而且生存期也会明显缩短,一般仅为6个月左右[4]。改善这部分患者的生存质量和延长其生存期,具有重要的临床意义。
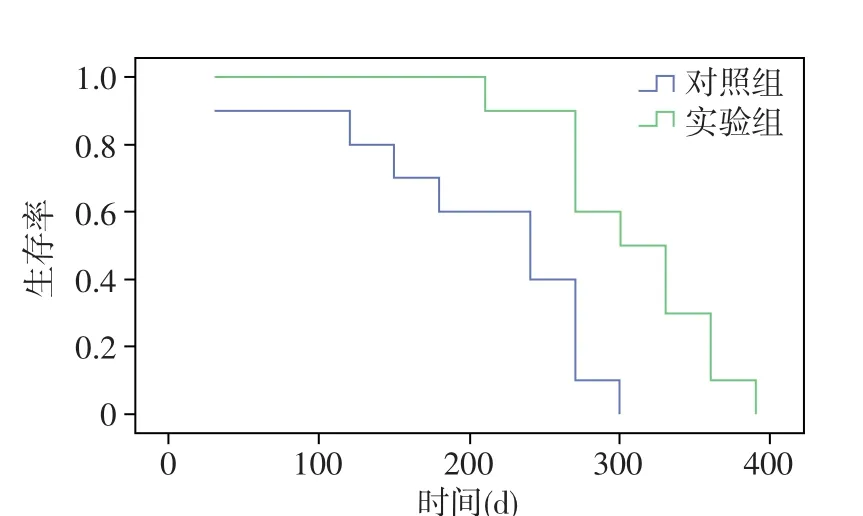
图1 实验组与对照组总生存期OS的对比

表1 实验组与对照组常见不良反应及并发症的比较[例(%)]
对于晚期胃癌的腹膜转移,传统的全身静脉化疗的疗效并不理想[9]。因此,对于肝、脑、骨和肺等脏器转移的治疗作用,也是十分有限的。腹腔热灌注化疗,虽然仅为腹腔局部治疗,对远处其它脏器转移的作用有限,但是对胃癌腹膜转移及其恶性腹水,却有良好的疗效[10-11],对于合并有腹膜和肝脑转移的晚期胃癌患者,理想的治疗措施应该是以达到控制腹膜转移和肝脑等脏器转移,从而改善患者生存质量,延长生存期为目的。
对合并有腹膜和肝脑转移的晚期胃癌患者进行腹腔热灌注治疗,就是采用体腔热灌注治疗系统,将含有化疗药品的灌注液或单纯生理盐水,加热至一定温度后,通过腹腔内预置的腹腔热灌注治疗系统的进、出水管道,进行腹腔内循环灌注,以清除腹腔内的游离癌细胞,杀灭微小病灶,治疗恶性腹水。特别是对癌性的恶性腹水具有十分显著的疗效,对提高这些患者的生存质量有重要意义。
据相关文献报道,恶性腹水患者在行腹腔热灌注治疗后,虽然原发肿瘤依然存在,甚至进一步发展,但是其恶性腹水却明显减少乃至消失,甚至在恶性腹水消失后,直至肿瘤进展至患者死亡时,恶性腹水也并无复发。尽管其确切机制尚未完全明了,但其对恶性腹水的良好治疗作用,已经显现出来了。
对合并腹膜和肝脑转移的晚期胃癌患者进行单纯全身化疗,对杀灭除腹腔以外的肿瘤病灶及游离于血液中的肿瘤细胞有重要作用,有助于抑制转移肿瘤病灶的进展和减缓病情的发展,改善由此引起的相关临床症状,是合并腹膜和肝脑转移晚期胃癌患者的重要治疗措施,能够改善胃癌患者的生存期[12],但是对恶性腹水的控制作用有限。腹腔热灌注化疗联合全身静脉化疗,是当前治疗这类患者较为理想的治疗措施。腹腔热灌注化疗的本质是热疗与化疗联合,发挥协同互补的治疗作用,其作用机理为:①通过热动力学效应,加快化疗药物与肿瘤细胞的作用,提高了化疗的敏感性,同时,也增加了其对化疗药物的通透性,使更多的化疗药物进入肿瘤细胞。例如在43℃下,癌细胞对丝裂霉素C的摄取量可增加至78%,药物的细胞毒作用也从30%提高至50%[13]。②加热可促进铂类等化疗药物与肿瘤细胞DNA发生交联,提高了化疗药物的杀伤力。③温热治疗可抑制DNA修复酶的活性,抑制化疗后的细胞损伤修复的机制,达到巩固化疗效果的目的。
相关临床研究表明:全身静脉化疗联合腹腔热灌注化疗比单纯全身静脉化疗的中位生存时间要明显延长[14-16]。然而,上述研究均只对晚期胃癌合并腹腔转移或合并脏器转移的分层研究,但对同时存在腹腔转移合并多脏器转移,是否还能从腹腔热灌注化疗中获益的研究甚少。本研究通过20例合并腹腔转移和肝脑转移的晚期胃癌患者,腹腔热灌注化疗联合全身静脉化疗临床疗效的观察,初步结果显示:腹腔热灌注化疗联合全身静脉化疗组的KPS评分改善率达60%,而单纯全身静脉化疗的组的KPS评分改善率仅20%,前组较后组的生存期也显著延长,说明腹腔转移合并肝脑等脏器转移的晚期胃癌患者,仍能从腹腔热灌注化疗中获益。
2组不良反应与并发症的发生率无统计学差异,结果表明:虽然腹腔热灌注治疗过程中,腹腔的腹膜及腹腔内脏器的血管床,可吸收热灌注液的大量热量,而引起患者体温升高等不良反应,但是并没有加重腹腔热灌注化疗联合全身静脉化疗的不良反应和并发症,单纯或联合化疗这两种治疗方法的不良反应和并发症没有叠加效应,说明腹腔热灌注化疗联合全身静脉化疗的临床应用是合理安全的。
随着腹腔热灌注化疗这项技术的临床广泛开展,其安全问题也逐渐受到了临床的高度关注。腹腔热灌注化疗,除了腹腔化疗的骨髓抑制、腹腔感染和粘连性肠梗阻等并发症外,腹腔热灌注治疗,还对患者的呼吸、循环等系统也有影响,因此,在腹腔热灌注化疗过程中,要有床旁生命监护仪检测,必要的镇静、止痛和吸氧、退热等措施,以确保治疗的安全。我们相信随着这项技术的日渐成熟和临床治疗经验的不断积累,上述不良反应及并发症的发生率一定会逐渐降低。
恶性肿瘤的疗效评价是一个综合性的复杂而长期的任务,本研究由于入选病例数不足,并且是单中心的回顾性研究,临床疗效观察的初步结果难免存在片面和错误之处,所得结论尚待今后大样本、多中心的随机对照研究,去进一步论证、完善或修正。
[1]Parkin DM.Global cancer statistics in the year 2000[J].Lancet Oncol,2001,2(9):533 -543.
[2]Sugarbaker PH,Yonemura Y.Clinical pathway for the management of resectable gastric cancer with peritoneal seeding:best palliation with a ray of hope for cure[J].Oncology,2000,58(2):96 -107.
[3]贾映东,彭 忠.腹腔镜辅助近端胃癌根治性切除术的疗效[J].中华消化外科杂志,2013,12(7):548 -549.
[4]Klaver YL,Hendriks T,Lomme RM,et al.Hyperthermia and intraperitoneal chemotherapy for the treatment of peritoneal carcinomatosis:an experimental study[J].Ann Surg,2011,254(1):125 -130.
[5]Jayne DG,Fook S,Loi C,et al.Peritoneal carcinomatosis from colorectal cancer[J].Br J Surg,2002,89(12):1545 -1550.
[6]Lemmens VE,Klaver YL,Verwaal VJ,et al.Predictors and survival of synchronous peritoneal carcinomatosis of colorectal origin:a populationbased study[J].Int J Cancer,2011,128(11):2717 -2725.
[7]文 灿,余汇洋,郭光金,等.CD105在胃癌组织中的表达及其临床意义[J].局解手术学杂志,2011,20(3):234 -236.
[8]Glehen O,Kwiatkowski F,Sugarbaker PH,et al.Cytoreductive surgery combined with perioperative intraperitoneal chemotherapy for the management of peritoneal carcinomatosis from colorectal cancer:a multi-institutional study[J].J Clin Oncol,2004,22(16):3284 -3292.
[9]Sugarbaker PH,Stuart OA,Vidal-Jove J,et al.Pharmacokinetics of the peritoneal-plasma barrier after systemic mitomycin C administration[J].Cancer Treat Res,1996,82:41 -52.
[10]Yonemura Y,de Aretxabala X,Fujimura T,et al.Intraoperative chemohyperthermic peritoneal perfusion as an adjuvant to gastric cancer:final results of a randomized controlled study[J].Hepatogastroenterology,2001,48(42):1776 -1782.
[11]Fujimoto S,Shrestha RD,Kokubun M,et al.Positive results of combined therapy of surgery and intraperitoneal hyperthermic perfusion for far- advanced gastric cancer[J].Ann Surg,1990,212(5):592 -596.
[12]Wagner AD,Grothe W,Haerting J,et al.Chemotherapy in advanced gastric cancer:a systematic review and meta-analysis based on aggregate data[J].J Clin Oncol,2006,24(18):2903 -2909.
[13]Elias D,Detroz B,Debaene B,et al.Treatment of peritoneal carcinomatosis by intraperitoneal chemo-hyperthermia:reliable and unreliable concepts[J].Hepatogastroenterology,1994,41(3):207 -213.
[14]Elias D,Lefevre JH,Chevalier J,et al.Complete cytoreductive surgery plus intraperitoneal chemohyperthermia with oxaliplatin for peritoneal carcinomatosis of colorectal origin[J].J Clin Oncol,2009,27(5):681-685.
[15]Franko J,Ibrahim Z,Gusani NJ,et al.Cytoreductive surgery and hyperthermic intraperitoneal chemoperfusion versus systemic chemotherapy alone for colorectal peritoneal carcinomatosis[J].Cancer,2010,116(16):3756-3762.
[16]Verwaal V J,van Ruth S,Witkamp A,et al.Long-term survival of peritoneal carcinomatosis of colorectal origin[J].Ann Surg Oncol,2005,12(1):65-71.

