三氧化钨光催化体系降解亚甲基蓝及反应级数的探讨
高 红,王学同
(1.天津现代职业技术学院,天津 300350;2.天津市津南区环保局,天津 300350)
利用半导体材料光催化降解水中污染物是目前比较热门的研究课题之一,光催化剂可以在反应中产生具有强氧化能力的空穴和羟基自由基,因而备受人们的关注。三氧化钨是一种半导体光催化材料,1985年,文学洙[1]首先报道了以三氧化钨为光催化剂处理印染废水的实验。但利用三氧化钨作为光催化剂,用于有机污染物的降解,过去报道仍然较少。我国钨的蕴藏量均居世界前列,其研究应用前景十分广阔。
亚甲基蓝作为一种碱性染料,在印染废水中颇具代表性,常作为光催化降解中的模型反应[2]。利用三氧化钨作为光催化剂,探讨其在降解亚甲基蓝模拟废水过程中的影响因素[3],并通过动力学研究为反应器的选型和放大提供理论基础。
1 实验部分
1.1 试剂与仪器
三氧化钨(化学纯),亚甲基蓝(分析纯)。722分光光度计,磁力搅拌器,白炽灯。
1.2 实验方法
取100mL一定浓度的亚甲基蓝溶液于反应器中,称取一定量三氧化钨,加入适量H2O2,放置于磁力搅拌器上,用紫外灯照射进行光照反应。反应过程中,取样、离心分离,取上清液在665nm的波长下测定溶液的吸光度,计算脱色率。
2 结果与讨论
2.1 单因素实验
在反应容器中加入亚甲基蓝模拟废水,加入光催化剂和H2O2,在光照射下,分别改变反应时间、催化剂用量、H2O2用量、模拟废水的初始浓度、pH值,进行模拟废水的光催化氧化处理,讨论这些因素对光催化反应的影响。
2.1.1 光催化剂用量对光催化效果的影响
在反应体系中加入不同量的三氧化钨光催化剂,并加入H2O2,在紫外灯照射下反应,每5min取样1次,测其吸光度,计算亚甲基蓝模拟废水的浓度百分比。降解过程中浓度百分比与时间的关系曲线如图1所示。

图1 不同三氧化钨用量下亚甲基蓝浓度随时间变化曲线
由图1的实验结果可知,随着催化剂用量的增加,亚甲基蓝的降解率迅速增大,但当催化剂增大到一定量时,降解率增大逐渐平缓,说明适当增加光催化剂的量能产生更多的活性自由基,增大反应的固-液接触面,加速光催化降解反应。光催化剂加入量较小时,光源产生的有效光子不能被完全转化成化学能,使得光子能量不能得到充分利用;而光催化剂加入过多又会造成催化剂颗粒对光的屏蔽散射,影响溶液的透光率而损失光能[4],这样会使光催化效率增加变缓。因此,适当的催化剂加入量是光催化反应的一个至关重要的因素。
2.1.2 H2O2用量对催化效果的影响
加入不同量的H2O2,进行光催化反应,测定不同H2O2加入量对光催化反应的影响。作降解过程中浓度百分比与时间的关系曲线如图2所示。

图2 不同H2O2用量下亚甲基蓝浓度随时间变化曲线
由图2的实验结果可知,加入H2O2可明显地提高亚甲基蓝的降解率。这是因为在反应过程中,会发生2种反应:一种是UV/光催化剂反应,另一种就是UV/H2O2反应,两者的结合会产生较强的降解作用。 H2O2在紫外光的照射下会产生具有强氧化能力的羟基自由基·OH,促进反应的进行。
另外,在反应过程中,产生的光生电子和光生空穴很容易复合,会抑制反应的进行。H2O2在反应过程中又是良好的电子捕获剂,氧气在光催化剂表面上具有良好的吸附性,易与光生电子反应,有效抑制电子与空穴的复合,使光催化反应持续进行[5]。H2O2在溶液中会产生O2,因此H2O2在体系中起着电子捕获剂的作用。在体系中加入H2O2会促进亚甲基蓝溶液的降解。
2.1.3 模拟废水的初始浓度对光催化效果的影响
改变亚甲基蓝模拟废水的初始浓度,在相同条件下进行光催化反应,测定不同初始浓度对光催化反应的影响。作降解过程中浓度百分比与时间的关系曲线如图3所示。
由图3的实验结果可知,模拟废水的初始浓度对处理的结果有明显的影响。亚甲基蓝模拟废水的初始浓度越低光降解效果越好。模拟废水的初始浓度过高会影响光的透过,达到相同降解率所需要反应的时间越长。由于染料的浓度将会影响吸附量的大小,随着浓度的增加,吸附量不断地增大。当浓度达到一定值以后,吸附趋于饱和,有机物被吸附在催化剂表面导致活性部位减少,再增大浓度,随时间的增加处理浓度减小变缓。
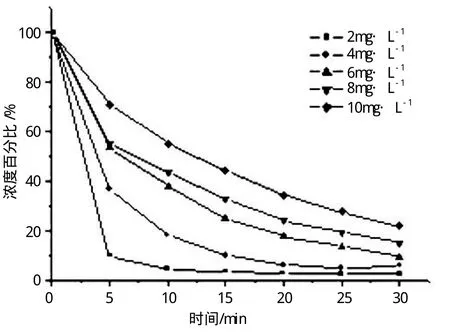
图3 不同初始浓度下亚甲基蓝浓度随时间变化曲线
2.1.4 模拟废水的pH值对光催化效果的影响
改变亚甲基蓝模拟废水的pH值,在相同条件下进行光催化反应,测定不同溶液pH值对光催化反应的影响。作降解过程中浓度百分比与时间的关系曲线如图4所示。

图4 不同pH值下亚甲基蓝浓度随时间变化曲线
模拟废水的pH值对不同的有机污染物的光催化降解过程的影响大不相同,其原因较为复杂,关键在于pH值直接影响催化剂表面所带电荷的性质和污染物在催化剂表面上的吸附行为。光催化氧化反应的较高速率出现在低pH值区、高pH值区还是中性值区都是有可能的。
2.1.5 光照时间对光催化效果的影响
改变光照时间,进行光催化反应,测定不同光照时间对光催化反应的影响。作降解过程中浓度百分比与时间的关系曲线如图5所示。

图5 不同时间下浓度随时间变化曲线
由图5的实验结果可知,在一定时间之前(约20min)亚甲基蓝的去除率随光照时间的增加而增大,过了这个时间后,随着光照时间的延长,光催化降解污染物的去除率增加比较缓慢。这是因为当光照稳定时,·OH和O2-的数目随光照时间增加而增加[6],当光照时间足够长时,有机物已经基本降解,所以出现缓慢趋势。
2.2 正交实验
为了进一步确定光催化反应的最佳反应条件,通过单因素实验,确定了反应条件对亚甲基蓝降解影响较大的3个因素,对每个因素选择3个水平条件,进行正交实验。在三氧化钨光催化体系中,由单因素实验结果可见,对亚甲基蓝降解影响较大的3个因素是催化剂用量、反应时间和H2O2用量。因素与水平表如表1所示。

表1 因素与水平表
在确定影响因素及水平的基础上,进行正交实验。根据正交表L9(34)设计9组实验,实验方法和单因素实验相同,得到处理后亚甲基蓝模拟废水的吸光度和脱色率如表2所示。根据实验结果,进行正交实验分析,数据如表3所示。
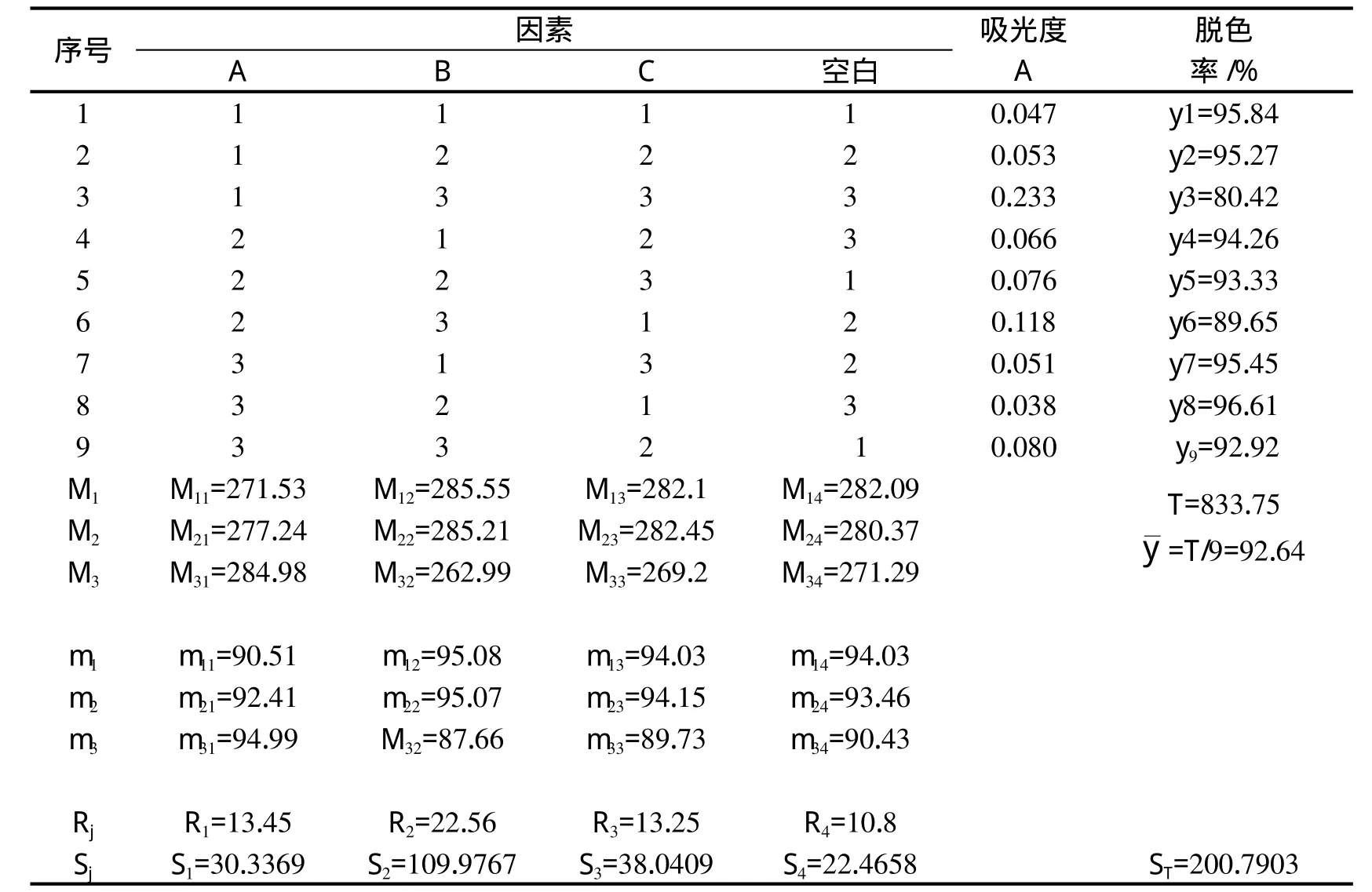
表2 正交实验表

表3 正交实验数据分析表
根据正交表信息和正交实验数据分析看出,各因素影响顺序为:反应时间>H2O2用量>三氧化钨用量。根据单因素实验、正交实验的结果,选择光催化反应的最佳条件是A3B1C2,即三氧化钨50mg、反应时间40min、1%的H2O24mL。在最佳反应条件下进行光催化降解实验,脱色率可达到96.6%。
2.3 不同复合体系中亚甲基蓝降解反应级数
有机物光催化降解用于水处理的有效性已得到了充分的证明,特别对处理通常意义上难降解的染料废水,在实验室中已取得了令人满意的结果。在向工业化迈进的过程中,反应器的选型及放大是2个亟待解决的关键性问题,这两者都离不开反应动力学的研究。
2.3.1 紫外光照射体系
配制10mg·L-1的亚甲基蓝模拟废水,置于紫外灯下照射40min,亚甲基蓝的浓度与光照时间的关系如图6所示。

图6 亚甲基兰浓度随光照时间的变化
利用图6中数据,作ln(C0/Ct)与光照时间t的关系曲线。由图7可见,ln(C0/Ct)—t之间符合直线关系,说明在该实验条件下亚甲基兰光催化降解反应为一级反应,直线的斜率即为反应速率常数k。
2.3.2 三氧化钨/UV体系
配制亚甲基兰模拟废水,加入三氧化钨,置于紫外灯下进行光照反应,亚甲基蓝的浓度与光照时间的关系如图8所示。
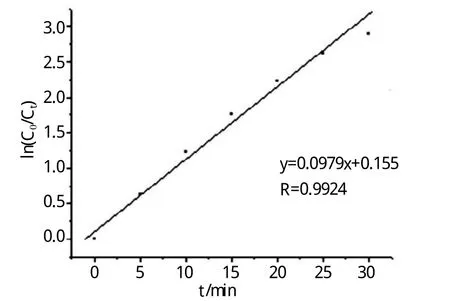
图7 ln(C0/Ct)与光照时间t关系图

图8 亚甲基蓝浓度随光照时间的变化
利用图8中数据,作1/Ct与光照时间t的关系曲线,见图9。由图9所示,1/Ct-t之间符合直线关系,说明在该实验条件下亚甲基蓝光催化降解反应为二级反应,直线的斜率即为反应速率常数k。

图9 1/Ct与光照时间t关系图
2.3.3 三氧化钨/UV/H2O2反应体系
配制亚甲基兰模拟废水,加入三氧化钨和H2O2,置于紫外灯下光照反应,亚甲基兰的浓度与光照时间的关系如图10所示。
利用图10中数据,作ln(C0/Ct)与光照时间t的关系曲线。由图11可见,1/Ct-t之间符合直线关系,说明在该实验条件下亚甲基兰光催化降解反应为二级反应,直线的斜率即为反应速率常数k。

图10 亚甲基兰浓度随光照时间的变化

图11 1/Ct与光照时间t关系图
利用最小二乘法进行线性拟合,可求得三氧化钨不同光催化降解体系下动力学方程及相应的参数如表4所示。

表4 三氧化钨不同光催化降解体系动力学方程及参数
由表4可知,三氧化钨光催化反应中,在UV反应体系中亚甲基兰降解反应是一级反应;在三氧化钨/UV和三氧化钨/UV/H2O2反应体系中,降解反应则是二级反应。这就说明在不同的复合高级氧化体系中,有机污染物降解的动力学方程和级数是不同的,在一定程度上可以认为有机污染物降解历程是不同的。
3 结论
1)在以三氧化钨作为光催化剂处理亚甲基兰模拟废水的反应中,影响处理效果的因素包括催化剂用量、模拟废水的初始浓度、H2O2用量、pH值和反应时间。通过单因素和正交实验,得到了最佳处理条件:三氧化钨用量50mg,反应时间40min,4mL H2O2。在此条件下进行光催化降解实验,亚甲基兰脱色率可达到96.6%。
2)通过动力学研究,在三氧化钨光催化反应中,在UV反应体系中亚甲基兰降解反应是一级反应,在UV/三氧化钨/H2O2反应体系中,降解也是一级反应;而在三氧化钨/UV反应体系中,降解反应则是一个二级反应。
[1] 文学洙.光催化法处理印染废水的研究[J].太阳能学报,1985,6(2):201-203.
[2] 李家珍.染料染色工业废水的处理[M].北京:化学工业出版社,1997.
[3] 解恒参,朱亦仁.三氧化钨的光催化氧化性能研究[J].工业用水与废水,2004(8):45-48.
[4] Dae-Sik Lee, Sang-Do Han, Jeung-Soo Huh, etal.Ntrogen oxidessensing characteristics of WO3-based nanocrystalline thin films gas sensor[J].Sensors and Actuators 1999(B60):57-63.
[5] 朱学文,廖列文,崔英德.半导体纳米材料的光催化及其应用[J].精细化工,2000,17(8):476-479.
[6] 王有乐,张庆芳.提高废水处理中光催化活性途径的探讨[J].工业水处理,2001,21(12):5-8.

