一种新型有机磷液晶传感器*
王诗鸣, 熊兴良, 李 广, 曾勇明
(1.重庆医科大学 附属第一医院 放射科,重庆400016;2.重庆医科大学 法医学与生物医学信息研究室,重庆 400016)
0 引 言
有机磷化合物是一类通常有毒的物质,可以以气态或液态的方式广泛存在于大气、土壤、植被和水体中,对环境的安全和人类的健康构成了很大的威胁,因而,开发一种可用于检测有机磷的传感器是十分必要的。
目前,用于检测有机磷的传感器主要采用气相色谱法[1]、表面声波法[2]和酶抑制法[3]等。其中,气相色谱法的检测精密度高,但需昂贵的检测仪器,不适宜广泛应用;表面声波法的检测灵敏度高,但易受周围环境(如水)的影响,稳定性差;酶抑制法因其对检测环境的温度具有极高的要求,限制了它在野外等复杂环境中的应用。因此,需要提出一种新技术,用来制作出不仅具有良好灵敏度和选择性,且可便携的、低廉的、可重复使用的有机磷传感器。
作为一种介于固体和液体之间的特殊功能材料,液晶已被应用于化学与生物传感器的研究中[4~8]。威斯康星大学的Shah R R等人[4]首先提出了一种用于检测有机磷的液晶传感器,它是将一薄层具有特异性目标分子识别能力的化学接收器淀敷到一具有nm级沟槽的超薄金膜上,使得其上的液晶分子能够沿着预期的某一方向取向,利用化学接收器与目标分子的特异性结合前后液晶呈现的光学表征的不同来实现对目标物的检测。使用这种传感器,只需1.5 min就能够检测出有机磷。之后,Adgate J L等人[5]提出一种传感器,可用来灵敏地检测有机磷杀虫剂。Yang K L等人[6]提出一种基于8CB的液晶传感器,用于检测甲基磷酸二甲脂(DMMP),其响应时间仅需1.5 min。
然而,上面提出的这些液晶传感器的制作方法都比较复杂,尤其预制自组装单分子层膜(SAMs)的过程较难处理,这些都大大降低了基于这些方法的液晶传感器的实用价值,从而促使将注意力放在一种新型液晶传感器的研究上,要求它具有简易的制作过程,在一个较长的时间内,可灵敏的、选择性的、可重复使用的检测有机磷。本文介绍了一种新型液晶传感器,其基底是通过在未经修饰的玻片表面上旋涂高氯酸铜无水乙醇溶液的方法制备而成,利用液晶与表面固定的Cu2+之间的相互作用来实现其在基底表面的垂直取向。在密封室通入DMMP前后,通过观察液晶的光学表征变化来对这种传感器的各项性能进行检测。
1 实验材料和方法
1.1 材 料
液晶4—戊基—4'—氰基联苯(5CB)购自石家庄华锐科技有限公司。六水高氯酸铜和DMMP购自Sigma-Aldrich(新加坡)。无水乙醇、甲苯和丙酮由重庆市川东化工(集团)有限公司提供。载玻片购自帆牌公司,使用玻璃刀将载玻片裁剪成实验所需的正方块状。铜载网购自北京中镜科技有限公司。
1.2 方 法
1.2.1 玻璃基底的处理
首先,将方形载玻片放入90 ℃的Piranha溶液中进行90 min的羟基化处理。取出,用超纯水冲洗3次。随后放入盛有3 % Decon—90的超声波清洗器中,在50 ℃,100 W条件下处理20 min。取出,先后用超纯水和无水乙醇进行2次冲洗。最后,再用大量超纯水彻底地冲洗4次。放入烘箱中,于103 ℃下烘烤30 min,备用。
1.2.2 玻璃基底表面的功能化
基底表面的功能化是通过在未经修饰的洁净玻片表面涂覆一薄层Cu2+的方法来实现的。首先,分别配置四种不同浓度的高氯酸铜无水乙醇溶液(0.1,1,2,5,10 mmol/L)。使用CE 100旋转涂覆机(厦门凯美特科学仪器有限公司)将无水乙醇和这四种溶液分别喷涂在5片经清洗处理后的玻片表面上。放入烘箱中,于103 ℃下处理90 min。然后在使用前于25 ℃条件下静置24 h。
1.2.3 液晶传感器的制作和性能测试
将一片铜载网置于基底表面上,使用移液器吸取0.3 μL 5CB,滴于其上,用镜头纸轻轻地拭掉铜载网上多出的过量液晶,传感器制备完成。然后,将其放入一自制的小密闭室,通过密闭室侧面的一微小圆孔与外面相通。通过一自制的气体发生装置提供本实验所需的气体。当5 %体积分数的DMMP通过侧壁的微小圆孔进入到密闭室内时,对液晶传感器的光学响应进行观察。通过打开密闭室、引入外面空气和再次关闭小室、通入DMMP气体实现对传感器的可重复性性能的检测。通过分别导入水汽、无水乙醇、甲苯和丙酮的等的气态物来对传感器的可选择性检测性能进行测试。
1.2.4 成像系统
在实验中,使用与偏光显微镜相连的数码相机(佳能PowerShot A640)获取液晶传感器的光学表征图像。偏光显微镜的两偏振片设置为正交。把需观察的液晶传感器置于偏光显微镜下。所有的实验图像均取自本成像系统。
2 结果和讨论
2.1 Cu2+对5CB取向的影响
为了评估Cu2+对液晶5CB取向的影响,把5CB分别滴凃在预处理有不同浓度Cu2+的玻璃基底上。通过偏光显微镜观察,如图1所示,发现未涂覆有Cu2+的传感器的光学表征呈亮态,表明5CB呈平行或倾斜取向;而涂覆有Cu2+的传感器的光学表征随时间逐渐由亮转暗直至全暗态,结合其在锥光模式下的图片,表明5CB此时呈垂直取向[7~13]。
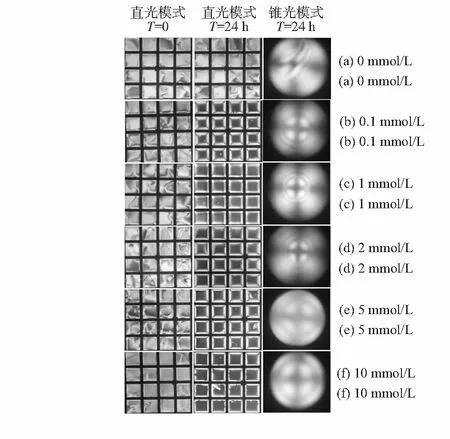
图1 相互作用24 h后不同Cu2+浓度对基底上的5CB的取向的影响
通过对传感器的光学表征的连续观察,发现其实现这种由亮转暗的光学变化所需的时间与Cu2+的浓度相关。如表1所示,Cu2+的浓度越高,液晶传感器转变为全暗态所需的时间越短。当Cu2+的浓度高至10 mmol/L时,传感器在6 min后就呈现出全暗态的光学表征。
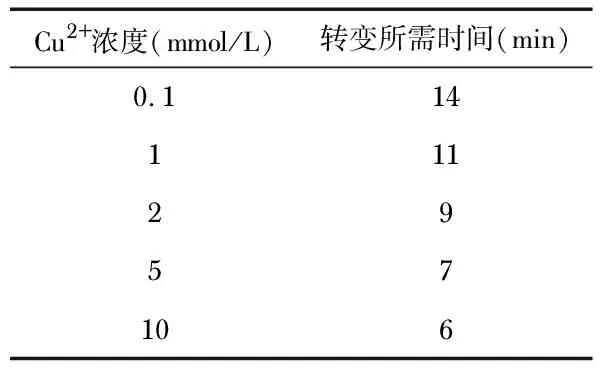
表1 Cu2+的浓度对液晶传感器从亮到全暗的光学转变所需时间的影响
对于产生这种光学变化的原因,这是由于基底表面上的Cu2+的存在,它使得5CB和Cu2+之间形成一弱键合物[11]或引起Cu2+-5CB界面上的双电层的形成[12],二者均可使得5CB呈垂直取向[7,13]。
2.2 对DMMP的检测和可重复性与可选择性
首先,使用一个自制的气体发生装置,将5 %体积分数的DMMP气体通入到一盛有这种传感器的密封室内,并利用正交偏光显微镜对传感器的光学表征进行观察。如图2所示,通入DMMP气体后,传感器的光学表征在1 min内逐渐从暗开始变亮,这表明5CB经历了一个从垂直到平行或倾斜的取向变化[6,10,11,13,14]。当打开密闭室,并停止DMMP气体的通入时,观察到液晶传感器的光学表征在5 min内逐渐回复到了其初始的暗态,表明5CB回复至其起初的垂直取向。当再次关闭密闭室,并通入DMMP气体,传感器的光学表征又从暗逐渐变为亮,而其他气体,如常见的干扰化合物水、乙醇、丙酮、甲苯等作为被测物通入时,则不会引起传感器的光学表征发生变化(如图3)。

图2 先后通入5 %的DMMP与空气时含有不同浓度的Cu2+液晶传感器的光学表征变化图
这是由于密闭室内通入DMMP气体时,DMMP上的磷酰基与Cu2+之间较强的共价键结合力取代了5CB中的氰基团与Cu2+之间的弱键合作用,从而引起液晶的取向从垂直转向平行(或倾斜),传感器呈现出从暗到亮的光学表征变化。当打开密闭室,重新暴露给空气后,传感器接触的DMMP气体快速减少,5CB与Cu2+之间的弱键合作用力再次占据主导,导致液晶的取向在较短的时间内重新变回垂直,传感器再次显示出暗态的光学表征。而其他干扰化合物气体则无磷酰基,不会引起传感器光学表征的变化。以上结果表明了这种液晶传感器能够在1 min之内检测出DMMP气体,并且这种检测是可重复性的和选择性的。

图3 含有2 mmol/L Cu2+的液晶传感器在测试前和分别连续25 min暴露给100 %水蒸汽、50 %无水乙醇、50 %丙酮、50 %甲苯的光学表征变化图
2.3 Cu2+的浓度对响应灵敏度的影响
为研究Cu2+的浓度对响应灵敏度的影响,将含有不同浓度(0.1, 1, 2, 5 ,10 mmol/L)Cu2+的液晶传感器在制备后的第二天时分别放入密闭室内,检测其对DMMP气体的响应能力。通过观察,发现传感器的光学响应速度与Cu2+的浓度有关,如图4所示,Cu2+的浓度越低,对DMMP的光学响应速度越快;当Cu2+的浓度低至0.1 mmol/L时,传感器在DMMP气体通入不到1 min的时间内就逐渐出现从暗到亮的光学表征变化,25 min后,几乎变为全亮态。当打开密闭室,并停止DMMP气体的通入后,含有高浓度Cu2+的液晶传感器的光学表征快速地回复到其初始的暗态,而含有较低浓度Cu2+的液晶传感器则需较长时间。

图4 先后通入5 %DMMP气体和空气时含有0.1,1,2,5,10 mmol/L Cu2+的液晶传感器的光学表征的平均灰度值随时间变化曲线图
这些都表明了这种液晶传感器对DMMP的响应速度与Cu2+的浓度密切相关。Cu2+的浓度越高,5CB的垂直定向越难以被打乱,响应灵敏度越低。
3 结 论
在本研究中,开发出一种可用于检测有机磷的新型液晶传感器。通过自制的系统,以DMMP作为被测物,对这种液晶传感器的性能进行了测试。在这种传感器中,仅使用Cu2+对其基底进行功能化处理。Cu2+能够引起5CB从平行到垂直的取向变化,从而使得传感器的光学表征从亮转为暗。当通入DMMP气体时,传感器在不到1 min的时间里就产生了从暗到亮的光学表征转变,在接连暴露给DMMP气体和空气时所产生的亮与暗的光学表征的变化证明了这种响应是可重复性的。而如水等其他干扰化合物则不会引起其光学表征的变化,表明了这种传感器对DMMP等有机磷的检测具有选择性。与此同时,其对DMMP气体的响应灵敏度与Cu2+的浓度密切相关,在实验浓度范围内(0.1~10 mmol/L),Cu2+的浓度越低,其光学响应速度越快,响应灵敏度越高。
参考文献:
[1] Trap H C,Schans M V D.Gas chromatographic techniques for the analysis of chemical warfare agents[J].LC GC Eur,2007,20:202-207.
[2] Nieuwenhuizen M S,Harteveld J LN. Studies on a surface acoustic wave(SAW)dosimeter sensor for organophosphorous nerve agents[J].Sensors and Actuators B,1997,107:167-173.
[3] Kim C S,Lad R J,Tripp C P.Interaction of organophosphorous compounds with TiO2and WO3surfaces probed by vibrational spectroscopy[J].Sensors and Actuators B,2001,76:442-448.
[4] Shah R R,Abbott N L.Principles for measurement of chemical exposure based on recognition-driven anchoring transitions in liquid crystals[J].Science,2001,293:1296-1299.
[5] Adgate J L,Bartekova A,Raynor P C,et al.Detection of organophosphate pesticides using a prototype liquid crystal monitor[J].Environmental Monitoring,2009,11:49-55.
[6] Yang K L,Cadwell K,Abbott N L.Use of self-assembled monola-yers,metal ions and smectic liquid crystals to detect organophosphonates[J].Sensors and Actuators B,2005,104:50-56.
[7] Bungabong M L,Ong P B,Yang K L.Using copper perchlorate doped liquid crystals for the detection of organophosphonate va-por[J].Sensors and Actuators B,2010,148:420-426.
[8] Cheng D,Sridharamurthy S S,Hunter J T,et al.A sensing device using liquid crystal in a micropillar array supporting struc-ture[J].Micro-electro-mechanical Systems,2009,18:973-982.
[9] Sen A,Acharya B R.Alignment of nematic liquid crystals at inorganic salt-liquid crystal interfaces[J].Liquid Crystals,2011,38:495-506.
[10] Bai Y,Abbott N L.Recent advances in colloidal and interfacial phenomena involving liquid crystals[J].Langmuri,2011,27:5719-5738.
[11] Cadwell K D,Alf M E,Abbott N L.Infrared spectroscopy of competitive interactions between liquid crystals,metals salts,and di-methyl methylphosphonate at surfaces[J].Phys Chem B,2006,11:26081-26088.
[12] Shah R R,Abbott N L.Coupling of the orientations of liquid crystals to electrical double layers formed by the dissociation of surface-immobilized salts[J].Phys Chem B,2001,105:4936-4950.
[13] Hunter J T,Pal S K,Abbott N L.Adsorbate-induced ordering transitions of nematic liquid crystals on surfaces decorated with aluminum perchlorate salts[J].Applied Materials & Interfaces,2010,2:1857-1865.
[14] Sridharamurthy S S,Cadwell K D,Abbott N L,et al.A microstructure for the detection of vapor-phase analytes based on orientatio-nal transitions of liquid crystals[J].Smart Materials and Structures,2008,17:1-4.

