老年胃癌患者全胃切除术后早期肠内营养的临床价值
邓 峰 茅伟达
(南京中医药大学江阴附属医院外科四病区,江苏 江阴 214400)
老年胃癌患者在术前多出现营养不良及免疫功能低下,另外,手术和创伤应激时机体的高代谢状态可进一步加重营养不良。然而手术后由于患者营养吸收障碍以及手术造成的人体应激反应进一步威胁着患者术后的营养状况〔1〕。全胃切除术的使用对患者生理功能产生巨大破坏,使患者出现营养代谢障碍。传统术后多采用肠外营养支持,虽然此种方式一定程度上缓解了患者的营养不良,但缺乏食物对肠蠕动的刺激,使大多数患者生理功能出现紊乱〔2〕。所以手术后对老年胃癌患者全胃切除术后的营养治疗有着很重要的意义。本文选取本院收治老年胃癌患者行根治性全胃切除术(D2),进行肠内营养和肠外营养治疗并比较两组治疗效果。
1 资料与方法
1.1一般资料 选取本院2009年1月至2013年12月收治的符合入选要求的老年胃癌患者80例,男42例,女38例,年龄60~79〔平均(66.62±8.12)〕岁。随机分为对照组(肠外营养组)40例和观察组(肠内营养组)40例。其中对照组男22例,女18例,年龄61~79〔平均(66.31±11.21)〕岁;观察组男20例,女20例,年龄60~77〔平均(67.91±8.23)〕岁。入选标准:术前均有明确的病理学诊断并确诊;术前未行化疗或放疗,均行了D2清扫术。所有患者无其他器官的重大疾病,无肠道功能上的障碍。两组患者年龄、性别、身体营养状况、疾病分期以及手术方式上差异无统计学意义(P>0.05),具有可比性。
1.2留置营养管 病人术晨经一侧鼻孔留置胃空肠营养管(以下简称营养管)和胃管,确定胃管及营养管位置在胃内无误后用胶布妥善固定在病人鼻翼侧。
1.3营养支持方法 对照组:根据患者个体生理特点计算术后全肠外营养的基本需要量,术后第1天开始,与肠内营养等氮、等热量,按热卡25~30 kcal·kg-1·d-1,其中 30%~40%由20%脂肪乳剂供给。氮0.15~0.2 g·kg-1·d-1供给,氮源为复方氨基酸注射液,非蛋白质热量的其余60%~70%由葡萄糖液供给。配成营养液,经中心静脉管输注,输液速度为50~135 ml/h,每天输注16~24 h,持续7~10 d。观察组:术后第1天待患者循环稳定后开始通过微泵经鼻饲营养管注入0.9%氯化钠注射液200 ml+肠内营养乳剂(TPF-T)200 ml 以20 ml/h持续泵入,观察患者无不适,给予能全力匀速泵入,速度控制在30~50 ml/h,能全力500 ml/d,营养液浓度由低到高,在术后4~5 d,逐渐增加至80~100 ml/h,达能全力1 000~1 500 ml/d,营养液温度控制在37℃~42℃,每日不足热量及液体量经静脉补充。观察组术中放置鼻肠管,将营养管远端置于空肠-吻合口远端约30~40 cm 处,妥善固定,术后均不放置胃管,术后7 d肠内营养可逐渐减量,过渡至流质、半流质饮食。
1.4观察项目 记录两组患者术后腹胀、恶心、呕吐和腹泻的发生率,体重损失,进流质饮食时间,首次肛门排气时间、排便时间、大便性状、住院时间、住院费用以及并发症发生情况等。抽取患者术后第1天和术后第7天的清晨空腹血,检测患者的血红蛋白(Hb)、血浆总蛋白(TP)、血浆清蛋白(ALB)等。
2 结 果
2.1两组患者临床指标结果 两组患者临床观察指标比较两组患者均顺利完成临床手术,术中血压、脉搏、心率等生命体征较平稳,未发生术中死亡病例。观察组患者在术后的进流质时间、排气时间、排便时间、住院时间及住院费用等方面较对照组明显有优势(P<0.05)。对照组术后并发症发生率27.5%(11/40),其中肺部感染6例,切口感染5例。观察组术后并发症发生率10.0%(4/40),其中肺部感染1例,腹腔感染3例。两组患者术后并发症相比具有显著性差异(P<0.05)。见表1。
2.2两组患者治疗后营养指标结果 术后第1天,观察组与对照组在Hb、ALB、TP等营养指标上均无显著性差异(P>0.05)。术后第7天,两组患者在Hb含量水平上比较,没有显著性差异(P>0.05),但是对照组在(ALP)、TP水平上显著低于观察组(P<0.05)。见表2。
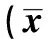
表1 两组患者临床指标结果比较±s,n=40)
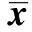
表2 两组被试Hb、ALB、TP等营养指标结果比较(g/L,±s,n=40)
3 讨 论
随着医学发展的不断更替,对于老年胃癌患者行全胃切除术后早期肠内营养支持的应用研究也越来越多。为了防止术后吻合瘘口的发生,患者一般需要禁食7 d以上。但就老年患者自身生理特点而言,各项生理指标都呈下降的趋势,特别是胃癌患者,在临床治疗中易发生异常情况,故多数行全胃切除术。然而老年患者术后的肠道功能恢复比较慢,肠道黏膜保护能力较弱,易发生因细菌破坏而造成的移位,从而造成术后恢复困难,并发症发生率及死亡率的比例上升。由此看来,老年胃癌患者行全胃切除术后早期肠内营养支持显得至关重要。而以往多认为,老年患者胃肠功能性退化,胃肠道手术造成的应激反应非常强烈,术后至少有3~5 d的胃肠麻痹,极大影响胃肠道对营养的吸收。导致术后多采用肠外营养支持,且对术后早期肠内营养支持的研究相对不足〔3〕。特别是老年胃癌患者,营养不良的状况明显高过正常人,而且由于全胃切除所造成的创伤进一步阻碍了营养摄入量,然而患者在术后对营养的需求又需要进一步加强。传统肠外营养支持法并不能满足患者的需要,从而导致患者的营养不良,免疫力下降,引发并发症的增加,严重的甚至会导致患者的死亡。
有研究认为,腹部手术完成后的2~3 d,肠道蠕动的功能发生障碍,因而将肛门恢复排气视为终止胃肠减压,并对患者进行肠内营养的标准〔4〕。然而仅就老年胃癌全胃切除患者而言,如果术前小肠的功能无异常现象发生,在术后2 h后小肠的功能就开始慢慢恢复,一般4~6 h可恢复完全,所以肠内营养一般可在术后不久就开始应用〔5〕。这些研究结果均为老年胃癌患者全胃切除术后早期肠内营养支持提供强大的理论依据。近年来的研究证实〔6,7〕,早期肠内支持可有效维持肠黏膜结构和功能的完整性,直接供给肠黏膜细胞营养物质,改善肠黏膜的营养状态,促进肠黏膜的增生修复,防止肠黏膜通透性降低,保持肠道正常的屏障功能,对维持机体的免疫功能、预防感染有着不可替代的重要作用,越来越多的证据表明,早期肠内支持对肠道的免疫刺激作用往往强于降低肠道内微生物易位的作用〔8〕。同时也能丰富患者术后营养需求,增加抵抗力,大大避免并发症的发生。
肠外营养虽然在现阶段的临床应用广泛,但其在治疗费用上、感染发生率上、肝脏损害等有一定的不足,而肠内营养不仅可以提供肠道的营养支持,在促进肠道功能的恢复上起到重要的作用,还降低了术后并发症的发生率。改善术后的营养状况以及促进肠道功能早期恢复根据病情合理的营养配方,正确的留置鼻饲管,认真观察和护理的前提下,早期应用肠内营养安全有效〔9,10〕。只要通过科学合理的护理方法,就能顺利完成肠内营养治疗,并疗效显著。改善了机体营养状态,对老年患者的肠道恢复更有利,术后恢复更快,减少术后并发症的发生,同时减少住院时间与费用。由此可见,肠内营养是促进全胃切除术后病人康复的保证,值得临床推广与研究。
4 参考文献
1黎介寿.肠内营养:外科临床营养支持的首选途径〔J〕.中国实用外科杂志,2003;23(2):67.
2陈淑凤. 早期肠内营养在胃癌根治术后患者中的应用〔J〕. 齐鲁护理杂志,2010;16(10):39-40.
3刘爱国.刘 璟.57例胃癌全胃切除术后患者早期肠内营养的临床观察〔J〕. 吉林医学,2010;31(23):3892-3.
4赵建铭,陆 岽,庄则豪.胃肠内营养现状及其在消化疾病中的应用〔J〕. 现代生物医学进展,2006;6(10):135-8.
5陈允锋. 早期肠内营养对胃癌行全胃切除术后肝功能的影响〔J〕. 海南医学,2009;20(9):182-4.
6李武平. 外科护理〔M〕. 北京:人民卫生出版社,2003:54.
7Koretz RL. Early enteral nutrition in the ICU〔J〕. Intensive Care Med,2010;36(6):1087-8.
8李 宁,黎介寿. 肠道营养重要性的再认识〔J〕.肠外与肠内营养,1998;5(1):1-2.
9卢 博. 危重患者的肠道营养支持应用分析〔J〕.蚌埠医学院学报,2008;33(5):553.
10Bozzetti F,Braga M,Gianotti L. Postoperative enteral versus parenteral nutrion in malnourished patients with gastrointestinal cancer:a randomised multicentre trial〔J〕. Lancet,2001;358(9292):1487-92.

