原子吸收光谱法测定复方氯化钠注射液中氯化钙含量
童永鑫,何宇新
(西华大学生物工程学院,四川 成都 610039)
体液是广泛分布于机体细胞内外的,由水和溶解于其中的电解质、低分子有机化合物以及蛋白质等组成,具有运输物质、调节酸碱平衡、维持细胞结构与功能等多方面作用的电解质混合溶液,因而体液正常的水、电解质代谢与生命活动息息相关。水、电解质的代谢紊乱与临床医学有密切而广泛的联系,它可作为病因引起许多疾病的发生,也可作为并发症与许多疾病伴行。它可导致酸碱平衡紊乱、休克、心力衰竭,从而使原发疾病恶化甚至发生恶性循环,危及生命[1-2]。
复方氯化钠注射液作为体液补充药,在体液水、电解质发生代谢紊乱的时候,能够迅速通过静脉输液进行体内水和电解质的调整。对于大容量注射剂,中间产品和成品检测过程中,迅速完成含量测定,既可以防止污染带入外源性热原,还可以大大提高生产效率和成品放行速度。《中国药典》2010版中对于复方氯化钠注射液中氯化钙含量测定采用的络合物滴定法繁琐复杂,操作时间长。原子吸收光谱法因其操作方便、检测迅速、重现性好、检测限度低,而受到广泛应用。本研究旨在建立一种采用原子吸收光谱法测定钙离子含量的方法,提高复方氯化钠注射液中氯化钙含量测定的效率。
1 实验部分
1.1 材料与试剂
氧化镧(La2O3,批号为F20110627),高纯试剂,纯度为4N(99.99%),国药集团化学试剂有限公司;氯化钠(NaCl,批号为20121017),江苏省勤奋药业有限公司;氯化钙(CaCl2·2H2O,批号为20100101),天津海光药业有限公司;氯化钾(KCl,批号为20120701),注射级,自贡鸿鹤制药有限责任公司;盐酸,分析纯,成都金山化学试剂有限公司;氢氧化钠,药用辅料级,批号为100920120602,湖南尔康制药股份有限公司;蒸馏水,广州屈臣氏食品饮料有限公司;乙二胺四乙酸二钠,天津市科密欧化学试剂有限公司;羟基萘酚蓝,上海迈坤化学有限公司;复方氯化钠注射液(批号为20121101),自制。
1.2 仪器与设备
电子天平(型号XS205Du),梅特勒托利多仪器(上海)设备有限公司;pH计(型号S20),梅特勒托利多仪器(上海)设备有限公司;安捷伦AA240原子吸收光谱仪,安捷伦科技有限公司;钙空心阴极灯,安捷伦科技有限公司。
1.3 实验方法
1.3.1 实验条件
燃气类型:空气-乙炔,空气体积∶乙炔体积=13.5∶2.2;灯电流为10 mA;检测波长为422.7 nm;狭缝宽度为0.5 nm。
1.3.2 溶液的配制[3-7]
1)氧化镧溶液的配制:称取29.32 g氧化镧,用25 mL去离子水润湿后,缓慢添加125 mL盐酸使氧化镧溶解,最后用蒸馏水稀释定容至500 mL。
2)系列标准溶液的配制:于50 mL的容量瓶中精密量取5 mL钙单元素标准溶液(1 000 μg/mL),用蒸馏水定容至刻度,即得标准溶液母液,质量浓度为100 μg/mL。准备6个100 mL的容量瓶,编号为0、1、2、3、4、5,分别往其中精密量取0.0、1.0、3.0、5.0、7.0、9.0 mL标准溶液母液,再分别加入2 mL氧化镧溶液,用蒸馏水定容至刻度,即得质量浓度分别为0 、1、3、5、7、9 μg/mL的系列标准溶液。
3)阴性对照溶液的配制:根据处方比例称取氯化钠0.850 0 g,氯化钾0.030 0 g,配制不含氯化钙的样品100 mL。移取上述溶液 5 mL于100 mL容量瓶中,再加入2 mL氧化镧溶液,用蒸馏水定容至刻度,即得阴性对照溶液。按照此法,重复配制3个阴性对照溶液。
4)供试样品的配制:移取复方氯化钠注射液(批号20121101)5 mL于100 mL容量瓶中,加入2 mL氧化镧溶液,用蒸馏水定容至刻度,即得供试样品溶液。按照此法,重复配制3个供试样品溶液。
5)羟基萘酚蓝指示液的配制:精密称取羟基萘酚蓝0.5 g,用蒸馏水溶解,再加入2滴0.1 mol/L的氢氧化钠溶液,摇匀,即得。
6)乙二胺四乙酸二钠滴定液的配制:称取乙二胺四乙酸二钠1.9 g于100 mL容量瓶中,用蒸馏水溶解定容至刻度。
1.3.3 标准曲线的测定[5]
采用原子吸收光谱法检测样品中的离子质量浓度,要求标准曲线的最佳分析范围的吸光度在0.1~0.6 之间,并且样品检测的吸光度在标准曲线的中间段。通过稀释或增加加样量,使最终样品检测的吸光度值在0.3~0.4左右。
确定了系列标准溶液的系列浓度后,将系列标准溶液按照原子吸收光谱法进行连续测定,以质量浓度C为横坐标,对应吸光度A为纵坐标做标准曲线,最终得到回归方程和相关系数。要求相关系数R2≥0.999 0。
1.3.4 样品中钙含量的测定
按照原子吸收光谱法先测定系列标准溶液,得到标准曲线和回归方程。再进行样品测定,系统自动按照标准曲线的回归方程将吸光度值代入得到样品中的钙离子含量。
2 实验结果与分析
2.1 标准曲线的测定
根据1.3.3的测定方法,得到钙离子含量测定的标准曲线的回归方程。标准曲线如图1所示。

图1 钙离子质量浓度与吸光度的标准曲线
由图1可知,钙离子含量测定的标准曲线的回归方程为A= 0.067 4C+ 0.001 1,相关系数R2=0.999 1,表明钙离子质量浓度在1~9 μg/mL之间,钙离子质量浓度与吸光度值呈良好的线性关系。
2 钙离子含量检测方法学考察
2.2.1 专属性考察[6-8]
复方氯化钠注射液是多电解质的混合灭菌水溶液,需要考察处方中非钙离子对钙离子含量测定的影响。通过对比阴性对照溶液与供试溶液的吸光度值,计算阴性对照样品的平均吸光度值占供试样品溶液的平均吸光度值的百分比a,以a反映处方中非钙离子对钙离子含量测定的影响。检测结果如表1所示。
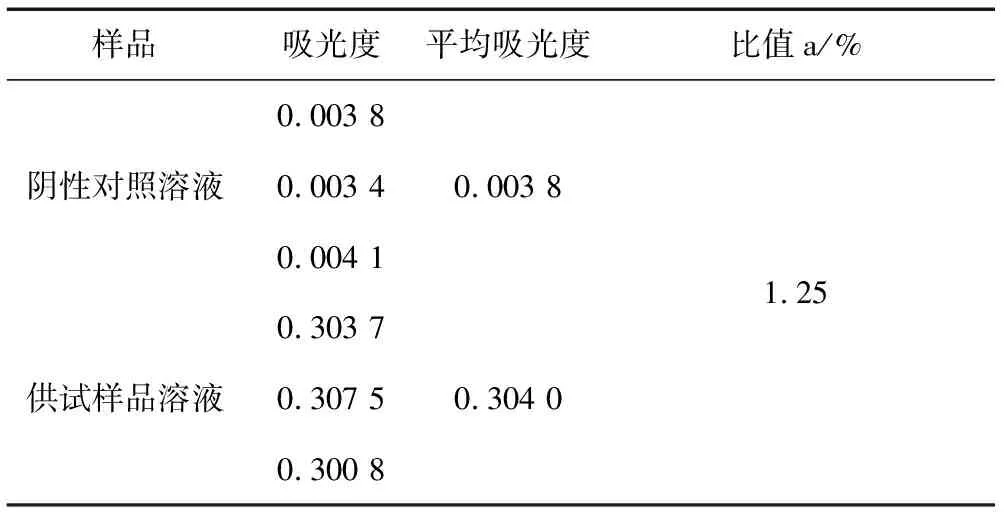
表1 专属性考察
由表1可知,阴性对照溶液的平均吸光度值占供试样品溶液吸光度值的1.25%,即a=1.25%。说明处方中,非钙离子成分对钙离子含量的测定干扰小,说明该法测定钙离子质量浓度专属性好。
2.2.2 耐用性考察[9]
根据《中华人民共和国药典》药品质量标准分析方法验证指导原则,需要考察系统测定条件有小的变动时,测定结果不受影响的程度。原子吸收光谱法测定钙离子的浓度,典型的变动因素有溶液的稳定性、燃气比例和供试溶液的温度,因此,从以下3个方面,考察该方法的耐用性。
1)溶液稳定性:按照供试溶液现用现配的原则,以及原子吸收光谱法含量测定迅速的特点,将溶液最长存放时间设定为3 h,考察3 h内供试溶液的稳定性。将配制好的供试溶液分别在存放时间为0、0.5、1、1.5、2、2.5、3 h后测定吸光度值。每个时间点重复测定3次,计算平均吸光度值,再计算7个时间段吸光度值的RSD值,要求RSD≤2%。结果如表2所示。
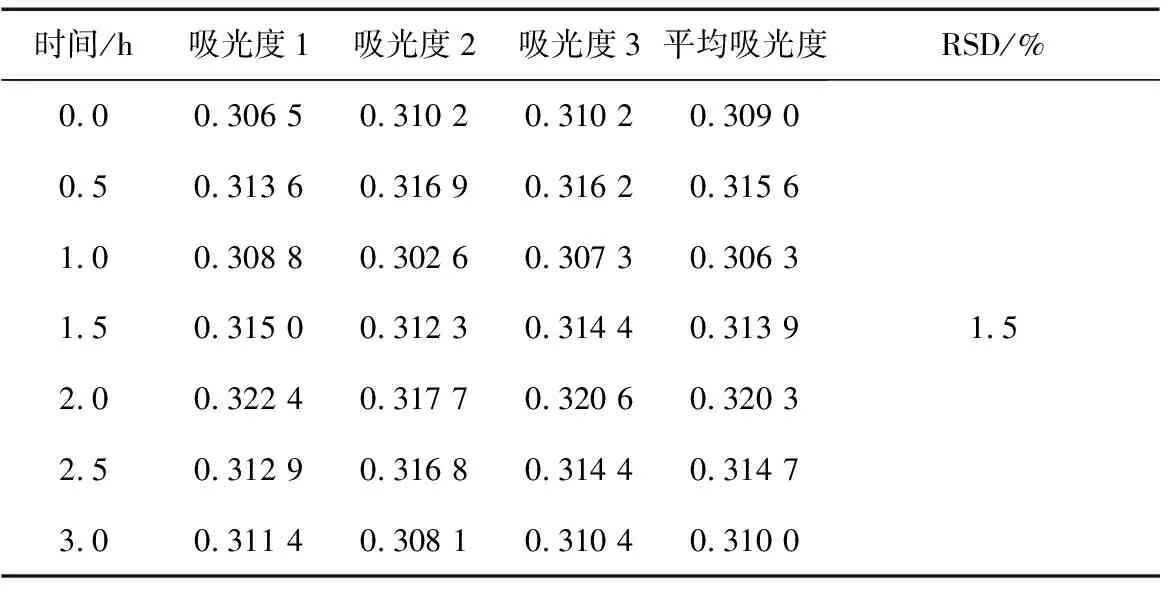
表2 溶液稳定性考察
由表2可知,供试样品3 h内7次吸光度测定结果的RSD值为1.5%,小于2%,说明3 h内测定样品结果差异微小,供试样品稳定性好。
2)燃气比例:燃气与助燃气之比小于化学计量比,火焰燃烧完全,氧化性强,不利于还原产物的形成,适用于钙的测定。本火焰原子吸收光谱仪测定钙默认的助燃比为13.5∶2.0,为了考察在偏离设备默认的助燃比的相对富燃焰对含量测定结果的影响,考察助燃比分别为13.5∶2.0、13.5∶2.2、13.5∶2.5条件下的吸光度值,每个助燃比平行测定3次,计算平均值,再计算3个助燃比条件下结果之间的RSD值,要求RSD≤2%。结果如表3所示。
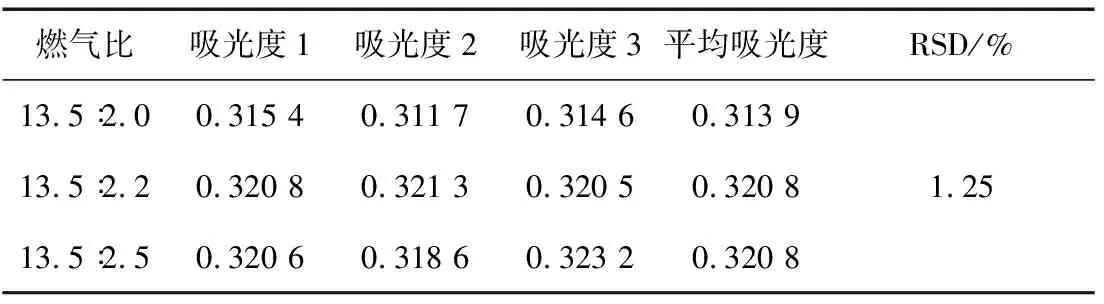
表3 燃气比例考察
由表3可知,3个助燃比条件下的平均吸光度值之间的RSD为1.25%,小于2%,说明钙离子在助燃比分别为13.5∶2.0、13.5∶2.2、13.5∶2.5的条件下,测定结果无明显差异。为了方便试验,助燃比选取13.5∶2.0。
3)供试溶液温度:供试溶液温度会影响到提升量和雾化效率。为了考察供试溶液温度(20~30 ℃)对含量测定结果的影响,将供试溶液分别放置在20、25、30 ℃的水浴锅中保温30 min后,按照原子吸收光度法测定供试样品溶液Ca2+的含量。每个温度条件下的样品测定3次,计算每个温度条件下的平均含量。计算3个温度条件下平均含量之间的RSD。检测结果如表4所示。

表4 溶液温度考察
由表4可知,溶液温度在20、25、30 ℃条件下,供试品Ca2+质量浓度的RSD值为0.36%。说明溶液温度在20~30 ℃之间,该测定方法能够对供试品的Ca2+质量浓度进行准确测定。
2.2.3 准确度考察(回收率)[8]
按照成品药液钙离子含量的80%、100%、120%,配制供试品溶液。于12个100 mL容量瓶中分别移取2.5 mL复方氯化钠注射液,再分别加入0.0、0.0、0.0、1.3、1.3、1.3、2.2、2.2、2.2、3.1、3.1、3.1 mL标准溶液母液,最后分别加入2 mL氧化镧溶液,用蒸馏水稀释,定容至刻度。按照原子吸收光度法进行连续测定,每个样品连续测定3次,分别计算各添加量下供试溶液含量的平均值。以标准母液添加量为0的样品的Ca2+含量为本底值,计算3个添加量下供试溶液的回收率,要求回收率应在98%~102%之间。结果如表5所示。
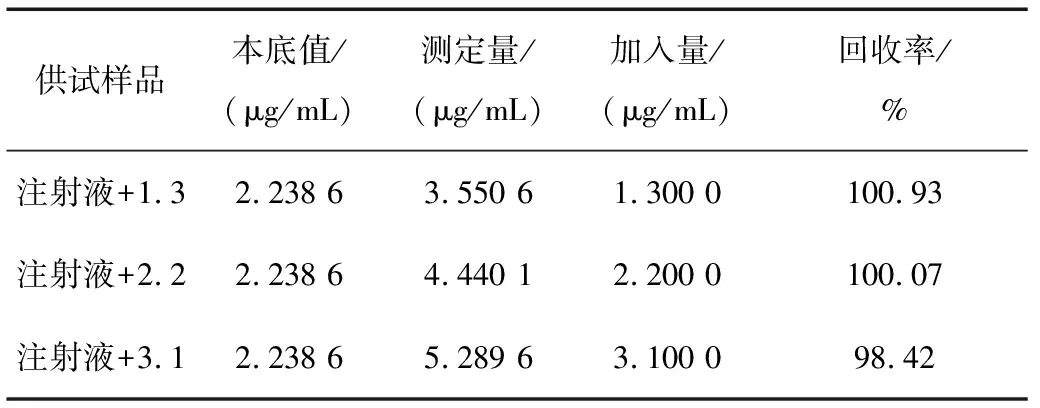
表5 回收率考察
由表5可知,3个添加量下供试溶液的回收率在98.42%~100.93%之间,说明该方法进行钙离子含量的测定,回收率符合要求,准确度好。
2.2.4 精密度考察
2.2.4.1 重复性[8]
重复配制6份供试样品溶液,按照原子吸收光度法进行连续测定供试品溶液Ca2+的质量浓度,每个样品连续测定5次,计算每个样品的平均质量浓度,再计算6个溶液平均质量浓度之间的RSD值,要求RSD值≤2%。结果如表6所示。

表6 重复性考察
由表6可知,6个溶液质量浓度之间的RSD为0.96%,低于2%,说明该方法测定供试品溶液中Ca2+的含量重复性好。
2.2.4.2 中间精密度[9]附录194-附录195
由试验操作人员A、B,分别于同一天配制3组平行供试样品,按照原子吸收光度法进行连续测定供试品溶液Ca2+的含量,每个样品测定5次,计算每个样品的平均质量浓度。再计算A、B两人共6个平均质量浓度之间的RSD值,要求RSD值≤2%。试验人员A于第2天,再次配制3组平行供试样品,测定供试样品溶液Ca2+的含量,每个样品测定3次,求得每个样品的平均质量浓度。再计算A第1天和第2天测得的6个平均浓度之间的RSD值,要求RSD值≤2%。结果如表7和表8所示。
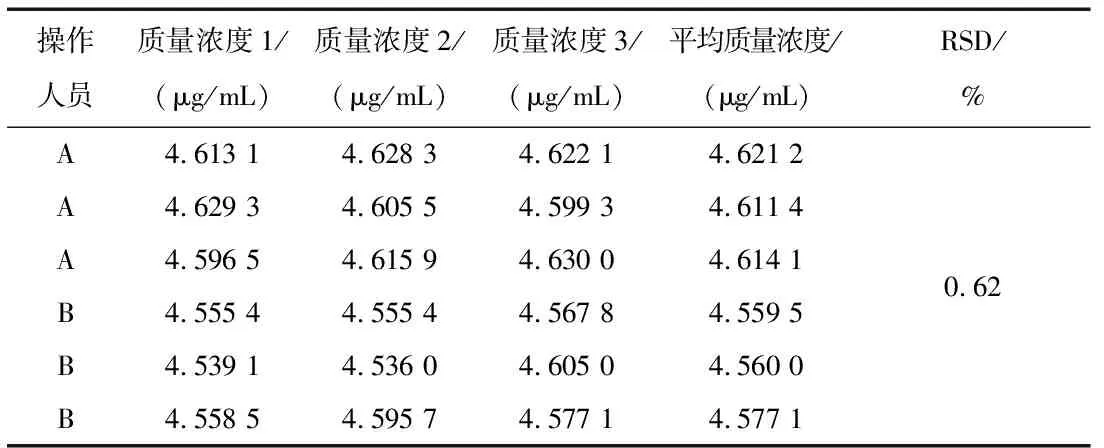
表7 组间精密度
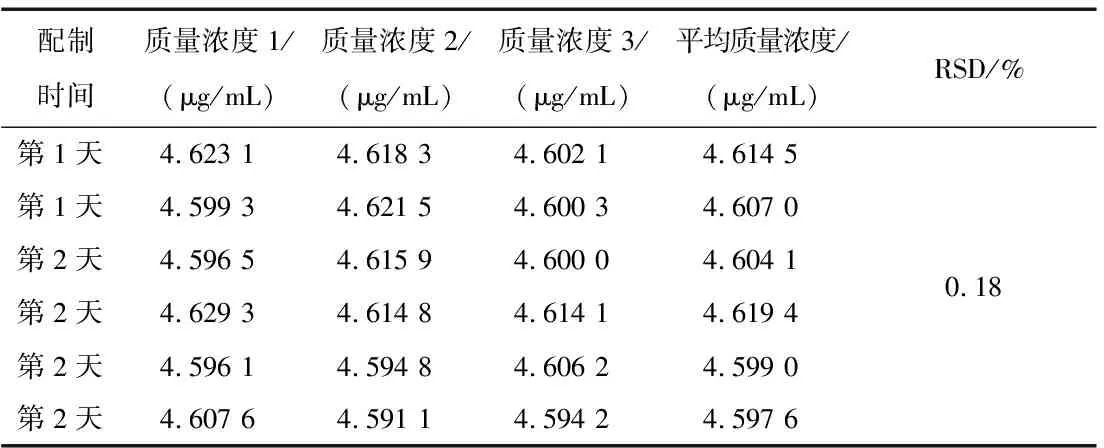
表8 日间精密度
由表7和表8可知,A、B两名试验操作人员测得的样品质量浓度之间的RSD值为0.62%,A操作人员两天测得的样品质量浓度之间的RSD值为0.18%,均小于2%,说明采用该方法测定Ca2+的含量,中间精密度好。
2.2.5 检测限[10]
按照原子吸收方法依次测定系列标准溶液的吸光度值,以质量浓度C为横坐标,吸光度值A为纵坐标做标准曲线,得到回归方程A=KC+b。然后连续测定空白溶液20次,计算20次含量测定的标准偏差S。根据下列方程计算检测限:
检测限=3×S/K
(1)
结果显示,线性回归方程为y=0.089 2x+ 0.009 4,即K为0.089 2,连续20次含量测定的标准偏差S为0.000 244,因此该方法进行钙离子含量的测定的检测限为0.008 206 μg/mL。
2.3 样品中氯化钙含量的测定
分别采用原子吸收光谱法和药典方法—络合滴定法进行复方氯化钠注射液中钙离子含量测定,再计算2种方法含量测定结果之间的RSD值,要求RSD值≤2%。
2.3.1 原子吸收光谱法
按照供试样品的配制方法,平行配制供试样品3个,按照原子吸收方法测定Ca2+的质量浓度C,每个样品测定3次,计算每个样品平均质量浓度。样品中CaCl2·2H2O的含量是测定出钙离子质量浓度后,按照下列方程式计算而得:
C(CaCl2·2H2O)=C(Ca2+)×3.676
(2)
2.3.2 络合滴定法[9]590
分别量取复方氯化钠注射液(批号20121101)100 mL,置于3个编号为1、2、3的200 mL锥形瓶中。分别加入1 mol/L氢氧化钠溶液15 mL和羟基萘酚蓝指示液3 mL,用0.025 mol/L乙二胺四乙酸二钠(EDTA-二钠)滴定液滴定溶液由紫红色变为纯蓝色。每1 mL EDTA-二钠滴定液相当于3.676 mg的CaCl2·2H2O。通过计算EDTA-二钠消耗体积,计算出CaCl2·2H2O含量。
2.3.3 两种方法测定结果
含量测定结果如表9和表10所示。

表9 原子光谱法含量测定结果

表10 络合滴定法含量测定结果
由表9和表10可知,原子吸收光谱法对复方氯化钠注射液(批号20121101)中CaCl2·2H2O的检测结果为0.032 929 6%~0.033 334 0% g/mL之间,络合物滴定法对复方氯化钠注射液(批号20121101)中CaCl2·2H2O的检测结果为0.033 488 4%~0.034 039 8% g/mL之间,均符合质量标准要求(含CaCl2·2H2O应为0.031%~0.035%g/mL)。并且2种方法含量检测结果之间的RSD值为1.21%,2种方法检测结果差异微小,原子吸收光谱法可以代替药典方法进行氯化钙含量测定。
3 结论
通过考察专属性,耐用性、准确度、精密度、检测限,采用原子吸收光谱法测定复方氯化钠注射液中氯化钙的含量,专属性好,精密度高,稳定性强,重复性好,并且对比药典方法,CaCl2·2H2O含量测定结果差异微小,且本法检测迅速,供试溶液配制方法简单,可以作为药典对复方氯化钠注射液钙含量测定的补充方法。
[1]王万铁.病理生理学[M].杭州:浙江大学出版社, 2009:12.
[2]杨凤琼.复方电解质葡萄糖R<,2>A注射液的研制[D].广州:广东工业大学,2008.
[3]李向荣.药剂学[M].杭州:浙江大学出版社, 2010:227.
[4]中华人民共和国卫生部.GB 5413.21—2010食品安全国家标准:婴幼儿食品和乳品中钙、铁、锌、钠、钾、镁、铜和锰的测定[S].北京:中国标准出版社,2010:1-7.
[5]黄北雄,陈启钊.火焰原子吸收法测定葡萄糖酸钙片的含量[J].中国医院药学杂志,2008,28(12):1040-1041.
[6]全英花,桂光云,王美玲,等.火焰光度法测定复方氯化钠注射液中氯化钾含量[J].中国药品标准,2008,9(5):358.
[7]黄北雄,陈启钊.火焰原子吸收法测定葡萄糖酸钙片的含量[J].中国医院药学杂志,2008,28(12):1041.
[8]毛士龙,吴亚利.火焰原子吸收光谱法测定复方醋酸钠注射液中钾含量[J].药物鉴定, 2010,19(9):31.
[9]中华人名共和国药典委员会.中华人民共和国药典:第二部 [K].北京:中国医药科技出版社, 2010.
[10]应英,汤鋆.原子吸收法测定滤膜中锡的方法学研究[J].中国卫生检验杂志,2011,21(9):2181.

