葛根饮片包装贮藏方法及其质量评价研究*
★ 钟凌云 马冰洁
(江西中医药大学药学院 江西 南昌 330004)
中药具有药源广泛,价格低廉,副作用小且疗效可靠的优点,故广受患者的青睐,但由于历史原因的影响,中药在包装、调剂、贮藏保存过程中依然存在不少问题,这直接影响中药的质量和疗效,甚至还可能因为包装运输不当而造成药品污染或产生不同程度的变质现象[1]。葛根是药食两用品种之一,作为一种流通及消耗量较大的大宗药材,其包装材料及储存条件的选择显得尤为重要。目前小包装饮片是饮片包装发展的重要趋势,本文模拟市售小包装饮片剂量,对葛根饮片从包装材料、包装条件以及贮藏条件等方面进行研究,并通过水分含量、浸出物含量、葛根素含量及微生物含量等构建葛根饮片小包装质量评价体系,为确立葛根饮片的包装贮藏条件奠定基础。
1 仪器与材料
1.1 仪器
封口机(周口佳特包装制品有限公司),Sartorius万分之一电子天平(梅特勒-托利多仪器上海有限公司),JZX-9070MBE数显鼓风干燥箱(上海博迅实业有限公司医疗设备厂),Sartorius万分之一电子天平(梅特勒-托利多仪器上海有限公司),Raytek Raynger ST20红外测温仪(美国雷泰公司(raytek)),中药粉碎机(长沙旭朗粉碎机械有限公司),50目标准筛(浙江省上虞市鑑湖仪器筛具厂),高效液相色谱仪(Dionex ΜLtiMate3000);PDA-3000二极管阵列紫外检测器;Chromeleon工作站。
1.2 材料
葛根饮片购自樟树天齐堂药业,经江西中医学院范崔生教授鉴定为豆科葛属多年生落叶藤本植物野葛Puerarialobata(wilId.)Ohwi的根;聚乙烯塑料袋,纸袋,铝箔袋。水为超纯水,氯化钠-蛋白胨缓冲液,乙醇为分析纯,葛根素对照品购自中国药品生物制品检定所,甲醇为色谱纯。
2 实验方法
2.1 葛根根饮片包装贮藏条件
2.1.1 葛根饮片小包装 根据2010版《药典》中葛根项下关于葛根饮片用量的规定,模拟市售小包装,每袋包装重量选为10g。分别采用聚乙烯塑料真空Ⅰ、聚乙烯塑料非真空Ⅱ、铝箔真空Ⅲ、铝箔非真空Ⅳ、纸袋非真空Ⅴ进行包装[2],以高温封口机封口使密封,60Co辐照,2k Gy灭菌。
2.1.2 储藏条件 中药饮片在生产、流通、贮藏过程中,保存条件一般可分为常温和低温两种,本课题结合实际需要,选定低温稳定性和常温稳定性两个方面对葛根饮片进行贮藏条件研究。
2.1.3 低温长期稳定性试验贮藏条件 不同包装材料和包装方法的葛根小包装饮片放置在冰箱内,温度设定为2~10℃,分别于于0,1,2,4,6,9,12个月检测水分、浸出物、葛根素含量及微生物限量。
1.2.4 常温长期稳定性试验贮藏条件 同包装材料和包装方法的葛根小包装饮片放置在常温留样室内,温度设定为10~30℃,室内具有一定的通风、光线及防蚊、防蝇、防鼠等设施,分别于0,1,2,4,6,9,12个月检测水分、浸出物、葛根素含量及微生物限量。
2.2 葛根饮片包装贮藏的检测研究[3]
2.2.1 水分测定研究 取供试品(先破碎成直径不超过3mm的颗粒)5g,平铺于干燥至恒重的扁形称量瓶中(厚度不超过5mm)精密称定,打开瓶盖在105℃干燥5h,将瓶盖盖好,移至干燥器中,冷却30min,精密称定,再在上述温度干燥1h,冷却,称重,至连续两次称重的差异不超过5mg为止。根据减失的重量,计算供试品中含水量。
2.2.2 浸出物含量测定研究 取供试品3克,精密称定,置于200mL的锥形瓶中,精密加入30%乙醇100mL,密塞,称定重量,静置1h后,连接回流冷凝管,加热至沸腾,并保持微沸1h。放冷后,取下锥形瓶,密塞,再称定重量,并用水补足减失的重量,摇匀,用干燥滤器滤过,精密量取滤液25mL,置已干燥至恒重的蒸发皿中,在水浴上蒸干后,于105℃干燥3h,置干燥器中冷却30min,迅速精密称定重量,得出浸出物含量。
2.2.3 葛根素含量测定研究[4]
2.2.3.1 色谱条件 色谱柱:Diamonsil C18(4.6mm×250mm,5μm);流动相:甲醇∶水(75∶25),检测波长:250nm,柱温:30℃,流速:1.0mL/min。
2.2.3.2 对照品溶液的制备 精密称取葛根素对照品2.5mg,置25mL容量瓶中,加30%乙醇溶液至刻度,摇匀,配成0.1mg/mL的溶液,作为对照品溶液。
2.2.3.3 供试品溶液的制备 取各样品粉末(过三号筛)约0.1g,精密称定,置具塞锥形瓶中,精密加入30%乙醇50mL,称定重量,加热回流30min,放冷,再称定重量,用30%乙醇补足减失的重量,摇匀,滤过,取续滤液,得供试品溶液。
2.2.3.4 标准曲线制备 精密吸取上述对照品溶液对照品溶液分别进样2.5,7.5,12.5,17.5,22.5μL以葛根素浓度X(μL/mL)为横坐标,峰面积Y为纵坐标,绘制标准曲线。得回归方程为Y=0.045X-0.8086(r=0.9997)。
2.2.3.5 精密度试验 精密吸取“2.2.3.2”项下对照品溶液10μL,按照上述色谱条件连续测定5次,记录峰面积,RSD为1.05%。
2.2.3.6 稳定性试验 取同一样品溶液,在相同的色谱条件下,在0,6,12,18,24h分别进样10μL,记录峰面积,RSD为0.91%。
2.2.3.7 重复性试验 精密称取同一样品5份,按“2.2.3.3”项下供试品的制备方法制备,分别测定,每次进样品10μL,RSD为1.42%。
2.2.3.8 加样回收率试验 精密称定已知含量的样品0.1g,精密添加一定量的葛根素对照品,按供试品的制备方法制备,依法测定,结果平均回收率为99.91%,RSD为0.31%。
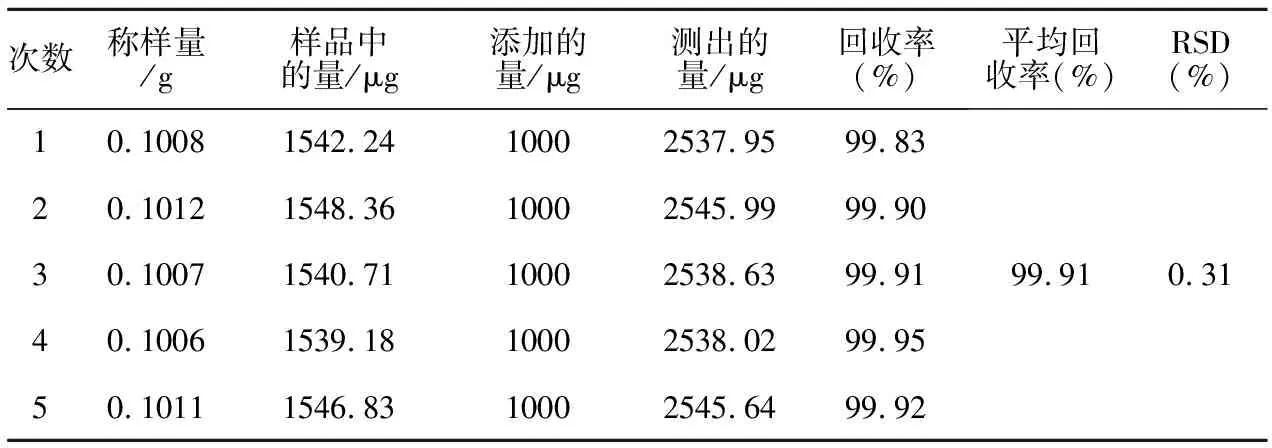
表1 葛根素加样回收率试验
2.2.4 微生物含量测定研究 以无菌操作称取检样5g,放入含45mL灭菌水的具玻塞锥形瓶中,振摇30min,即为1∶10稀释液。用灭菌吸管吸取1∶10稀释液10mL,注入灭菌试管中,另用1mL灭菌吸管反复吹吸50次,使霉菌孢子充分散开。取1∶10稀释液1mL注入含有9mL灭菌水的试管中,另换一支1mL灭菌吸管吹吸五次,此液为1∶100稀释液。
按上述操作做10倍递增稀释液,每稀释一次,换用一支1mL灭菌吸管,根据对样品的污染情况估计,选择三个合适的稀释度,分别在做10倍稀释液的同时,吸取1mL稀释液于灭菌平皿中,每个稀释液做2个平皿,然后将凉至45℃左右的培养基注入平皿中,并转动平皿使之与样液混匀,待琼脂凝固后,倒置于25℃~28℃温箱中,3d后开始观察,共培养观察5d。
计算方法:通常选择菌落数在10~150之间的平皿进行计数,同稀释度的两个平皿的菌落平均数乘以稀释倍数,即为每克检样中所含霉菌和酵母菌数。
2.3 结果
不同包装材料、包装方式和贮藏条件下水分、浸出物、葛根素和微生物含量结果见图1-6。
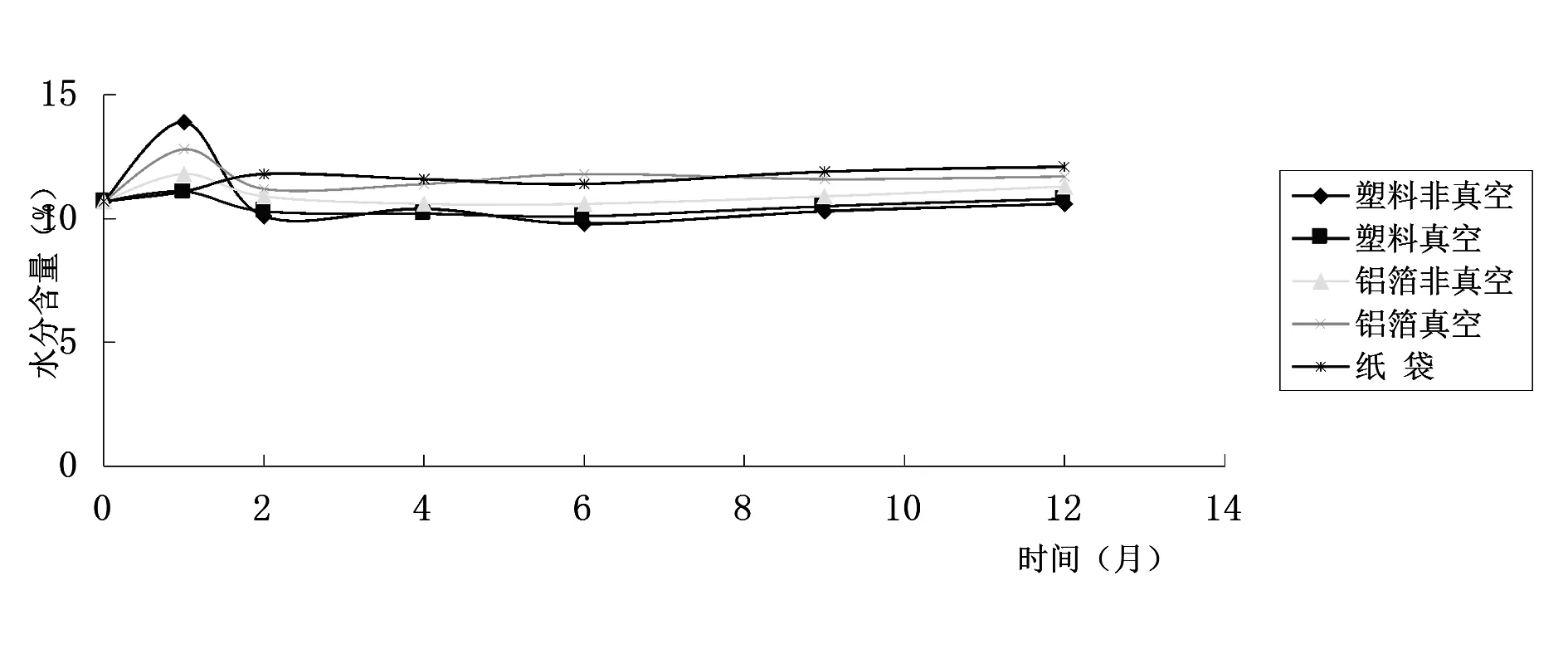
图1 低温条件下葛根饮片水分含量趋势图
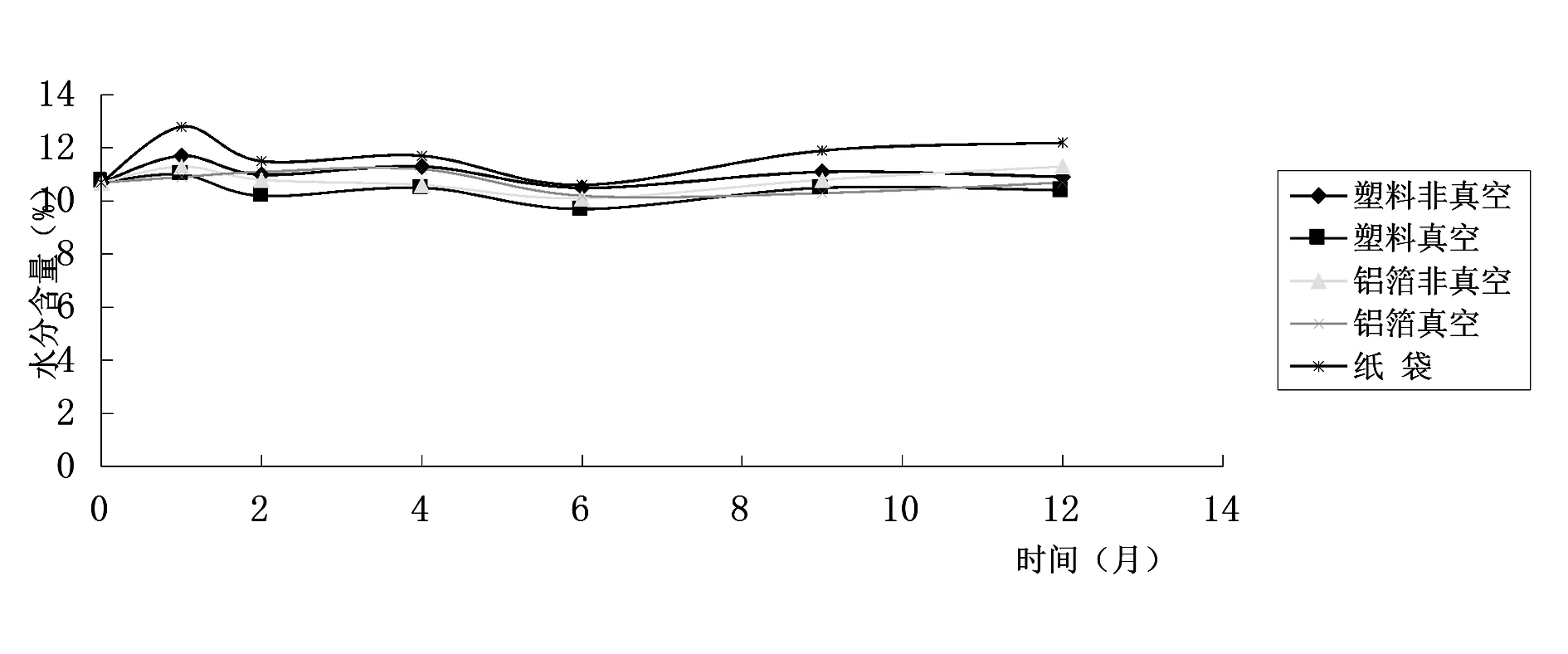
图2 常温条件下葛根饮片水分含量趋势图
从低温及常温条件下水分含量可以看出,纸袋包装的葛根饮片水分含量较高,其他包装材料及条件的葛根饮片水分含量差别不大;不同包装贮藏条件下葛根饮片水分含量随时间变化不明显。
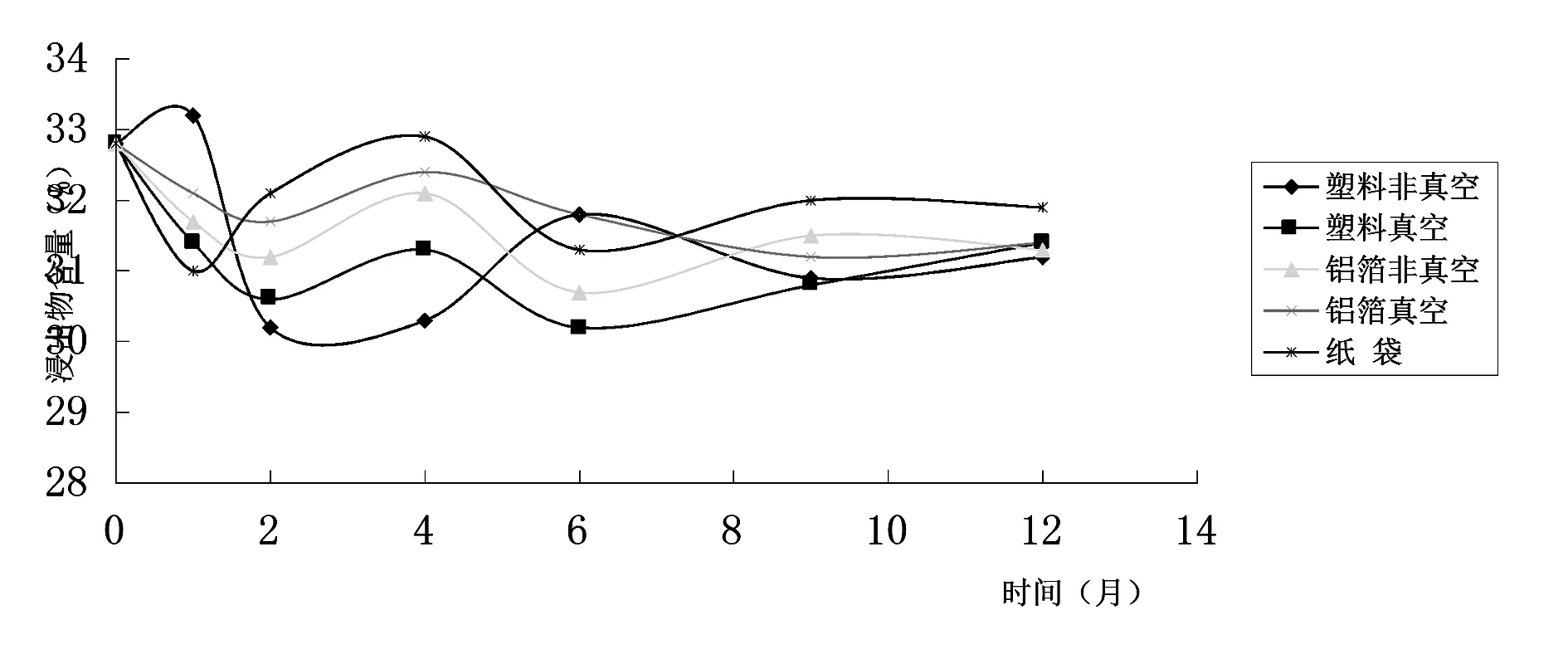
图3 低温条件下葛根饮片浸出物含量趋
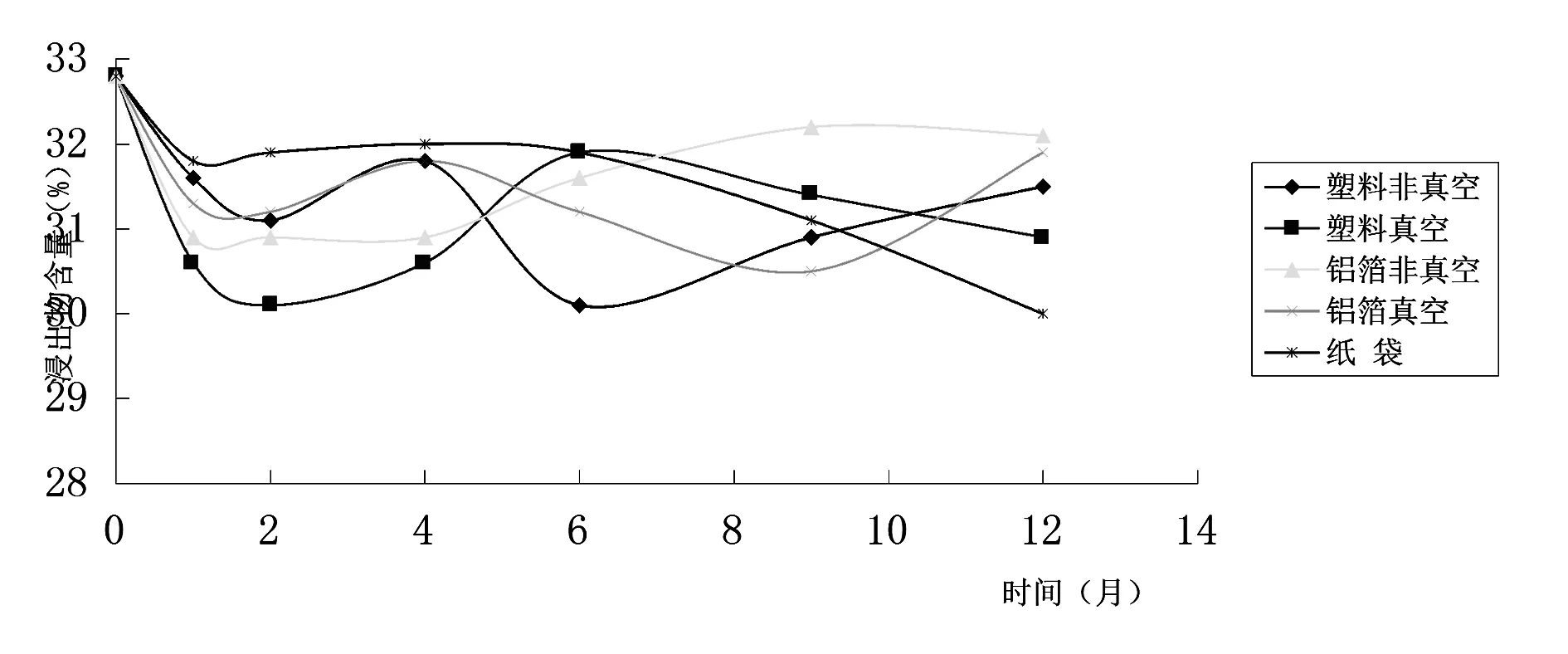
图4 常温条件下葛根饮片浸出物含量趋势图
从低温及常温条件下葛根饮片浸出物含量可以看出,浸出物含量整体趋势随着时间变化而减少,但减少幅度不大,基本能符合2010版药典中关于葛根饮片浸出物含量的要求。
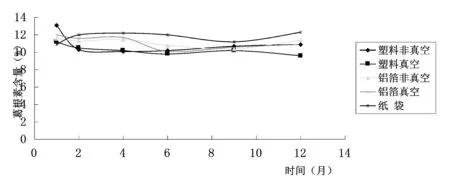
图5 低温条件下葛根饮片葛根素含量趋势图
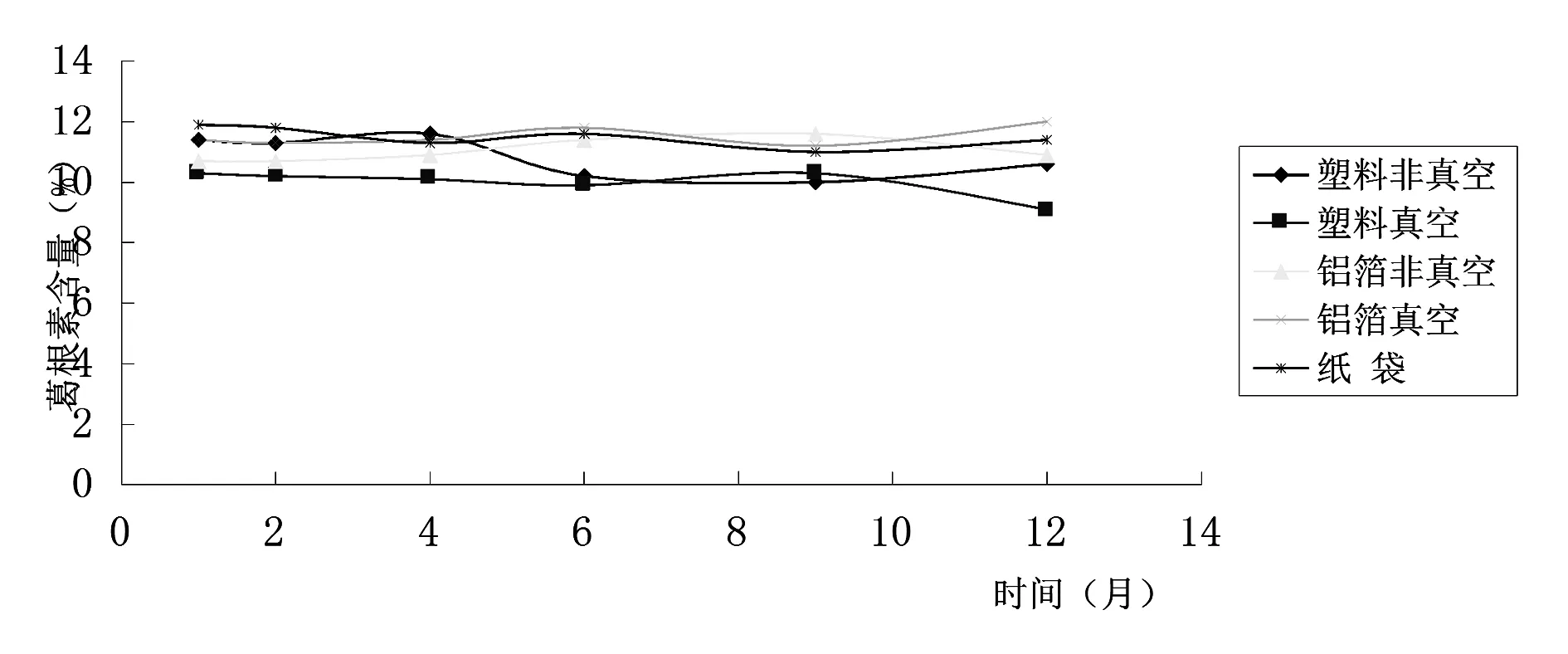
图6 常温条件下葛根饮片葛根素含量趋势图
从低温及常温条件下葛根饮片葛根素含量变化可以看出,不同包装贮藏条件下葛根饮片中葛根素含量差别不大,其中常温下铝箔真空包装含量较高,低温下纸袋包装含量较高;不同包装贮藏条件下葛根饮片中葛根素含量随时间变化不明显。
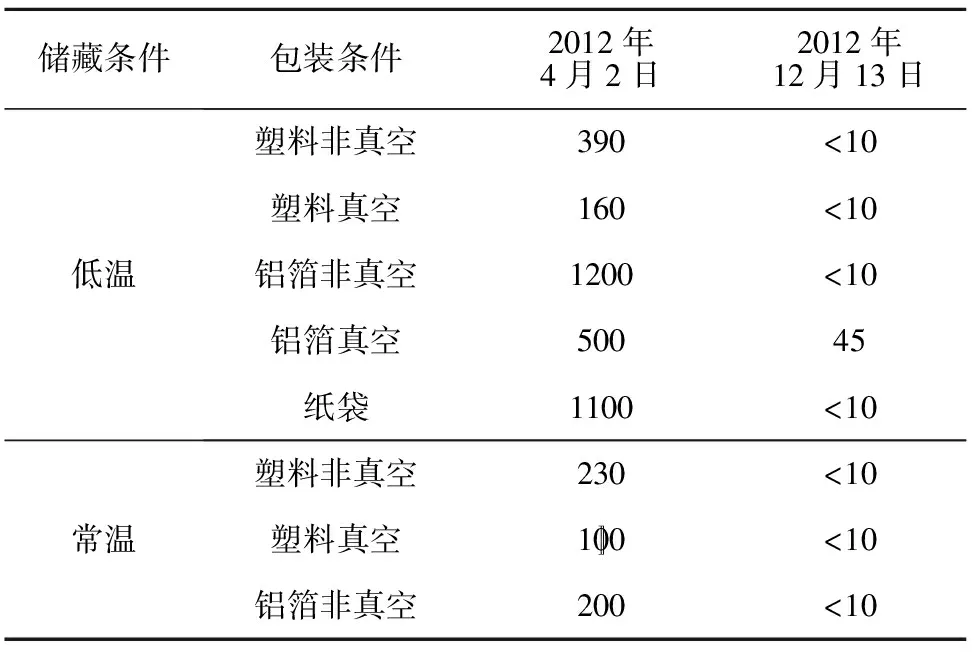
表2 不同包装贮藏样品中霉菌和酵母菌量(cfu/g)
从低温及常温条件下葛根饮片微生物变化可以看出,葛根饮片中霉菌和酵母菌含量经过一段时间贮藏后显著减少。
3 小结与讨论
从低温及常温条件下水分含量、浸出物、葛根素含量和微生物限量结果可以看出,除了纸袋包装的葛根饮片水分含量变化较大外,其他包装材料及条件的葛根饮片水分含量差别不大,随时间变化不明显;浸出物含量整体趋势随着时间变化而减少,但减少幅度不大,基本能符合2010版药典中关于葛根饮片浸出物含量的要求;葛根素含量差别不大,其中常温下铝箔真空包装含量较高,低温下纸袋包装含量较高;霉菌、酵母菌量贮藏一段时间后,饮片中微生物的量急剧减少。综合经济因素考虑,选择塑料非真空包装、常温贮藏可作为葛根小包装饮片的包装贮藏条件。
中药小包装饮片有利于饮片的保管、贮藏、运输,还能保证饮片的质量和卫生[5]。目前的小包装饮片包装材料有很多,以聚乙烯塑料使用为多.塑料透明度高,便于饮片质量检查及性状鉴别,但是长期存储可能会与饮片成分产生化学性反应,同时塑料还存在着一定的致癌、环境污染等安全隐患[6]。本课题仅针对12个月内葛根饮片的包装贮藏方法及进行质量评价研究,但对于长期贮藏对其质量的影响尚未开展研究,还有待于进一步考察。此外,饮片生产企业则应从保证饮片产品质量和方便消费者使用这两点出发,根据饮片的成分、性状、使用等多方面综合考虑饮片包装材料的选择及适宜的贮藏条件,为中药饮片小包装的推广应用奠定基础。
[1]朱卫星,李爱光,陈方,等.中药包装贮藏的研究概况[J].时珍国医国药,2006,17(11):2 304-2 305.
[2]王添生,何新荣.对中药饮片小包装规格的探讨[J].广东药学院学报,2004,20(2):107-108.
[3]国家药典委员会.中国药典.一部[S].北京:中国医药科技出版社,2010.
[4]黄建锋,周清,戚海英,等.广东不同产地葛根中葛根素和大豆苷元的含量测定[J].广东药学院学报,2013,4:013.
[5]何玉华.中药饮片小包装与中药调配[J].中国医院药学杂志,2007,27(4):549-550.
[6]楼步青,林华.中药饮片小包装的质量控制[J].时珍国医国药,2008,19(12):3 071-3 071.

