注射用硝普钠在葡萄糖注射液中稳定性考察
林小明,韦宝含,曾 毅,韦平原,梁汉钦,谢伟乾,陈明忠
0 引言
注射用硝普钠(SNP)是一种速效和短时作用的血管扩张药[1-2],目前广泛地用于治疗高血压急症和急性心力衰竭,是治疗高血压急症及急性心力衰竭的常用药物[3]。此外,硝普钠还可用于控制术中出血和主动脉手术、嗜铬细胞瘤手术、心脏手术引起的高血压[4]。由于其水溶液不稳定[3],见光易分解生成氰化物,输入体内增加对人体的毒性,临床上需临用前配制,避光使用[5]。但其溶液避光保存和应用的时间目前有关文献和各生产厂家说明书尚未有统一观点,有文献认为24 h[3-6],也有文献认为12 h[3-5]、8 h[7]、或6 h[8]、4 h[9]。出现这样不同的结论,可能与使用药物的环境有关。为解决这一问题,我们对SNP与5%葡萄糖注射液(5%GS)的配伍液,在不同环境条件下进行了稳定性研究,现报道如下。
1 仪器与试药
仪器:SSI1500高效液相色谱仪(美国Scientific Systems Inc);GWF-5J 型微粒分析仪(天河医疗器械设备有限公司);pHS-2C型精密酸度计(上海雷磁仪器厂);UV-2401可见紫外分光光度仪(日本岛津)。试药:SNP(晋城海斯制药有限公司,规格:50 mg,批号:20120501)。5%GS(广西裕源药业有限公司,规格:500 mL,批号:L12101908);硝普钠对照品(中国药品生物制品检定所,批号:101137-201101);甲醇为色谱纯;硫酸氢铵四丁基为色谱纯;磷酸氢二钠、磷酸等为分析纯。
2 方法与结果
2.1 试验用水制备 取注射用水,用0.45 μm微孔滤膜过滤,初滤液弃去,得试验用水。经检测符合中国药典2010版微粒检查用水有关规定。
2.2 试验用具准备 于层流净化台上将试验用具用试验用水冲洗至洁净,备用。
2.3 考察溶液的配制 根据药品说明书规定的浓度范围,取SNP 5支,分成C、D 2份,C份4支,D份1支,在层流净化台上,分别用5%GS 1 000 mL溶解成C(0.2 mg/mL)、D(0.05 mg/mL)两组溶液,摇匀。
2.4 考察条件
2.4.1 取新配制的C、D 两组溶液在规定条件下(用避光套避光:于20 ℃室温下,于35 ℃水浴中;无避光套避光:于20 ℃室温下,于35 ℃水浴中)放置,分别于0~26 h中每隔2 h取样对配伍液稳定性进行考察。
2.4.2 取新配制的C、D 两组溶液在规定条件下(无避光套,于20 ℃室温下,于35 ℃水浴中,距溶液20 cm处,用150 W白炽灯光照射)分别放置0~130 min,每隔10 min取样对配伍液稳定性进行考察。
2.4.3 取新配制的C、D 两组溶液在规定条件下(用避光套避光,于20 ℃室温下,于35 ℃水浴中,距溶液20 cm处,用150 W白炽灯光照射)分别放置0~260 min,每隔20 min取样,对配伍液稳定性进行考察。
2.5 考察指标和测定方法 在层流净化台上采样,按性状、pH值、不溶性微粒、紫外-可见吸收光谱、含量的顺序进行观察及测定。
2.5.1 性状 取配伍溶液,在澄明度检测仪白色、黑色的背景下各观察6 s。内容包括颜色、可见异物。
2.5.2 pH 用酸度计测定溶液的pH。
2.5.3 不溶微粒 按《中国药典》2010年版微粒检测法中的光阻法检查。
2.5.4 紫外-可见吸收光谱 用紫外-可见分光光度计,于200~760 nm波长范围内扫描,以同批溶媒为空白对照。
2.5.5 含量 按文献[10-11]报道方法测定。
2.6 考察结果
2.6.1 溶液外观性状的变化 在室温20 ℃及水浴35 ℃,室内自然光照条件下,有避光套避光时:C、D 两组SNP溶液在0~26 h各时间点溶液的颜色均为淡棕色,无可见变化,澄明度符合规定,未发现可见异物。无避光套避光时,溶液澄明度均符合规定,未发现可见异物,但是C、D 两组SNP溶液颜色随放置时间延长而发生改变。室温20 ℃时,C、D 两组溶液均在12 h开始变为淡黄色,至26 h时变为黄色。水浴35 ℃时,C、D 两组溶液均在4 h开始变为淡黄色,至16~20 h变为黄色,22~26 h时变为深黄色。
在实验室内用150 W白炽灯相距20 cm照射下,C、D 两组溶液颜色随放置时间延长而发生改变,在相同温度和光照条件下,无避光套避光组比有避光套避光组变化迅速。在光照和避光条件相同时,35 ℃比20 ℃变化迅速。溶液澄明度均符合规定,未发现可见异物。
无避光套避光:在20 ℃时,C、D 两组溶液变为蓝色时间均为40 min。在35 ℃时,C、D 两组溶液变为蓝色时间均为30 min。有避光套避光:在20 ℃时,C、D 两组溶液变为蓝色时间均为160 min。在35 ℃时,C、D 两组溶液变为蓝色时间均为100 min。
2.6.2 溶液pH值的变化 室内自然光,有避光套避光,在室温20 ℃及水浴35 ℃的条件下,C、D 两组SNP溶液在0~26 h各时间点的pH值均无明显变化,见图1。

图1 避光,室温20 ℃和水浴35 ℃时不同时间硝普钠配伍溶液的pH值
室内自然光,无避光套避光,在室温20 ℃及水浴35 ℃的条件下,C、D 两组SNP溶液在0~26 h各时间点溶液的pH值随放置时间延长而发生变化,C、D 两组溶液pH值均先变小后升高。在20 ℃时,C、D 两组溶液pH值降至最小的时间均为放置12 h时,以后逐渐升高;在35 ℃时,C、D 两组溶液pH值降至最小时间均为放置4 h时,以后逐渐升高。见图2。从图2可以看出:无避光套避光时,溶液pH值变化与浓度大小无关,与温度有一定关系,35 ℃比20 ℃变化更快。
从图3~4可以看出:在实验室内用150 W白炽灯相距20 cm照射条件下,溶液pH值随放置时间延长而发生改变,溶液pH值均先变小后升高。在相同温度和光照条件下,无避光套组比有避光套组变化迅速。在相同的光照和避光条件相同时,35 ℃比20 ℃变化迅速。溶液pH值变化与SNP浓度不显相关性。
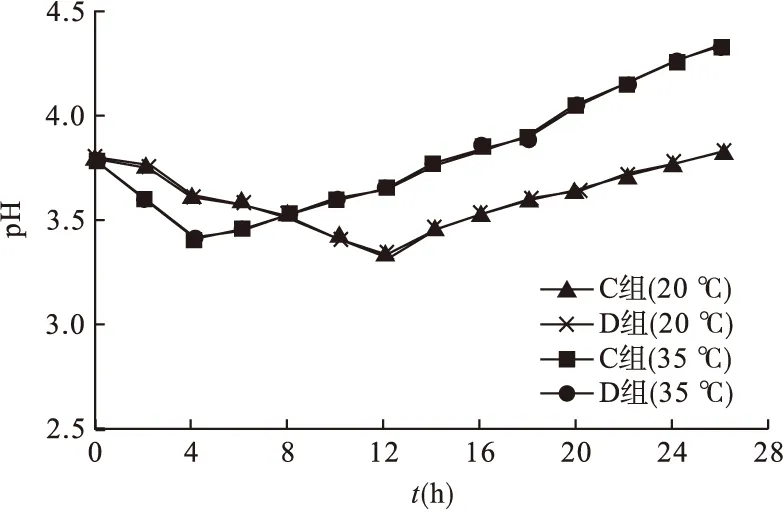
图2 未避光,室温20 ℃和水浴35 ℃条件下不同时间硝普钠配伍溶液的pH值
无避光套避光:C、D 两组溶液pH值,在20 ℃时变至最小时间为放置20 min,在35 ℃时变至最小时间为放置10 min,见图3。
有避光套避光:C、D 两组溶液pH值,在20 ℃变至最小时间为放置80 min,在35 ℃时变至最小时间为放置40 min,见图4。

图3 未避光,室温20 ℃和水浴35 ℃,150 W白炽灯照射条件下不同时间硝普钠溶液的pH值
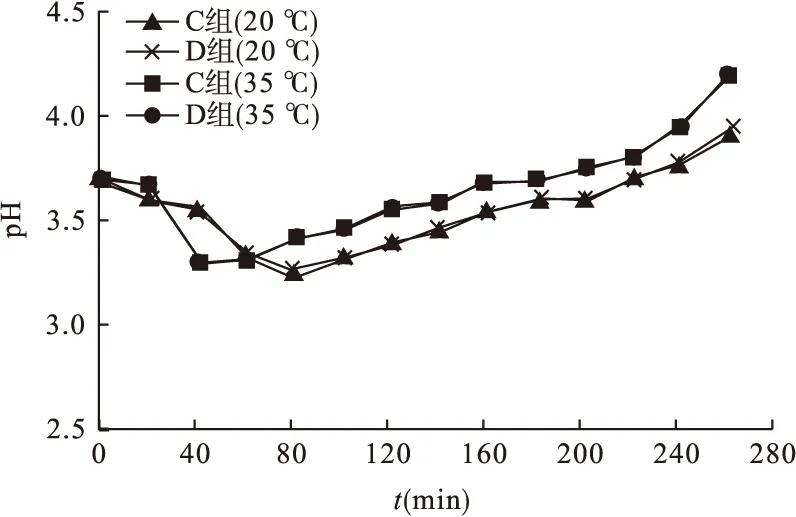
图4 避光,室温20 ℃和水浴35 ℃,150 W白炽灯照射条件下不同时间各硝普钠溶液的pH值
2.6.3 溶液不溶性微粒变化 C、D 两组 SNP溶液在实验规定的各种条件下,在各时间观察点其不溶性微粒均符合《中国药典》2010年版有关规定。
2.6.4 溶液紫外—可见吸收光谱的变化 室内有避光套避光,在室温20 ℃及 水浴35 ℃条件下,C、D 两组SNP溶液在0~26 h各时间点的紫外-可见吸收光谱无明显改变。见图5。
室内无避光套避光,在室温20 ℃及 水浴35 ℃条件下,C、D 两组SNP溶液在0~26 h各时间点的紫外-可见吸收光谱随着时间延长而出现改变,其变化为在254 nm处吸收峰呈逐渐降低,394 nm处吸收峰呈逐渐升高。从光谱的图形无法判断20 ℃与35 ℃两者之间的变化差异。见图5。
在室内无避光套或有避光套避光,用150 W白炽灯相距20 cm照射条件下,C、D 两组SNP溶液在各时间观察点紫外-可见吸收光谱出现了明显变化。其变化为随时间延长,在254 nm处吸收峰呈逐渐降低,394 nm处吸收峰呈逐渐升高。在相同的条件下,有避光套组比无避光套组变化慢。从光谱的图形看,相同条件下20 ℃与35 ℃两者之间无明显的差异。见图5。

图5 C组溶液在不同条件下放置的光谱吸收
2.6.5 溶液硝普钠含量变化 有避光套避光,在室温20 ℃及 水浴35 ℃条件下,C、D 两组SNP溶液在0~26 h各时间点的SNP含量无明显改变。结果见图6。
无避光套避光,在室温20 ℃及 水浴35 ℃条件下,C、D 两组SNP溶液在0~26 h各时间点的SNP含量均随着时间延长逐渐降低,并且35 ℃时比20 ℃时下稍快。见图7。
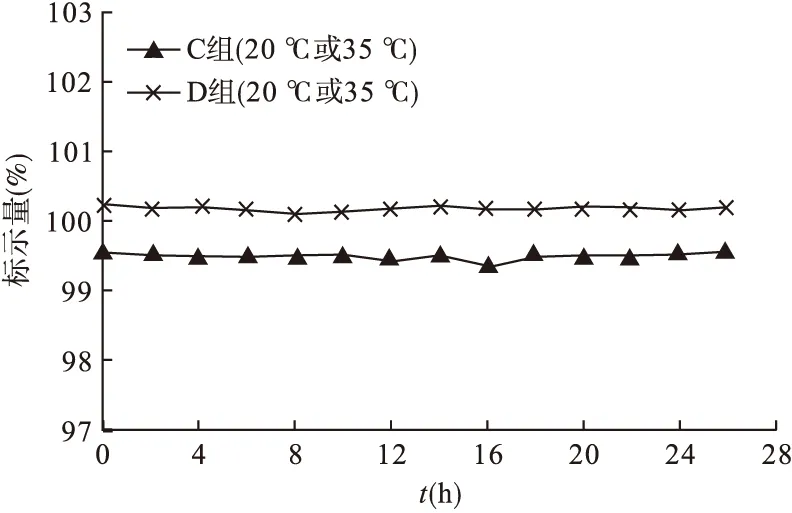
图6 避光,室温20 ℃及水浴35 ℃条件下不同时间硝普钠的含量

图7 未避光,室温20 ℃及水浴35 ℃条件下不同时间硝普钠的含量
在室内无避光套或有避光套避光,用150 W白炽灯相距20 cm照射条件下,C、D 两组SNP溶液在各时间观察点SNP含量均随着时间延长而逐渐降低。从图8和图9可以看出:在相同温度和光照条件下,有避光套组下降缓慢,无避光套组下降迅速;避光条件和光照条件相同时,35 ℃时比20 ℃时下降快。

图8 避光,室温20 ℃和水浴35 ℃,150 W白炽灯照射条件下不同时间硝普钠的含量
3 讨论
3.1 光照是影响SNP的5%GS溶液稳定性的重要因素,溶液的稳定性与光照的强度密切相关,光照强度越强,SNP的分解就越快。本试验果表明:在用避光套避光,且无强光照射条件下,SNP的5%GS溶液于室温20 ℃或水浴35 ℃中放置26 h质量均无变化。但无避光条件下,SNP的5%GS溶液不稳定;即使有避光套避光,在强光照射下,SNP的5%GS溶液的稳定性也受影响,这说明避光套对强光不能完全避光,只能减弱光照。因此,临床无论是配制还是使用SNP的5%GS溶液均应严格避光,即使使用避光套避光,也要避免阳光和强光照射,从而保证临床用药安全有效。

图9 未避光,室温20 ℃和水浴35 ℃,150 W白炽灯照射条件下不同时间硝普钠的含量
3.2 在严格避光、温度于20~35 ℃的条件下,26 h内温度对SNP的5%GS溶液的稳定性没有影响。不避光,或避光不严时,药物的分解与温度有关,温度越高,分解越快。本试验研究结果也表明了SNP的5%GS溶液浓度为0.2~0.05 mg/mL时,药物的降解与浓度无关,这说明临床应用使用这一浓度范围是有科学道理的。
3.3 本项研究之所以选择室温20 ℃和水浴35 ℃作为考察温度,主要是考虑南方北方或季节变化而造成的环境温度不同可能对SNP的5%GS溶液稳定性产生的影响。研究结果表明,SNP的5%GS溶液配制使用过程中只要严格避光,地域或季节温度差异对其稳定性没有影响。
3.4 本研究结果表明 不同的避光条件,SNP的5%GS溶液外观或其内在质量变化时间不同。因此,文献记载[3-5,7-9]或各厂家说明规定使用时间有较大的不同(分别为24 h和12 h、8 h、6 h、4 h)可能与实验观察条件不同有关。综上所述,5%GS作为SNP的溶媒,在严格避光的条件下,溶液从配制到使用完全控制在26 h内是科学的,且可减少药物的浪费,减轻患者经济负担,减少护理人员工作量。
参考文献:
[1] 黄竟,刘芳,翟所迪.硝普钠致氰化物中毒及其防治[J].药物不良反应杂志,2007,9(4):267-271.
[2] 赵妙珍,靳增录.硝普钠临床应用疗效分析[J].长治医学院学报,2003,17(2):106:107.
[3] 徐中林,赵义发,吴兰兰.硝普钠临床应用的有效性和安全性回顾性分析[J].重庆医科大学学报,2003,31(1):110-112.
[4] 张亚娜,高艳萍.硝普钠的临床应用[J].中国现代药物应用,2009,3(10):105-106.
[5] 陈新谦,金有豫,汤光.新编药物学[M].第17版.北京:人民卫生出版社,2011:405.
[6]开月梅,丁小容,胡金森.硝普钠溶液配置后不同时间段的稳定性[J].罕少疾病杂质,2004,11(5):24-25.
[7]张家铨,吴景时,程鹏.常用药物手册[M].北京:人民卫生出版社,2000:237-238.
[8]张振路.临床护士药物使用手册[M].广州:广东科技出版社,2003:87-88.
[9]徐叔云.中华临床药物学[M].北京:人民卫生出版社,2003:808.
[10]林小明,韦宝含,曾毅,等.HPLC法测定硝普钠氯化钠注射液中硝普钠的含量[J].北方药学,2013,10(12):11-12.
[11]林小明,韦宝含,曾毅,等.HPLC法测定硝普钠葡萄糖注射液中硝普钠的含量[J].临床合理药杂志,2014,7(3):84-85.

