锰铁冶炼烟尘灰中锰锌的浸出实验研究
杨逢时,苏毅,李国斌,胡亮
(昆明理工大学化工学院,云南 昆明 650500)
锰铁冶炼烟尘灰是电炉法高温还原生产锰铁合金时产生的烟尘经收尘得到的工业粉状废渣,主要含有铁、锰、锌、钾等元素,是一种很好的二次资源。但由于其含Mn、Zn量较低,使其回收利用较为困难,目前工业上主要是将该烟尘灰与细粒锰精矿混合烧结[1],返回生产系统循环利用,但该法烟尘损失大,且在返回利用时会影响锰铁合金冶炼的正常炉况。
本试验通过水浸提取烟尘灰中的钾元素,同时富集原料中的锰锌元素,然后再通过在还原剂[2-5]存在的条件下酸浸分离出 Mn、Zn,以期达到同时回收Mn、Zn元素的目的,可为锰铁冶炼烟尘灰的综合利用提供一条有效的途径,实现二次资源的综合利用,达到节能减排的目的。
1 实验部分
1.1 实验原料
实验所用原料锰渣为广西某公司锰铁冶炼烟尘灰,其主要成分如表1所示,实验中其他试剂均为分析纯。

表1 原料的主要成分质量分数 单位:%
该烟尘灰的主要成分有锰、钾、锌等,对于含量较高的钾,采用水浸出的方法对其进行预处理,以提取钾元素。取1kg锰废渣加入2L水,室温搅拌1h,使可溶性钾盐溶于水,过滤后用1500mL水分3次洗涤滤渣,干燥并研磨,留待后续酸浸实验使用。
1.2 实验方法
在 500mL三口烧瓶中加入质量分数为 10%~35%的硫酸溶液,在室温~90℃水浴锅控温、不断搅拌的条件下加入处理后的锰渣 60g,加入还原剂FeSO4·7H2O,使高价态的锰还原成 Mn2+,反应时间1~6h。反应结束后用氨水调pH值至4~5,继续搅拌半小时,使Fe3+以沉淀形式水解析出,过滤收集浅棕色滤液,留待后续实验处理。用150mL水分3次洗涤滤饼,将滤渣干燥恒重后,称重并研磨,分析其锰、锌含量,从而得到锰和锌的浸出率。主要反应方程式如式(1)。
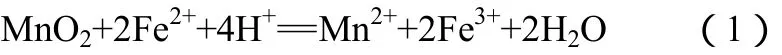
1.3 分析方法
1.3.1 锰的分析
按GB/T 1506—2002《锰矿石锰含量的测定电位滴定法和硫酸亚铁铵滴定法》的硫酸亚铁铵方法进行分析。
1.3.2 锌的分析
按GB/T 14353.3—1993方法进行分析。
2 结果与讨论
2.1 原料水浸出处理
对水浸出处理后的锰渣原料进行分析,其主要成分如表2所示。经水浸出烟尘灰,原料中钾含量由17.26%降至5.93%,同时锰含量由20.37%提高至30.23%,锌含量由8.95%升至12.68%,从而达到了浸取钾元素、富集锰锌元素的目的。
2.2 硫酸浓度对浸出率的影响

表2 处理后锰渣的主要成分质量分数 单位:%
图1为 H2SO4质量分数对 Mn、Zn浸出率的影响。实验条件:处理后的锰渣60g,液固比(mL/g)为5∶1,搅拌速率300r/min,反应温度90℃,反应时间4h,FeSO4·7H2O用量55g。由图1可以看出,锰和锌的浸出率受硫酸浓度的影响较大,随着硫酸质量分数的提高,呈现“~”型的变化趋势。当硫酸质量分数在20%时,锰浸出率达到94.41%,锌的浸出率为82.71%,均达到最高值。当硫酸质量分数>20%,硫酸逐渐过量,反应终点调pH值至4~5,所加浓氨水也增加,成本增加,且导致过滤时有白色晶体析出,过滤困难。因此,本实验选择H2SO4质量分数20%为本实验最佳工艺。
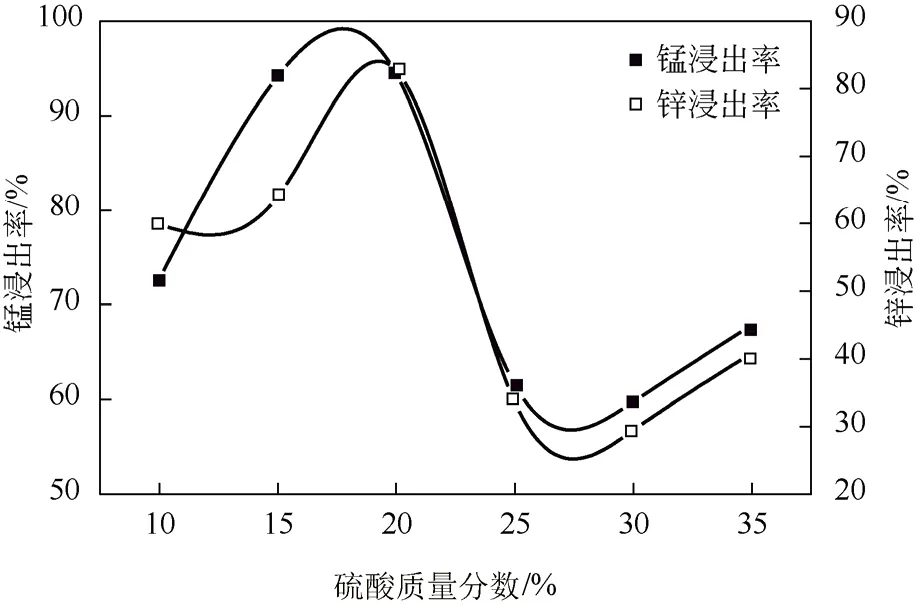
图1 H2SO4质量分数对Mn、Zn浸出率的影响
2.3 反应时间对浸出率的影响
图2为反应时间对Mn、Zn浸出率的影响。实验条件:处理后的锰渣60g,液固比(mL/g)为5∶1,硫酸质量分数20%,搅拌速率300r/min,反应温度90℃,FeSO4·7H2O用量55g。由图2可以看出,随着反应时间的增加,锰浸出率呈现W型波动,锌浸出率呈现先增后减的趋势。当反应时间在4h时,锰和锌的浸出率均达到最高值。因此,本实验选择反应时间4h为本实验最佳工艺。
2.4 反应温度对浸出率的影响
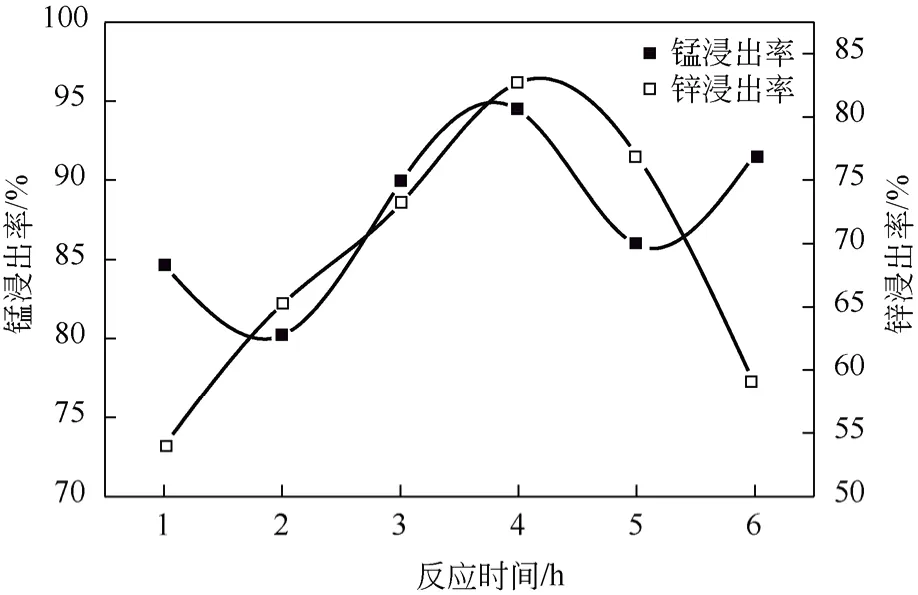
图2 反应时间对Mn、Zn浸出率的影响
图3为反应温度对Mn、Zn浸出率的影响。实验条件:处理后的锰渣60g,液固比(mL/g)为5∶1,硫酸质量分数 20%,搅拌速率 300r/min,反应时间4h,FeSO4·7H2O用量55g。由图3可以看出,随着反应温度的提高,锰锌浸出率呈现明显的增加趋势。当反应在室温(25℃)进行时,此时没有采用水浴锅控温,由于反应自身放热,体系温度实际为45~50℃,导致锰锌浸出率趋势异常偏高。当温度为90℃时,锰锌浸出率最高。因此,本实验选择反应温度90℃为本实验最佳工艺。
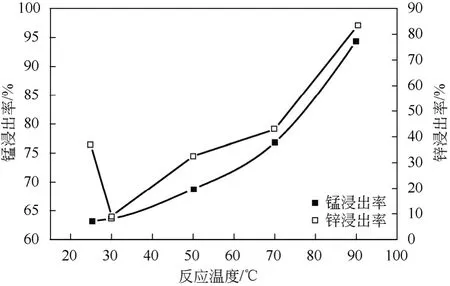
图3 反应温度对Mn、Zn浸出率的影响
2.5 液固比对浸出率的影响
图4为液固比对Mn、Zn浸出率的影响。实验条件:处理后的锰渣60g,硫酸质量分数20%,搅拌速率 300r/min,反应温度 90℃,反应时间 4h,FeSO4·7H2O用量55g。由图4可以看出,随着液固比的增加,锰锌浸出率均呈现明显的先增后减趋势。当液固比为4∶1时,锌浸出率达到88.87%;当液固比为5∶1时,锰浸出率提高至94.41%,锌浸出率下降至82.71%。考虑到锰渣处理主要是锰的回收利用,因此,本实验选择液固比5∶1为本实验最佳工艺。
2.6 FeSO4·7H2O加入量对浸出率的影响
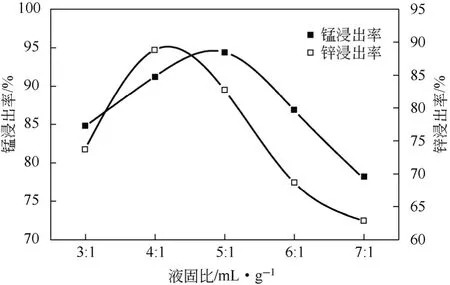
图4 液固比对Mn、Zn浸出率的影响
图5为FeSO4·7H2O加入量对Mn、Zn浸出率的影响。实验条件:处理后的锰渣 60g,液固比(mL/g)5∶1,硫酸质量分数 20%,搅拌速率300r/min,反应温度90℃,反应时间4h。由图5可以看出,当不加 FeSO4·7H2O 时,锌的浸出率达92.87%,而因原料中高价锰未被还原成Mn2+,致使锰的浸出率仅为67.95%。随着FeSO4·7H2O加入量的增加,锰浸出率呈现波动上升的趋势。当FeSO4·7H2O 加入量为 75g时,锰浸出率提高至96.76%,锌浸出率达到84.88%。因此,本实验选择FeSO4·7H2O加入量75g为本实验最佳工艺。
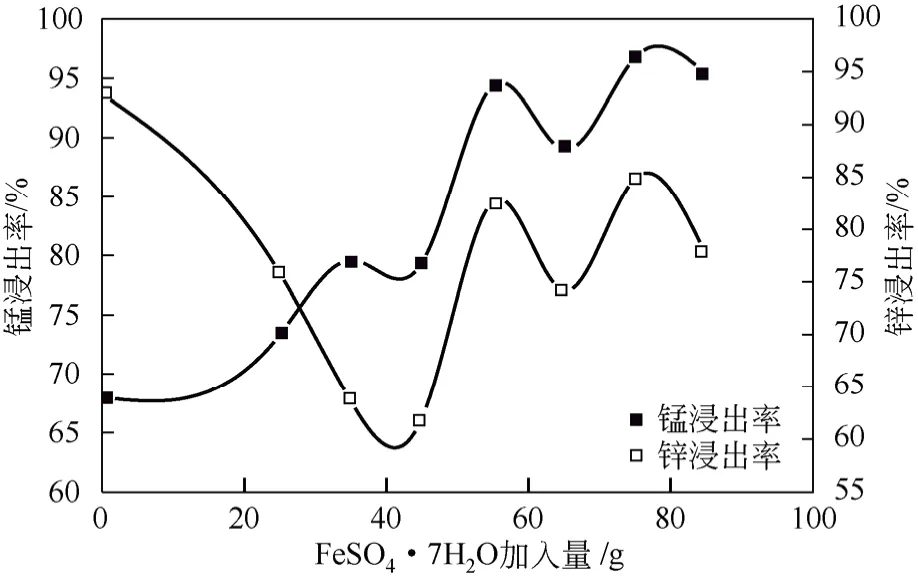
图5 FeSO4·7H2O加入量对Mn、Zn浸出率的影响
2.7 搅拌速率对浸出率的影响
图6为搅拌速率对Mn、Zn浸出率的影响。实验条件:处理后的锰渣60g,液固比(mL/g)5∶1,硫酸质量分数20%,反应温度90℃,反应时间4h,FeSO4·7H2O用量75g。由图6可以看出,搅拌速率对锰锌浸出率影响不是很大,当搅拌速率在300r/min时,锰浸出率最大。因此,本实验选择搅拌速率300r/min为本实验最佳工艺。
3 结 论
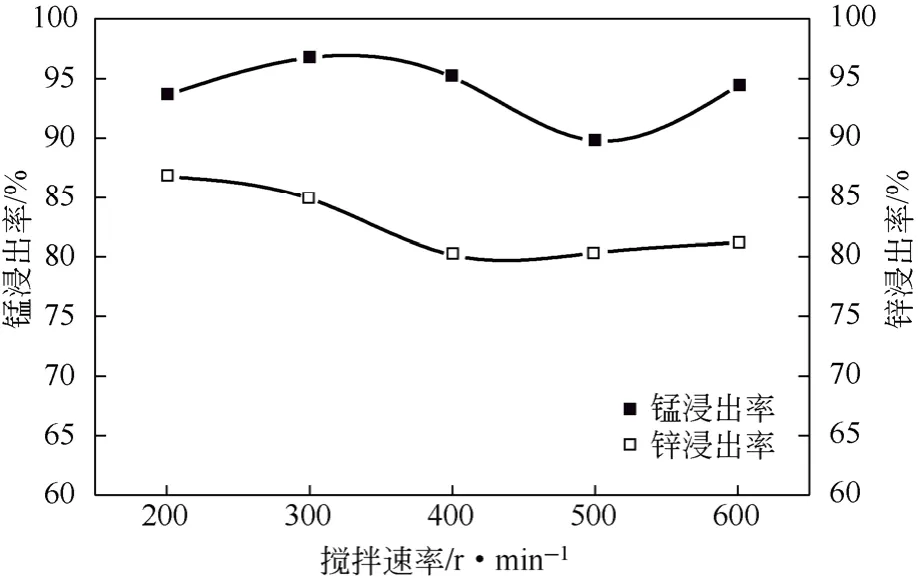
图6 搅拌速率对Mn、Zn浸出率的影响
(1)以锰铁冶炼烟尘灰为原料,硫酸亚铁为还原剂,采用硫酸浸出,反应结束后,调pH值至4~5脱铁,锰浸出率为96.76%,锌浸出率为84.88%。
(2)硫酸浸出锰铁烟尘灰最佳工艺条件为:H2SO4质量分数为20%,反应时间为4h,反应温度为90℃,液固比为5∶1,还原剂FeSO4·7H2O加入量为75g,搅拌速率为300r/min。
[1]谢红艳,王吉坤,马进,等. 从锰除尘灰中浸出锰的实验研究[J]. 中国锰业,2011,29(2):18-20.
[2]兰翠玲,张金磊,罗霞. 低贫软锰矿浸出硫酸锰工艺条件的研究及应用[J]. 应用化工,2013,42(4):683-685.
[3]陶长元,李敏,刘作,等. 利用复杂含锰废渣提取金属锰的研究[J].中国稀土学报,2012,30:565-570.
[4]蔡振勇,易清风,刘汉勇,等. 废铁屑还原软锰矿制备高纯硫酸锰工艺研究[J]. 中国锰业,2011,29(3):28-31.
[5]沈慧庭,覃华,黄晓毅,等. 某含锰冶金渣中锰和铅的综合回收研究[J]. 金属矿山,2009,6:171-176.

