乙酸乙酯-乙腈-1-乙基-3-甲基咪唑三氟甲磺酸盐物系等压汽液平衡数据的测定
丁邦琴,张 双,李 卓,曹 玲,许 文,李群生
(1. 南通职业大学 化学与生物工程学院,江苏 南通 226007;2. 北京化工大学 化学工程学院,北京 100029;3. 昌吉学院 化学与应用化学系,新疆 昌吉 831100)
乙酸乙酯-乙腈-1-乙基-3-甲基咪唑三氟甲磺酸盐物系等压汽液平衡数据的测定
丁邦琴1,张 双2,李 卓2,曹 玲3,许 文2,李群生2
(1. 南通职业大学 化学与生物工程学院,江苏 南通 226007;2. 北京化工大学 化学工程学院,北京 100029;3. 昌吉学院 化学与应用化学系,新疆 昌吉 831100)
在101.32 kPa下,用改进的Othmer釜测定了含离子液体1-乙基-3-甲基咪唑三氟甲磺酸盐([emim]OTf)的乙酸乙酯-乙腈物系的等压汽液平衡数据;采用NRTL方程对实验数据进行关联,关联效果良好。实验结果表明,加入[emim]OTf后,乙酸乙酯-乙腈二组分物系汽液平衡线发生偏离,[emim]OTf含量越高,偏离程度越大;[emim]OTf具有明显的盐析效应,当[emim]· OTf 的含量达到5%(x)时,就可消除乙酸乙酯-乙腈物系的共沸点;[emim]OTf可作为乙酸乙酯-乙腈萃取精馏的萃取剂。
汽液平衡;乙酸乙酯;乙腈;1-乙基-3-甲基咪唑三氟甲磺酸盐;NRTL方程
乙腈是一种重要的有机中间体,广泛应用于制药、石油化工、合成纤维等领域[1]。乙腈的广泛应用源于它有极好的溶剂性能。此外,乙腈还有许多其他优良性质:低凝固点、低沸点、低黏度和相对较低的毒性[2]。乙酸乙酯是一种应用非常广泛的脂肪酸酯,具有优良的溶解性和快干性[3]。制药工程中经常遇到乙酸乙酯和乙腈的混合物[4-7],而乙酸乙酯与乙腈在常压下形成共沸物,一般的精馏方法无法将其分离。
环境问题日益突出,离子液体作为一种绿色溶剂得到关注,也将越来越多地被应用于萃取过程[8]。为了实现将离子液体作为萃取剂应用于萃取精馏过程中,含离子液体体系的汽液平衡和活度系数等基础数据就显得尤为重要[9]。Li等[10]研究了1-丁基-3-甲基咪唑六氟磷酸盐([bmim]PF6)对乙酸乙酯-乙腈物系汽液平衡的影响,当[bmim]· PF6含量达到5%(x)时,能消除乙酸乙酯-乙腈物系的共沸点。1-乙基-3-甲基咪唑三氟甲磺酸盐([emim]OTf)具有较高的稳定性[11],研究[emim]OTf对乙酸乙酯-乙腈物系汽液平衡的影响有积极的意义。
本工作在101.3 kPa下,测定乙酸乙酯-乙腈-[emim]OTf三组分物系的等压汽液平衡数据,并讨论了[emim]OTf对乙酸乙酯-乙腈二组分物系汽液平衡的影响。
1 实验部分
1.1 试剂
乙酸乙酯:分析纯,北京化工厂;乙腈:分析纯,天津市福晨化学试剂厂;[emim]OTf:纯度大于 99 %(w),上海成捷化学有限公司。
1.2 汽液平衡数据的测定方法
采用改进的Othmer平衡釜[12]测定汽液平衡数据。实验试样采用称重法配制,电子天平的精度为0.1 mg。将60 mL试样加入到Othmer平衡釜中加热至沸腾,平衡室温度不变时为物系达到平衡,保持平衡状态约30 min后,采用微量进样器分别从汽相和液相取样口取样分析,每次取样间隔约为15 min。
1.3 分析方法
采用北京京科瑞达科技有限公司SP7800型气相色谱仪分析试样的组成。分析条件:Propak-Q填充柱(3 m × 0.3 mm),TCD温度453.15 K,柱温403.15 K,气化室温度443.15 K,载气(氢气)流量50 mL/min。采用面积归一化法定量,试样摩尔分数的最大偏差为0.002。
2 结果与讨论
2.1 实验装置的可靠性标定
为了验证实验装置的可靠性,实验测定的乙酸乙酯-乙腈二组分物系的汽液平衡数据见表1,与文献值[10]进行对比的结果见图1。由图1可见,乙酸乙酯-乙腈二组分物系的汽液平衡数据与文献值[10]基本吻合,乙酸乙酯的汽相摩尔分数的最大偏差为0.004。
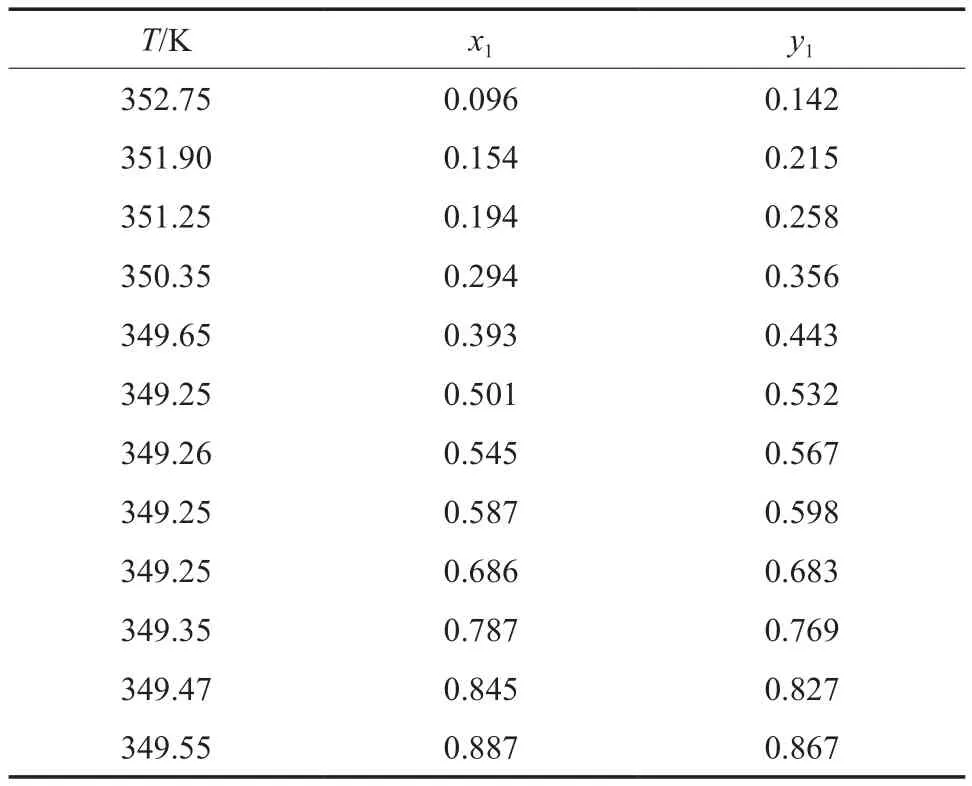
表1 在101.3 kPa下乙酸乙酯(1)-乙腈(2)物系汽液平衡数据Table 1 Vapor-liquid equilibrium(VLE) data for the ethyl acetate(1)-acetonitrile(2) binary system at 101.3 kPa

图1 在101.3 kPa下乙酸乙酯(1)-乙腈(2)物系的汽液平衡曲线Fig.1 VLE curves of the ethyl acetate(1)-acetonitrile(2)binary system at 101.3 kPa.
采用Herington经验方法[13]检验实验数据的热力学一致性。图2为乙酸乙酯-乙腈物系热力学一致性检验图,计算过程中涉及到的Antoine常数采用文献值[14]。利用面积积分法求得图2中区域A和B的积分值分别为SA= 0.063,SB= 0.060。偏差(D)和压力熵(J)分别由式(1)和式(2)求得:
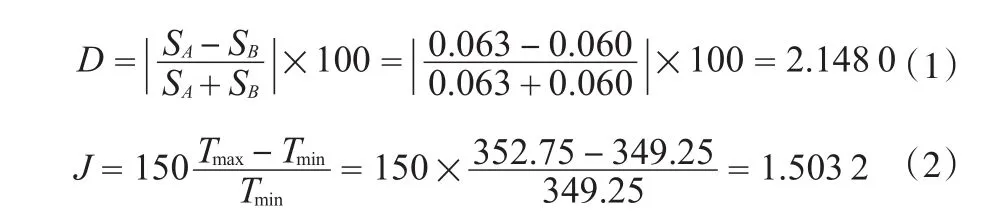
式中,Tmax,Tmin分别为实验数据中的最高和最低平衡温度,K。由于 | D-J | = | 2.148 0-1.503 2 | =0.644 8 < 10,则乙酸乙酯-乙腈物系汽液平衡数据满足热力学一致性检验。

图2 乙酸乙酯(1)-乙腈(2)物系的热力学一致性检验图Fig.2 Thermodynamic consistency test of the ethyl acetate(1)-acetonitrile(2) system.
2.2 汽液平衡数据
乙酸乙酯-乙腈-[emim]OTf三组分物系的等压汽液平衡数据见表2。组分的活度系数(γ)和乙酸乙酯对乙腈的相对挥发度(α12)的计算方法见文献[15-16]。
2.3 模型关联
目前,在含离子液体的汽液平衡数据的关联和预测的热力学模型中,NRTL[10],UNIQUAC[17],e-NRTL[11]等方程应用的最为广泛。因此,选用NRTL方程对乙酸乙酯-乙腈二组分物系及乙酸乙酯-乙腈-[emim]OTf三组分物系汽液平衡数据进行关联。采用非线性最小二乘法,目标函数(F)为:

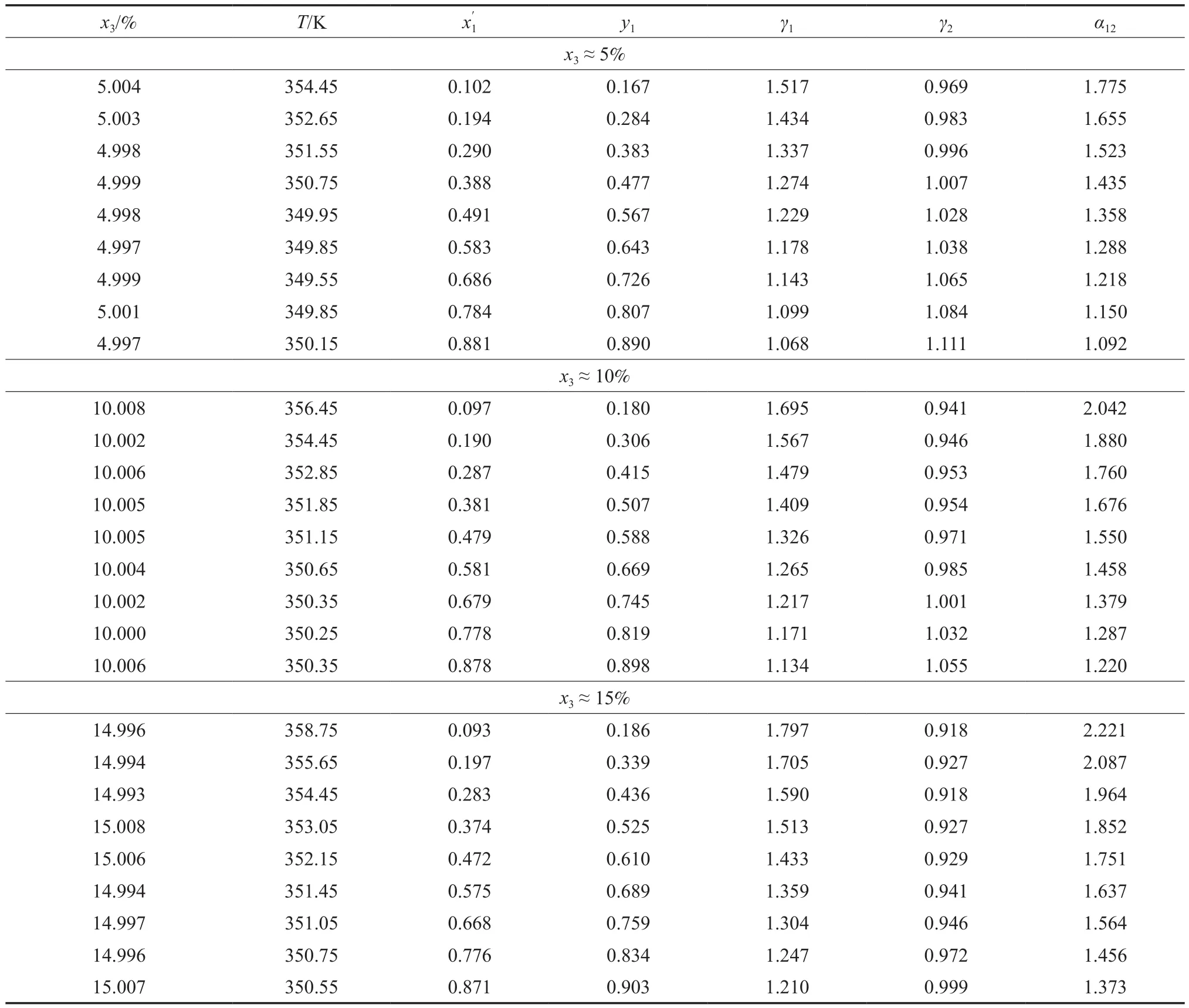
表2 乙酸乙酯(1)-乙腈(2)-[emim]OTf(3)物系的等压汽液平衡数据(101.3 kPa)Table 2 Isobaric VLE data for the ethyl acetate (1)-acetonitrile (2)-[emim]OTf (3) system at 101.3 kPa
式中,γ1和γ2分别为组分1和2的活度系数。
在关联过程中,先由乙酸乙酯-乙腈二组分物系汽液平衡数据确定乙酸乙酯-乙腈的相互作用参数,然后根据乙酸乙酯-乙腈-[emim]OTf三组分物系汽液平衡数据确定乙酸乙酯-[emim]OTf、乙腈-[emim]OTf的相互作用参数,关联结果见表3。平均相对偏差(ARD)的计算式为:

式中,n为实验数据点的个数。

表3 NRTL方程的关联结果Table 3 Results correlated by the NRTL model
2.4 讨论
乙酸乙酯-乙腈-[emim]OTf三组分物系的y-x′相图以及T-x′(y)图分别见图3和图4。离子液体[emim]OTf对乙酸乙酯-乙腈物系相对挥发度的影响见图5。
由图3~5可看出,[emim]OTf在乙酸乙酯整个浓度范围内均表现出了明显的盐析效应,乙酸乙酯-乙腈-[emim]OTf三组分汽液平衡线偏离乙酸乙酯-乙腈二组分的汽液相平衡线,且随[emim]· OTf含量的增大偏离程度增大,当[emim]OTf摩尔分数达到5%时,该物系共沸点消失。
另一方面,随[emim]OTf含量的增大,三组分物系的平衡温度也逐渐升高,这意味着对乙酸乙酯-乙腈二组分物系分离能量的需求增大。但鉴于离子液体可以避免常规的有机盐或萃取剂对环境的污染,[emim]OTf仍具有作为萃取剂应用于乙酸乙酯-乙腈的萃取精馏中的潜力。
当[emim]OTf加入乙酸乙酯-乙腈二组分物系后,[emim]OTf对二元物系汽液平衡的影响是由[emim]OTf和不同溶质分子间的相互作用力的不同引起的。
[emim]OTf可以视为一种弱电解质,乙腈的极性要强于乙酸乙酯,故极性较强的乙腈与[emim]OTf的相互作用力要强于乙酸乙酯与[emim]OTf的相互作用力,这就使得乙腈分子受到了“绑定”作用,自由乙酸乙酯的分子数量增加,从而提高了乙酸乙酯对乙腈的相对挥发度。

图3 乙酸乙酯(1)-乙腈(2)-[emim]OTf(3)三组分物系的y-x′相图(101.3 kPa)Fig.3 Isobaric y-x′phase diagram for the ethyl acetate (1)-acetonitrile (2)-[emim]OTf(3) ternary system at 101.3 kPa.
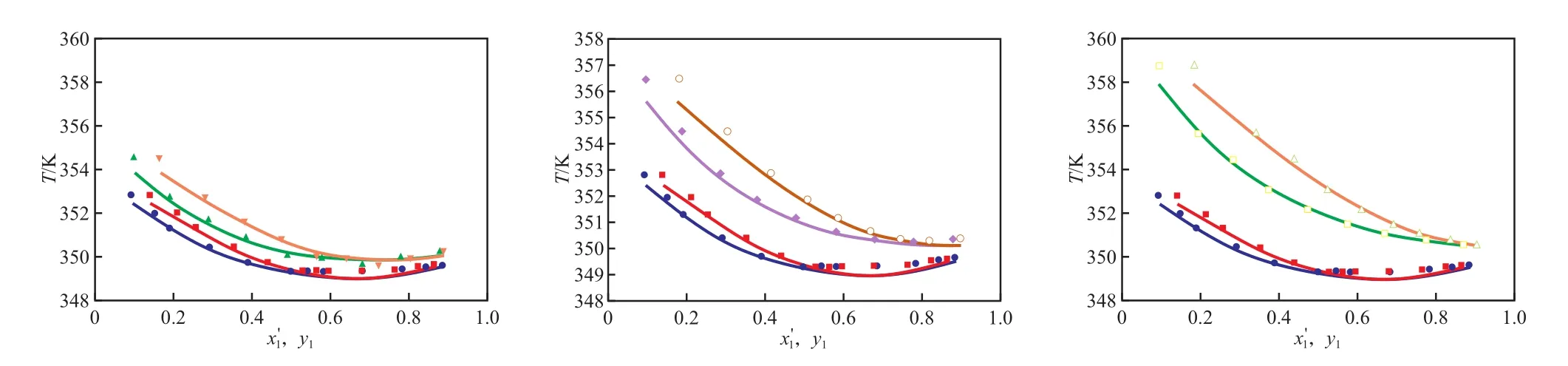
图4 乙酸乙酯(1)-乙腈(2)-[emim]OTf(3)三组分物系的T-x1′(y)图Fig.4 T-x1′(y) diagram for the ethyl acetate(1)-acetonitrile(2)-[emim]OTf (3) ternary system.
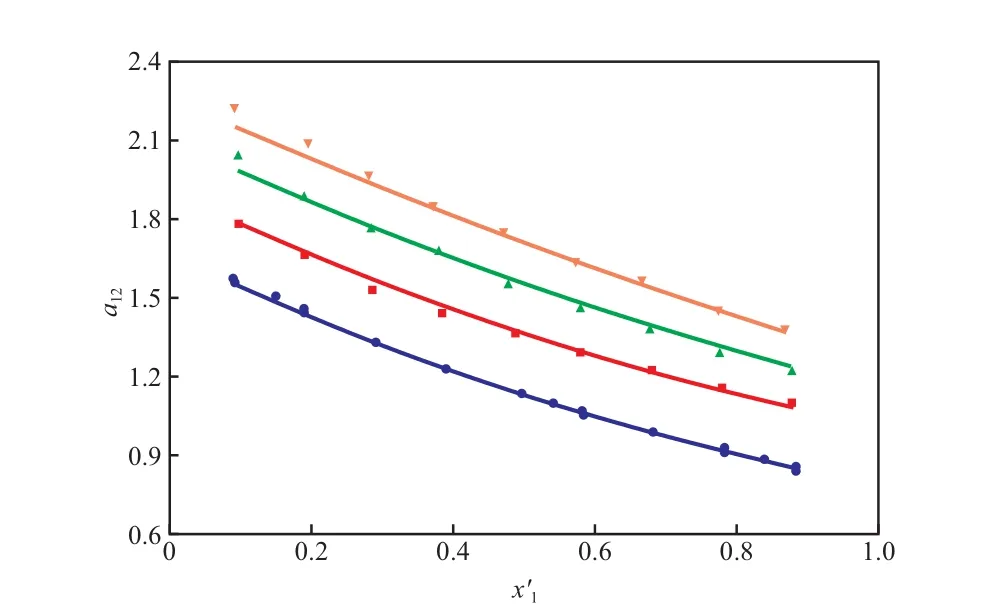
图5 [emim]OTf对乙酸乙酯-乙腈物系相对挥发度的影响(101.3 kPa)Fig.5 Effects of[emim]OTf on α12at 101.3 kPa.
3 结论
1)在101.32 kPa下,测定了[emim]OTf含量(x)分别为5%,10%,15%时的乙酸乙酯-乙腈-[emim]OTf三组分物系的汽液平衡数据。在乙酸乙酯-乙腈物系中加入[emim]OTf后,提高了乙酸乙酯对乙腈的相对挥发度,当[emim]OTf含量达到5%(x)时,该物系共沸点消失。
2)采用NRTL方程对乙酸乙酯-乙腈二组分物系及乙酸乙酯-乙腈-[emim]OTf三组分物系的汽液平衡数据进行关联,得到的活度系数的实验值与计算值的平均相对偏差分别为0.49%的0.80%,关联效果良好。
[1] 丁立,周荣琪,段占庭. 制药废液中回收乙腈与DMF[J]. 精细化工,2000,17(3):140 - 142.
[2] McConvey I F,Woods D,Lewis M,et al. The Importance of Acetonitrile in the Pharmaceutical Industry and Opportunities for Its Recovery from Waste[J]. Org Process Res Dev,2012,16(4):612 - 624.
[3] 刘明. 乙酸乙酯的市场需求与生产方法[J]. 化学工业与工程技术,2004,25(5):54 - 56.
[4] Fatta D,Achilleos A,Nikolaou A,et al. Analytical Methods for Tracing Pharmaceutical Residues in Water and Wastewater[J]. TrAC Trend Anal Chem,2007,26(6):515 - 533.
[5] 沈建忠,项新华,张跃,等. 家禽肌肉组织中硝基咪唑类药物残留高效液相色谱检测法研究[J]. 中国农业科学,2003,36(6):700 - 703.
[6] 高文平,李拜,袁云刚. 高效液相色谱法测定复方青黛丸中靛玉红含量[J]. 中国药业,2007,16(17):28.
[7] 王建华,刘心同,王修林,等. 气相色谱-负化学源质谱法测定蜂蜜和奶粉中氯霉素残留量[J]. 化学分析计量,2004,3(2):26 - 33.
[8] 张景涛,朴香兰. 离子液体及其在萃取中的应用研究进展[J]. 化工进展,2001,20(12):16 - 19.
[9] 孟凡宝,李东风. 离子液体在萃取精馏领域应用的基础性研究进展[J]. 石油化工,2010,39(12):1395 - 1401.
[10] Li Qunsheng,Cao Ling,Sun Xueting,et al. Isobaric Vapor-Liquid Equilibrium for Ethyl Acetate + Acetonitrile + 1-Butyl-3-Methylimidazolium Hexafluorosphate at 101.3 kPa[J]. J Chem Eng Data,2013,58(5):1112 - 1116.
[11] Orchillés A V,Miguel P J,Vercher E,et al. Using 1-Ethyl-3-Methylimidazolium Trifuoromethanesulfonate as an Entrainer for the Extractive Distillation of Ethanol + Water Mixtures[J]. J Chem Eng Data,2009,55(4):1669 - 1674.
[12] 李群生,朱久娟,张继国,等. 乙酸乙酯-乙醇-1-乙基-3-甲基四氟硼酸咪唑盐物系等压汽液平衡数据的测定[J]. 石油化工,2008,37(8):810 - 814.
[13] 朱自强,姚善泾,金彰礼. 流体相平衡原理及其应用[M].杭州:浙江大学出版社,1990.
[14] 王松汉. 石油化工设计手册:(第1卷)石油化工基础数据[M]. 北京:化学工业出版社,2002:473 - 475.
[15] Gironi F,Lamberti L. Vapour-Liquid Equilibrium Data for the Water-2-Propanol System in the Presence of Dissolved Salts[J]. Fluid Phase Equilibria,1995,105(2):273 - 286.
[16] 李群生,邢风英,雷志刚. 异丙醇-水-1-乙基-3-甲基四氟硼酸咪唑盐物系等压汽液平衡数据的测定[J]. 石油化工,2008,37(1):67 - 71.
[17] Lei Zhigang,Arlt W,Wasserscheid P. Separation of 1-Hexene and n-Hexane with Ionic Liquids[J]. Fluid Phase Equilibria,2006,241(1):290 - 299.
(编辑 李治泉)
Isobaric Vapor-Liquid Equilibrium for Ethyl Acetate-Acetonitrile-1-Ethyl-3-Methylimidazolium Trifluoromethanesulfonate Ternary System
Ding Bangqin1,Zhang Shuang2,Li Zhuo2,Cao Ling3,Xu Wen2,Li Qunsheng2
(1. College of Chemical and Biological Engineering,Nantong Vocational University,Nantong Jiangsu 226007,China;2. College of Chemial Engineering,Beijing University of Chemical Technology,Beijing 100029,China;3. Department of Chemistry & Applied Chemistry,Changji University,Changji Xinjiang 831100,China)
The isobaric vapor-liquid equilibrium (VLE) data for the ethyl acetate and acetonitrile system containing an ionic liquid,1-ethyl-3-methylimidazolium trifuoromethanesulfonate([emim]· OTf),were measured at 101.32 kPa in a modifed Othmer still. The experimental data were correlated by means of the NRTL model. The VLE curve of the ethyl acetate-acetonitrile system containing[emim]OTf deviated from the curve of the ethyl acetate-acetonitrile system without [emim]OTf and the deviation increased with increasing the content of [emim]OTf. [emim]OTf exhibited a saltingout effect,and the azeotropic point of the system could be eliminated when the mole fraction of [emim]· OTf reached 5%. The results showed that [emim]OTf can be used as an entrainer for the extractive distillation of the ethyl acetate-acetonitrile system.
vapor-liquid equilibrium;ethyl acetate;acetonitrile;1-ethyl-3-methylimidazolium trifuoromethanesulfonate;NRTL model
1000 - 8144(2014)12 - 1405 - 05
TQ 013.1
A
2014 - 06 - 04;[修改稿日期] 2014 - 08 - 23。
丁邦琴(1971—),女,江苏省海安市人,硕士,副教授,电邮 ntdbq@sina.com。联系人:李群生,电话 010 -64446523,电邮 975770462@qq.com。
江苏省高等职业院校高级访问学者计划资助项目(2013FX072)。

