喜炎平注射液溶血的分光光度法检查
邱海强
(江苏省无锡药品检验所,江苏 无锡 214028)
喜炎平注射液溶血的分光光度法检查
邱海强
(江苏省无锡药品检验所,江苏 无锡 214028)
目的建立喜炎平注射液溶血检查的分光光度方法。方法按《中国药典》2010年版一部方法配制供试品溶液、阴性对照和阳性对照溶液,用分光光度法测定吸光度,并计算溶血率,检测波长545 nm。结果溶血率上限定为5%,样品的溶血率均<1%。结论喜炎平注射液可以用分光光度法进行溶血检查,其灵敏度高于药典方法。
喜炎平注射液;溶血;分光光度法
喜炎平注射液,主要成分为穿心莲内酯总磺化物,具有清热解毒、止咳止痢的作用,临床用于支气管炎、扁桃体炎、细菌性痢疾等。其现行质量标准为国家药品标准WS-10863(ZD-0863)-2002-2011Z,规定“溶血与凝聚”项按《中国药典》2010年版一部附录ⅩⅢ H溶血与凝聚检查法进行[1]。药典附录溶血与凝聚检查法是经典的传统方法,检验结果采用目测观察。主要缺点:检验结果靠检验者的经验来判断,主观干扰较大;由于采用目测观察,当对检验结果有异议时,难以提供客观的数据来佐证检验结果。现采用分光光度法测定供试品溶液的吸光度并计算溶血率,对喜炎平注射液的溶血检查方法进行了改进。
1 仪器与试药
1.1 仪器:Cary100紫外-可见分光光度计,SPX-250B-Z型生化培养箱,均经检定合格。80-2型离心沉淀器。
1.2 动物:普通级新西兰家兔,体质量3.5 kg,雄性,实验动物使用许可证号SYXK(苏)2014-0012号。
1.3 试药:喜炎平注射液,规格2 mL∶50 mg,批号20110526、20120423、20121217、2013012402、2013030802、2013033003,江西某药业有限公司(依次编为样1~样6)。氯化钠注射液,规格500 mL∶4.5 g,批号131012ZT,安徽某药业有限责任公司。纯化水。
2 方法与结果
2.1 2%红细胞混悬液的制备:取兔心血,按《中国药典》2010年版一部附录ⅩⅢ H规定的方法,制成2%红细胞混悬液[2]+92。
2.2 药典标准检验:取洁净玻璃试管,按表1所示依次加样,混匀后立即置37 ℃温育,3 h后观察溶血和凝聚反应。如溶液呈澄明红色,管底无细胞残留或有少量细胞残留,表明有溶血发生;若有棕红色或红棕色絮状沉淀,轻轻倒转3次仍不分散,表明可能有红细胞凝聚发生,显微镜下观察有红细胞凝集,则为凝聚。溶血或凝聚均以“+”表示。如红细胞全部下沉,上清液无色澄明,表明无溶血发生;无棕红色或红棕色絮状沉淀,表明无红细胞凝聚发生。均以“-”表示。结果6批供试品按药典标准检验,溶血与凝聚检查均符合规定。见表2。
2.3 分光光度法检查:参照GB/T 14233.2-2005中“溶血试验”方法,并以该标准规定的溶血率5%作为合格上限。按表1所示加样,6批喜炎平注射液供试品管、阴性对照管、阳性对照管平行各3管,6批供试品对照管各1管。混匀后立即置37 ℃温育3 h。1500转/分离心15 min,取上清液。
2.3.1 取6批供试品对照溶液,以氯化钠注射液为空白,按紫外-可见分光光度法,在波长200~800 nm范围内进行扫描。6批结果一致,选2号样品见图1。
2.3.2 供试品对照溶液吸光度的测定:以氯化钠注射液为空白,用分光光度法在545 nm处测定供试品对照溶液吸光度,结果见表3。
图1表明,喜炎平注射液的最大吸收波长在300 nm以下,在400~800 nm范围内,吸光度很小。而溶血反应产生的血红蛋白,其最大吸收波长为545 nm[3],因此,样品本身对血红蛋白的检测干扰很小。同时,检测供试品溶液时,是以供试品对照溶液作空白,其影响可完全消除。表3结果进一步证实了这一结论。
2.3.3 供试品溶液吸光度检测及溶血率计算:以氯化钠注射液作空白,检测波长545 nm,测定阴性对照(3管)和阳性对照(3管)溶液的吸光度。分别以6批供试品对照溶液为空白,测定6批供试品溶液(各3管)的吸光度。以3管吸光度的平均值计算溶血率[3],结果6批供试品的溶血率均<1%。参照GB/T 14233.2-2005溶血试验的判断标准,溶血率<5%,则判定样品溶血检查符合规定[3]。分光光度法与药典方法结果一致。见表4。
溶血率(%)计算公式:%=(A-B)/(C-B)×100%。式中A、B、C分别为供试品溶液、阴性对照、阳性对照的吸光度。
2.3.4 “不合格样品”的制备及检测:取2、4、6号喜炎平注射液,按表5加样,混匀后立即置37 ℃温育3 h,取出观察溶血结果。3批供试品均在9号管开始出现明显溶血现象,8号管隐约可见轻微溶血,而1~7号管均无明显溶血现象。再1500转/分离心15 min,取上清液。离心后8号管上清液可见较明显的溶血现象。按2.3.3方法测定吸光度并计算溶血率,阴性、阳性对照采用表4数据。结果见表6、表7。

表1 喜炎平注射液溶血与凝聚药典检查方法

表2 喜炎平注射液溶血与凝聚药典检查结果

表3 供试品对照溶液545 nm波长吸光度

表4 供试品溶液吸光度及溶血率结果
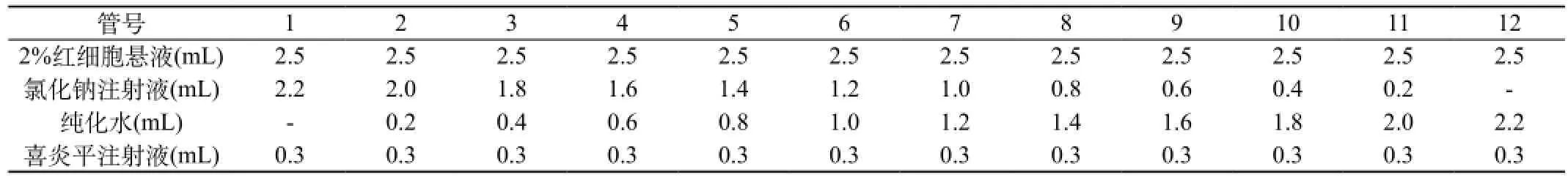
表5 “不合格样品”的制备

表6 “不合格样品”吸光度结果

表7 “不合格样品”溶血率结果

图1 喜炎平注射液扫描结果
表7结果表明,目测法与分光光度法相比,当溶血率约为5%~7%时仅能观察到轻微溶血现象,而观察到明显溶血现象时的溶血率已达到17%。上述实验结果证明,采用分光光度法,比药典方法能更灵敏地检查出溶血现象。
3 讨 论
3.1 喜炎平注射液的主要原料穿心莲内酯总磺化物由中药材提取而成,成分较为复杂,容易引起过敏反应、溶血、红细胞凝聚等不良反应,因此除注射剂通用的热原、无菌检查外,现行的法定标准规定了溶血与凝聚、异常毒性、过敏反应的检查。
3.2 按法定标准检验时,由于红细胞的沉降不可能完全,因此轻微溶血所产生的血红蛋白,其颜色被红细胞掩盖,造成判断困难。同时药典标准中对溶血的描述为“试管中的溶液呈澄明红色”,其红色的程度无法定量,检验者的判断各有不同,容易造成误判。采用分光光度法则可避免这一缺点。
3.3 药典规定对红细胞凝聚采用显微镜下观察。随着显微摄像技术的逐步推广,建议将红细胞凝聚的检查结果拍照留存,以保存检验的原始证据。
[1] 国家食品药品监督管理局.WS-10863(ZD-0863)-2002-2011Z.国家药品标准[S].
[2] 国家药典委员会.中华人民共和国药典:一部[S].北京:化学工业出版社,2010:附录30.
[3] 国家质量监督检验检疫总局.GB/T 14233.2-2005.中华人民共和国国家标准[S].
The Spectrophotometric Method for the Hemolysis Examination of Xiyanping Injection
QIU Hai-qiang
(Wuxi Institute for Drug Control, Wuxi 214028, China)
ObjectiveTo establish a spectrophotometric method for the hemolysis examination of Xiyanping injection.MethodThe sample solution, negative control solution and positive control solution were prepared according to the method of Chinese Pharmacoperia (2010 edition, Vol Ⅰ), the light absorbance at the wavelength of 545 nm was detected using spectrophotometric method, and the hemolysis rate was calculated.ResultThe upper limit of the hemolysis rate was 5%, and the hemolysis rate of all of the samples was less than 1%.ConclusionThe spectrophotometric method can be used for the hemolysis examination of Xiyanping injection, the sensitivity is higher than that of the Pharmacoperia method.
Xiyanping injection; Hemolysis; Spectrophotometry
R282.710.5
B
1671-8194(2014)29-0070-02

