盐酸巴马汀的光谱性质研究
张跃淑,史文波,李俊芬
(1.中国建筑材料工业地质勘察中心山西总队,山西 太原 030031;2.山西大学化学化工学院,山西 太原 030006)
盐酸巴马汀的光谱性质研究
张跃淑1,史文波1,李俊芬2*
(1.中国建筑材料工业地质勘察中心山西总队,山西 太原 030031;2.山西大学化学化工学院,山西 太原 030006)
在不同极性和不同酸度介质中考察并探讨了巴马汀的荧光光谱和紫外光谱特性.随着溶剂极性的增加,巴马汀的溶解性增大,吸收峰强度明显增大且红移.巴马汀的荧光发射光谱受溶剂极性的影响也很显著.随着溶剂极性的降低,源于醇式巴马汀的第二个荧光发射带紫移且荧光强度显著提高,而第一个发射带对极性不敏感.pH对巴马汀溶液的吸收和荧光光谱影响都较小.量子产率在二氯甲烷溶剂中达到最大.结果表明,巴马汀对周围介质环境的敏感程度较高.
盐酸巴马汀;光谱性质
0 引言
许多中草药中提取出的生物碱类化合物为抗癌药物,异喹啉生物碱是其中最大的一类,有关研究已引起人们的广泛关注[1~3].巴马汀(Pal)是一种典型的异喹啉生物碱,是中药黄柏、黄连、三棵针和南天竹等许多药用植物的有效成分,具有抗菌、降压、利胆及抗癌等生物活性.
关于巴马汀的分离提取、药理性质和毒性等已有很多报导[4~6].如由盐酸巴马汀制成的黄藤素软胶囊,具有较强的抑制霉菌、葡萄球菌、淋球菌、支原体、衣原体和抗酸性分析杆菌的作用,临床常用于妇科炎症、呼吸道炎症、外科感染、菌痢、肠炎及结膜炎等疾病的治疗.荧光光谱法对于揭示物质的内在性质有着特殊的地位[7].荧光的激发光谱、发射光谱、量子产率和荧光寿命等参数不仅和分子内荧光发色基团的本身结构有关,而且还对周围环境十分敏感.通过测定上述有关荧光参数的变化可研究荧光发色团所在部位的微环境特征及其变化.巴马汀的吸收和荧光性质仅偶见文献中[8~10],未见系统报导.因此研究介质环境对巴马汀的吸收和荧光光谱性质的影响对于理解生物碱分子的药理性质和功能具有重要意义.
1 实验部分
1.1 仪器与试剂
CaryEcl i ps型荧光光谱仪(美国VARIAN公司);TU-1901型双光束紫外可见分光光度计(北京普析通用仪器有限责任公司);pH S-29A型酸度计(上海雷磁创益仪器仪表有限公司);
盐酸巴马汀(化学对照品,中国药品生物制品鉴定所),用二次蒸馏水配制成1×10-3mol/L储备液;Bri t t on-Robi son缓冲溶液配制方法:在100 mL的三酸混合液中(H3BO3,H3PO4,H Ac,浓度均为0.04 mol/L),加入相应体积的NaOH(0.2 mol/L)按比例配制pH 1.81~11.80之间的缓冲溶液;pH 12.80使用氢氧化钠饱和溶液;其余试剂均为分析纯;所有水溶液均为二次亚沸蒸馏水.
1.2 实验方法
1.2.1 紫外吸收光谱测量
准确称取5份等质量的盐酸巴马汀,置于10 mL容量瓶中,分别加入不同溶剂溶解,稀释至刻度并摇匀.另吸取一定体积的巴马汀储备液至10 mL比色管中,以不同pH值的缓冲溶液稀释到刻度,充分摇匀,然后将上述溶液分别转移至1 cm比色皿中,以相应的溶剂或缓冲溶液做空白,扫描吸收光谱.实验温度为25±0.5℃.
1.2.2 荧光光谱测量
将1.2.1中溶液置于石英杯中,在荧光仪上扫描荧光光谱.激发和发射狭缝设为10 nm,扫描速度为600 nm·m i n-1.实验温度为25±0.5℃.
1.2.3 荧光量子产率测量
以硫酸奎宁0.05 mol/L硫酸溶液的量子产率0.55为参比,测量不同溶剂中巴马汀的荧光量子产率.
2 结果与讨论
2.1 溶剂对盐酸巴马汀光谱的影响
2.1.1 溶剂对吸收光谱的影响
巴马汀的基本结构(图1)为5,6-二氢二笨并[a,g]喹啉阳离子,并在2,3,9,10位上进行取代.乙氧基和甲氧基这些助色团上的氧原子上的孤对电子和芳环上的π电子体系相互作用,使得共轭体系增大,导致其吸收光谱较其基本结构出现明显红移.巴马汀在不同极性的水和醇溶剂中的吸收光谱如图2所示.在200~500 nm范围内有四个明显的吸收峰.随着溶剂极性的降低,处于紫外区的三个吸收带的吸收强度明显增大,尤其是从水到甲醇,增大了近3倍.同时,第3个和第4个吸收带的波长有8~9 nm的明显红移,而短波长的两个吸收峰红移则不明显.以上现象说明巴马汀在有机溶剂中有更好的溶解度,极性小的溶剂对其吸收更有利.

图1 盐酸巴马汀的结构式

图2 巴马汀(2×10-6mol/L)在不同溶剂中的吸收光谱
2.1.2 溶剂对荧光光谱的影响
在水和不同极性醇溶剂中扫描巴马汀的荧光光谱,如图3所示.其中左图是巴马汀在不同溶剂中的荧光激发光谱.四个激发峰分别为241,273,348,458 nm,与四个吸收蜂对应.随溶剂极性的增大,巴马汀的激发峰位置并不改变,但荧光强度迅速减弱.这是由于受激辐射时巴马汀发生了π→π*跃迁,其电子激发态比基态有更大的极性所致.右图是巴马汀在不同溶剂中的荧光发射光谱,由415 nm和540 nm两个发射带组成,其短波长415 nm处的峰非常弱,与小檗碱类似[8].发射峰位置也不随着溶剂极性的变化而变化.
巴马汀在不同溶剂中的荧光参数见表1.由表可见,巴马汀荧光光谱的两个发射带受溶剂的影响并不相同.第一个发射带在甲醇溶剂中略为明显,其余溶剂中不明显.在水溶剂中无第二个发射带.然而,随着溶剂极性的减小,540 nm左右的发射带荧光增强非常明显,并且伴随着荧光发射峰的紫移.显然,该发射带对其周围介质环境更敏感,这是因为二者激发态的极性差别较大,即第二个带的激发态比第一个带的激发态有更大的极性,弱极性环境更有利于巴马汀的荧光发射.改变甲醇/水混合溶剂中二者的比例,巴马汀的激发光谱位置几乎不变,而发射光谱强度随水的比例增大而减小.当水溶剂所占比例小于20%,能够明显看到长波长530 nm处的发射带.当水溶剂所占的比例继续增大,则此发射带消失,仅有较弱的第一个发射带.
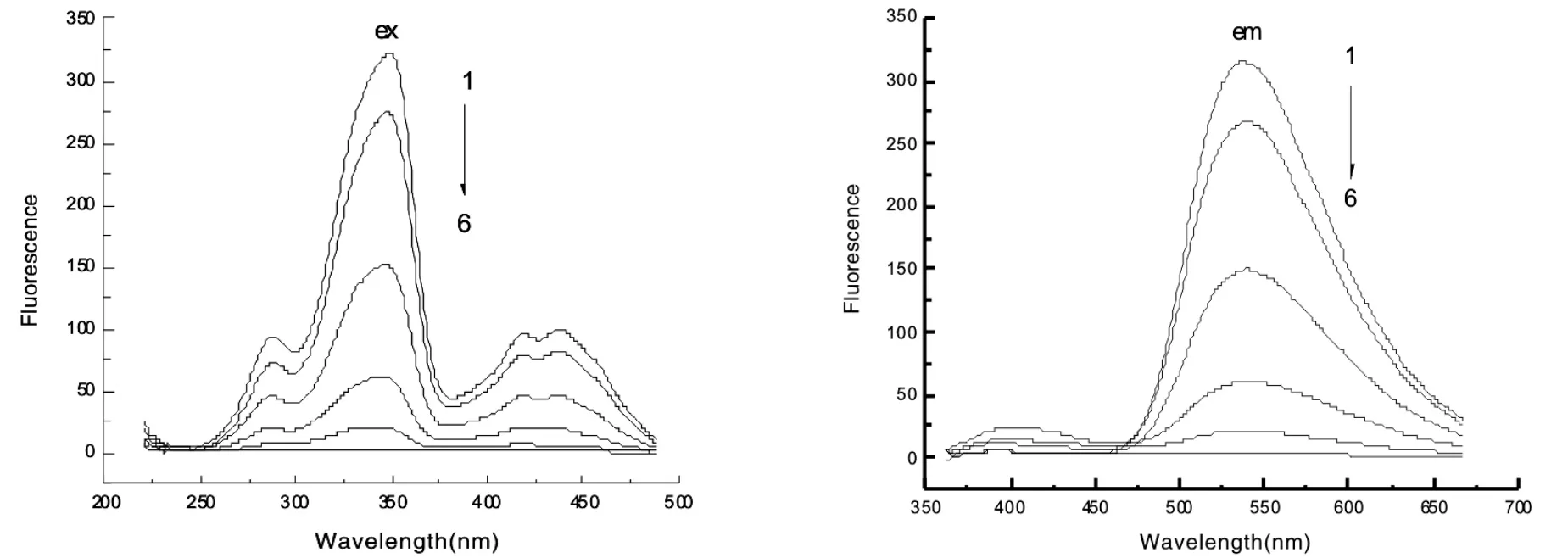
图3 巴马汀(1×10-5mol/L)在不同醇溶剂中的荧光激发光谱(λex=530 nm)和发射光谱(λem=350 nm)
小檗碱的两个荧光发射带分别来自于1La和1Lb带的振动跃迁[9].小檗碱有季铵盐式与醇式两种形式,并可以相互转化[10].基于两种化合物的结构和实验现象的相似性,因此540 nm的发射谱带可归于醇式巴马汀的荧光发射,而416 nm的荧光发射谱带是其季铵盐式的荧光发射所引起,该形式对溶剂极性不敏感.在水溶液中主要以季铵盐形式存在,随着溶剂极性的减弱,季铵盐式会向醇式转化,荧光显著增强.

表1 溶剂极性对盐酸巴马汀的荧光光谱的影响
2.2 pH对盐酸巴马汀光谱的影响
2.2.1 pH对光谱的影响
图4A为不同酸度条件下巴马汀的吸收光谱.由图可见,在pH=2.23时,吸光度最大.在整个pH范围内,巴马汀吸收光谱的强度和位置变化都很小,表明巴马汀在水溶液中是高度稳定的.
选用巴马汀荧光比较强的第二个荧光带考察.实验发现,在不同pH溶液中,巴马汀的荧光强度和荧光光谱位置均未发生明显的改变(图4B).这是由于巴马汀的阳离子荧光体是极弱的酸(pKa=15.7),不能与溶液中的H+或OH-离子形成氢键.即在pH 1.20~12.80范围内都是巴马汀阳离子在发光,故其荧光强度几乎不随溶液pH的变化而变化.

图4 不同酸度条件下巴马汀的吸收光谱(2×10-6mol/L,图A)和荧光光谱(1×10-5mol/L,图B)pH1-10:2.23,1.74,9.34,8.0,5.68,11.78,12.80,5.76,4.18,1.34
2.3 盐酸巴马汀的荧光量子产率(φf)
以硫酸奎宁作参比测定荧光量子产率(φf),结果见表2.在水溶液中生物碱的荧光量子产率很低.可能是N原子通过系间窜越或自旋/轨道相互作用引起电子激发态失活而导致荧光很弱.随着溶剂极性的减小,巴马汀的量子产率不断增大.在正丙醇溶剂中,量子产率比水中提高了100多倍.尤其是在二氯甲烷中荧光量子产率可增大到0.29,荧光光谱见图5.

图5 巴马汀在各种溶剂中的荧光发射光谱
3 结论
巴马汀是很强的两亲阳离子,具有碱性,其四个甲氧基是电子给体基团,可以降低巴马汀分子基态和激发单重态之间的电子转移能量,从而影响其吸收和荧光强度.在不同极性和不同酸度介质中考察了巴马汀的荧光和紫外光谱特性.实验表明,巴马汀对周围介质环境的敏感程度较高,可作为荧光探针用于生命科学研究,为了解该药物的抗癌活性及设计新型抗癌药物提供依据和参考.

表2 不同极性溶剂中巴马汀的荧光量子产率
[1]R U N G SITIY A K O R N A .,W ILA IR A T P.,PA N LJPA N B .O n the pH -dependence ofbinding ofberberine to D N A[J].J.Pharm .Pharm acol.1981(33):125~1129.
[2]李华春,覃明丽,谭克俊.硅钨酸与盐酸巴马汀相互作用光谱研究及其分析应用.化学学报,2012(6):747~752.
[3]K IM S.H ,SH IN D .S,O H M .N ,C H U N G S.C,LE E J.S,O H K .B .Inhibition ofthe bacterialsurface protein anchoring transpeptidase sortase by isoquinoline alkaloids[J].B iosci.B iotech.B iochem.2004,68(2):421~424.
[4]SH IN J.S,K IM E .I.,K A I M ,A N D LE E M .K .Inhibition of dopam ine biosynthesis by protoberberine alkaloids in PC 12 cells[J].N eurochem icalR esearch,2000,25(3):363~368.
[5]H SIE H P.C,SIE G E L S.A .,R O G E R S B,D A V IS D ,LE W IS K .B acteria lacking a m ultidrug pum p:a sensitive toolfor drug discovery[J].Proceedings ofthe N ationalA cadem y ofSciences ofthe U nited States ofA m erica,1998,95(12):6602~6606.
[6]TE G O S G .,STE R M ITZ F.R .,LO M O V SK A Y A O ,LE W IS K . M ultidrug pum p inhibitors uncover rem arkable activity of plantantim icrobials[J].A gents and C hem otherapy,2002,46(10):3133~3141.
[7]邢军,徐卫宾.薄层荧光扫描测定止痢冲剂盐酸小檗碱及盐酸巴马汀的含量[J].济宁医学院学报,2001,24(2):64~65.
[8]赵长春,于俊生.介质环境对小檗碱荧光光谱影响的研究[J].药物分析杂志,2000,20(2):109~110.
[9]C A SPA R C E Z.,.K O M O R SK Y L.S.,LO V R IC M .The ultravioletand visible absorption spectra ofberberrubine[J].C an J C hem,1982(60):970~974.
[10]赵长春,于俊生,章杰兵.药物与DNA的相互作用的研究-I.小檗碱作为DNA的发光开关及pH的影响[J].无机化学学报,1997(13):325~329.
(编辑 杨乐中)
O657
A
1673-1808(2014)03-0037-04
2013-10-23
国家自然科学基金(No.21105060)
张跃淑(1968-),女,山西平陆人,中国建筑材料工业地质勘察中心山西总队,高级工程师,研究方向:分析化学;
史文波(1968-),男,山西怀仁人,中国建筑材料工业地质勘察中心山西总队,高级工程师,研究方向:分析化学;
李俊芬(1974-),女,山西大学化学化工学院,副教授,博士,研究方向:分子光谱分析.

