天麻素氯化钠注射液的质量标准研究
刘 剑 闫建坤
1.内蒙古自治区红十字会包头朝聚眼科医院药械科,包头 014060;2.包头市卫生学校基础科,包头 014030
天麻素氯化钠注射液的质量标准研究
刘 剑1闫建坤2
1.内蒙古自治区红十字会包头朝聚眼科医院药械科,包头 014060;2.包头市卫生学校基础科,包头 014030
目的 建立天麻素氯化钠注射液的质量标准。 方法 采用紫外-可见分光光度法测定处方中天麻素的含量。 结果 由紫外扫描可知天麻素在220 nm波长处有最大吸收,而氯化钠及其他辅料在220 nm处几乎无吸收,不干扰本试验。 结论 采用紫外-可见分光光度法,方法操作简单,准确可靠,重复性好,可作为天麻素氯化钠注射液的质量控制方法。
天麻素氯化钠注射液;质量标准;紫外-可见分光光度法
天麻素注射液[1-5]主要成分为名贵药材天麻[6-9]的有效单体天麻素,具有镇静,抗惊厥,抗癫痫,镇痛,增加脑血流量,改善椎-基底动脉、小脑前下动脉、小脑后下动脉、密路动脉及内耳供血不足,保护神经细胞,促进心肌细胞能量代谢的功能,临床上被广泛应用于眩晕[10-15](梅尼埃病、药毒性眩晕、前庭神经元炎、椎-基底动脉供血不足等)、神经痛(三叉神经痛、坐骨神经痛、枕大神经痛等)、头痛(神经衰弱及神经衰弱综合征、血管性头痛、紧张性头痛、脑外伤综合征、偏头痛等)及癫痫的辅助治疗。本试验采用紫外-可见分光光度法对制剂中所含的天麻素进行含量测定。
1 仪器与试药
UV-754紫外分光光度计(上海电子光学技术研究所);天麻素氯化钠注射液供试品由内蒙古自治区红十字会包头朝聚眼科医院制剂室生产:规格100 ml,天麻素0.2 g与氯化钠0.9 g(批号为110106、110107、110108);对照品天麻素由中国药品生物制品鉴定所提供:规格20 mg,批号110807-201104。
2 方法与结果
2.1 性状
取本品目检,结果3批样品性状均为无色澄明液体。
2.2 鉴别
①本品为以氯化钠为溶剂的注射液,参照氯化钠注射液项下的鉴别操作如下:取本品适量,加稀硝酸使成酸性后,滴加硝酸银试液,即生成白色凝乳状沉淀;分离,沉淀加氨试液即溶解,再加稀硝酸酸化后,沉淀复生成。取处方中除氯化钠外的样品适量,同法操作,溶液澄清无沉淀。取本品适量,置试管中,加等量的二氧化锰,混匀,加硫酸湿润,缓缓加热,即发生氯气,能使用水湿润的碘化钾淀粉试纸显蓝色。3批样品均呈正反应。取处方中除氯化钠外的样品适量,同法操作,无气体产生。
②参照天麻素的质量标准,取本品适量(相当于天麻素10 mg),加热挥至快干,加硫酸 2 ml,溶液呈樱桃红色。取氯化钠溶液及辅料适量,同法操作,结果可见3批样品的鉴别1及鉴别2均呈正反应(表1)。

表1 天麻素氯化钠注射液的鉴别
③天麻素注射液采用红外鉴别,考虑到本品为注射剂,红外鉴别易受辅料的干扰,而天麻素的分子结构中有特殊的紫外发色团-苯环,故考虑将其特征紫外吸收作为一项鉴别,具体操作如下:取含量测定项下的溶液,照紫外-可见分光光度法(中国药典2010年版二部附录ⅣA)测定3批样品及对照品的最大吸收波长。3批样品均为λmax1=220 nm,λmax2=269 nm,在220、269 nm波长处有最大吸收(表1)。
2.3 检查
参照中国药典2010年版二部的有关规定,对本品进行pH值、溶液的澄清度与颜色、可见异物、不溶性微粒、装量、细菌内毒素、无菌等项目的检查。
2.3.1 pH值
取本品,依法测定pH值(中国药典2010年版二部附录ⅥH),结果3批样品pH值为5.7、5.8、5.7。本品pH值均在5.0~6.0范围内,考虑到人体的耐受性和生产的可控性,将本品的pH值定为:5.0~7.0。
2.3.2 不溶性微粒
取本品,依法检查(中国药典2010年版二部附录ⅨC),结果3批样品不溶性微粒检查均符合规定。
2.3.3 可见异物
取本品,依法检查(中国药典2010年版二部附录ⅨH),结果3批样品可见异物检查均符合规定。
2.3.4 装量
取本品,依法检查(中国药典2010年版二部附录ⅩF),结果3批样品装量检查均符合规定。
2.3.5 重金属
取本品20 ml,加醋酸盐缓冲液(pH值3.5)2 ml与水使成25 ml,依法检查(中国药典2010年版二部附录ⅧH第一法),结果三批样品重金属检查均<10/ 1000万。
2.3.6 细菌内毒素
2.3.6.1 限值确定 参考中国药典2010年版二部氯化钠注射液质量标准中对细菌内毒素的限值规定为0.5 EU/ml,因此本品的限值定为0.5 EU/ml。
2.3.6.2 干扰试验 取供试品,用上述两个厂家的鲎试剂进行干扰试验(照中国药典2010年版二部附录ⅪE项下方法进行),结果天麻素氯化钠注射液对鲎试剂的凝集反应无增强或抑制作用,不干扰测定。
2.3.6.3 供试品细菌内毒素检查 供试品溶液的制备:取本品,照细菌内毒素检查法(中国药典2010年版二部附录ⅪE)进行测定,3批样品细菌内毒素均<0.5 EU/ml,订入质量标准。
2.3.7 无菌
取本品,照薄膜过滤法,依法检查(中国药典2010年版二部附录ⅪH),结果3批样品无菌检查均符合规定。
2.4 含量测定
参考国家药品标准天麻素注射液(WS1-XG-023-2001)和中国药典2010年版二部“氯化钠注射液”,对本品中的天麻素和氯化钠进行含量测定。
2.4.1 天麻素含量测定方法
照天麻素注射液(WS1-XG-023-2001),用紫外-可见分光光度法(中国药典2010年版二部附录ⅣA)测定。
2.4.1.1 检测波长的选择 取天麻素原料适量,加0.9%的氯化钠溶液溶解并稀释至16 μg/ml,照紫外-可见分光光度法 (中国药典2010年版二部附录ⅣA)测定。由紫外扫描图可知,本品在220 nm与269 nm波长处有最大吸收波长。参照天麻素注射液(WS1-XG-023-2001),将本试验的检测波长定为220 nm。
2.4.1.2 氯化钠及其他辅料的干扰 取处方中除天麻素外的等比例的辅料适量,照紫外-可见分光光度法(中国药典2010年版二部附录ⅣA)测定。由紫外扫描图可知,氯化钠及其他辅料在220 nm处几乎无吸收,不干扰本试验。
2.4.1.3 线性关系试验 取天麻素对照品16.2 mg,精密称定,置50 ml量瓶中,加0.9%的氯化钠溶液溶解并稀释至刻度,摇匀,分别精密量取1、2、4、5、8 ml,分置100 ml量瓶中,加0.9%的氯化钠溶液稀释至刻度,摇匀,取上述5种溶液照分光光度法(中国药典2005年版药典二部附录ⅣA),以0.9%的氯化钠溶液为空白,在220 nm波长处测定吸收度,以其吸收度(A)为纵坐标,其浓度(C)为横坐标,进行线性回归,回归方程A=1868.2C+1049.9,结果表明r为0.9998,天麻素在3.24~25.92 μg/ml浓度范围内与吸收度呈良好的线性关系。
2.4.1.4 稳定性试验 取本品适量 (约相当于天麻素200 mg),置250 ml量瓶中,加0.9%的氯化钠溶液稀释至刻度,摇匀,作为供试品溶液。于室温下放置8 h,分别于0、1、2、4、6、8h测定,取供试品溶液照分光光度法(中国药典2010年版药典二部附录ⅣA),以0.9%的氯化钠溶液为空白,在220 nm波长处测定吸收度,考察样品含量稳定性,结果表明8 h内测定方法稳定。
2.4.1.5 精密度试验 取110106批样品适量 (约相当于天麻素200 mg),置250 ml量瓶中,加0.9%的氯化钠溶液稀释至刻度,摇匀,作为供试品溶液。取供试品溶液照分光光度法 (中国药典2010年版药典二部附录ⅣA),以0.9%的氯化钠溶液为空白,在220 nm波长处测定吸收度,连续测定6次,结果表明本法精密度良好,天麻素的RSD为0.16%。
2.4.1.6 回收率试验 精密称取天麻素约为12、16、19 mg(每组称取3个平行样),分置100 ml量瓶中,按处方量加入辅料,加0.9%的氯化钠溶液溶解并稀释至刻度,摇匀,各精密移取2 ml分置25 ml量瓶中,加0.9%的氯化钠溶液稀释至刻度,摇匀,作为供试品溶液。另精密称取经105℃减压干燥3 h的天麻素对照品适量,按同法制成每毫升中含16 μg的溶液,作为对照品溶液,取供试品溶液及对照品溶液,照分光光度法(中国药典2010年版药典二部附录ⅣA),以0.9%的氯化钠溶液为空白,在220 nm波长处测定吸收度,结果表明本品天麻素含量测定回收率良好(表2)。
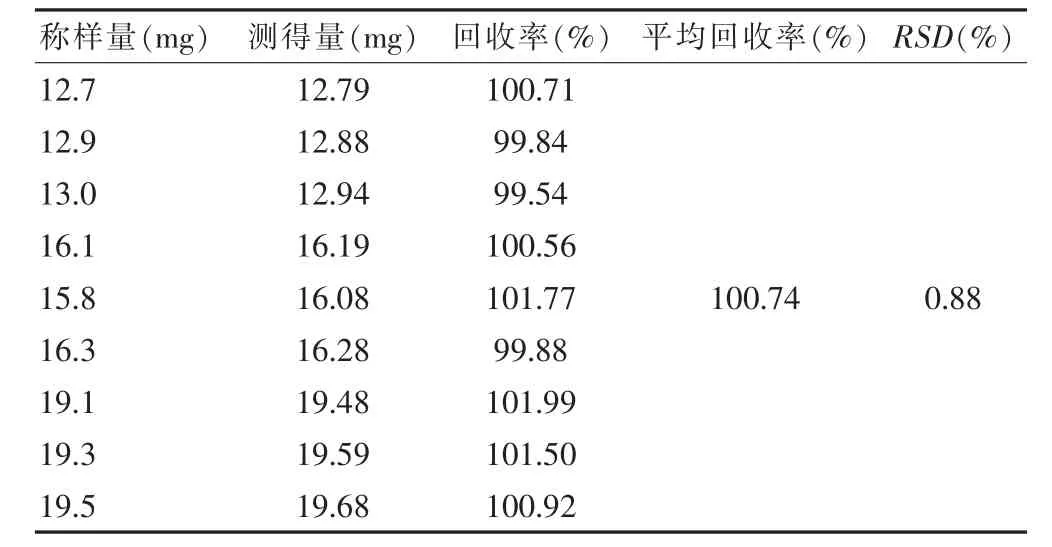
表2 本品天麻素含量回收率试验结果
2.4.1.7 含量测定 精密量取本品20 ml,置250 ml量瓶中,加0.9%的氯化钠溶液稀释至刻度,摇匀,即制得供试品溶液。另精密称取经105℃减压干燥3 h的天麻素对照品适量,加0.9%的氯化钠溶液制得每毫升中含16 μg的溶液,作为对照品溶液,取上述两种溶液照分光光度法 (中国药典2010年版药典二部附录ⅣA),以0.9%的氯化钠溶液为空白,在220 nm波长处测定吸收度,计算本品中天麻素的含量,结果3批样品天麻素含量为101.47%、100.26%、102.01%。以上数据表明,3批样品天麻素含量均在 90.0%~110.0%范围内,订入质量标准。
2.4.2 氯化钠
取本品,照中国药典2010年版“氯化钠注射液”含量测定方法对本品的氯化钠进行含量测定。
2.4.2.1 测定方法 精密量取本品10 ml,置100 ml锥形瓶中,加水40 ml、2%糊精溶液5 ml与荧光黄指示剂5~8滴,用硝酸银滴定液(0.1 mol/L)滴定。每毫升的硝酸银滴定液(0.1 mol/L)相当于5.844 mg的氯化钠。
2.4.2.2 天麻素及辅料的干扰试验 取处方中除氯化钠外的其他组分10 ml,加水40 ml溶解并稀释至刻度,2%糊精溶液5 ml与荧光黄指示剂5~8滴,用硝酸银滴定液(0.1 mol/L)滴定。所耗硝酸银滴定液的量为0.01 ml,表明天麻素及辅料在此试验中几乎无干扰。
2.4.2.3 线性关系试验 取氯化钠约1.4023 g,置100 ml的洁净量瓶中,加水溶解并稀释至刻度,摇匀,精密量取1、2、4、5、8 ml,置不同的100 ml量瓶中,加水稀释至刻度,精密量取上述溶液10 ml,置不同的100 ml锥形瓶中,加水40 ml、2%糊精溶液5 ml与荧光黄指示剂5~8滴,用硝酸银滴定液(0.1 mol/L)滴定。扣除空白,以滴定体积为纵坐标,氯化钠浓度为横坐标,进行线性回归,结果r为0.9999,表明氯化钠在70.4~105.6 mg范围内与滴定体积呈良好的线性关系。
2.4.2.4 重复性试验 取本品(批号:110106),照上述方法重复测定6次含量,结果表明,本法重复性较好,氯化钠的RSD=0.10%。
2.4.2.5 回收率试验 取氯化钠为72、90、108 mg(每组称取3个平行样),分置100 ml锥形瓶中,按处方量加入天麻素及辅料,加水20 ml溶解,再加水40 ml、2%糊精溶液5 ml与荧光黄指示剂5~8滴,用硝酸银滴定液(0.1 mol/L)滴定。扣除空白,计算回收率。结果可见氯化钠回收率良好(表3)。
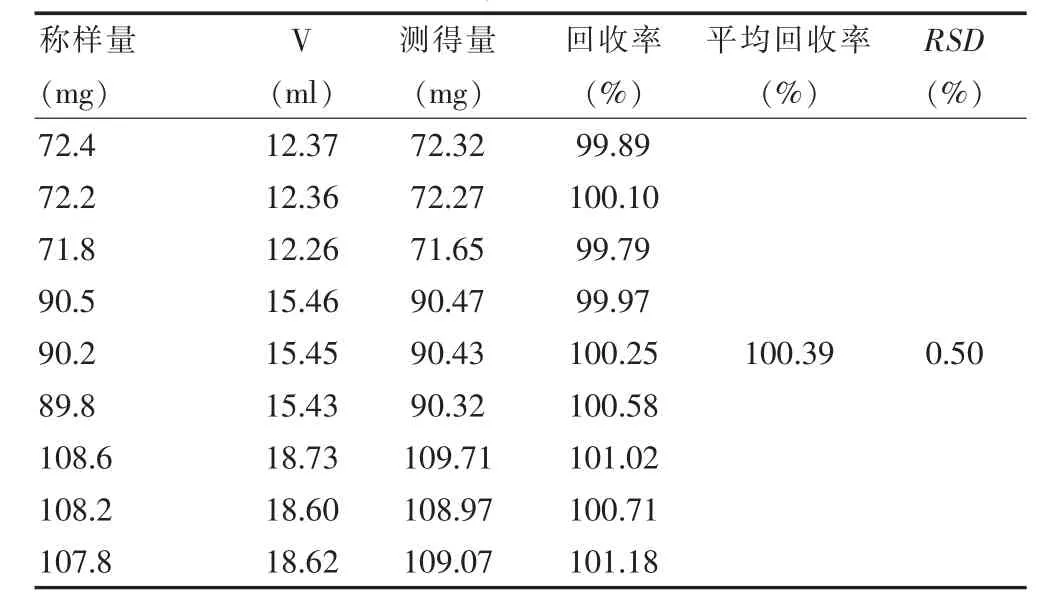
表3 本品氯化钠含量测定回收率试验结果
2.4.2.6样品测定 精密量取本品10 ml,置100 ml锥形瓶中,加水40 ml、2%糊精溶液5 ml与荧光黄指示剂5~8滴,用硝酸银滴定液(0.1 mol/L)滴定,计算氯化钠的含量。每毫升硝酸银滴定液(0.1 mol/L)相当于5.844 mg的氯化钠。结果3批样品氯化钠含量为101.25%、102.00%、100.41%,表明3批样品氯化钠含量均在90.0%~110.0%范围内,订入质量标准。
3 讨论
参照“天麻素注射液”国家标准(WS1-XG-023-2001)中含量测定项,对天麻素的含量测定方法进行设计并经方法学验证可行;参照中国药典2010年版氯化钠注射液标准,对本品的氯化钠进行含量测定方法设计,并经方法学验证可行,方法操作简单,准确可靠,重复性好,可作为天麻素氯化钠注射液的质量控制方法。
[1]WS1-XG-023-2001.天麻素注射液[S].
[2]国家药典委员会.中华人民共和国药典2010年版二部[M].北京:中国医药科技出版社,2009.
[3]李捷伟,刘吉祥.常用药物辅料手册[M].上海:第二军医大学出版社,2000.
[4]毕殿洲.药剂学[M].4版.北京:人民卫生出版社,2003.
[5]吕国平,王春芹,蔡中琴.天麻素注射液的药理及临床研究[J].中草药,2002,33(5):附3~附5.
[6]张淑芹,朱虹,张永会.天麻的药理作用及临床应用[J].内蒙古中医药,1995,(S1):79.
[7]任德成.天麻的药理研究及临床应用[J].江西中医学院学报,1998,10(3):142-143.
[8]金文姗,田德蔷.天麻的化学和药理研究概况[J].中药研究与信息,2000,2(6):21-23.
[9]范玉奇,李文兰,王艳萍,等.天麻化学成分及药理性质研究的进展[J].药品评价,2005,2(4):309-312.
[10]刘军生,檀战山,崔立波,等.天麻素注射液治疗颈性眩晕的临床观察[J].中国中西医结合急救杂志,2002,9(2):88.
[11]陈静,刘世喜,胡国华,等.天麻素注射液治疗眩晕的多中心随机单盲对照试验[J].中国循证医学杂志,2004,4 (12):864-870.
[12]周宏友.天麻素注射液治疗中老年眩晕临床疗效评价[J].中国临床药理学与治疗学,2003,8(4):471-472.
[13]任广智.天麻素注射液治疗椎基底动脉供血不足临床观察[J].中国医院药学杂志,2002,22(7):46.
[14]冯晓东,黄新生.天眩清注射液治疗内耳眩晕病的临床观察[J].中草药,2001,32(10):102.
[15]韩增灿,曹秀兰.天麻素注射液治疗眩晕症76例疗效观察[J].右江医学,2001,29(5):444.
《中国医药导报》杂志
欢迎订阅 欢迎投稿
《中国医药导报》杂志是国家卫生和计划生育委员会主管、中国医学科学院主办的医药卫生期刊,现为旬刊,国内统一刊号:CN11-5539/R,国际标准刊号ISSN1673-7210,邮发代号:80-372,本刊系中国科技核心期刊(中国科技论文统计源期刊)、美国化学文摘(CA)收录期刊、解放军医学图书馆中文生物医学期刊文献数据库收录期刊,所刊登的文章被万方数据、中国知网、中文科技期刊数据库全文收录。每期定价20元,全年36期优惠价540元。
本刊设专家论坛、综述、论著、实验研究、药理与毒理、临床研究、药物与临床、麻醉与镇痛、医学检验、病理分析、影像与介入、病例报告、医疗器械、中医中药、生物医药、药品检验、制剂与技术、药师与临床、不良反应监测、药物经济学、调查研究、护理研究、教育研究、科研管理、法规与标准、卫生研究、医疗管理、产业与市场、医药监管、工作探讨等栏目。是广大医药卫生科研、教育、医护、药事、经营管理等人员了解医药研究进展、发展动态,展示医药科研成果,学习先进经验,探讨工作难题,交流和提高业务学术水平的得力助手,也是发表医药学术论文的阵地。在本刊发表的论文可获得继续教育学分。本刊订户凭订阅单复印件投稿优先发表。
社 址:北京市朝阳区通惠家园惠润园(壹线国际)5-3-601邮编:100025
投稿热线:010-59679061 59679063 发行热线:010-59679533
传 真:010-59679056 投稿信箱:yydb@vip.163.com
网 址:www.yiyaodaobao.com.cn
Quality standard study of gastrodin sodium chloride injection
LIU Jian1YAN Jian-kun2
1.Department of Drug and Equipment,Baotou Chaoju Ophthalmic Hospital of Red Cross in Inner Mongolia Autonomous Region,Baotou 014060,China;2.Basic Science,Health School of Baotou City,Baotou 014030,China
ObjectiveTo establish the quality standard of gastrodin sodium chloride injection.MethodsGastrodin content in the formulation was quantitatively determined by ultraviolet-visible spectrophotometry.ResultsThe gastrodin had maximum absorbance at 220 nm by ultraviolet-visible scanning,while the sodium chloride and other auxiliary material had no obvious absorbance and no interference for this research.ConclusionUltraviolet-visible spectrophotometry is a easy,precise and repeatable method.It can used as a quality control method for the gastrodin sodium chloride injection.
Gastrodin sodium chloride injection;Quality standard;Ultraviolet-visible spectrophotometry
R927.11
A
1674-4721(2014)10(c)-0008-04
2014-08-11本文编辑:李亚聪)

