人工泪滴眼液无菌检查方法验证的探讨
宫瑞中王 丽王峻峰张 琳冀 明王 婧邓自新程爱华
(1 山西省眼科医院,山西 太原 030002;2 山西省药检所,山西 太原 030001)
人工泪滴眼液无菌检查方法验证的探讨
宫瑞中1王 丽1王峻峰1张 琳1冀 明1王 婧1邓自新2程爱华2
(1 山西省眼科医院,山西 太原 030002;2 山西省药检所,山西 太原 030001)
目的 建立我院制剂人工泪滴眼液的无菌检查法。方法 依据《中国药典)2010年版二部附录ⅪH无菌检查法,分别采用直接接种法、薄膜过滤法对人工泪滴眼液进行无菌检查方法研究。结果 直接接种法与薄膜过滤法都满足验证要求,但因我院制剂人工泪滴眼液为微黏稠澄明液体,薄膜过滤法不易操作,过滤困难,而直接接种法方便操作的同时还可以定量计算污染率。结论 直接接种法可以作为我院制剂人工泪滴眼液进行无菌检查的首选方法。
人工泪滴眼液;直接接种法;薄膜过滤法;方法验证
我院制剂人工泪滴眼液用于无泪液患者及干燥性角膜炎、结膜炎,为了确保临床用药安全,需对其进行无菌检查。按照《中国药典》2010年版二部附录ⅪH无菌检查法的要求[1,2],我们分别采用直接接种法和薄膜过滤法对3批人工泪滴眼液进行了无菌检查的方法学验证[3],结果表明我院制剂人工泪滴眼液采用直接接种法是行之有效的。
1 实验材料
1.1 仪器
SPX-250B-Z型生化培养箱(上海博迅实业有限公司医疗设备厂);MJX-205B-Z型霉菌培养箱(上海博迅实业有限公司医疗设备厂);MLS-3780高压蒸汽灭菌器(三洋电机株式会社)。
1.2 本实验所用菌株
金黄色葡萄球菌[CMCC(B)26003]、大肠埃希菌[CMCC(B)44102]、枯草芽孢杆菌[CMCC(B)63501]、生孢梭菌[CMCC(B)64941]、铜绿假单胞菌[CMCC(B)10104]、白色念珠菌[CMCC(F)98001]、黑曲霉[CMCC(F)98003](本实验所用菌株均购自中国食品药品检定研究院,均为第三代)。
1.3 培养基及试药
营养琼脂培养基(批号12330)、营养肉汤培养基(批号1203122)、硫乙醇酸盐培养基(批号1304102)、玫瑰红钠琼脂培养基(批号120410)、改良马丁培养基(批号120515)、改良马丁琼脂培养基(批号120113),以上均由中国食品药品检定研究院提供。人工泪滴眼液(批号20130603、20130607、20130613由山西省眼科医院制剂室生产)。
2 方法与结果
验证环境为10000级洁净条件下的局部100级单向流空气区域内进行。实验环境无菌室及洁净台按《医药工业洁净室(区)悬浮粒子、浮游菌和沉降菌的测试方法》的现行国家标准进行洁净验证,测定结果符合规定。
2.1 菌液制备
2.1.1 接种金黄色葡萄球菌、枯草芽孢杆菌、大肠埃希菌、铜绿假单胞菌的新鲜培养物少许至营养肉汤培养基10 mL中,接种生孢梭菌的新鲜培养物至硫乙醇酸盐流体培养基中,35 ℃培养24 h,取此培养物1 mL加0.9%的无菌氯化钠注射液9 mL,10倍递增稀释至<100 cfu/mL的菌悬液,做活菌计数备用。具体见表1。
2.1.2 接种白色念珠菌的新鲜培养物至10 mL改良马丁培养基中,25 ℃培养48 h,取此培养液1 mL加0.9%的无菌氯化钠注射液9 mL,采用10倍递增稀释法,稀释至10-5,使菌数约<100 cfu/mL。
2.1.3 接种黑曲霉的新鲜培养物至改良马丁琼脂培养基中,25 ℃培养5 d,加入5 mL的含0.05%(mL/mL)聚山梨酯80的0.9%的无菌氯化钠注射液,将孢子洗脱,吸出孢子悬液至无菌试管内,用含0.05%(mL/mL)聚山梨酯80的0.9%的无菌氯化钠注射液制成每 1mL含孢子数<100 cfu/mL的孢子悬液。
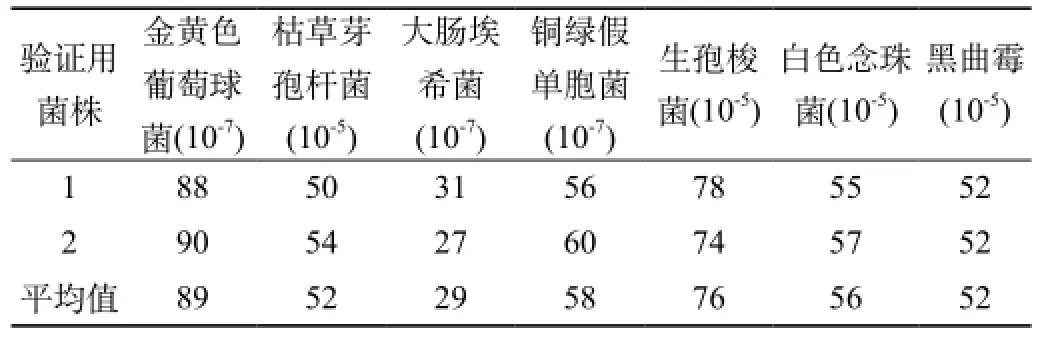
表1 验证试验用活菌计数
2.2 培养基适用性检查
2.2.1 无菌性检查
取上述硫乙醇酸盐流体培养基、改良马丁培养基(每批培养基随机抽取不少于5瓶)各制备成灭菌溶液,在相应条件下培养14 d,结果表明为无菌生长。
2.2.2 灵敏度检查
取装有12 mL的硫乙醇酸盐流体培养基的试管9支,分别接种<100 cfu的金黄色葡萄球菌、铜绿假单孢菌、枯草芽孢杆菌、生孢梭菌各2支,另1支不接种作为空白对照,32 ℃培养3 d;取5支装量为9 mL的改良马丁培养基,分别接种<100 cfu的白色念珠菌、黑曲霉各2支,另1支不接种作为空白对照,25 ℃培养5 d,逐日观察结果。结果表明,加菌的培养基管均生长良好,而空白对照管均无菌生长,因此灵敏度检查符合规定。见表2。
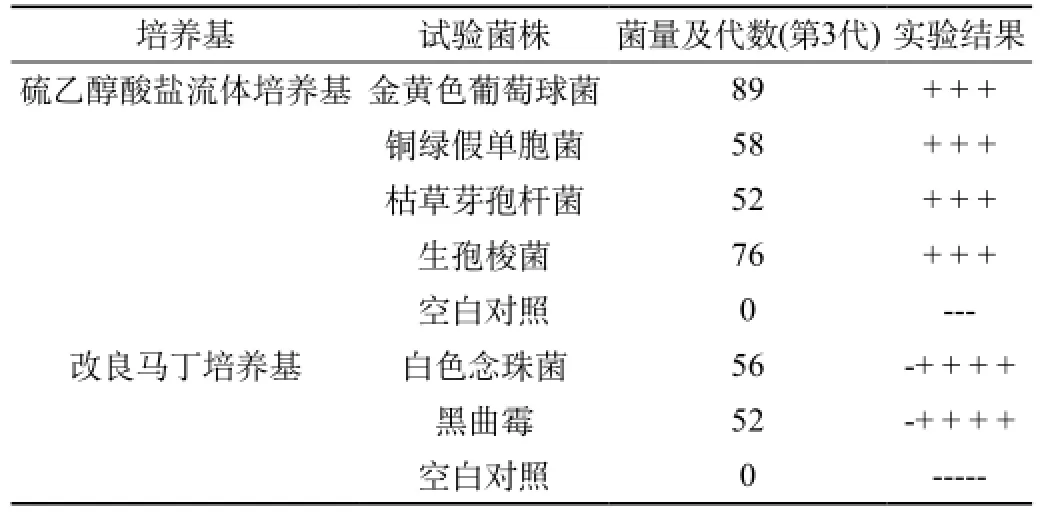
表2 培养基灵敏度试验
2.3 方法验证
2.3.1 薄膜过滤法
①阳性组:将制备好的各试验菌液分别接种至相应的培养基(50毫升/支)中。②试验组:取15支样品,过滤于一次性三联集菌器中,将样品注入无菌氯化钠注射液中,过滤,再用无菌氯化钠注射液冲洗,在最后一次的冲洗液中加入相应的试验菌液1 mL,冲洗完后,将滤膜取下,接种至相应培养基中。③样品组:方法同试验组,但不加相应的试验菌液。④阴性对照组:另取同批次的一支硫乙醇酸盐流体培养基和一支改良马丁培养基作为阴性对照。将上述各组置规定温度下培养3~5 d,逐日观察,结果见表3。试验中发现,同对照组比较,含样品的各组中的试验菌均生长良好,并与各阳性对照组中相应的菌落生长情况相似,阴性对照组无菌生长,表明样品在此检验条件下无抑菌作用,但试验中发现,由于人工泪滴眼液的性状为无色的微黏稠澄明液体,难以通过滤膜,薄膜过滤法不易操作,影响试验的顺利进行,因此不建议采用薄膜过滤法进行人工泪滴眼液的无菌检查。
2.3.2 直接接种法
①试验组:取样6支,其中4支每支取样2 mL加至硫乙醇酸盐流体培养基20 mL中,其余2支每支取样2 mL加至改良马丁培养基20 mL中,再分别加入6株试验菌。②阳性组:另取一装有同体积相应培养基的试管,加入等量试验菌,作为阳性组。③样品组:分别取样2 mL加至硫乙醇酸盐流体培养基和改良马丁培养基。④阴性对照组:另取同批次的硫乙醇酸盐流体培养基和改良马丁培养基作为阴性对照。将上述各组置规定温度下培养3~5 d,逐日观察,结果见表4。
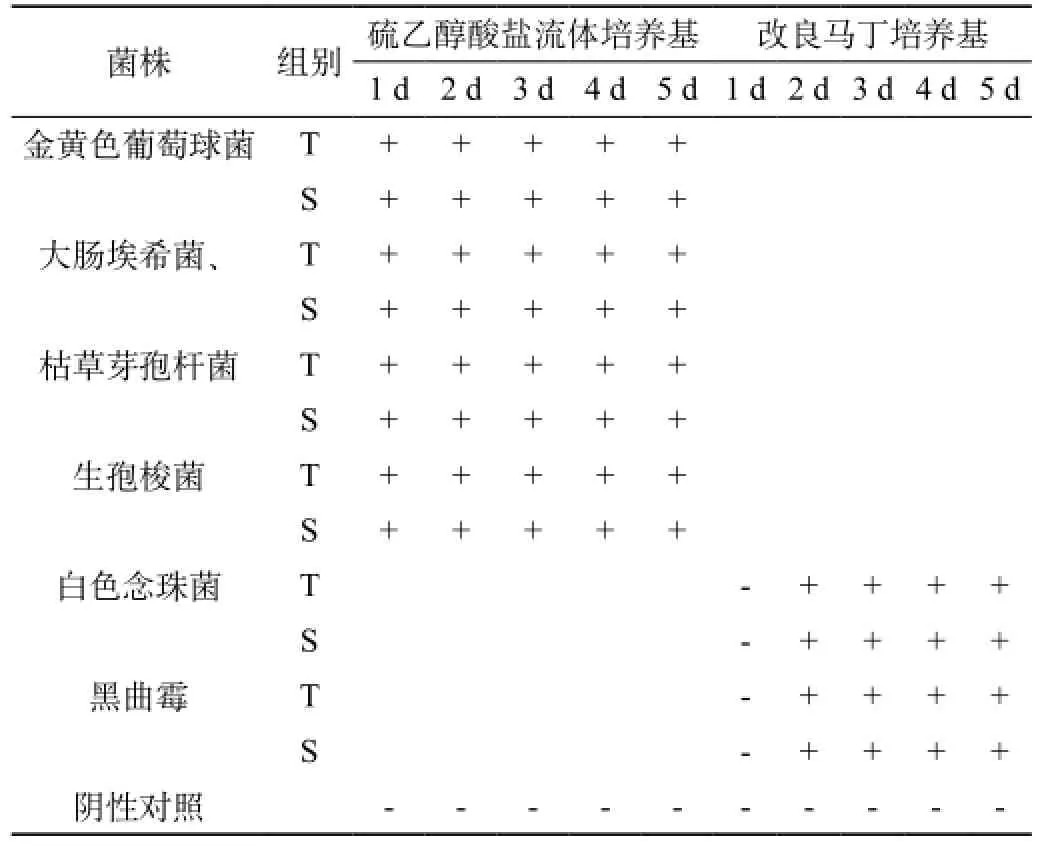
表3 薄膜过滤法验证试验各组生长情况
结果表明,供试品各管中的试验菌均生长良好,则说明供试品的该检验量在该检验条件下无抑菌作用或其抑菌作用可以忽略不计,可以按照直接接种法在该检查条件下进行供试品的无菌检查。因此直接接种法从检验方法到实验操作上都适合人工泪滴眼液的无菌检验。
3 结 论
综上所述,按照《中国药典》(2010年版)可采用直接接种法或薄膜过滤法进行人工泪滴眼液的无菌检查,在两法的方法验证中,我院制剂人工泪滴眼液对对照菌均无抑制作用。鉴于人工泪滴眼液为微黏稠的液体,直接接种法与薄膜过滤法更加方便易行、污染概率小,且在方法验证后的大规模试验中能定量计算人工泪滴眼液的污染率,更能体现方法的科学性和检验结果的准确性,是我院制剂人工泪滴眼液无菌检查的首选方法。
[1] 国家药典委员会.中华人民共和国药典2010年版(二部)附录103[M].北京:中国医药科技出版社,2010.
[2] 赵亚丽,吴英.双黄连注射液无菌检查的方法验证[J].黑龙江医药,2011,24(1):31-33.
[3] 李彩霞.参芪注射液无菌检查的方法验证[J].海峡药学,2010, 22(6): 35-36.
R446
B
1671-8194(2014)18-0089-02

