基于技术审评的全瓷义齿用氧化锆瓷块的质控要求
李竹,梁文 ,迟戈,李非,马艳彬,杨牧
辽宁省食品药品监督管理局 技术审评中心,辽宁 沈阳 110003
基于技术审评的全瓷义齿用氧化锆瓷块的质控要求
李竹,梁文 ,迟戈,李非,马艳彬,杨牧
辽宁省食品药品监督管理局技术审评中心,辽宁沈阳110003
0 前言
全瓷义齿用氧化锆瓷块以氧化锆为主要材料,用于制作牙科固定义齿的冠、桥、嵌体、贴面,与以粉状形式提供的全瓷义齿用氧化锆材料产品不同。
目前我国生产该类产品的企业并不多,通过国家食品药品监督管理局网站搜索,数据库显示国内注册的有6项、进口注册有2项,基于其制作全瓷义齿的优点,氧化锆瓷块应用量逐年升高,在国产医疗器械产品中具有一定代表性。同时,该类产品按照《医疗器械分类目录》,其管理类别为I I类6863-7金属、陶瓷类义齿材料,即其安全性和有效性应加以必要的控制。因此分析研究这类产品的安全性和有效性,全面掌握性能要求是十分必要的。
目前,用氧化锆瓷块制作全瓷义齿的临床应用情况文献中有报道。Fischer 等人[1]认为,氧化锆瓷块相较以往的氧化铝瓷块,有更高的机械力学参数,极限超载能力强,三单位桥义齿的承受力约为2000N。就制作的桥体而言,二氧化锆全瓷冠瓷块较二氧化铝全瓷冠瓷块而言,显示出极佳的机械性能和长时间的可靠性。但并不是所有患者都适合全瓷义齿,选择全瓷固定义齿时必须评估颌间距离以确保支架和饰瓷有足够空间。颌间距离小、连接体面积不能满足要求的患者(如深覆合浅覆盖,基牙临床牙冠短),基牙松动、进行性牙周病患者;有严重副功能运动、夜磨牙等不良习惯的患者均不适于全瓷义齿[2-4]。
从我国注册技术审评角度,降低上述风险发生的一个有效手段就是对氧化锆瓷块性能要求进行严格控制。本文基于各国行业标准和指南文件[5-6],临床应用实际情况及笔者从事注册技术审评工作的经验,对氧化锆瓷块的结构组成、作用机理、技术要求、风险分析、临床要求5个方面进行了分析研究,旨在进一步规范氧化锆瓷块产品的技术性能要求,尤其是原材料要求和加工义齿工艺控制。
1 氧化锆瓷块的结构组成
氧化锆瓷块按照形状,分为圆柱体、长方体及定制几何体(图1)。
氧化锆瓷块主要成份为氧化锆、氧化钇、氧化铝及其他氧化物。材料成分(重量百分比)举例:氧化锆(含氧化铪、氧化钇)(Z r O2+HfO2+Y2O3)≥99%;氧化钇(Y2O3)4.5%~6.0%;氧化铪(HfO2)≤5%;氧化铝(A l2O3)≤0.5%;其他氧化物≤0.5%。

图1 氧化锆瓷块
2 工作原理
(1)氧化锆瓷块的成型工艺。国内外生产企业一般采用等静压成型或干压成型两种工艺,氧化锆瓷块典型生产工艺流程,见图2。关键工艺是粉体成型和瓷坯预烧结,对产品的性能指标有直接影响。少数国外生产企业如美国Glidewell采用注浆成型工艺。等静压成型或干压成型的优点是工艺简单、适合大工业生产;缺点是透光性稍差,整体性能略低。注浆成型的优点是瓷块透光性好,整体性能如强度、密度等较高;缺点是工艺复杂。

图2 氧化锆瓷块典型生产工艺流程图
(2)氧化锆瓷块是制作全瓷义齿的材料,相当于制作金属烤瓷修复体的金属基底,如钴铬合金。氧化锆瓷块通常采用CA D/CA M(计算机辅助设计/计算机辅助制造)方法制作全瓷义齿,制作流程如下:① 对牙齿或牙模进行数字扫描,获得牙齿或牙模三维数据;② 按照牙模数据进行CA D过程,设计瓷块加工模型;③ 采用数控机床按照瓷块加工模型进行CA M过程,制成全瓷义齿内冠;④ 全瓷义齿内冠经空气烧结或真空烧结,以达到临床使用要求的强度和美观效果;⑤ 用瓷粉在全瓷义齿内冠表面上釉,形成瓷瓷结合,制作出全瓷义齿。
3 技术要求
(1)企业针对手动系统和兼容的自动加工系统推出的不同形状的氧化锆瓷块都应有尺寸和误差要求。
(2)氧化锆瓷块表面应无斑点裂纹及可见异物。
(3)氧化锆瓷块密度为(标示值±0.05)g/cm3。
(4)氧化锆瓷块烧结密度应>6.0g/ cm3。
(5)按YY 0716-2009中规定的三点弯曲试验(或双轴弯曲试验)测试,经说明书规定的程序烧结后的样块,挠曲强度应>800MP a(或根据不同用途参照I S O6872标准中关于挠曲强度的要求)。
(6)按YY 0716-2009中规定的Ⅱ型陶瓷的试验方法进行试验,按说明书规定的程序烧结后的样块,化学溶解性应<100μg/cm2。
(7)氧化锆瓷块的生物相容性应按照标准Y Y/T0268的规定选择试验项目,一般要求评价产品的细胞毒性、口腔粘膜刺激性、迟发型超敏反应、亚慢性(亚急性)全身毒性及遗传毒性。
(8)按YY 0716-2009中规定的方法进行试验时,氧化锆瓷块中铀-238的活性浓度<1.0B q/g。
(9)按ISO13356-2008中4.2规定的原子吸收光谱分析等方法进行试验时,氧化锆瓷块的成分应符合企业声称的产品成分。
4 风险分析
风险分析可参照YY/T0316-2008《医疗器械风险管理对医疗器械的应用》的有关要求,产品定性定量分析是否准确;危害分析是否全面;风险可接收准则,降低风险的措施及采取措施后风险的可接收程度,是否有新的风险产生;是否确定了风险管理的范围、规定和人员职责分工;是否确定了风险反馈的规定及信息收集情况。
依据Y Y/T0316附录E列举了氧化锆瓷块的危害分析(表1),还应结合具体产品的情况评估。针对产品的各项风险,生产企业应采取应对措施,确保风险降到可接受的程度。
风险判定及分析考虑的问题包括:材料微量辐射等因素是否会导致使用中出现不正常结果,操作信息包括操作方法的准确性、警示性语言、注意事项、运输及意外机械破坏可能存在的危害等。
5 临床要求
氧化锆瓷块产品属于制作全瓷义齿的材料,全瓷义齿属于定制式固定义齿中的一种,依据《关于印发豁免提交临床试验资料的第二类医疗器械目录(试行)的通知》(国食药监械[2011]475号)文件,定制式固定义齿可以豁免提交临床试验资料,因此本产品也可豁免临床试验,但应同时提交申报产品与已上市同类产品的对比说明。对比说明应当包括工作原理、产品材质、结构组成、主要技术指标、预期用途等内容。
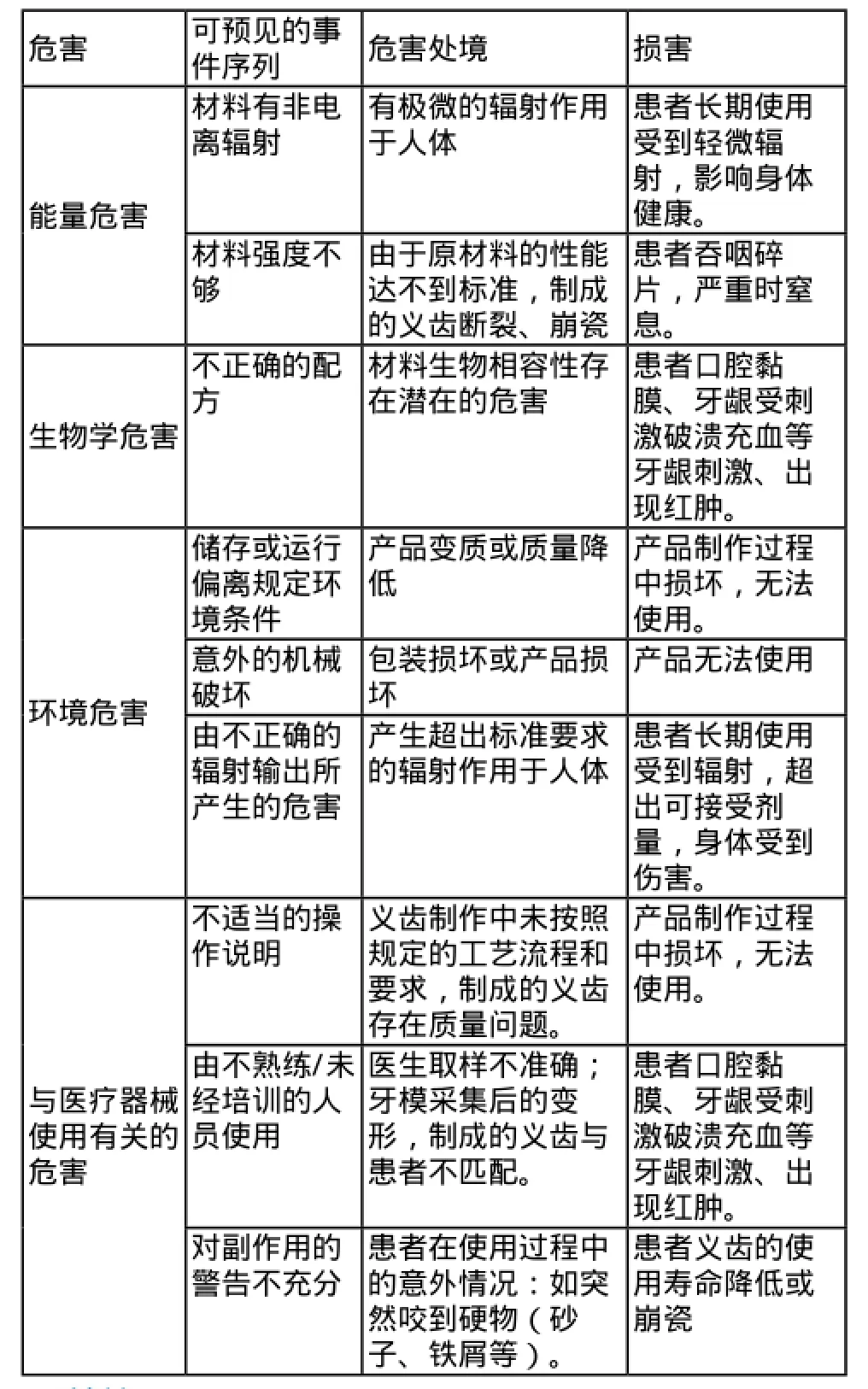
表1 氧化锆瓷块危害分析
6 结论
氧化锆瓷块是制作全瓷义齿的材料,主要特点半透性和生物相容性好。用氧化锆瓷块制作全瓷义齿具有极佳美观性和良好的生物相容性,受到医生和患者的推崇。目前口腔固定义齿全瓷修复已成为主要的发展趋势之一,因其有足够的厚度,能在保证瓷强度的同时增强美观性;又因其生物相容性好,不会引起过敏反应。这些均是金属烤瓷修复不可比拟的优势[7-8]。氧化锆瓷块需求日益增加,从监管层面,为保证氧化锆瓷块产品的安全性和有效性,应加强对氧化锆瓷块产品原材料性能要求,氧化锆的含量是否符合标准规定等监管,同时评价其生产瓷块工艺是否成熟可控。从行业层面,上市后的临床应用,加强对用瓷块加工全瓷义齿工艺的控制,以保证产品质量;从使用层面,医疗机构应对比不同材料制作义齿的风险和受益,选取有质量保证的瓷块产品,严格注意制作全瓷义齿的程序和烧结温度及事项。
[参考文献]
[1] Fischer H,Weber M,Marx R.Lifetime prediction of allceramic bridges by computational methods[J].J Dent Res,2003,82(3):238-242.
[2] 张蕾,骆小平.全瓷固定修复的工艺、材料及应用现状[J].口腔颌面修复学杂志,2007,8(3):212-215.
[3] 张兰. 二氧化锆全瓷系统在口腔修复科中的临床应用与发展趋势[J].医学理论与实践,2011,(5):520-522.
[4] 邓薇,杨永进,蔡兴伟,等.二氧化锆全瓷冠在前牙美容修复中的应用[J].口腔颌面修复学杂志,2011,(2):101-103.
[5] 国家食品药品监督管理局.中国医疗器械监管技术基础[M].北京:中国医药科技出版社,2009.
[6] 国家食品药品监督管理局.全瓷义齿用二氧化锆瓷块注册术审查指导原则[S].2012.
[7] 战德松,李柘.牙列缺损修复材料-从金属烤瓷系列到全瓷系列[J].中国实用口腔杂志,2008,1(4):242-245.
[8] 闫嘉群,宋蓉,印明晶,等.In-ceram氧化铝全瓷冠与氧化锆全瓷冠在前牙修复中的临床效果比较[J].哈尔滨医科大学学报, 2011,45(4):349-351.
本文作者:李竹,硕士,主要从事中药鉴定及医疗器械评审。
作者邮箱:lizhu81@163.com
[中图分类号]R783.6;R197.39
[文献标志码]B
doi:10.3969/j.issn.1674-1633.2014.02.022
[文章编号]1674-1633(2014)02-0077-03
收稿日期:2013-06-03修回日期:2013-12-23
Technical-Evaluation-Based Quality Control Requirements of All-Ceramic Zirconia Tiles
LI Zhu, LIANG Wen, CHI Ge,LI Fei, MA Yan-bin, YANG Mu
Technical Evaluation Center, Liaoning Food and Drug Administration, Shenyang Liaoning 110003, China
[摘要]目的从技术审评角度,研究全瓷义齿用氧化锆瓷块产品的安全性和有效性。方法基于各国行业标准和指南文件,对全瓷义齿用氧化锆瓷块产品从结构组成、工作原理、技术要求、风险分析、临床要求5个方面进行了分析研究。结论从技术审评角度,为保证产品的安全性和有效性,应加强对全瓷义齿用氧化锆瓷块的原材料和生产工艺的控制。
[关键词]全瓷义齿;氧化锆瓷块;固定义齿;技术审评;生产工艺
Abstract:ObjectiveTo investigate the security and effectiveness of all-ceramic zirconia tiles fromthe perspective of technical evaluation.MethodsBased on the relevant standards and guidance documents in this fi eld fromvarious countries and regions, the research was carried out focusing on the structure, principle, technical requirements, risk analysis and clinical trial of the all-ceramic zirconia tiles.ConclusionFromthe perspective of technical evaluation, the rawmaterials and production techniques of the all-ceramic zirconia tiles should be enhancedly controlled so as to ensure the security and effectiveness.
Key words:all-ceramic dentures; zirconia tiles; fixed dentures; technical evaluation; production techniques

