温度对滴滤池硝化过程氧化亚氮释放的影响
王亚宜,陈 玉,周 东,林喜茂 (同济大学环境科学与工程学院,污染控制与资源化研究国家重点实验室,上海200092)
温度对滴滤池硝化过程氧化亚氮释放的影响
王亚宜*,陈 玉,周 东,林喜茂 (同济大学环境科学与工程学院,污染控制与资源化研究国家重点实验室,上海200092)
研究了某大学污水处理厂的一个滴滤池(生物膜系统)随季节变化N2O的释放特征.结果表明,滴滤池中N2O的释放浓度范围为0~18.21×10-6,释放量为20.5~554g N2O/(m3∙a),其释放因子(N2O-N/进水NH3-N)为0.1%~0.8%.N2O释放量与季节变化有关,夏季产生量较高而春季较少,空气和进水的温差是影响滴滤池中硝化作用和N2O释放的主要因素,7月份时气温和水温温差较小,导致空气中的氧气无法充入水中,水中溶解氧的不足使得滴滤池硝化不完全,N2O释放量最高.另外,N2O释放量的昼夜变化规律表明,滴滤池的N2O释放、硝化作用和温度变化相关,通过在线监测N2O释放和水温/气温温度变化可以间接反映滴滤池的生物硝化效果.
N2O;滴滤池;温差;生物膜;硝化作用
氧化亚氮(N2O)是一种强温室气体,其全球增温潜势约是CO2的320倍[1],来源有自然因素和人为因素,污水生物处理过程是一个潜在人为源[2].很多研究均证明污水的生物脱氮处理过程会有N2O的释放[3-9]; Kampschreur等[8]总结,在实际城镇污水处理厂的脱氮过程中可能有0~14.6%的氮转化为N2O释放.
污水处理过程N2O的释放主要发生在硝化和反硝化阶段,随着各国对污水处理厂出水中氮素控制的严格,城市污水厂必须进行脱氮工序, N2O释放潜能也随之增加,这可能会将环境污染问题从水体转移到大气中[4-5,8].因此,研究污水脱氮过程N2O的产生机理及预测和控制影响N2O释放的运行参数尤为重要.
目前对于污水处理过程N2O的释放研究主要围绕合成废水或纯培养的活性污泥系统展开[7,11-14],较少有针对生物膜系统,尤其是滴滤池生物膜系统.滴滤池具有稳定性好、维护安装费用低、易于操作控制以及硝化效果好等优点[15-16].随着氮素排放标准的提高,污水处理厂需对原有工艺进行升级改造,滴滤池虽是脱氮单元的较好选择,但也存在增加N2O释放的可能性.Søvik等[17]证实,滴滤池中N2O的释放多源于硝化的不完全.在英国,滴滤池占到了污水处理中生物单元的60%~70%,然而,滴滤池中N2O的释放和硝化反硝化的关系还鲜有研究和报道.
滴滤池中供氧的唯一方式是通过自然通风实现空气循环,而空气循环效果取决于污水温度(由进水温度决定)与环境空气的温度差.因此,气水温差决定了滴滤池可利用的氧气量,进而影响N2O释放.目前有关温度对氨氮去除和N2O产生潜在影响的研究仍然较少.本实验以英国克兰菲尔得大学污水处理厂(Cranfield University Sewage Treatment Works,CUSTW)的生物滴滤池为研究对象,旨在更清晰地揭示N2O产生机理,探究温度等环境因素对滴滤池中N2O释放的影响,评估滴滤池中N2O释放量及确定能够减少N2O排放的最佳条件.
1 材料与方法
1.1 污水厂工艺
CUSTW的主体工艺为生物膜系统,工艺流程如图1(a)所示,主要处理校园生活污水,服务人数为6000人/a,污水流量为385~1008m3/d,平均流量为525m3/d.检测N2O释放的对象为第一级的一个滴滤池[图1(b)],其高度为1.8m、直径为12m,填料为蜂窝状斜管填料.该滴滤池水力负荷大于4.64m3/(m2∙d),属于高负荷处理方式.
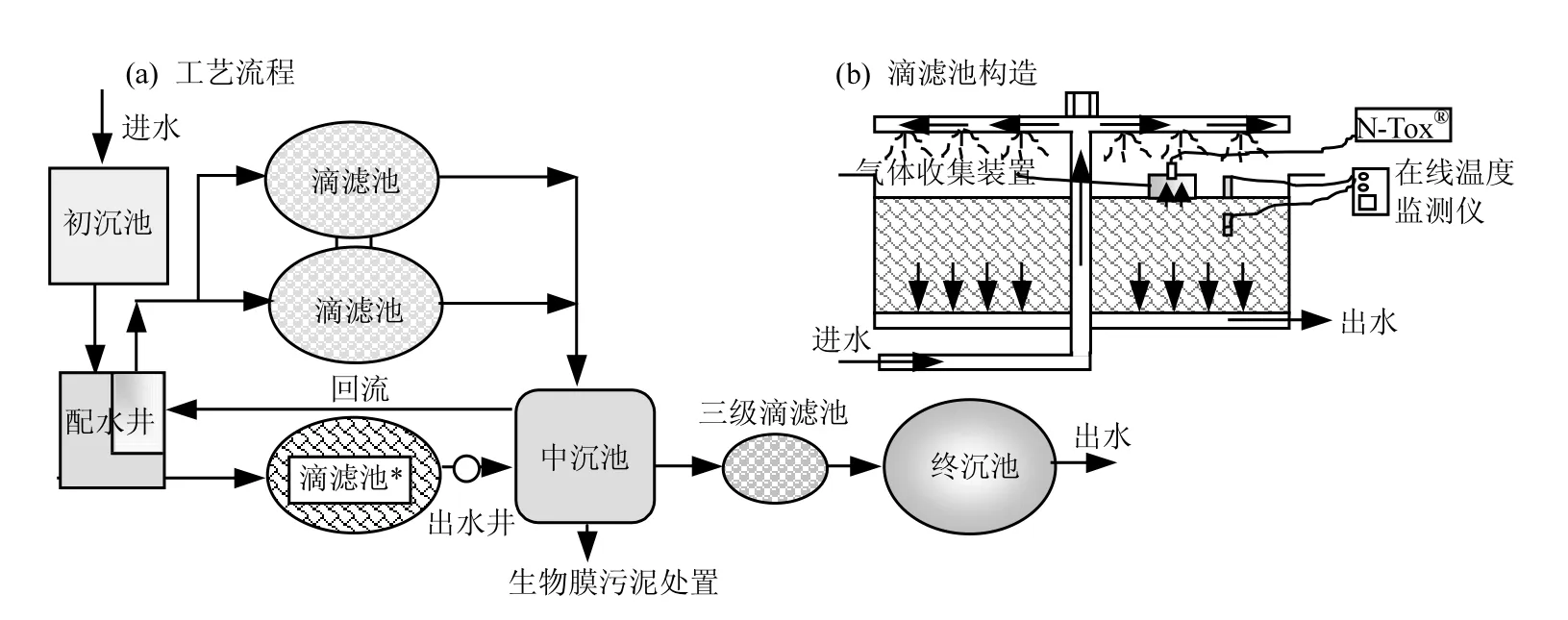
图1 污水处理厂工艺流程及滴滤池构造Fig.1 The wastewater treatment process in Cranfield University Sewage Treatment Works and the structure of the trickling filter
1.2 取样和分析
本实验从1月31日开始在线监测N2O排放量,其中在3月17日~5月31日期间,每周取进出水水样3次,取样时间均为12:00~15:00,分析结果表明,水质周际变化较小,故在后续实验阶段(6月1日~8月30日),每周取水样改为2次.同时也开展了昼夜24h定时采集进出水水样的实验,揭示滴滤池昼夜的水质变化和N2O释放的关系.
采用N-Tox®(Water Innovate Ltd, UK)分析仪测量N2O气体浓度(60s记录1次),该仪器测量范围为0~200×10-6,检测限低于0.5%.通过两个温度探针(Delta-T, DL-2, Cambridge, UK)测量水气交界处空气温度和滴滤池50cm深度处的温度,每隔5min记录1次.测试点的天气情况从英国气象局网站获取.
进出水的总氮(TN),NH3-N, NO2--N, NO3--N, COD和磷通过哈希试剂法(Vwr International adapted from Standard Methods)检测,BOD5和混合液悬浮固体浓度(Mixed liquor suspended solids,MLSS)则通过标准方法APHA[18]来测量.
1.3 空气量计算
为计算滴滤器中N2O释放量,采用欧根方程(Ergun Equation, 1952) [式(1)]和薛定谔方程[15][式(2)]计算空气流速:
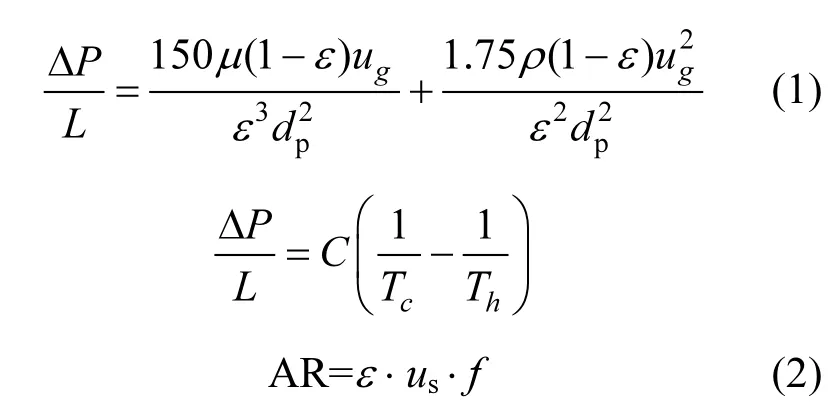
式中:ΔP为通过滤料的压降, Pa;L为滤料高度,m;ε为滤料空隙率,无量纲;μ为液体黏度;ρ为液体密度,kg/m3;dp为颗粒直径,m;Tc为低温区温度,℃;Th为高温区温度,℃;us为表面流体速度,m/s;C为常数,取值3462(℃⋅Pa)/m;AR为空气流速,m3/s;f为滴滤池面积,m2.
2 实验结果
2.1 滴滤池随季节的硝化效果变化
系统中进水总氮为24~60.8mg/L,其中氨氮为13.5~51mg/L,硝酸盐氮为0.5~2.4mg/L,亚硝酸盐氮含量可忽略不计.由图2可知,实验中,出水氨氮浓度在3~4月为(15.4±5.6)mg/L,5~6月为(13.5± 5.8)mg/L, 7~8月为(19.4±3.3)mg/L.在BOD5平均负荷为0.34kg/(m3∙d)情况下,滴滤池氨氮的去除率为(51±18.4)%.据报道,在13~15℃的高速滴滤池中硝化速率可以达到1.8g/(m2∙d),在三级滴滤池中,当进水处氨氮浓度高且BOD5/TKN比值低时,最大的氨氮去除率范围为1.2~2.9g/(m2∙d)[15].本研究中,3~4月、5~6月和7~8月平均环境温度分别为6,12.5,15.2℃,相应的硝化速率依次为(0.68± 0.16),(0.50±0.18),(0.29±0.10)g/(m2∙d).本研究的滴滤池由于采用的自然通风充氧形式,同时进水中又含有较高的BOD5,故其硝化效率相较于三级硝化滴滤池低.另一方面,因进水含有BOD5,在滴滤池中发现了总氮的去除.
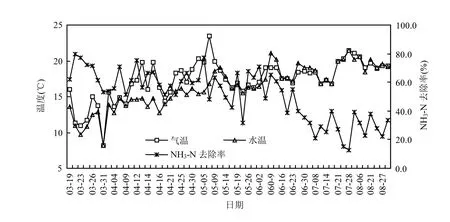
图2 滴滤池随气水温差变化对NH3-N的去除率Fig.2 The variations of temperature differences of air and wastewater and NH3-N removal efficiency
2.2 滴滤池N2O释放的季节性变化特点
如图3所示,在滴滤池运行过程可观测到N2O的产生,且呈现明显的季节性:夏季释放量升高而春季减少,且夏季>冬季>春季(表1);同时,在温度较高的晴天比温度较低的多云和雨天N2O释放量更多.
冬季至春季的环境温度变化并未明显影响N2O的释放,而到夏季(6月下旬至8月)水温接近于环境温度,N2O释放量明显增加(图3和表1);在3~5月间,空气与水体温差在10:00~16:00左右时上升1℃(图3).同时,并未发现N2O释放量与水力负荷间具有显著相关性.
2.3 昼夜N2O释放和温度变化的关系
比较4月18日、5月4日和7月1日24h的温度及N2O释放发现,滴滤池N2O释放量的昼夜变化与气水温差变化存在相关性,气温和水温的变化幅度的不同对N2O的释放产生显著影响,一旦水温和空气温度接近时,滴滤池N2O的释放量立即增加(图4).
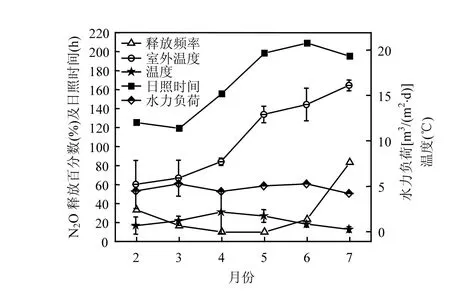
图3 滴滤池内N2O释放量随季节变化规律Fig.3 the variations of the monthly N2O emission frequency
2.4 氨氮(NH3-N)去除与N2O释放
由图5和图6可见,5月12日及6月30日中,白天进水的氨氮量逐渐增加,并在19:00~20:00之间达到一个最高浓度;随后,在晚间和晨间有小幅下降.两个测量日中,CUSTW进水氨氮浓度未发生明显的波动,但出水氨氮浓度和氨氮去除率(在8:00~22:00之间测得)却呈现不同结果.在5月12日8:00~17:00,气水温差增大,氨氮去除率随之下降;当气水温度相同时,氨氮去除率持续下降(图5和图6).6月30日的氨氮去除率为28%~35%,远远低于5月12日的氨氮去除率(图6).上述结果正好符合温度差假设:气水温差越大,氨氮的去除率越高.此外,在6月30日,晚间和第二天早晨的出水硝态氮浓度与白天维持在一个水平上,这说明只要有温度差,即使环境温度下降,滴滤池内的硝化作用速率也不会下降.
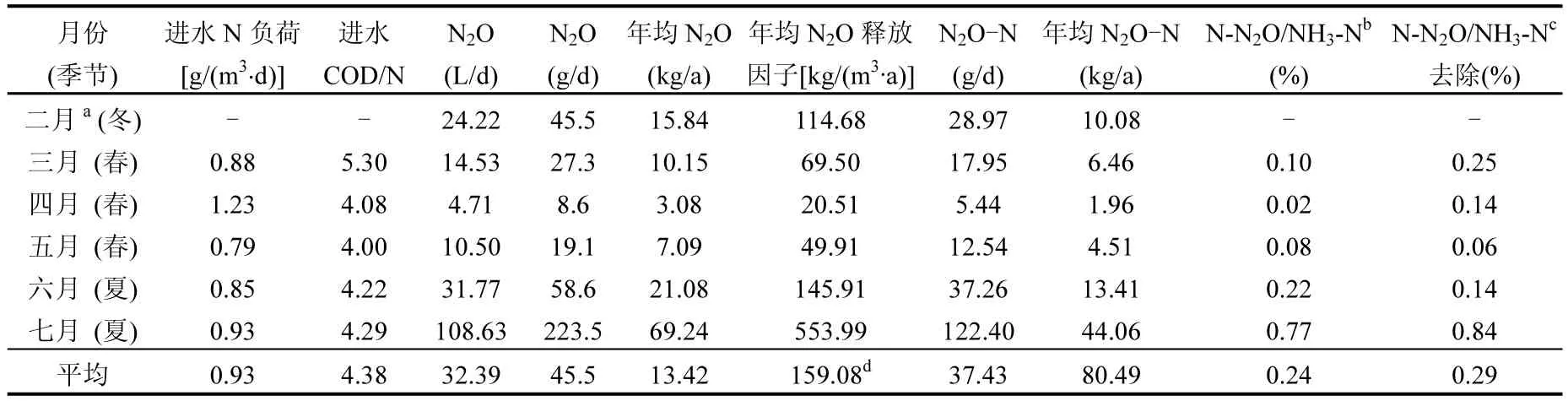
表1 N2O释放的月际变化Table 1 Monthly average emission of N2O-N as percentage of the yearly average loading of NH3-N (based on the data during February to July)
如图5所示,5月12日和6月30日的N2O释放浓度在08:00~22:00之间均有增加,在次日00:00~08:00时N2O释放量减少,其中6月30日N2O释放量高于5月12日.在5月12日的09:30~16:00之间,空气与水的温差幅度较大,N2O的释放量很少.随后,在16:00左右温差消失,出现了N2O释放峰值,其浓度约为4.86×10-6.此后,在22:00时左右,气水温差再次增加,相应监测到N2O释放量较小(图5c).该现象与图中氨氮去除率先增加后逐渐降低的趋势相吻合.在6月30日,气水温度整天都较接近,故在08:00~24:00之间持续检测到N2O的释放,此时的氨氮去除率与5月12日的相比,处于一个较低的水平.6月30日N2O浓度在14:00达到最高(7.76×10-6),明显高于5月12日的峰值(4.86×10-6) (图5c和图5d).
3 讨论
3.1 滴滤池中硝化反应与N2O的释放
试验结果表明,气水温差较环境温度更能决定滴滤池最终的硝化率(图2).温差变小引起空气循环流动不足,因此尽管环境温度较高,硝化率也会降低.在本研究中,氨氮去除率的最高和最低值分别发生在早春和夏季,这与Metcalf等[15]报道的滴滤池内的硝化反应速率在夏季会降低的结论相吻合.
N2O释放量的昼夜和季度性变化均表明:在自然通风充氧的滴滤池中,气水温差较环境温度对N2O释放影响更大.N2O的月释放量与月平均气水温差呈明显的指数关系(n=6时,r2=0.98)(图7),这一结果证明,气水温差可能直接决定N2O的释放.
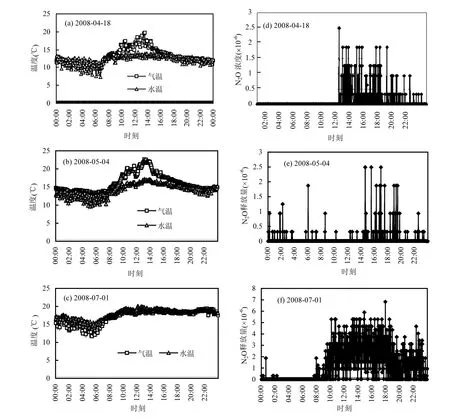
图4 典型日N2O释放量与气水温差变化的关系Fig.4 The relationship between daily N2O emission frequency and daily temperature difference between air and water (absolute values)
相反,月平均温度与每月N2O释放无显著相关性(r2=0.64)(图7).另外,对N2O释放量的日变化分析发现,一旦气水温度相等,滴滤池N2O持续释放(图4和图5).气水温度接近引起的溶解氧不足是导致滴滤池内N2O释放量过高的原因.N2O释放的时间长短取决于空气与水温温度接近的时间长短.通常来说,气水温差越大,滴滤池内N2O释放量就越小(图4b和图4e).
3.2 影响滴滤池内N2O产生的其他因素
除了空气和水之间的温度差引起的充氧效果直接影响N2O的释放外,气候因素如环境温度、空气压力、滴滤池的湿度也对滴滤池N2O排放有直接或间接的影响.
在英国,夏季高温通常引起较低的气压,从传质角度来说,低气压会导致局部压力下生物膜传质系数的降低,进而加剧硝化作用不完全而促使N2O的释放.同时,空气压力对N2O从液相到气相的释放影响显著.温暖期低气压条件下,从液相释放到大气中的N2O比高气压条件下要高,这使得滴滤池在低气压条件下可能产生更高的N2O.这些气候因素引起的综合效应可以很好地解释即便空气和水之间存在温度差,即溶解氧充足,仍然可能观测到滴滤池N2O的释放.此外,对滴滤池和连续进水的研究结果证明,本研究滤池内的大气湿度对N2O的排放几乎没有影响.

图5 滴滤池24h内温度变化与N2O释放Fig.5 Temperature variations and N2O emission within 24hours in the TF
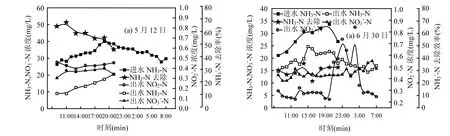
图6 滴滤池内24h内氮素变化Fig.6 Nutrient variation profiles during 24hours in the TF
已有研究表明,好氧曝气池(采用人工配水)N2O的产生与进水氮负荷及有机负荷均呈相关性[19].Kimochi等[6]研究发现,生活污水处理过程中N2O的释放量在进水碳氮比(C/N)较低时会增加.然而,在本研究中,从N2O释放量的月变化来看,进水水质指标如氨氮负荷或者C/N与N2O产生并无明显的相关性(表1).这可能有两方面的原因:实验期间进水氨氮负荷自始至终均维持在0.79~1.23gN/(m3∙d),且无明显波动(表1),这说明氨氮负荷仍未高到足以影响N2O释放;就进水C/N来说,它主要影响反硝化脱氮途径N2O的释放,然而,在本研究滴滤池中,几乎没有反硝化途径,这削弱了进水C/N比对N2O释放的影响[11].
3.3 微生物的新陈代谢对滴滤池内N2O产生机制的影响
滴滤池N2O的释放特点与生物膜内微生物的活动,即硝化与反硝化有关.由于本研究滴滤池对总氮的去除较少,因此生物硝化是产生N2O的主要来源.在生物硝化过程,N2O的产生途径有两种可能:1)硝化菌反硝化作用,即氨氮硝化为NO2-后被还原为N2O,主要由氨氧化菌(AOB)来完成,是个生物过程;2)氨氧化过程的中间产物(如羟氨,NH2OH)的分解[9,11].NH2OH被氧化成NO2-分为两个过程:NH2OH先被氧化为不稳定的亚硝酰基团(NOH);然后NOH再被氧化为NO2-.在NH2OH的氧化过程中,可能会出现NOH的积累.而不稳定的NOH会分解产生N2O[14,19].由于NOH分解产生N2O的过程并不需要酶的作用,所以该过程并非生物反应,而是化学反应.一般认为,NOH化学分解产生N2O的途径在城市污水硝化处理中并不占主导地位.
很多研究证明,硝化过程产生N2O的主要原因是溶解氧的缺乏[2,7,12,20-22].Hooper等[20]报道,在低溶解氧(DO)条件下,羟氨的不完全氧化导致了N2O产生.Tallec等[7]的研究也表明,活性污泥二级处理过程中DO浓度1mg/L的情况下,N2O的释放量较高;他们认为,在低DO条件下(0.1~2mg/L),N2O的释放有两种途径:自养硝化细菌反硝化作用和异养反硝化作用.在本研究的滴滤池中也出现了同样现象,即当气水温度较接近时(表明硝化过程氧气不足),观察到较多的N2O释放(图4和图5).
在本滴滤池中,认为AOB反硝化作用是产生N2O的主要途径,即在低DO条件下,AOB体内的反硝化酶将NO2-还原为N2O.另一方面,在滴滤池生物膜微环境中,因氧气扩散受限,使得DO浓度沿着生物膜厚度方向呈现梯度变化,从而形成了缺氧/厌氧边界,这也会诱发N2O的释放.这种现象类似于活性污泥絮体中的同步硝化反硝化(SND)过程:Zeng等[23]报道过DO扩散受限,在絮体边缘会形成好氧区,而絮体内部则形成缺氧区,这种分布会在好氧-缺氧区边界引起亚硝酸盐的积累,一旦边界处亚硝酸盐的积累达到一定浓度,便会引起N2O的释放.在本研究的滴滤池N2O释放也可能源于同样机制.滴滤池系统N2O产生的确切机制有待进一步证实.
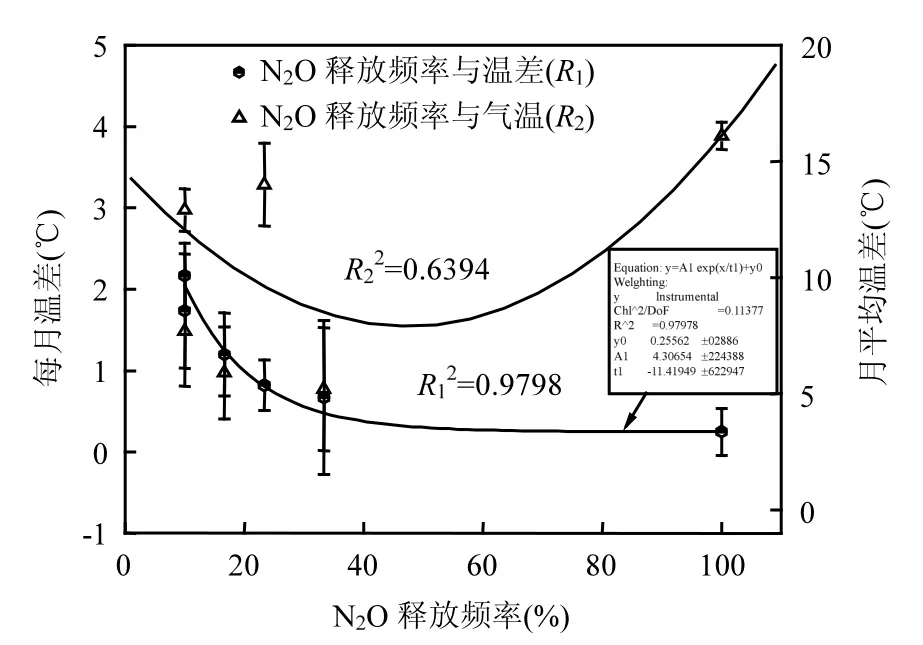
图7 N2O释放与每月气水温差变化的关系Fig.7 N2O emission in relation to temperature differences between wastewater and air
3.4 滴滤池污水处理厂的全球变暖贡献
滴滤池N2O释放量的变化范围为8.6~223.5g/d和3.2~69.2kg/a(平均13.4kg/a ),其变化取决于气水温度接近相等(DO受限)周期的长短与程度.本研究中N2O释放量变化范围为20.5~554g/(m3∙a),年平均值为159.1g/(m3∙a),这与活性污泥法原位处理工艺的N2O的释放量相吻合[5,24].Czepiel等[5]在生活污水处理厂的曝气池内(Durham, USA)监测N2O的释放量,得出N2O年总释放量为3.2×104g,水相中为242.4g/(m3∙a).同样,Kimochi等[6]监测日本的一个间歇曝气活性污泥系统中的N2O释放量发现,在间歇曝气的运行条件下,年N2O释放量的变化范围为(0.43~1.89)×103g,其中水相中的N2O释放量为5.89~25.87g/(m3∙a).后来,Tallec等[7]在Valenton污水厂中监测N2O释放,结果显示N2O释放量变化范围为0.05~0.16g/(m3∙a).这些研究中N2O释放量的不同主要是由处理工艺、操作条件及环境因素的不相同等引起的.
在本研究中,0.1%~0.8%的进水氨氮均以N2O-N的形式释放(表1),这与前人的研究数据相吻合:0.0037%~1.4%[17]和0.02%~0.53%[24].另外, Valenton污水处理厂中N2O释放量为氨氮总量的0.1%~0.4%[7],同样接近于本实验中所得结果.
本实验首次对生物滤池中N2O释放进行定量研究,这些数据可以作为滴滤池生物膜系统N2O释放量和释放特征的参考.虽然从滴滤池中释放到大气中的总N2O与总微生物转换的氮素相比很少,然而,随着排入废水中的氮素的增加,尤其是处理高氨氮工业废水时,污水处理厂中N2O释放量也会随之增加.因此,在应对全球变暖的问题上,监测N2O的释放与阐明N2O的释放机制,并提出相应减排方案尤为重要.同时,由于N2O的释放直接反应了水厂的运行情况,测量N2O的释放对水厂管理同样重要.
在减少或控制滴滤池中N2O的产生方面,为了在特定时间(如夏季)防止滴滤池(底部)供氧不足,建议在自然通风滴滤池中安装强制通风系统.
4 结论
4.1 对于自然通风的滴滤池,气水温差对N2O的释放产生较大影响:气水温差越小,溶解氧不足,滴滤池中释放的N2O越多.N2O的释放可能主要来自AOB参与的反硝化过程.
4.2 滴滤池中N2O的释放量的变化范围为0~18.21×10-6,其中进水氨氮中0~0.24%以N2O的形式释放出来.滴滤池中N2O的释放量随着季节变化,夏季最高,春季最少.为了减少滴滤池中N2O的释放,增加强制通风可能较为有效.
4.3 N2O的释放与氨氮的去除有显著的相关性,通过在线监测N2O的释放可以预测滴滤池的硝化效果.
[1] IPCC—Intergovernmental panel on climate change. Climate change 2001—the scientific basis [R]. Contribution of working group I to the third assessment report of the intergovernmental panel on climate change. Cambridge, UK: Cambridge University Press, 2001.
[2] Park K Y, Lee J W, Inamori Y, et al. Effects of fill modes on N2O emission from the SBR treating domestic wastewater [J]. Water Sci. Technol., 2001,43(3):147–150.
[3] Zheng H, Hanaki K, Matsuo T. Production of nitrous oxide gas during nitrification of wastewater [J]. Water Sci. Technol., 1994, 306:134–141.
[4] SuÈmer E, Weiske A, Benckiser G, et al. Influence of environmental conditions on the amount of N2O released from activated sludge in a domestic wastewater treatment plant [J]. Experientia., 1995,51:419–422.
[5] Czepiel P, Crill P, Harriss R. Nitrous oxide emissions from municipal wastewater treatment [J]. Environ. Sci. Technol., 1995,29:2352–2356.
[6] Kimochi Y, Inamori Y, MizuochiM, et al. Nitrogen removal and N2O emission in a full-scale domestic wastewater treatment plant with intermittent aeration [J]. J. Fermentation and Bioengineering, 1998,86(2):202–206.
[7] Tallec G, Garnier J, Billen G, et al. Nitrous oxide emissions from secondary activated sludge in nitrifying conditions of urban wastewater treatment plants: effect of oxygenation level [J]. Water Res., 2006,40:2972–2980.
[8] Kampschreur M J, Temmink H, Kleerebezem R, et al. Nitrous oxide emission during wastewater treatment [J]. Water Res., 2009,43(17):4093-4103.
[9] Kampschreur M J, Poldermans R, Kleerebezem R, et al. Emission of nitrous oxide and nitric oxide from a full-scale single-stage nitritation-anammox reactor [J]. Water Sci. Technol., 2009, 60(12):3211-3217.
[10] Hanaki K, Hong Z, Matsuo T. Production of nitrous oxide gas during denitrification of wastewater [J]. Water Sci. Technol., 1992,26(5/6):1027–1036.
[11] Itokawa H, Hanaki K, Matsuo T.Nitrous oxide production in high-loading biological nitrogen removal process under low COD/N ratio condition [J]. Water Res., 2001,353:657–664.
[12] Butler M D, Stephenson T, Stokes L, et al. Dinitrogen oxide detection for nitrification failure early warning systems [J]. Water Sci. Technol., 2005,52(8):249–256.
[13] Lemaire R, Meyer R, Taske A, et al. Identifying causes for N2O accumulation in a lab-scale sequencing batch reactor performing simultaneous nitrification, denitrification and phosphorus removal [J]. J. Biotechnol., 2006,122(1):62–72.
[14] Kampschreur M J, Tan N C G, Kleerebezem R, et al. Effect ofdynamic process conditions on nitrogen oxides emission from a nitrifying culture [J]. Environ. Sci. Technol., 2008,42:429–435.
[15] Metcalf and Eddy Inc. Wastewater engineering: Treatment and reuse (Fourth Edition) [M]. New York, McGraw-Hill Companies, Inc, 2003.
[16] Pearce, P. Trickling filters for upgrading low technology wastewater plants for nitrogen removal [J]. Water Sci. Technol., 2004,49(11/12):47–52.
[17] Søvik A K, Kløve B. Emission of N2O and CH4from a constructed wetland in southeastern Norway [J]. Sci. Tot. Environ., 2007,380:28–37.
[18] APHA. Standard Methods for Examination of Water and Wastewater [S]. 20th ed.; American Public Health Association: Washington, DC, 1998.
[19] Colliver B B, Stephenson, T. Production of nitrogen oxide and dinitrogen oxide by autotrophic nitrifiers [J]. Biotechnology Advances, 2000,18(3):219–232.
[20] Hooper A B, Vannelli T, Bergmann D J, et al. Enzymology of the oxidation of ammonia to nitrite by bacteria.Antonie van Leeuwenhoek [J]. International Journal of General and Molecular Microbiology, 1997,71(1/2):59–67.
[21] Noda N, Kaneko N, Mikami M, et al. Effects of SRT and DO on N2O reductase activity in an anoxic-oxic activated sludge system [J]. Water Sci. Technol., 2003,48(11/12):363–370.
[22] Butler M D, Wang Y Y, Cartmell E, et al. Nitrous oxide emissions for early warning of biological nitrification failure in activated sludge [J]. Water Res., 2009,43(5):1265-1272.
[23] Zeng R J, Lemaire R, Yuan Z, et al. Simultaneous nitrification, denitrification, and phosphorus removal in a lab-scale sequencing batch reactor [J]. Biotechnol. Bioengi., 2003,84(2): 170–178.
[24] Johansson A E, Kasimir Klemedtsson A, Klemedtsson L, et al. Nitrous oxide exchanges with the atmosphere of a constructed wetland treating wastewater: Parameters and implications for emission factors [J]. Chemical and Physical Meteorology, 2003,55(3):737-750.
日常防护型口罩将出国标
目前,雾霾再袭华北地区,作为防护手段的口罩再次成为人们热议的话题.那么,面对市场上种类繁多的口罩,该如何规范相关企业设计和生产?
在日前举办的消费品安全标准“筑篱”专项行动启动仪式上,国家标准化管理委员会相关负责人称,《日常防护型口罩技术规范》预计年底前将公布征求意见稿,新国标的制定实施将有利于规范日常防护型口罩市场,解决消费者选择困难的问题.
近两年频繁出现的雾霾天气带动了口罩等防霾用品的热销,但因缺乏国家标准,日常防护型口罩存在标签标识不统一等突出问题,使得消费者选择困难.
据了解,目前国内现行的口罩标准有3个:《呼吸防护用品—自吸过滤式防颗粒物呼吸器》(GB 2626-2006)、《医用防护口罩技术要求》(GB 19083-2010)、《医用外科口罩》(YY 0469-2011).按照标准分类,第一个属于劳动防护类产品标准,后两个属于医用防护产品标准,由于使用环境、防护对象不同,其中任何一个标准都不能完全适用于普通公众日常使用的防护型口罩.由于没有标准规范,企业及检测机构对于日常防护口罩的检测都是自己选择标准,造成市场上同类产品出现不同检测结果的混乱局面.
据了解,《日常防护型口罩技术规范》将涉及口罩原料要求、结构要求、标签标识要求、外观要求等,主要指标包括功能性指标,如颗粒物过滤效率、呼气吸气阻力指标、密合性指标等;作为纺织品,还涉及甲醛含量、pH值,以及大肠杆菌菌群数量、真菌菌落总数等指标.
值得一提的是,新国标还将根据大气污染程度对口罩进行分级、分类,如根据大气污染程度,分为重度污染适用、中度污染适用、轻度污染适用;同时,针对不同人群对口罩的性能要求做了区分,如针对成人、儿童、体弱者,要求设定不同的呼气阻力指标等.
摘自《中国环境报》
2014-10-21
Impact of temperature on nitrous oxide emission in a tricking filter.
WANG Ya-yi*, CHEN Yu, ZHOU Dong, LIN Xi-mao (State Key Laboratory of Pollution Control and Resources Reuse, School of Environmental Science and Engineering, Tongji University, Shanghai 200092, China). China Environmental Science, 2014,34(11):2796~2804
As a powerful greenhouse gas,nitrous oxide (N2O) is found in wastewater treatment plants. The factors influencing N2O emission from a natural-draft trickling filter (TF) was investigated in situ by treating domestic wastewater. The concentration of N2O released from TF varied between 0~18.21×10-6and the amount of N2O emission was estimated to be 20.5~554g N2O/(m3∙a), representing 0.1%~0.8% of oxidized ammonia. Variations of N2O emission followed the seasonal weather pattern, with more N2O emission in the summer period and less in the spring. Temperature differences between air and water were the most influential environmental factors governing the nitrification and the N2O emission patterns in TF. The highest N2O emission occurred in July when temperature differences between air and water were minimal, causing insufficient oxygen availability and incomplete nitrification. The daily patterns indicated that N2O emission was closely correlated with the variations of nitrification and temperature differences, which made it possible for using on-line temperature or N2O monitor to identify the nitrification failures.
nitrous oxide;tricking filter;temperature difference;biofilm;nitrification
X703.5
A
1000-6923(2014)11-2796-09
王亚宜(1977-),女,浙江上虞人,教授,博士,主要从事可持续污水生物处理理论及新技术的研究.发表论文60余篇.
2014-01-24
国家自然科学基金资助项目(51178325;51378370);中央高校基本科研业务费专项基金;上海市科技人才项目(12QH1402400)
* 责任作者, 教授, yayi.wang@tongji.edu.cn;wyywater@126.com

