硝酸分解钠硼解石制备硼酸的工艺研究
朱 军,仲剑初,王洪志
(大连理工大学化工学院,辽宁大连116024)
硝酸分解钠硼解石制备硼酸的工艺研究
朱 军,仲剑初,王洪志
(大连理工大学化工学院,辽宁大连116024)
以玻利维亚钠硼解石矿为原料,采用硝酸酸解硼矿制备硼酸。考察了钠硼解石的洗矿和酸解工艺,结果表明:在洗矿工艺中,控制液固体积质量比为6 mL/g和洗矿时间为20~30 min,氯离子的脱除率达到92.17%;在酸解工艺中,控制硝酸用量为理论用量的90%、液固质量比为5、反应温度为60℃和反应时间为40~60 min,硼的浸出率达到98%以上。在上述工艺条件下进行硼酸母液循环研究,结果显示,随着循环次数的增加,虽然母液中的硝酸钙和硝酸钠不断积累,其质量浓度不断增加,但硼酸的质量浓度保持稳定。合适的循环次数有利于硼的回收和母液中硝酸盐浓度的提高,使母液可以用于生产硝酸钠和碳酸钙等附加值高的副产品。
钠硼解石;硝酸;硼酸;洗矿
硼酸是一种基础硼化学品,用途十分广泛。硼酸主要应用在陶瓷和搪瓷、无碱玻璃纤维、高硼硅玻璃、冶金、核能等工业中[1-2]。此外,硼酸还可以作为其他硼化物的原料,如碳化硼、氮化硼、硼酸锌、硼酸钙、硼砂、硼酸酯等,这些硼的衍生物广泛应用于磨料、高温陶瓷、润滑油、阻燃剂、高能燃料、高分子复合工程材料、医药、航空航天等领域[3-4]。
目前,国内外主要以天然的硼矿资源(如硬硼钙石、钠硼解石、硼镁石)为原料,采用不同的无机酸(如盐酸、磷酸、硫酸、硝酸)来生产硼酸[5]。其生产方法可简单概括为“一步法”和“两步法”,一步法就是利用硫酸分解高品位的硼矿来生产硼酸;两步法则是以硼矿生产的硼砂为原料与硫酸或硝酸进行复分解反应制备硼酸,但是这种工艺生产成本较高,不是生产硼酸的主要方法[6-7]。
中国主要是以高品位的纤维硼镁石矿为原料,采用硫酸分解一步法工艺生产硼酸。但是近年来,由于中国纤维硼镁石矿资源接近枯竭,高品位硼镁矿十分稀缺,造成一步法硼酸的产量逐年减少,进口硼酸逐渐占据了主导地位[8]。因此,中国开始从南美和土耳其进口高品位硼矿来生产硼酸。但是,如果采用硫酸来酸解硼矿,其副产品芒硝的附加值不高,导致硼酸的生产成本增加。基于上述因素,实验研究了以玻利维亚钠硼解石矿为原料,采用硝酸酸解硼矿制备硼酸的新工艺。
1 实验部分
1.1 实验原料、试剂及仪器
原料:钠硼解石矿,来自玻利维亚。
试剂:65%~68%(质量分数)硝酸、盐酸、氢氧化钠、甘露醇、乙二胺四乙酸二钠,以上试剂均为分析纯。
仪器:DF-101S型集热式恒温加热磁力搅拌器、SHZ-D(III)型循环水式真空泵、AL204型电子天平、DHG9076A型电热恒温鼓风干燥烘箱、DWS-51型钠离子浓度计、JSM6360-LV型扫描电子显微镜、D/MAX-2400型X射线衍射仪等。
1.2 实验原理及方法
玻利维亚钠硼解石原矿属于高原盐湖型矿物,含有部分氯离子。首先需要对原矿进行擦洗,脱除矿物中的氯离子,以免氯离子随酸解液进入系统腐蚀设备同时加大硼酸分离难度。水洗后获得的钠硼解石精矿采用质量分数为65%~68%的硝酸分解,反应式如下:

反应后的液-固体系,经过滤分离出矿渣,矿渣经热水洗涤后排除,剩下的酸解液用于硼酸的结晶。由上式反应式可知,硝酸分解钠硼解石的主要产物为H3BO3、Ca(NO3)2和 NaNO3,因此,硝酸分解钠硼解石的酸解液是一个H3BO3-Ca(NO3)2-NaNO3-H2O四元盐水体系,硼酸分离过程实际上是一个四元盐水体系的相平衡问题。由于钠和钙的硝酸盐溶解度大,而硼酸的溶解度小,硼酸可在低温下从酸解液中分离出来,但是该体系比较复杂,需要控制体系温度,使硼酸结晶析出[9]。分离硼酸后的母液返回配料参与酸解反应,用于循环回收硼,同时可增加母液中硝酸钙和硝酸钠的浓度,以便于硝酸盐的蒸发回收。
1.3 分析方法
采用甘露醇-碱滴定法测定硼的质量分数(以B2O3表示);采用EDTA络合滴定法测定钙镁的质量分数(以CaO和MgO表示);采用硝酸银沉淀滴定法测定氯离子的质量分数(以Cl-表示);采用pNa电极法测定钠的质量分数(以Na2O表示)[10]。
2 结果与讨论
2.1 钠硼解石原矿的组成及物相分析
实验所用的玻利维亚钠硼解石矿属于高原盐湖型矿物,其中含有少量的杂质。对钠硼解石原矿进行X射线衍射分析,结果见图1。从图1可知,钠硼解石原矿中主要包括3种物相:钠硼解石、氯化钠和透钙磷石。为了确定钠硼解石原矿的组成,对其进行了化学分析,结果见表1。由表1可知,钠硼解石原矿中B2O3质量分数达到33.19%,Cl-质量分数在5%以上。
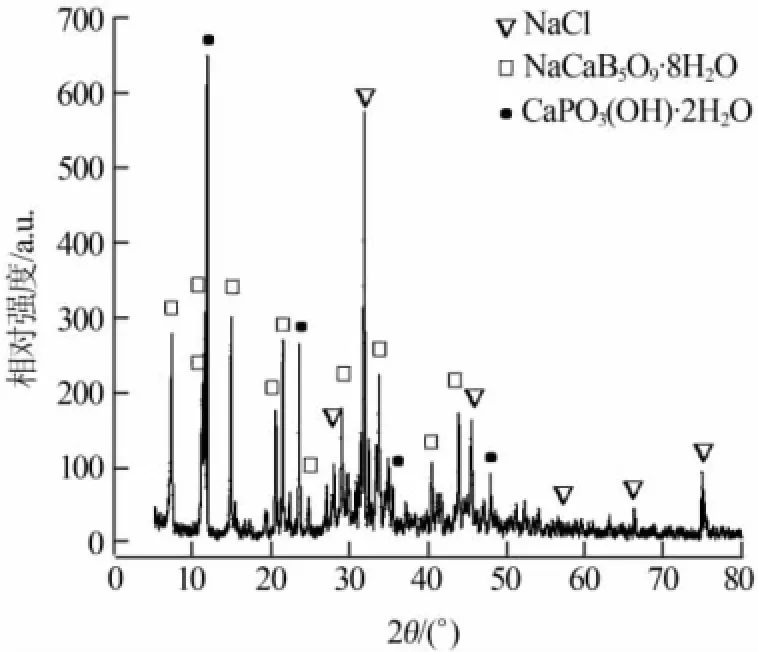
图1 钠硼解石原矿X射线粉末衍射谱图
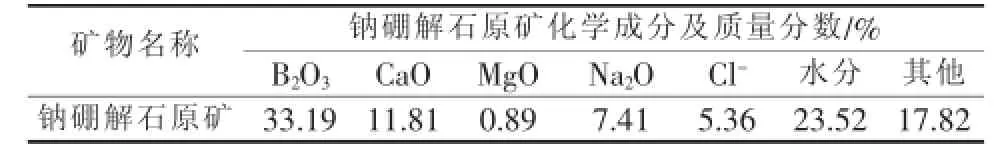
表1 钠硼解石原矿主要化学组成
2.2 洗矿工艺
由表1可知,钠硼解石原矿中含有较高含量的氯离子,若直接用硝酸酸解,氯离子会进入酸解液中,在酸性条件下不仅对设备有严重的腐蚀作用,还会与酸解液中其他游离的阳离子组合成盐类,增加多元盐水体系的复杂性,导致后续硼酸结晶分离的条件更难控制,并且随着硼酸母液循环的进行,氯离子不断积累,积累的氯离子会影响硼酸的纯度。因此,在酸解钠硼解石原矿之前,必须通过水洗脱除大部分的氯离子,获得钠硼解石精矿。
实验考察了液固体积质量比(mL/g)对脱氯效果的影响。取25 g钠硼解石原矿,加入不同体积的去离子水,在室温搅拌洗矿1 h,脱氯结果如图2所示。从图2可知,随着液固体积质量比的增加,氯离子的脱除率和B2O3的损失率都在增加。当液固体积质量比小于6 mL/g时,随着液固体积质量比的增加脱氯效果增加明显,之后继续增加液固体积质量比氯的脱除率增加很缓慢;而B2O3的损失率随着液固体积质量比的增加几乎呈线性增长。所以合适的液固体积质量比为6 mL/g。
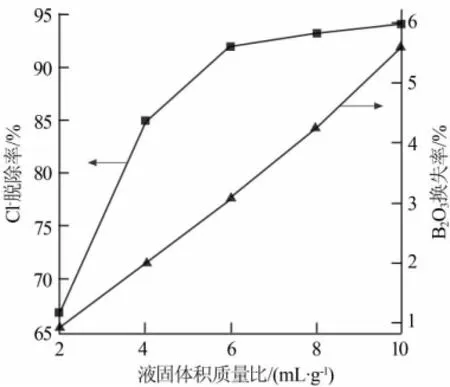
图2 液固体积质量比对脱氯效果的影响
固定液固体积质量比为6 mL/g,在室温下搅拌,考察洗矿时间对脱氯效果的影响,结果如图3所示。由图3可以看出,当洗矿时间大于30 min时,氯离子的脱除率和B2O3的损失率只有微弱的增加,变化不大,即使洗矿时间为10 min时,氯离子的脱除率也已经达到90.44%。这主要是因为大部分的氯离子都以NaCl的形式存在于钠硼解石原矿中,NaCl极易溶于水,因此在很短的时间内就可脱除。所以最佳的洗矿时间为20~30 min。
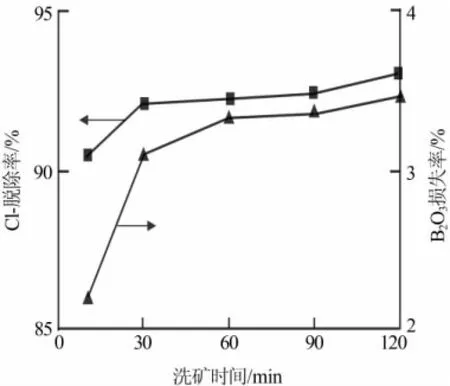
图3 洗矿时间对脱氯效果的影响
在以上工艺条件下洗矿,氯离子的脱除率达到92.17%。对洗矿并烘干后的钠硼解石精矿进行XRD分析和化学成分分析得出:钠硼解石精矿XRD谱图中没有出现NaCl衍射峰,说明洗矿过程中洗掉了大部分氯离子;钠硼解石精矿中Na2O和CaO的质量分数分别为 5.61%和 13.51%,B2O3质量分数为39.93%,氯离子质量分数为0.56%。
2.3 酸解工艺
对钠硼解石精矿采用硝酸酸解。实验研究了HNO3用量对钠硼解石酸解反应的影响,以B2O3的浸出率表示,结果见图4,并对滤渣做XRD分析,结果见图5。

图4 硝酸用量对钠硼解石分解率的影响

图5 不同硝酸用量获得滤渣XRD谱图
从图4可知,当硝酸用量为理论用量的0.6~0.9时,随着硝酸用量的增加B2O3浸出率一直在增加,之后继续增加HNO3的用量,B2O3的浸出率增加不明显。从图5a和图5c可知,当硝酸用量为理论用量的0.6时,滤渣为未反应完全的钠硼解石;当硝酸用量为理论用量的1.1时,滤渣主要为析出的H3BO3。综上所述,硝酸用量小于理论用量的0.9倍时,硝酸的用量不够;当硝酸用量大于理论用量的0.9倍时,虽然B2O3浸出率略有增加,但是过滤留在滤渣里的H3BO3增加,需要用水洗涤滤渣回收这一部分H3BO3,增加了工艺成本。因此,从生产效益考虑,硝酸的最佳用量应该为理论用量的0.9。从图5b可知,硝酸用量为理论用量的0.9时,滤渣中只剩下透钙磷石[CaPO3(OH)·2H2O]和夹带的很少量的H3BO3。
实验研究了液固质量比对分解反应的影响。不同的液固质量比影响B2O3的浸出率和H3BO3的结晶率,实验结果如图6所示。由图6可以看出,B2O3的浸出率随着液固质量比的增大而增大,但H3BO3的结晶率却随着液固质量比的增大先增大后减小。当液固质量比超过5时,B2O3的浸出率几乎没有太大的变化,而H3BO3的结晶率却呈线性下降。综合考虑,液固质量比控制在5较为适宜。

图6 液固质量比对分解反应的影响
温度的变化同样影响钠硼解石的分解。实验研究了温度对分解反应的影响,结果表明:当温度为50~60℃时,随着温度的升高,B2O3浸出率一直在增加,其值为92.68%~98.26%;温度为70~80℃时,随着温度的升高,B2O3浸出率反而减小,其值为88.10%~79.62%。对其滤渣进行XRD分析,结果如图7所示。由图7可以看出,50℃时酸解滤渣的主要成分是未分解完全的钠硼解石;70℃时酸解滤渣的主要成分为戈硼钙石(CaO·3B2O3·5H2O),即钠硼解石在分解过程中生成了一种新的含硼化合物,并随滤渣的过滤被排出,所以B2O3的浸出率减小。而当温度为60℃时,B2O3的浸出率达到98.26%。综上所述,60℃为合适的分解温度。

图7 不同温度分解钠硼解石获得滤渣XRD谱图
时间对酸解反应也有一定的影响。实验结果显示,随着时间的延长,B2O3的浸出率先增大后减小。根据滤渣的XRD谱图可知,时间太短,钠硼解石没有完全分解;时间太长,如同温度对分解反应的影响一样,钠硼解石在分解过程中生成了戈硼钙石,使得B2O3浸出率减小。因此,实验确定了40~60 min为合适的反应时间。
在以上最佳工艺条件下进行酸解,B2O3浸出率达到98.44%。
2.4 结晶方式对硼酸形貌及粒度的影响
影响硼酸结晶形状及粒度的因素很多,降温速度对硼酸晶体的大小影响很大[11-12]。实验研究了不同的冷却方式对晶体形貌和粒度大小的影响,结果如图8所示。从图8可以发现,快速冷却得到的晶体相互重叠或聚集成团,呈细小的薄片状;自然冷却得到的晶体比较分散,呈现大的块状或鳞片状。研究表明,冷却速度过快,硼酸晶体析出也快,晶粒很细,容易聚集成团,晶体形状多为薄片状;降温速度慢,有利于晶体的持续生长,容易得到大块状的晶体。

图8 不同结晶方式所得硼酸SEM照片
搅拌也会影响硼酸晶体的形貌和大小。有搅拌和无搅拌条件所得硼酸晶体SEM照片见图9。从图9可以看出,有搅拌条件下得到的硼酸晶体颗粒比较小,呈块状和粉末状;无搅拌条件得到的硼酸晶体颗粒比较大,除了少量的呈颗粒状或块状外,还有一部分呈柱状。因为在搅拌条件下,可使溶液的过饱和度快速消失,产生大量晶核,因此得到的是小颗粒粉末状或块状的晶体;而静置的溶液,溶液过饱和度消失较慢,产生的晶核较少,易得到的是较大的块状或柱状晶体。

图9 有无搅拌条件所得硼酸晶体SEM照片
2.5 母液循环实验研究
根据确定的最佳工艺条件,进行母液循环实验,结果见表2。从表2可以看出,随着循环次数的增加,虽然母液中Ca(NO3)2和NaNO3不断积累,其质量浓度也在不断增加,但是H3BO3的质量浓度没有太大的变化,稳定在50 g/L左右,所以返回的硼酸在每次循环中都被结晶析出。因此,合适的循环次数,有利于硼酸的回收,最终循环后的母液还可以用于生产轻质碳酸钙和硝酸钠等副产品。
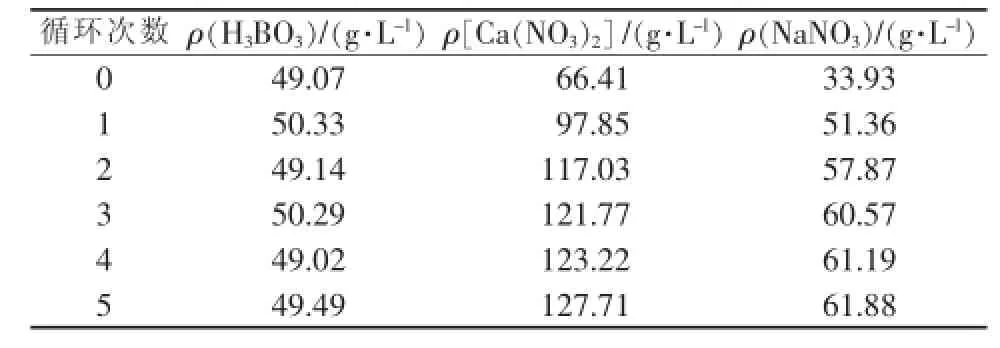
表2 母液循环实验结果
3 结论
1)玻利维亚钠硼解石原矿中含有氯离子,在酸解之前必须先进行原矿擦洗,适宜的洗矿工艺条件:液固体积质量比为6 mL/g,洗矿时间20~30 min。此条件下氯离子脱除率达到92.17%,获得的钠硼解石精矿中B2O3质量分数从33.19%增加到39.93%,氯离子质量分数从5.36%减少到0.56%。
2)采用硝酸对钠硼解石精矿进行酸解,酸解反应的最佳工艺条件:HNO3用量为理论用量的0.9,液固质量比为5,反应温度为60℃,反应时间为40~ 60 min。在此条件下,B2O3的浸出率达到98.44%。
3)对硼酸过滤后的母液进行循环,每次循环后的母液中Ca(NO3)2和NaNO3不断积累,质量浓度不断增加,但是H3BO3的质量浓度维持在50 g/L左右,所以适当的循环次数有利于硼的回收,循环后的母液可以用于生产轻质碳酸钙和硝酸钠等附加值高的副产品。
[1] Ciftci H.Modelling and kinetic analysis of boric acid extraction from ulexite in citric acid solutions[J].Can.Metall.Q.,2012,51(1):1-10.
[2] 刘然,薛向欣,姜涛,等.硼及其硼化合物的应用现状与研究进展[J].材料导报,2006,20(6):1-4.
[3] 张亨.硼酸生产研究进展[J].宁波化工,2012(3):19-26.
[4] Nizamettin Demirkiran.Dissolution kinetics of ulexite in ammonium nitrate solutions[J].Hydrometallurgy,2009,95(3):198-202.
[5] Kuskay B,Bulutcu A N.Design parameters of boric acid production process from colemanite ore in the presence of propionic acid[J]. Chem.Eng.Process.,2011,50(4):377-383.
[6] 孙新华,孙天纬,卓健,等.西藏硼镁矿制取硼酸联产碳酸镁工艺研究[J].无机盐工业,2011,43(11):46-48.
[7] 于长水,宋海燕,安峰.硼酸制备工艺综述[J].化工科技市场,2009,32(6):17-18.
[8] 展红全,江向平,罗志云,等.浸萃联合法制取硼酸新工艺[J].陶瓷学报,2012,33(1):6-10.
[9] 史建斌,别慧玲.采用钠硼解石生产硼酸的工艺研究[J].无机盐工业,2005,37(9):38-39.
[10] 王斐斐.硬硼钙石和钠硼解石矿酸解制硼酸的工艺研究[D].大连:大连理工大学,2012.
[11] 宫殿亭,李凤华,樊占国,等.高纯硼酸制备过程中的结晶动力学[J].过程工程学报,2008,8(6):1158-1162.
[12] 赵龙涛,李入林,张海明.影响硼酸结晶形状的因素[J].海湖盐与化工,2003,32(5):15-17.
联系方式:jczhong@dlut.edu.cn
Study on preparation of boric acid by leaching ulexite with nitric acid
Zhu Jun,Zhong Jianchu,Wang Hongzhi
(School of Chemical Engineering,Dalian University of Technology,Dalian 116024,China)
Ulexite,a sodium-calcium borate hydrate(Na2O·2CaO·5B2O3·16H2O)from Bolivia,was used as raw material in the preparation of boric acid with nitric acid.With washing ulexite and leaching ulexite concentrate,the Cl-removal and B2O3extraction processes of ulexite were investigated,respectively.Results indicated that in the washing process of ulexite,Clremoval rate reached up to 92.17%with liquid volume to solid mass ratio of 6 mol/L and washing time of 20~30 min,and under the conditions of nitric acid consumption being 90%of theoretical addition,liquid-to-solid mass ratio of 5∶1,reaction temperature of 60℃,and reaction time of 40~60 min,the B2O3extraction rate of ulexite concentrate could achieve more than 98%in the decomposition process.Mother liquor was obtained by boric acid filtration,with the recycle of mother liquor continued,both calcium nitrate and sodium nitrate in mother liquor were accumulated,but boric acid concentration was generally remained a fixed value,thus the proper cycles were dedicated to boric acid recovery and increasing concentrations of nitrate in mother liquor.The Ca,Na-containing nitrate solution after recycle could be used to produce calcium carbonate or sodium nitrate as by-products.
ulexite;nitric acid;boric acid;washing
TQ128.5
A
1006-4990(2014)03-0036-05
2013-09-17
朱军(1987- ),男,硕士研究生,主要从事无机功能材料的研究开发与利用。
仲剑初

