山菊降压片中生决明子代替炒决明子有效成分变化
张 杰, 张振秋, 米宝丽, 曲 园(辽宁中医药大学, 辽宁 大连 116600)
[饮片炮制]
山菊降压片中生决明子代替炒决明子有效成分变化
张 杰, 张振秋*, 米宝丽, 曲 园(辽宁中医药大学, 辽宁 大连 116600)
目的 用高效液相色谱法研究山菊降压片 (山楂、菊花、盐泽泻、夏枯草、小蓟、炒决明子) 中生决明子代替炒决明子后绿原酸、木犀草苷、橙黄决明素、黄决明素、决明素、大黄素、大黄酚、大黄素甲醚等8个成分含有量的变化。 方法 采用 Agilent ZORBAX SB-C18色谱柱 (4.6mm×250mm, 5 μm) , 体积流量 1.0mL/min, 柱温为30 ℃。流动相Ⅰ为乙腈-0.1%磷酸溶液, 梯度洗脱, 检测波长为 348 nm, 测定绿原酸、 木犀草苷的量。 流动相Ⅱ为乙腈-0.1%磷酸溶液, 梯度洗脱, 检测波长为 284 nm, 测定橙黄决明素、 黄决明素、 决明素、 大黄素、 大黄酚、 大黄素甲醚的量。结果 本方法所测定的8个成分的进样量与峰面积呈良好的线性关系,山菊降压片中生决明子代替炒决明子后, 上述 8 个成分都有不同程度的降低, 其中大黄酚、 大黄素甲醚分别降低了 2 倍、 2.8 倍。 结论 山菊降压片中使用炒决明子较为合理。
山菊降压片;决明子;生熟互换;高效液相色谱法
山菊降压片由山楂、菊花、盐泽泻、夏枯草、小蓟、炒决明子六味药组成,具有平肝潜阳的功能,用于阴虚阳亢所致的头痛眩晕、耳鸣健忘、腰膝酸软、五心烦热、心悸失眠;高血压病见上述证候者[1]。 《中国药典》 2010 年版规定本方以炒决明子中大黄酚的量为质控指标,不足以全面控制该药的内在质量[1]。 另外, 文献报道该药多为测定酸水解后大黄酚的量[2-3]。 决明子是卫生部颁 布的药食同源的药材, 《中国药典》 2010 年版规定的决明子饮片有生决明和炒决明子,具有降血压、降血脂、 保肝等药 效[1,4-12]。 绿原 酸 是 山楂、 菊 花、 夏枯草、小蓟共有的活性成分,具有明显的降压作用, 而 且 疗 效 平 稳、 无 毒、 无 副 作 用[13-14]; 木 犀草苷对高血压及心脑血管疾病的治疗均有一定的作用[15-16]; 橙 黄 决 明 素、 黄 决 明 素、 决 明 素、 大 黄素、大黄酚、大黄素甲醚是决明子降压的主要活性成分[4]。 为了更好地控制本药质量, 本研究对该药上述成分进行了测定。目前,决明子生炒品无论是单方还是在复方中都没有得到合理应用,在临床应用中存在混用的情况,缺乏明确的规范。本研究利用高效液相色谱法研究山菊降压片中生熟决明子互换后上述8个指标性成分量的变化,为决明子在复方中合理利用以及山菊降压片的质控提供参考依据。
1 仪器与试药
1.1 仪器 Agilent-1100 型高效液相色谱仪, 配置四元梯度泵、 在线脱气机、 VWD检测器; sartorius CP225D十万分之一电子天平 ( 德国), AR2140 OHAVSAdventure分析天平。
1.2 试 剂 与 药 品 绿 原 酸 (a,批 号 110752-200212)、 木犀草苷 (b, 批号 11720-201106)、 大黄素 (f, 批 号 110757-200206)、 大 黄 酚 (g, 批 号110796-201017)、 大 黄 素 甲 醚 (h,批 号 110758-201013) 均购买于中国食品药品检定研究院, 供含量测定用。 橙黄决明素 (c, 批号 20120514)、 黄决明素 (d, 批 号 20120419) 和 决 明 素 (e, 批 号20120419) 均购于上海永恒生物科技有限公司,纯度均大于98%。 本研究所用的决明子产地为河北保定,由辽宁中医药大学李峰教授鉴定为豆科植物决明 Cassia obtusifolia L.或小决明 Cassia tora L.的干燥成熟种子。山菊降压片 (炒决明子)、 新山菊降压片 (生决明子) 和炒决明子均为本室依法[1]自制得到 (生、 炒决明子为同一来源)。 乙腈为 HPLC级(OCEANPAK ALEXATIVE CHEMICAL), 甲醇为 色谱纯 (西陇化工股份有限公司), 磷酸为分析纯,水为娃哈哈纯净水。
2 方法与结果
2.1 对照品溶液的制备 精密称取绿原酸、 木犀草苷、橙黄决明素、黄决明素、决明素、大黄素、大黄酚、大黄素甲醚适量,分别加甲醇制成绿原酸为 153.2 μg/mL、 木犀草苷为 140.4 μg/mL、 橙黄决 明 素 为 228.8 μg/mL、 黄 决 明 素 为 112.8 μg/mL、 决明素为 120.4 μg/mL、大黄素为 50.40 μg/m L、 大黄酚为 149.6 μg/m L、 大黄素甲醚为51.60 μg/m L的单一对照品贮备液, 备用。 精密量取绿原酸、木犀草苷、橙黄决明素、黄决明素、决明素、大黄素、大黄酚、大黄素甲醚对照品贮备液适量,用甲醇稀释,制成每 1 mL分别含绿原酸、木犀草苷为 76.60、 56.16 μg/mL的混合对照品溶液Ⅰ以及每1 mL分别含橙黄决明素、 黄决明素、决明素、 大黄素、 大黄酚、 大黄素甲醚为 6.656、14.19、 4.625、 4.766、 1.613、 10.47、 5.934 μg/mL的混合对照品溶液Ⅱ。
2.2 供试品溶液的制备 取山菊降压片的干膏,约3 g, 精密称定, 置圆底烧瓶中, 精密加入甲醇50 mL, 称定质量, 加热回流 1 h, 放至室温, 再称定质量,用甲醇补足减失的质量,摇匀,滤过,取续滤液,用微孔滤膜 (0.45 μm) 滤过, 即得。
2.3 阴性液的制备 按工艺方法制备同时缺山楂、菊花、夏枯草、小蓟的阴性样品Ⅰ和缺决明子的阴性样品Ⅱ, 按 “2.2” 项下方法操作, 分别制成阴性样品溶液Ⅰ和阴性样品溶液Ⅱ。
2.4 色谱条件
2.4.1 色谱条件Ⅰ (分析绿原酸, 木犀草苷)
Agilent ZORBAX SB-C18色谱柱 (4.6 mm×250 mm,5 μm); 流动相为乙腈 (A)-0.1% 磷酸水溶液(B), 梯度洗脱 [0 min,A-B(10 ∶90); 11 min,A-B(18 ∶82)]; 检测波长为 348 nm, 体积流量为1.0 mL/min, 柱温为 30 ℃, 进样量为20 μL。 对照品及样品色谱图见图1。
2.4.2 色谱条件Ⅱ (分析橙黄决明素, 黄决明素,决明素, 大黄素, 大黄酚, 大黄素甲醚) Agilent ZORBAX SB-C18色谱柱 (4.6 mm×250 mm, 5 μm);流动相为乙腈 (A)-0.1%磷酸水溶液 (B), 梯度洗脱 (0 min, 26%A; 17 min,42%A;32 min,53%A; 40 min, 63%A); 检测波长为 284 nm, 体积流量为 1.0 m L/min, 柱 温为 30 ℃, 进样量为20 μL。对照品与样品的色谱图见图 1。
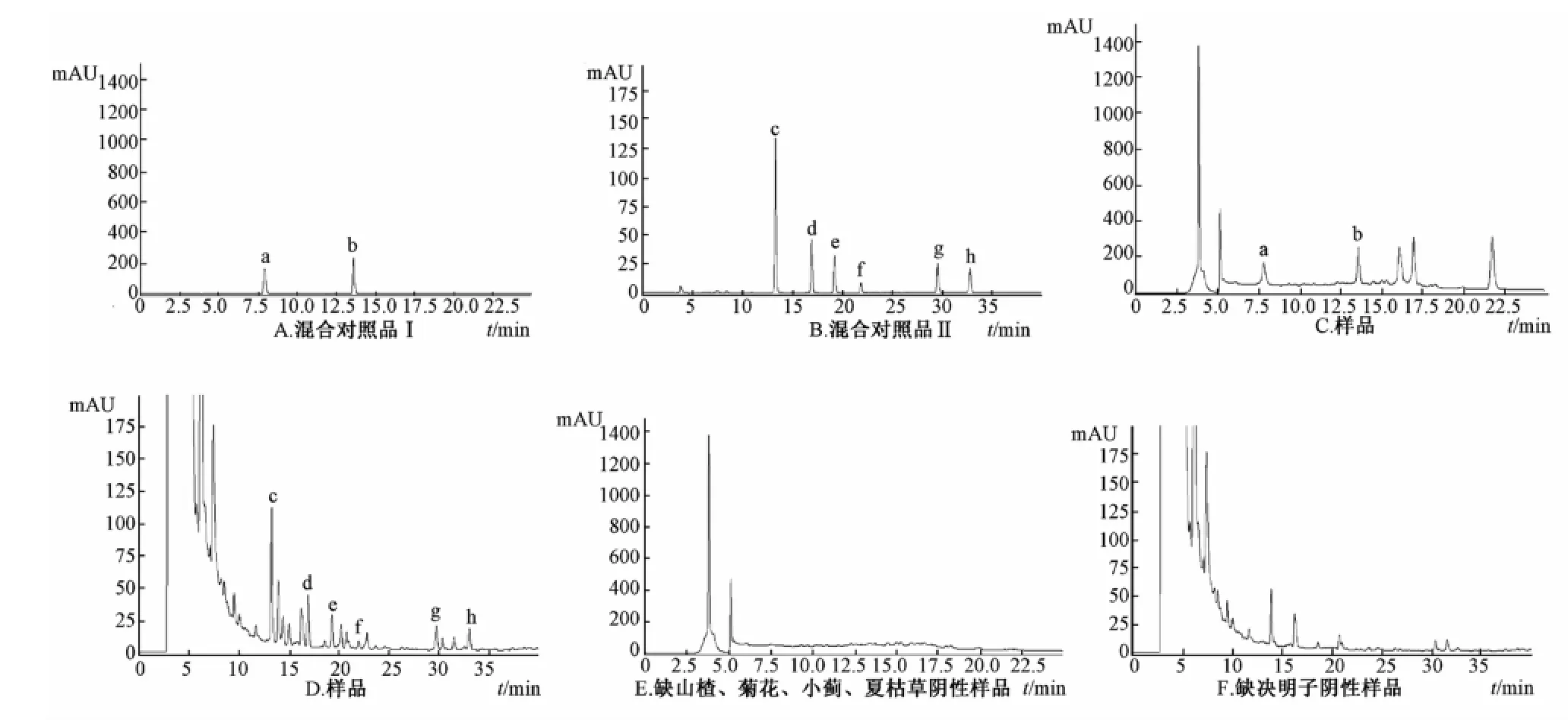
图1 混合对照品、 样品和阴性样品 HPLC色谱图Fig.1 HPLC chromatogram s of m ixed reference substances, sam p le and negative sam p le
2.5 方法学验证
2.5.1 专属性考察 精密吸取混合对照品溶液Ⅰ和Ⅱ、 供试品溶液及阴性溶液Ⅰ和Ⅱ各 20μL, 分别注入液相色谱仪,记录色谱图。由图1可见,在与对照品色谱峰相应的位置上,供试品具有相同保留时间的色谱峰,而相应的阴性液在相应保留时间处无干扰。
2.5.2 标准曲线与线性范围 精密吸取混合对照品Ⅰ和Ⅱ各 2、 5、 10、 15、 20 μL, 分别在色谱条件Ⅰ、Ⅱ依次进样,测定峰面积。以对照品进样量(μg) 为横坐标, 以峰面积为纵坐标, 绘制标准曲线,结果见表1。
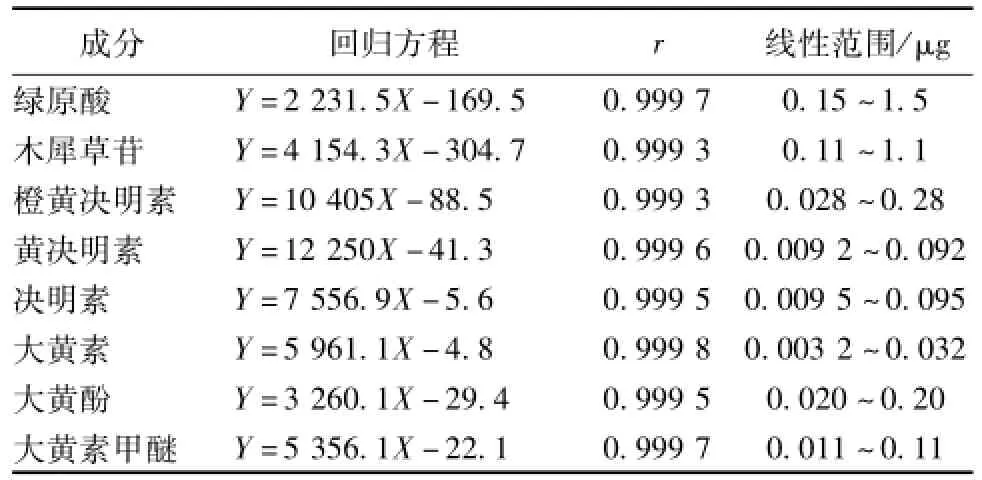
表 1 8个成分的标准曲线方程、 相关系数和线性范围Tab.1 Regression equations, correlation cofficients, and linear ranges of eight constituen ts
2.5.3 精密度试验 精密吸取山菊降压片 (批号为 20130113) 样品的供试品溶液 20 μL, 分别在色谱条件Ⅰ和Ⅱ下连续进样 6 次, 记录峰面积。 a、b、 c、 d、 e、 f、 g、 h 的 RSD(n=6) 分 别 为0.26%、 0.19%、 0.59%、 0.56%、 0.88%、0.84%、 0.83%、 0.99%, 表明仪器精密度良好。
2.5.4 稳定性试验 精密吸取山菊降压片 (批号为 20130113) 样品的供试品溶液 20 μL,室温下分别于 0、 2、 4、 6、 12、 24 h 进样测定, a、 b、 c、d、e、f、 g、h 峰 面 积的 RSD(n=6) 分 别 为0.32%、 0.31%、0.89%、 1.2%、 0.9%、 1.6%、1.1%、 1.3%, 表明供试品溶液在 24 h 内稳定性良好。
2.5.5 重复性试验 取同一山菊降压片 (批号为20130113) 的干膏粉末约 3 g, 共 6 份, 精密称定,按 “2.2” 项下方法制备供试品溶液, 分别在色谱条件Ⅰ和Ⅱ下进样20 μL, 记录峰面积, 计算各成分量及 RSD。a、b、c、d、 e、f、 g、 h 的平均含有量 (n=6) 分 别 为 0.24、 0.14、 0.030、0.010、0.010、 0.003 7、 0.025、 0.012 mg/片, RSD分别为 0.24%、 0.11%、 1.9%、 0.44%、 0.78%、1.6%、 0.31%、 1.6%。
2.5.6 加样回收率试验 取 “2.5.5” 项下已测定的山菊降压片 (批号为 20130113) 样品 6 份,每份各取约 1.5 g干膏粉末, 精密称定。 分别精密加入 a、 b、 c、 d、 e、 f、 g、 h 的对照 品 贮 备 液7.60、 4.8、 0.63、 0.45、 0.38、 0.35、 0.81、1.15 m L, 按 “2.2” 项下方法制备供试品溶液,分别在色谱条件Ⅰ和Ⅱ下进样 20 μL, 计算回收率。 结果 a、 b、 c、d、e、 f、g、 h 的平均回收率(n=6) 分 别 为 100.2%、 100.9%、 98.6%、99.8%、 101.6%、 102.4%、 99.7%、 101.1%。RSD 分 别 为 1.0%、 1.0%、 2.0%、 1.9%、1.3%、 0.9%、 1.2%、 1.8%。 见表 2。
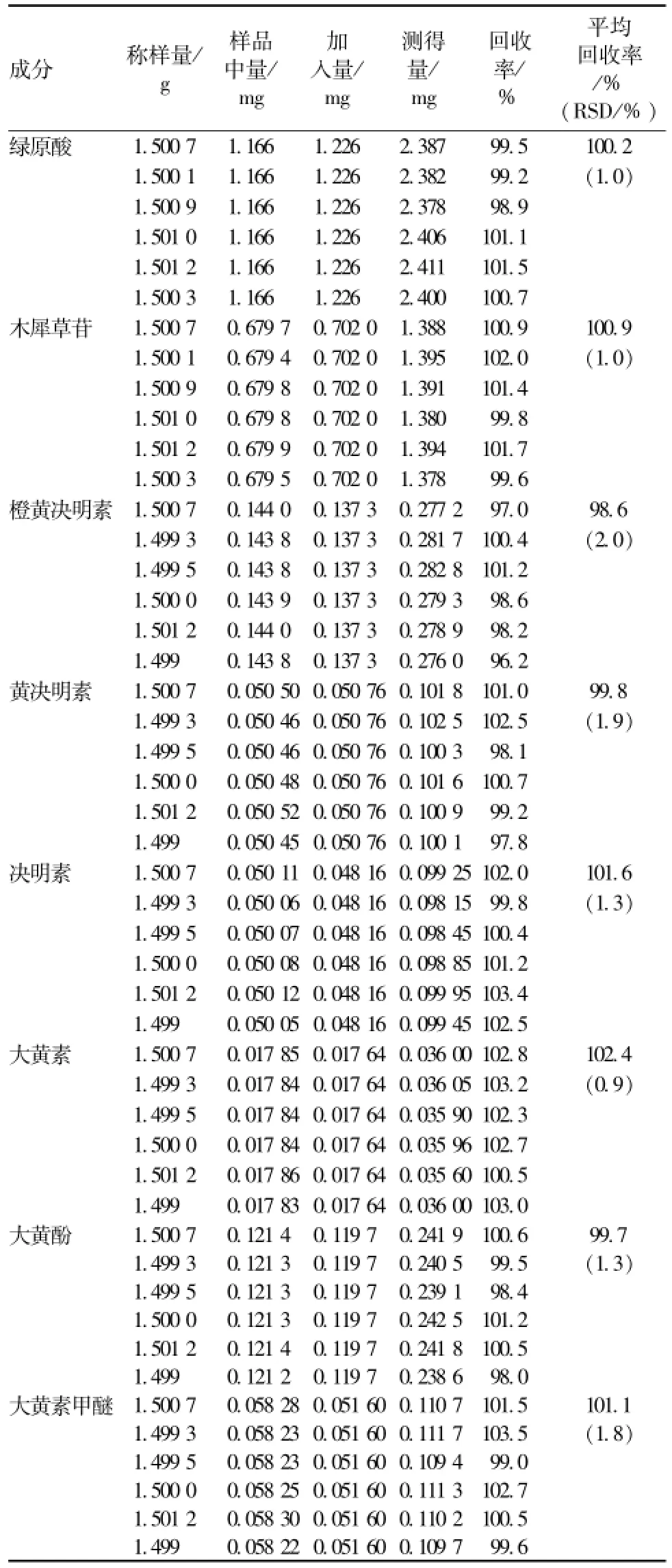
表2 8个成分回收率考察Tab.2 Results of recovery tests for eight constituents
2.5.7 样品测定 取 3 批自制山菊降压片 (批号为 20130113、 20130114、 20130115) 和新 山菊降压片 ( 批 号 为 20130124、 20130125、 20130126) (0.3 g/片) 样品溶液, 依法进样测定,计算各成分的量, 结果见表3。
3 讨论
3.1 供试品溶液处理方法的考察 曾比较了超声、回流2种提取方式及甲醇、乙醇2种提取溶剂,结果表明甲醇回流提取效率最高。比较用甲醇回流1、 2 h的提取效率, 结果发现回流 1 h已提取完全,故选用甲醇回流1 h提取。本方法采用甲醇回流直接测定样品中游离的橙黄决明素、黄决明素、决明素、大黄素、大黄酚、大黄素甲醚成分的量,较酸水解法操作简单、经济、安全。由于绿原酸易分解,实验操作中均采用避光操作。
3.2 测定方法的选择 曾摸索过同时测定绿原酸、木犀草苷、橙黄决明素、黄决明素、决明素、大黄素、大黄酚、大黄素甲醚成分的量, 由于 《中国药典》 2010 年版规定山菊降压片为水提, 供试品溶液中大极性成分比较多,而且上述8个成分极性差距比较大,所以利用多指标成分测定的方法,测定所述8种成分。
3.3 成分分析 本实验将 《中国药典》2010 年版收载的山菊降压片处方中规定的炒决明子互换成生决明子,依法自制得山菊降压片 (炒决明子) 和新山菊降压片 (决明子), 比较生炒决明子互换后,处方中绿原酸、木犀草苷、橙黄决明素、黄决明素、决明素、大黄素、大黄酚、大黄素甲醚的含有量差异,其中橙黄决明素、黄决明素、决明素、大黄素、大黄酚、大黄素甲醚为决明子中的成分,绿原酸、木犀草苷为处方中其他药中含有的主要成分。比较测定结果可看出,生炒决明子互换后,山菊降压片中橙黄决明素、黄决明素、决明素、大黄素、大黄酚、大黄素甲醚的量均比新山菊降压片中相应的成分量高,其中大黄酚、大黄素甲醚差异最明显 (山菊降压片中大黄酚、 大黄素甲醚比新山菊降压片分别高 2 倍、 2.8 倍左右), 可能是决明子经过炮制相应的苷在高温炮制时被破坏成游离形式释放出来,此结果与文献报道相符。另外山菊降压片中绿原酸、木犀草苷的量均比新山菊降压片中相应成分量高,结合中药理论知识,可能是炒决明子有助于方中其他药的有效成分溶出,起到提高药效的作用。综上所述,山菊降压片中使用炒决明子是合理的,但建议在临床上进一步研究加以确证。本实验为研究生、炒决明子在处方中的合理应用提供一定的理论依据。
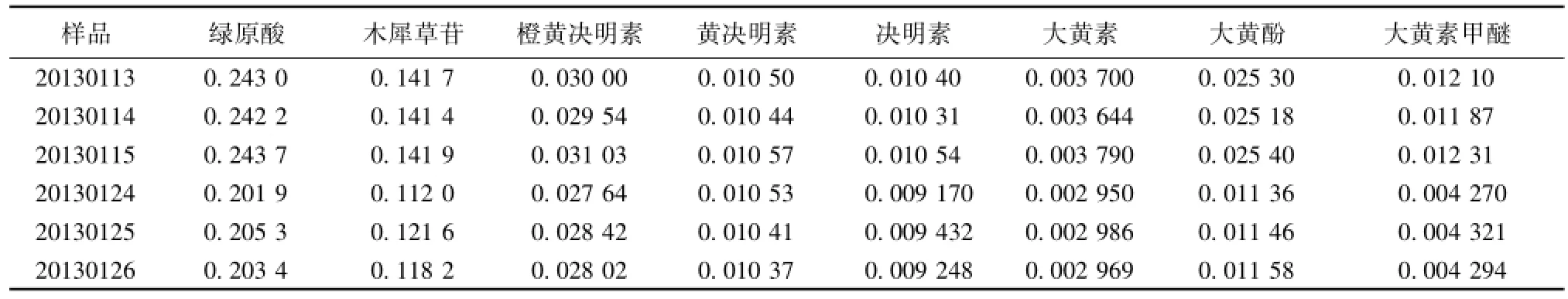
表 3 山菊降压片中 8 个成分测定结果 (mg·片-1, n=3)Tab.3 Contents of eight constituents in Shanju Jiangya Tablets( mg·片-1, n=3)
3.4 小结 本实验采用山菊降压方中山楂、 菊花、夏枯草和小蓟中含有的绿原酸、菊花中含有的木犀草苷,决明子中含有的橙黄决明素、黄决明素、决明素、大黄素、大黄酚、大黄素甲醚为指标进行测定,结果显示该法具有操作简便、测定结果准确、重复性好、特征性强的特点,能有效控制该药的质量。
[ 1 ] 国家药典委员会.中华人民共和国药典:2010 年版一部[S].北京: 中国医药科技出版社, 2010:136, 468.
[ 2 ] 张晓丽, 曹爱民, 沙 明.HPLC测定山楂降压片中大黄酚的 含 量 [ J].药 物 分 析 杂 志, 1998, 18( 增 刊 ): 180-181.
[ 3 ] 毕宏岩, 周 虹.HPLC法测定山菊降脂片中大黄酚的含量[J].辽宁中医杂志, 2006, 33(12):1626.
[4] 李续娥,郭宝江,曾 志.决明子蛋白质、低聚糖及蒽醌苷降压作用的实验研究 [J].中草药, 2003, 34(9): 842-843.
[5] 潘正军,陆 祈,潘 丽,等.决明子水提液对高血压小鼠血压血脂及肾脏结构的影响[J].中国实验方剂学杂志. 2010, 16(13):203-206.
[6] 俞发荣,连秀珍,王小琦.决明子不同部位提取物的调血脂作用[J].中国临床康复, 2006, 10(39):110-112.
[7] 何菊英,刘松青,彭永富,陈泽莲.决明子降血脂作用机制研究[J].中国药房, 2003, 14(4):202-204.
[8] 李明元,罗孟军,叶 娉,等.橙黄决明素的降血脂作用研究[J].中药药理与临床, 2008, 24(6):36-37.
[9] 林冬静,金 政.决明子提取物对急性肝损伤保护作用的实验研究[ J] .时珍国医国药, 2006, 17(2):214-215.
[10] 金香子, 金 政, 蔡英兰.决明子水提物对 D-半乳糖中毒大鼠急性肝损伤的保护作用[J].时珍国医国药, 2007,18(3):582-583.
[11] 牛艳芬, 赵 彤, 曾 涛, 等.决明子提取物对小鼠酒精性肝损伤保护作用的研究 [ J].毒理学 杂志, 2010, 24 (1):58-61.
[12] 暴 昕.中药决明子提取物对肝损伤的实验研究[J].中国民康医学, 2011, 23(4):1020.
[13] Sih C J, Ravikumar P R, Huang F C, et al.Separation and synthesis of pinoresinol diglucoside moides olive[ J] .J Am Chem Soc, 1976, 98(17):5412.
[14] 张鞍灵, 马 琼, 高锦明, 等.绿原酸及其类似物与生物活性 [ J] .中草药, 2001, 32(2):173-176.
[15] 李星霞, 郭 澄.木犀草素的药理活性研究[J].中国药房, 2007, 18(18):1421-1423.
[16] 郑虎占, 黄泽宏, 余 靖.中药现代研究与应用: 第 2 卷[M].北京: 学苑出版社, 2000.
Content changes of stir-frying Cassiae Semen rep lacement w ith raw one in Shanju Jiangya Tablets
ZHANG Jie, ZHANG Zhen-qiu*, MIBao-li, QU Yuan
(Liaoning University of Traditional Chinese Medicine, Dalian 116600, China)
AIM To study content changes of chlorogenic acid, luteoloside, aurantio-obtusin,chryso-obtusin, obtusin, emodin, physcion, and chrysophanol in Shanju Jiangya Tablets when fried Cassiae Semen was replaced by raw Cassiae Semen by HPLC.METHODS The sampleswere separated on an Agilent ZORBAX SB-C18column(4.6 mm×250 mm, 5 μm)column at a flow rate of 1.0 mL/min and the column temperature was at room temperature.Themobile phaseⅠwas acetonitrile-0.1%phosphoric acid aqueous for determination of chlorogenic acid and luteoloside with gradient elution, and detection wavelength was 348 nm.The mobile phaseⅡ was acetonitrile-0.1%phosphoric acid aqueous for determination of aurantio-obtusin, chryso-obtusin, obtusin, emodin, physcion, and chrysophanolwith gradient elution, and detection wavelength was 284 nm.RESULTS Eight determined constituents had a good linear relationship between content of each constituent and peak area.Eight constituents were degraded to some degrees when fried Cassiae Semen was replaced by raw Cassiae Semen.Chrysophanol and physcion were reduced by 2 fold, respectively.CONCLUSION Using fried Cassiae Semen in Shanju Jiangya Tablets ismore reasonable.
Shanju Jiangya Tablets; Cassiae Semen; swap for raw and processed product;HPLC
R284.1
:A
:1001-1528(2014)02-0348-05
10.3969/j.issn.1001-1528.2014.02.029
2013-04-15
国家中医药行业科研专项 (20110700703)
张 杰 (1987—) , 男, 硕士生, 研究方向: 药物分析。 E-mail:13478536926@163.com
*通信作者: 张振秋 (1964—) , 男, 教授, 博士生导师, 研究方向: 中药质量标准。 Tel:(0411)87586058, E-mail:zhangzhenqiu@ sina.com

