甘草酸与脱氧胆酸钠分子自组装胶束的形成及稳定性研究
贺俊杰, 张振海, 陈 彦*
(1.江苏省中医药研究院 国家中医药管理局中药释药系统重点研究室, 江苏 南京 210028; 2.南京中医药大学 附属中西医结合医院, 江苏 南京 210046)
甘草酸与脱氧胆酸钠分子自组装胶束的形成及稳定性研究
贺俊杰1,2, 张振海1, 陈 彦1,2*
(1.江苏省中医药研究院 国家中医药管理局中药释药系统重点研究室, 江苏 南京 210028; 2.南京中医药大学 附属中西医结合医院, 江苏 南京 210046)
目的 研究甘草酸与脱氧胆酸钠分子自组装胶束的形成及其影响因素。 方法 以粒径、 PDI和 Zeta电位为指标, 考察了甘草酸与脱氧胆酸钠分子自组装胶束形成的最佳摩尔比, 考察了不同温度、 不同 pH等条件下胶束的稳定性; 运用扫描电镜法、 差示扫描量热法等分析方法对胶束的物相进行表征, 并应用 HPLC法测定胶束溶液中甘草酸的量。 结果 当甘草酸与脱氧胆酸钠分子的摩尔比为 1 ∶2 时, 所形成的胶束的载药量质量分数为 49.30%, 平均粒径为(103.6 ±2.9) nm, PDI为 (0.059 ±0.002), Zeta电位为 - (45.5 ±0.4) mV。 该胶束在 4 ~37 ℃温度范围内及pH2.0 ~5.5 时稳定。 结论 本研究发现甘草酸与脱氧胆酸钠能够自组装形成胶束。
甘草酸;脱氧胆酸钠;胶束
甘草酸 (结构见图 1) 是甘草中重要的活性成分, 具有 抗 炎[1-2]、 抗病 毒[3]及 抗 肿 瘤[4]的 作 用。由于甘草酸相对分子质量及极性较大,脂溶性较低,导致口服生物利用度低,影响了药物疗效的发挥。胶束是表面活性剂在溶液中的浓度超过某一临界值后,其分子或离子自动缔合成胶体大小的聚集体质点微粒,文献报道胶束可以提高药物稳定性及生物利用度[5-8]。形成胶 束常用的表面活性 剂有胆酸盐、磷脂、壳聚糖等, 其中脱氧胆酸钠 (结构见图1) 是胆酸盐的一种, 本研究发现甘草酸与脱氧胆酸钠可以形成澄清透明具有淡蓝色乳光的胶束溶液,该胶束粒径小,有可能促进甘草酸在胃肠道的吸收,因此本研究筛选了甘草酸与脱氧胆酸钠形成胶束溶液的最佳摩尔比,并考察了温度、放置时间、 离心、 稀释以及 pH值对该胶束稳定性的影响。
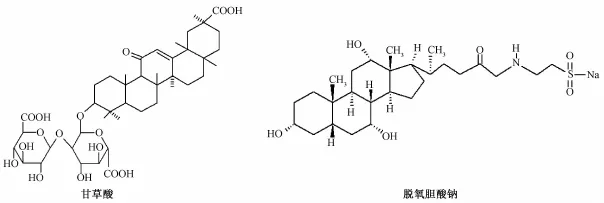
图 1 甘草酸 (相对分子质量: 822.92) 与脱氧胆酸钠 (相对分子质量: 414.55) 的化学结构Fig.1 Structure of glycyrrhizin( M r: 822.92) and sodium deoxycholate( M r: 414.55)
1 仪器和材料
Agilent1200 高效液相色谱仪 (美国 Agilent公司); Nano-ZS 型马尔文粒径测定仪 (英国马尔文公司); DSC 200 F3 Maia(德国 Netzsch 公司); Tecnai 12 型透射电子显微镜 (荷 兰艾克 赛普公 司);METLER TOLEDO分析天平、 METLER TOLEDO pH计 (瑞士梅特勒-托利多分析仪器有限公司)。
甘草酸 (纯度≥98%,南京替斯艾么中药研究所); 脱氧胆酸钠 (纯度≥99%, 上海笛柏化学品技术有限公司), 其余试剂均为色谱纯或分析纯。
2 方法和结果
2.1 甘草酸与脱氧胆酸钠自组装胶束溶液的制备
精密称取甘草酸与脱氧胆酸钠适量,分别配成等体积的水溶液,依次取甘草酸与脱氧胆酸钠水溶液各1 mL, 然后分别依次加入到烧杯里,直到两种溶液加完,在磁力搅拌器下混匀,即得胶束溶液。
2.2 甘草酸与脱氧胆酸钠摩尔组成比例筛选 精密称取甘草酸与脱氧胆酸钠适量, 加入到5 mL量瓶中,分别配成甘草酸与脱氧胆酸钠摩尔比为1 ∶5、 1 ∶4、 1 ∶3、 1 ∶2、 1 ∶1、 2 ∶1、 3 ∶1、4 ∶1、 5 ∶1 的溶液, 观察溶液的外观, 经激光散射粒度测定仪测定,结果见表1。 当二者摩尔比在1∶4 到 3 ∶1 范围时, 溶液澄清透明、 有淡蓝色乳光,已自组装成了胶束,平均粒径小,分布均匀 (见图2), 其中在甘草酸与脱氧胆酸钠摩尔比为1 ∶2时, 粒径最小,为 103.6 nm。 通过透射电镜观察胶束的外观形态为球形 (见图3)。 所以选择甘草酸与脱氧胆酸钠摩尔比1∶2为该胶束形成的最佳比例,并以此比例进行胶束稳定性实验。
2.3 胶束物相的表征
2.3.1 胶束平均粒径、 PDI及 Zeta电位的测定
取胶束适量,采用马尔文激光散射粒度测定仪,在25 ℃下测定胶束的粒径。 平均粒径为 103.6 nm,多 分 散 指 数 ( PDI) 为 0.059, Zeta电 位 为-45.5 mV。 粒径分布见图 2, 表明该胶束粒径较小,分布均匀。
表1 甘草酸与脱氧胆酸钠分子组成比例的优选 (, n=3)Tab.1 Optim ization of themolar ratio of glycyrrhizin and sodium deoxycholate(, n=3)

表1 甘草酸与脱氧胆酸钠分子组成比例的优选 (, n=3)Tab.1 Optim ization of themolar ratio of glycyrrhizin and sodium deoxycholate(, n=3)
甘草酸与脱氧胆酸钠摩尔比 平均粒径/nm PDI Zeta电位 /mV 外观1 ∶5 236.5 ±6.1 0.236 ±0.017 -(36.8 ±1.4) 不透明1 ∶4 201.5 ±2.9 0.154 ±0.006 -(37.5 ±0.5) 透明、淡蓝色乳光1 ∶3 167.4 ±7.4 0.052 ±0.003 -(39.8 ±0.5) 透明、淡蓝色乳光1 ∶2 103.6 ±2.9 0.059 ±0.002 -(45.5 ±0.4) 透明、淡蓝色乳光1 ∶1 158.5 ±6.8 0.119 ±0.007 -(40.6 ±0.5) 透明、淡蓝色乳光2 ∶1 130.5 ±4.5 0.166 ±0.004 -(39.8 ±0.6) 透明、淡蓝色乳光3 ∶1 149.5 ±3.8 0.162 ±0.004 -(32.9 ±0.4) 透明、淡蓝色乳光4 ∶1 234.2 ±6.5 0.399 ±0.011 -(26.9 ±0.2) 不透明5 ∶1 2 053.2 ±81.1 1.0 ±0 -(22.6 ±0.6) 不澄清透明

图 2 甘草酸与脱氧胆酸钠摩尔比1 ∶2 时胶束溶液的粒径分布图Fig.2 Mean droplet size ofm icelle( molar ratio of glycyrrhizin and sodium deoxycholate 1 ∶2) by intensity
2.3.2 胶束的外观形态 将载有 Formvar支持膜的铜网置于蜡板上,在膜上分别滴胶束溶液1滴,自然晾干 30 min, 再滴加 2%磷钨酸 1 滴, 自然晾干 10 min, 用滤纸吸走 多余的 液体, 置于 Tecnai 12型透射电子显微镜下观察微乳的形态,透射电镜图见图3, 表明胶束的外观圆整, 分布较均匀,胶束内部可见白色不规则形状的物质,可能是甘草酸与脱氧胆酸钠疏水基团组成的疏水核。

图 3 胶束的透射电镜图 ( ×48 000)Fig.3 M orphology of m icelle by TEM
2.3.3 差示量热扫描分析 (DSC) 测试条件为铝坩埚; 气氛为氮气; 升温速率为 10.00 ℃ /min;升温范围为 0 ~450 ℃。 分别对甘草酸原料药、 脱氧胆酸钠、甘草酸与脱氧胆酸钠的固体混合物(摩尔比1 ∶2)及胶束的冻干粉进行DSC分析, 结果见图4。

图4 甘草酸原料药 (A)、 脱氧胆酸钠 (B)、 甘草酸与脱氧胆酸钠的固体混合物 (C) 及胶束 (D) 的 DSC曲线Fig.4 DSC curves of glycyrrhizin( A) , sodium deoxycholate( B) , solid m ixture of glycyrrhizin and sodium deoxycholate( C) and m icelle( D)
DSC曲线图显示: 甘草酸原料药在 85、 201 ℃两处出现明显的吸热峰; 脱氧胆酸钠在361 ℃处出现一个明显的吸热峰;甘草酸与脱氧胆酸钠的固体混合物分别在 85、 201、 361 ℃出现明显的吸热峰,说明甘草酸和脱氧胆酸钠的晶型没有改变,二者为简单的物理混合物;胶束冻干粉中甘草酸和脱氧胆酸钠的特征峰消失, 在275 ℃处出现一个新的吸热峰,说明甘草酸可能以非晶体形式存在,提示药物与辅料结合形成了胶束。
2.4 胶束的稳定性研究
2.4.1 温度与放置时间对胶束稳定性的影响 取甘草酸胶束溶液适量3份,分别放置在4℃、室温及37 ℃条件下1 个月后,未见分层、 絮凝、 破坏现象,经马尔文粒径测定仪测定各项参数,结果见表2。 结果表明胶束溶液依然澄清透明, 有淡蓝色乳光,各项参数无明显变化,说明在考察的范围内该胶束稳定。
表2 温度对该胶束溶液稳定性的影响 (, n=3)Tab.2 Effect on stability of m icellar solution by tem perature(, n=3)

表2 温度对该胶束溶液稳定性的影响 (, n=3)Tab.2 Effect on stability of m icellar solution by tem perature(, n=3)
温度/℃ 平均粒径 /nm PDI Zeta电位/mV 外 观4有淡蓝色乳光25 103.6 ±2.9 0.059 ±0.001 -(45.7 ±0.4) 澄清透明,有淡蓝色乳光37 105.6 ±2.1 0.065 ±0.002 -(46.2 ±0.7) 澄清透明,102.4 ±2.5 0.061 ±0.002 -(46.8 ±0.6) 澄清透明,有淡蓝色乳光
2.4.2 离心与稀释对胶束溶液稳定性的影响 取1.0 mL甘草酸胶束溶液于 1.5 mL离心管中, 以11 000 r/min离心 30 min,胶束澄清透明,不分层,说明高速离心对该胶束溶液的稳定性没有明显影响。
取甘草酸胶束 1.0 mL, 将其稀释 10 倍、 100倍,经马尔文粒径测定仪测定各项参数,结果见表3。 结果表明该胶束仍然澄清透明,稀释10 倍淡蓝色乳光明显, 稀释 100 倍有微弱的淡蓝色乳光, 表明稀释对该胶束系统无明显影响。
表3 稀释对胶束稳定性的影响 (, n=3)Tab.3 Effect on stability ofm icellar solution by dilution(, n=3)

表3 稀释对胶束稳定性的影响 (, n=3)Tab.3 Effect on stability ofm icellar solution by dilution(, n=3)
稀释 倍数 平均 粒径 /nm PDI Zeta电位 /mV有淡蓝色乳光10 97.3 ±2.3 0.045 ±0.005 -(47.8 ±0.6) 澄清透明,有淡蓝色乳光100 86.9 ±3.6 0.064 ±0.008 -(48.4 ±0.9) 澄清透明,外观0 104.5 ±2.8 0.052 ±0.004 -(44.6 ±0.4) 澄清透明,有淡蓝色乳光
2.4.3 不同 pH值对胶束稳定性的影响 取甘草酸胶束溶液 10 份, 分别用 1 mol/L的盐酸溶液和氢氧化钠溶液调 pH为 2.0、 3.0、 4.0、 5.0、 5.5、6.0、 6.5、 7.0、 7.4、 8.0, 观察胶束外观状态的变化并经马尔文粒径测定仪测定,结果见表4。结果表明 pH为 2.0、 3.0、4.0、 5.0、 5.5 的胶束外观及平均粒径无明显变化, 而 pH为 6.0、 6.5、7.0、 7.4、 8.0 的胶束淡蓝色消失, 为澄清透明的溶液, 说明胶束溶液在 pH2.0 ~5.5 时较稳定。
表 4 不同 pH对胶束稳定性的影响 (, n=3)Tab.4 Effect on stability of m icellar solution by differen t pH values(, n=3)

表 4 不同 pH对胶束稳定性的影响 (, n=3)Tab.4 Effect on stability of m icellar solution by differen t pH values(, n=3)
外观2.0 110.88 ±3.23 0.106 ±0.003 -(47.58 ±0.64) 澄清透明,pH 平均粒径 /nm PDI Zeta电位/mV有淡蓝色乳光3.0 108.36 ±2.08 0.059 ±0.003 -(41.98 ±0.43) 澄清透明,有淡蓝色乳光4.0 102.55 ±2.92 0.050 ±0.004 -(47.69 ±0.52) 澄清透明,有淡蓝色乳光5.0 110.19 ±2.81 0.049 ±0.001 -(48.25 ±0.51) 澄清透明,有淡蓝色乳光5.5 103.15 ±3.28 0.049 ±0.002 -(46.25 ±0.41) 澄清透明,有淡蓝色乳光6.0 1 205.45 ±22.67 1.000 ±0.000 -(2.52 ±0.33) 澄清透明6.5 989.26 ±31.26 0.956 ±0.120 -(1.56 ±0.28) 澄清透明7.0 2 036.25 ±59.96 0.859 ±0.161 -(3.36 ±0.42) 澄清透明7.4 1 985.41 ±79.20 1.000 ±0.000 -(2.59 ±0.46) 澄清透明8.0 1 678.12 ±46.27 1.000 ±0.000 -(6.98 ±0.39) 澄清透明
2.5 胶束溶液中甘草酸含有量的考察[9-14]
2.5.1 色 谱 条 件 ZORBAX SB-C18色 谱 柱(4.6 mm×150 mm, 5 μm); 流动相为乙腈-0.5%醋酸水溶液 (36 ∶64); 柱温 30 ℃; 检测波长250 nm;体积流量 1.0 mL/min; 进样体积 20 μL。在此色谱条件下, 甘草酸的保留时间为 7.2 min。液相图谱见图5。

图5 甘草酸的 HPLC图Fig.5 HPLC chromatogram of glycyrrhizin
2.5.2 胶束样品溶液的配制 精密称取甘草酸与脱氧胆酸钠各 5 mg(摩尔比为 1 ∶2), 按 “2.1”项下方法制备成胶束溶液 10 mL。 精密量取胶束溶液 1.3 mL于 1.5 mL离心管中, 11 000 r/min 离心15 min, 取上清液 1.0 mL于 10 mL量瓶中, 加入甲醇, 并稀释到刻度, 超声 5 min, 即得胶束样品溶液。
2.5.3 线性关系的考察 精密称取甘草酸对照品2.60 mg, 置于5 mL量瓶中, 用甲醇溶解并定容至刻度, 制成质量浓度为 520 μg/mL的贮备液。 精密量取贮备液30、 60、 125、 250、 500 μL分置于 5个1 m L量瓶中, 用甲醇稀释定容至刻度, 得甘草酸标准溶液。 按 “2.4.1” 项下方法测定, 绘制标准曲线, 得回归方程为 A=8.739 2C+33.373,相关 系 数 r=0.999 9, 表 明 甘 草 酸 在 15.6 ~260 μg/mL范 围 内, 峰 面 积 A 与 质 量 浓 度 C(μg/mL) 呈良好的线性关系。
2.5.4 精密度试验 取甘草酸对照品溶液,按“2.4.1”项下方法, 日内进样 6 次, 其 RSD值为0.44%; 日间连续 6 d 进样, 其 RSD值为 0.83%,结果表明本法日间、日内精密度良好。
2.5.5 重复性试验 取同一甘草酸胶束样品 6 份,按样品溶液的处理方法进行处理,制备成待测液后, 按 “ 2.4.1 ” 项 下 方 法 测 定, 其 RSD 值 为0.29%, 结果表明本法重复性良好。
2.5.6 稳定性试验 取甘草酸胶束样品, 按样品溶液的处理方法进行处理,制备成待测液后,按“2.4.1” 项下方法, 在 0、 2、 4、 6、 8、 12 h 进样, RSD值为 0.52%, 表明甘草酸胶束在 12 h 内稳定性良好。
2.5.7 回收率试验 分别精密量取甘草酸胶束溶液适量, 甘草酸对照品适量, 置10 m L量瓶中, 加甲醇溶 解 并定容至 刻 度, 超 声 10 min, 11 000 r/min 离 心 15 min, 进 样 测 定, 计 算 回 收 率 为(99.6 ±0.47)% (n=5), 表明本法回收率较好。2.5.8 胶 束 溶 液 中 甘 草 酸 的 测 定 结 果 取“2.4.2” 项下胶束样品溶液1.0 m L, 加入到10 mL量瓶中, 用甲醇定容至刻度,然后取 1.0 mL稀释液, 加入到10mL量瓶中,用甲醇定容,即得胶束供试液, 按上述色谱条件进样 20 μL, 以标准曲线计算得质量浓度为 0.486 mg/m L, 由公式 “载药量= [甘草酸量/(甘草酸 +脱氧胆酸钠量)] × 100%” 计算, 载药量为49.30%。
3 讨论
本研究发现甘草酸与脱氧胆酸钠能够自组装形成胶束。该胶束的疏水内核可能是由甘草酸中的五元环与脱氧胆酸钠中的四元环组成,两化合物的其余亲水基团构成胶束的壳。甘草酸与脱氧胆酸钠摩尔比为1∶2时, 该胶束溶液澄清透明, 有淡蓝色乳光, 外观为球状, 平均粒径在100 nm左右, PDI为 0.059, Zeta电位为 -45.5 mV, 平均粒径较小,分布均匀,带大量的负电荷,保证了胶束的稳定性。 该胶束在4 ℃、 室温及37 ℃下稳定性较好;稀释、高速离心及长时间放置基本不影响其稳定性; 而 pH对该胶束溶液有较明显的影响, 在 pH 2.0 ~5.5 时较稳定。
本实验室前期研究发现甘草酸在大鼠胃肠道内吸收很差,有效吸收渗透系数仅为 0.1, 导致甘草酸的口服生物利用低。该胶束的形成有可能提高甘草酸的口服生物利用度,有待进一步深入研究。
[ 1 ] Arjumand W, Sultana S.Glycyrrhizic acid: A phytochemical with a protective role against cisplatin-induced genotoxicity and nephrotoxicity[ J] .Life Sci, 2011 , 89(13/14) : 422-429.
[ 2 ] Matsui S, Matsumoto H, Sonoda Y, etal.Glycyrrhizin and related compounds down-regulate production of inflammatory chemokines IL-8 and eotaxin 1 in a human lung fibroblast cell line[J] .Int Immunopharm, 2004, 4(13) : 1633-1644.
[ 3 ] Sasaki H, TakeiM, KobayashiM, et al.Effectof glycyrrhizin,an active component of licorice roots, on HIV replication in cultures of peripheral blood mononuclear cells from HIV-seropositive patients[ J] .Pathobiology, 2002-2003 , 70 ( 4 ):229-236.
[ 4 ] 段伟奇, 姬胜利.甘草酸抗病毒活性的研究进展[J].中草药, 2007, 38(4): 附 1-附 4.
[ 5 ] Talelli M, Rijcken C J, Oliveira S, etal.Nanobody-Shell functionalized thermosensitive core-crosslinked polymericmicelles for active drug targeting[ J] .J Controlled Release, 2011, 151(2): 183-192.
[ 6 ] TalelliM, Rijcken C J, Oliveira S, et al.Reprint of″ Nanobody-Shell functionalized thermosensitive core-crosslinked polymericmicelles for active drug targeting″ [ J] .JControlled Release, 2011 , 153(1) : 93-102.
[ 7 ] Sun P, Zhou D, Gan Z.Novel reduction-sensitive micelles for triggered intracellular drug release[ J].J Controlled Release,2011, 155(1): 96-103.
[ 8 ] Aliabadi H M, Elhasi S, Mahmud A, et al.Encapsulation of hydrophobic drugs in polymeric micelles through co-solvent evaporation: The effect of solvent composition onmicellar properties and drug loading[ J] .Int J Pharm, 2007, 329 ( 1/2 ):158-165.
[ 9 ] 郝明虹, 杜树山, 姚雪花, 等.HPLC测定铁笛口服液中甘草酸 的 含 量 [ J].中 国 中 药 杂 志, 2008, 30 (15 ):1917-1918.
[10] 许栋明, 程可建.RP-HPLC同时测定温胆汤中甘草苷、 柚皮苷、 橙皮苷和甘草酸[J].中国中药杂志, 2011, 36(1): 45-47.
[11] 宋九华, 王 刚, 刘素君.HPLC测定九味羌活丸中黄芩苷、 甘草酸和异甘草素含量[J].中成药, 2010, 32(11):1914-1916.
[12] 张 翔, 韩继永.HPLC法同时测定养血化瘀合剂中阿魏酸、 甘 草 苷 和 甘 草 酸 [ J].中 成 药, 2011, 33 ( 4 ):622-625.
[13] 刘 勇, 韩桂茹, 封淑华.HPLC法同时测定归脾丸中甘草酸与藁本内酯[J].中成药, 2011, 33(4): 667-669.
[14] 包小红, 周 娟, 伍丕娥.HPLC法测定玄麦甘桔颗粒中甘草酸和哈巴俄苷[J].中成药, 2011, 33(4): 625-628.
Preparation and stability of self-assem blingm icelle based on glycyrrhizin and sodium deoxycholate
HE Jun-jie1,2, ZHANG Zhen-hai2, CHEN Yan1,2*
(1.Key Laboratory of New Drug Delivery System of ChineseMeteria Medica, Jiangsu Provincial Academy of ChineseMedicine, Nanjing 210028, China; 2. Hospital of Integration of Chinese and Western Medicine Affiliated to Nanjing University of TCM, Nangjing 210046, China)
glycyrrhizin; sodium deoxycholate; micelle
R944
: A
: 1001-1528(2014)05-0941-06
10.3969/j.issn.1001-1528.2014.05.013
2013-06-11
江苏省中医药领军人才项目 (LJ200913)
贺俊杰 (1986—) , 男, 硕士生。 Tel:(025)85608672, E-mail: a518518100@126.com
*通信作者: 陈 彦, 博士, 研究员, 研究方向: 中药新剂型新技术。 Tel:(025)85608672, E-mail: ychen202@hotmail.com

