安素治疗胃肠道恶性肿瘤相关营养不良患者50例临床观察
陈奕贵* 蔡雄超 林景辉 邹思平 余家密
(福建医科大学教学医院福建省肿瘤医院消化内科,福建 福州 350014)
安素治疗胃肠道恶性肿瘤相关营养不良患者50例临床观察
陈奕贵* 蔡雄超 林景辉 邹思平 余家密
(福建医科大学教学医院福建省肿瘤医院消化内科,福建 福州 350014)
目的 观察胃肠道恶性肿瘤相关营养不良患者口服安素肠内营养支持治疗后对营养相关生化指标影响,探讨口服安素肠内营养治疗对改善胃肠道恶性肿瘤患者的营养状况的疗效。方法 通过监测胃肠道恶性肿瘤患者肝、肾功能、血清白蛋白、前白蛋白、血红蛋白、体质量及体力状态等的变化,观察口服安素肠内营养治疗疗效及不良反应。结果 通过口服安素肠内营养治疗,提高了患者血中前白蛋白、白蛋白、CRE水平,对维持血中血红蛋白的水平、稳定患者的体质指数、提高患者的体力状态具有一定的作用,未发现明显不良反应。结论 口服安素能改善患者营养指标、减轻营养不良程度,提高体力状态评分、稳定体质指数,未见明显不良反应,为患者的进一步治疗,特别是化疗创造了更好的条件。
胃肠道肿瘤;肠内营养治疗;安素
肿瘤患者由于各种原因常常导致营养不良,临床上有40 %~80 %的癌症患者伴有不同程度的营养不良[1],特别是消化系统肿瘤患者营养不良的发生率更是高达85 %以上[2]。营养不良是肿瘤患者病情加重和死亡的重要原因[3]。由于医师观念或患者经济的原因,我国临床肿瘤医师对营养支持治疗的重要性还未得到足够的重视,对肿瘤患者进行营养评估,并对其提供专业的健康教育和营养咨询、营养治疗经常不到位,大多数肿瘤患者的营养状况堪忧。
胃肠道恶性肿瘤患者是营养不良的高发人群,营养不良可增加肿瘤治疗后并发症发生率,延长住院时间,增加病死率,因此对胃肠道恶性肿瘤患者进行营养支持尤为重要。肠内营养符合生理,营养全面,有助于保护胃肠道屏障功能及免疫功能,价廉且使用方便。因此,对于有胃肠道功能的患者,首选肠内营养。
肠内营养治疗是肿瘤综合治疗中不可缺少的一部分,发挥肠内营养治疗在肿瘤综合治疗中的作用,有助于肿瘤综合治疗疗效提高,改善患者生存质量。
本文对50例胃肠道腺癌患者实施安素口服肠内营养治疗,现将临床观察报道如下。
1 资料与方法
1.1 一般资料
于2012年1月至10月收治的晚期胃肠道腺癌50例,其中胃癌27例,肠癌23例,年龄25~68岁(中位年龄56岁)。经NRS 2002评估存在营养不良风险或已经存在营养不良,且均有一定的胃肠道功能,给予安素口服肠内营养支持治疗。
1.2 方法
1.2.1 营养评估
按NRS(Nutritional Risk Screening) 2002版评估营养不良风险。在患者入院第2天早晨完成NRS 2002评估,具体方法参考文献[4]。NRS≥3分时判断为有营养风险,给予口服安素营养支持治疗。口服安素1个月后再进行NRS评估及生化指标复查、体质指数测定、体力状态评分,观察营养状态变化。
1.2.2 安素口服用量
以患者自主经口服用为主,如果无法达到必须热卡,配合少量肠外营养支持来达到热量和氮的平衡。制备250 mL安素液:在杯中加入200 mL凉水,缓慢地搅拌下加入安素(ENSURE)粉剂6匙(55.8 g),搅拌直到溶解。400 g的安素(ENSURE)粉剂可制备7份250 mL的服用量。根据进食量,适当增减安素服用量,建议每次50~250 mL,每日2~7次。
1.2.3 生化指标及血常规检测
1.2.3.1 测量入院时及1个月后谷丙转氨酶(ALT)、谷草转氨酶(AST)、尿素(BUN)、肌酐(CRE)等肝、肾功能指标,并根据患者肝、肾功能的情况调整营养素的供给量。
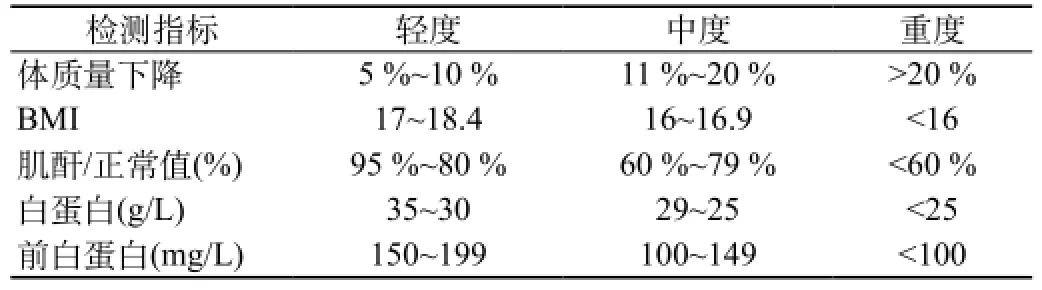
表1 营养不良分三度

表2 营养支持治疗前后50例患者观察指标变化

表3 营养支持治疗前后50例患者观察指标变化
1.2.3.2 测定住院时及1个月后血清白蛋白(ALB)、血清前白蛋白(PA)、血红蛋白(HGB)等各项数据,结合其他数据对患者进行营养评估,制定出能量、蛋白质的供给量,达到改善机体的营养状况、提高免疫力的目的。
1.2.3.3 测定住院时及1个月后的体质量变化,计算体质指数的变化。体质指数(Body Mass Index,简称BMI)=体质量(kg)/身高的平方(m2),是反映营养状况的基本数据,WHO建议体质指数正常值为18.5~25。
根据入院后NRS评估结合生化等检测结果,将营养不良分为三度,见表1。
1.2.3.4 体力状态评分:按照Karnofsky(卡氏评分,KPS)标准评定,分为0~100分。
1.3 统计学方法
采用SPSS11.0统计分析软件,应用配对t检验方法,以P<0.05为差异有统计学意义。
2 结 果
2.1 NRS营养不良风险评估及营养支持治疗情况
65例患者入院时进行NRS2002评估,有50例患者存在营养不良风险,发生率为76.9 %,其中胃癌为77.1 %(27/35),肠癌为76.7 %(23/30),差异无显著性。入院后有营养不良风险的50例患者进行了安素口服营养支持治疗,服用安素量为2~6杯/天,其中有1例患者觉得口感不好,需要肠外营养补充进食不足,6例患者食欲不好时加用少量肠外营养支持。安素营养治疗前后NRS评估数据见表2,营养不良程度变化见表4。

表4 营养支持治疗前后50例患者营养营养不良程度变化
2.2 生化检测结果
2.2.1 肝、肾功能指标
我院丙氨酸转氨酶、天冬氨酸转氨酶、尿素氮、肌肝正常值分别为5~40 IU/L、5~40 IU/L、3.10~7.40 µmol/L、60~130 µmol/L。安素营养治疗前后谷丙转氨酶、谷草转氨酶、尿素氮、肌酐检测数据见表2。
2.2.2 临床营养指标
我院白蛋白、前白蛋白、血红蛋白正常值分别为35.0~54.0 g/L、 200~400 mg/L、100~150 g/L。安素营养治疗前后白蛋白、前白蛋白、血红蛋白检测数据见表3。
2.2.3 营养支持治疗前后50例患者营养营养不良程度的变化
见表4。
3 讨 论
晚期消化道肿瘤患者大多有营养不良。本研究中患者通过NRS评估,营养不良风险发生率高达76.9 %。营养不良的患者易发生胃肠道排空延缓,对化、放疗不耐受,恢复缓慢等状况,严重的还会导致患者因机体的身体素质下降无法接受抗肿瘤治疗,使病情进一步恶化,导致肿瘤患者因营养不良而死亡。体质量下降超过10 %的患者肿瘤发病率和病死率升高,20 %~50 %的肿瘤患者死于营养不良或恶液质,而非肿瘤本身[5]。研究显示,营养不良的肿瘤患者住院时间延长[6],短期内再入院率升高[7],住院费用增加,并发症发生率和病死率均较高[8]。
目前尚无循证医学证据支持营养支持治疗能降低晚期消化道肿瘤患者的病死率,但许多资料显示可以改善患者的营养状况,提高患者的生活质量,为肿瘤的综合治疗创造条件,间接地改善患者的生存。晚期消化道肿瘤患者营养支持的适应证包括:因肿瘤本身或肿瘤治疗,如化、放疗而导致恶心、呕吐、纳差,不能摄取足够的营养;发生肠瘘、严重感染、胃肠功能障碍等并发症;需施行姑息性手术或侵入性治疗的围手术期;患者或其家属意愿。
所有消化道肿瘤患者在入院时应接受营养筛选,如果患者具有营养风险,应制定出营养支持计划。营养风险(nutritional risk,NR)是指营养因素导致临床结局(outcome)受影响的风险。目前有多个筛选工具,如主观全面评估(SGA)、营养风险筛选(NRS 2002)、简易营养评估(MNA)。所有筛选工具都具有优缺点。NRS 2002易于使用,包括有关营养状况受损的3个项目和有关疾病严重度的3个项目,如果总分≥3分,具备营养支持的指征。NRS 2002经过ESPEN共识的修定,是一个简易和快速的程序,可以由医护人员完成。它具有足够的灵敏度以检测几乎全部具有营养风险的患者。2006年,该工具被中国肠外肠内营养分会(CSPEN)列为肠外肠内营养支持适应证的有用工具(A级证据)[9]。本研究中,我们亦将经过营养风险筛选(NRS 2002),总分≥3分,定为消化道肿瘤患者营养支持的指征。当然有以下情况之一即判定为营养不良,亦予以口服安素肠内营养支持治疗:成年人在3个月内体质量下降超过原有体质量(除去人为因素) 的10 %;血红蛋白<8 g/L;血清白蛋白<32 g/L。
营养支持的方法可分为肠外与肠内两大类,选择的依据是:患者的病情是否允许经胃肠道进食;胃肠道的供给量是否可以满足患者的需要;患者的胃肠功能是否紊乱;患者有无肠外营养支持的禁忌,如心力衰竭、肾功能障碍等。
肠外营养支持主要靠静脉营养,不仅费用较高,而且输液导管的保留、无菌配液技术等致使其必须在有经验的医护人员管理下才能实施。单纯的完全胃肠外营养易出现感染及代谢并发症;长期静脉营养可导致肠黏膜萎缩、黏膜细胞再生不良、肠道消化酶的活性下降等,继而导致肠屏障功能削弱,引起肠道菌群易位诱发肠源性感染,而肠源性感染是危重患者多脏器功能衰竭的重要原因[10]。
肠内营养,不论是口服还是管饲,不但合乎生理,而且都比静脉营养便宜并易于管理;肠内营养至少与静脉营养同样有效;在维持机体免疫功能方面,肠内营养优于肠外营养;肠内营养可以逆转癌症患者很多有害的代谢作用,如逆转负氮平衡、抑制内源性糖原异生反应等;特殊的肠内营养素(营养物质中含谷氨酰胺、精氨酸、RNA和ω-3脂肪酸)可能会提高患者的存活率[11,12];晚期胃肠肿瘤患者免疫能力下降低下,肠内营养可以有助于维护肠黏膜屏障与免疫调控功能,从而降低肠道细菌易位和感染的发生。因此,对于晚期胃肠道肿瘤患者,使用肠内营养的临床意义更为重大,只有在肠内营养无法实施时才考虑选用静脉营养。本研究中患者均有一定胃肠道功能,予口服安素肠内营养支持治疗,在获得肠内营养同时,还可以维护肠黏膜屏障与免疫调控功能。只有口服不足时,才配合少量肠外营养支持作为补充。
肠内营养支持治疗是晚期消化道肿瘤患者一个重要的治疗方法,掌握适应证、选择合适的营养途径及营养制剂种类都是非常重要的。
在对消化道肿瘤患者的手术治疗、放疗、化疗、姑息性治疗等过程中,肠内营养支持贯彻始终。在面对每一个具体的消化道肿瘤患者时,选择建立合适的肠内营养途径是我们必须解决的临床课题。选择适合每一个具体消化道肿瘤患者的肠内营养制剂,也是临床的实用问题。新型的针对消化道肿瘤患者的肠内营养制剂,是今后一段时间的研究方向。安素为肠内全均衡营养粉剂,是一种完整的蛋白营养制剂,含有微量矿物质、铬、硒和钼,没有麸质,无致癌、致突变和生殖毒性,可提供高质量营养,能增强营养、造血及免疫功能,适用于肠道功能消化吸收好的患者。本品为淡黄色粉末,气芳香、味甜。本品与水混合后为低渣流质,可作为日常营养补充或完全饮食替代,口服或管饲后能提供均衡的营养供给。亦可用于药物,手术或心理方面的原因而导致的不能正常进食或营养不良的患者。安素(Ensure)粉剂能提供1.06 Kcal/mL能量,它的热量分配为14.2 %蛋白质,54 %碳水化合物,31.8 %脂肪。安素(Ensure)粉剂具有等渗性,重量渗克分子浓度为443 mOsm/kg水。因此只要正确的服用就不会因渗透压导致腹泻。所以,本研究中采用了安素口服进行肠内营养治疗。本研究中患者仅有1例认为口感不好,需要肠外营养补充,另有6例患者因食欲差,需要肠外营养补充,其余患者口服2~6杯安素,1个月后患者营养风险NRS及一般状态KPS评分均有改善,BMI稳定。这期间80 %患者还接受了以化疗为主的抗肿瘤治疗。说明安素口服改善了患者的一般状态、稳定了患者体质量。
陈焕伟等[13]研究发现:血清前白蛋白和视黄醇结合蛋白浓度在全胃肠外营养1周后明显增加,血清白蛋白水平稍下降,转铁蛋白浓度基本没有变化。吴国豪等[14]认为:血清白蛋白半衰期长达18~20 d,不适合于住院患者的营养评估;前白蛋白虽然半衰期短(2~3 d),在判断蛋白质急性改变方面更为敏感,但要注意很多疾病状态可对血清前白蛋白浓度产生影响,使其应用受到限制。所以在临床上应用传统指标评价患者营养状态时应考虑多指标、 多方法来进行全面评价。本研究采用了综合检测血清白蛋白、前白蛋白、BUN、CRE及HGB、体质量来评估患者营养情况。结果显示:安素口服1个月后,虽然体质量、HGB保持稳定,但血清白蛋白、前白蛋白、BUN、CRE有了明显提高;口服安素前50例患者均有不同程度营养不良,口服安素后5例患者已经无营养不良,其余45例患者营养不良程度亦有不同程度减轻。综合评估结果是营养不良程度得到了改善。
在抗肿瘤治疗中因治疗所产生的不良反应对患者的肝、肾功能及免疫力都有一定的损坏[15,16]。从本研究可以看到,给予肠内营养治疗维持或提高了体内前白蛋白、白蛋白以及血红蛋白的水平,肝、肾均在正常水平,对缓减患者肝、肾功能的损伤有一定的作用。可以说,肠内营养治疗对提高患者的营养状况,为肿瘤治疗奠定基础具有一定的作用。
胡秀娟等[17]认为:肿瘤患者消瘦症状评分较高,且与生活质量具有很大的相关性,仅次于疲乏,良好的营养状况可能对患者的生活质量有利,为治疗的顺利进行创造条件。
总之,口服安素能改善营养指标、减轻营养不良程度,提高体力状态评分、稳定体质指数,未见明显不良反应,为患者的进一步治疗,特别是化疗创造了更好的条件。
[1] Thoresen L,Fjelds tad I,KrogstadK,e t al.Nutritional status of patients with advanced cancer: The value of u sing the subjective global assessment of nutritional status as a screening tool[J]. Palliate Med,2002,16(1) : 33-42.
[2] Rose A.Oncology Nursing Secrets [M].Phrladephia: Henley & Bolfus Inc,2001: 365-384.
[3] 胡雁.实用肿瘤护理[M].上海:上海科学技术出版社,2007: 8.
[4] 中华医学会.临床诊疗指南:肠外肠内营养学分册[M].北京:人民卫生出版社,2007:15-21.
[5] 胡雁.实用肿瘤护理[M].上海:上海科学技术出版社,2007:8.
[6] Bauer J,Capra S,Ferguson M.Use of the scored Patient Generated Subjective Global Assessment (PGSGA) as a nutrition assessment tool in patients with cancer[J].Eur J Clin Nutr,2002,56 (8):779-785.
[7] Planas M,Audivert S,Perez- Portabella C,et al.Nutritional status among adult patients admitted to anuniverity affiliated hospital in Spain at the time of genome[J].Clin Nutr,2004,23 (5):1016-1024.
[8] Aorreia MI,Waitzberg DL.The impact of malnutrition on morb idity,mortality,length of hosp ital stay and costs evaluated through a multivariate model analysis[J].Clin Nutr,2003,22(3): 235-239.
[9] 中华医学会.临床诊疗指南:肠外肠内营养学分册[M].北京:人民卫生出版社,2007:15-21.
[10] Braunschweig CL,Levy P,Sheean PM,et al.Enteral compared with parenteral nutrition: a metaanalysis[J].Am J Clin Nutr,2001,74(4): 534-542.
[11] 唐云,李荣,田文,等.免疫肠内营养支持对胃肠道肿瘤患者术后的作用[J].军医进修学院学报,2001,22(3):177-179.
[12] 江志伟,黎介寿,李宁,等.肠内免疫营养对胃癌手术病人免疫功能及炎性反应的调理作用[J].肠外与肠内营养,2000,7(4):200-203.
[13] 陈焕伟,甄作均,潘文松.前白蛋白和视黄醇结合蛋白在肠外营养评估中的意义[J].肠外与肠内营养,2001,7(8): 149- 151.
[14] 吴国豪,刘中华,全应军,等.普外科住院患者营养状况评价[J].中华普通外科杂志,2004,19(12) : 732-734.
[15] 林锋.恶性肿瘤患者营养支持的纷争与共识[J].临床营养学现状,2009,1(1):76-79.
[16] 江志伟,黎介寿,李宁.恶性肿瘤患者的肠内营养支持[J].临床营养学现状,2009,1(3) : 46-47.
[17] 胡秀娟,廖春莲,梁军.癌症病人症状与生活质量的相关性研究[J].护理研究,2006,20(4):875-876.
R735
:B
:1671-8194(2014)02-0113-03
*通讯作者:E-mail:chengg6811@163.com

